Мезо ксантин эффект после: Мезоксантин (Meso-Xanthin F199) – высокоактивный препарат последнего поколения для инъекционного введения, разработанный в США лабораторией ABG Lab, известной нам уже по производству другого омолаживающего препарата — Мезовартон.
Мезоксантин (Meso-Xanthin F199) – высокоактивный препарат последнего поколения для инъекционного введения, разработанный в США лабораторией ABG Lab, известной нам уже по производству другого омолаживающего препарата — Мезовартон.
Meso-Xanthin F199 (Мезоксантин) — инъекционный препарат для для омоложения кожи лица, шеи и декольте. Активный состав веществ тормозит процессы старения, активизирует обновление клеток и улучшает их жизнедеятельность.
Показания:
-
Морщины, потеря тонуса и эластичности, гравитационный птоз I–II степени -
Обезвоженная, сухая кожа -
Синдром акне и постакне -
Жирная кожа -
Кожа «курильщика» -
Розацеа -
Устранение пигментных пятен и профилактика их образования -
Фотодерматит, себорейный дерматит -
Восстановление кожи после срединных и глубоких пилингов, лазерных шлифовок и других инвазивных процедур -
Подготовка кожи к пластической операции -
Реабилитация кожи после пластической операции
Противопоказания:
Существуют прямые и относительные противопоказания. Проконсультируйтесь со своим врачом.
Проконсультируйтесь со своим врачом.
-
хронические заболевания в стадии рецидива -
острые воспалительные заболевания кожи в местах предполагаемых инъекций -
непереносимость анестетиков -
прием антикоагулянтов -
эндокринные нарушения -
беременность -
лактация -
атопические заболевания кожи -
индивидуальная непереносимость компонентов, входящих в состав препарата -
возраст моложе 18 лет
Восстановительный период
После процедуры возможны синяки, покраснения, папулы, отеки. Покраснение сохраняется первые пару часов, отеки и папулы — от 2 до 5 дней, синяки — от 3 до 10. Уже на следующий день возможно нанесение тонального средства с целью камуфляжа синяков, или сразу после процедуры камуфляж стерильным тональным средством.
Покраснение сохраняется первые пару часов, отеки и папулы — от 2 до 5 дней, синяки — от 3 до 10. Уже на следующий день возможно нанесение тонального средства с целью камуфляжа синяков, или сразу после процедуры камуфляж стерильным тональным средством.
Особенности процедуры
Благодаря количеству — 1,5 мл в шприце, за 1 процедуру можно «проработать» не только кожу лица, но и шею, а также верхнее и нижнее веко. Перед процедурой вам будет предложена аппликационная анестезия. Папулы видны преимущественно в зоне шеи и вокруг век. Всего необходимо от 3–4 до 5–6 процедур курсом, 1 раз в 7–14 дней.
Что лучше: Мезоксантин или Мезовартон?
Оба препарата созданы на основе нестабилизированной гиалуроновой кислоты, схожи по действию, однако отличаются набором аминокислот, пептидов, факторов роста и других компонентов.
В каком возрасте колоть препарат?
Мезовартон и Мезоксантин предназначены для разной возрастной аудитории.
-
Людям до 40 лет — рекомендуется колоть Мезоксантин -
Пациентам 40 лет и более — комбинация препаратов или Мезовартон в отдельности.
Наиболее подходящий для вас препарат может определить только специалист.
Мезоксантин ( Meso-Xanthin F199 )
Meso-Xanthin — Сияй ярче
Разработан лабораторией ABG Lab LLC, производится на контрактном производстве BNC Korea
Инъекционный препарат (Объем 1,5 мл.) для интенсивного «очищения» клеток кожи от вредных веществ и повреждений, эффективно восстанавливающий качество кожи, в следствии чего, кожа «светится здоровьем изнутри».
Эпигенетическая терапия клеток кожи!
Инновационная разработка в области anti-age терапии клеток от лаборатории ABG LAB (USA).
Как замедлить процесс старения и качественно улучшить состояние кожи?
Причиной преждевременного старения клеток являются ряд причин, среди которых неблагоприятное влияние внешней среды, воздействие УФ-лучей, а также нездоровый образ жизни, которые в совокупности приводят к появлению пигментных пятен, высыпаниям и ухудшению качества и структуры кожи. Топические препараты не в силах справиться с данными проблемами и дают лишь кратковременные результаты, так как в данном случае воздействовать на кожу необходимо изнутри.
Топические препараты не в силах справиться с данными проблемами и дают лишь кратковременные результаты, так как в данном случае воздействовать на кожу необходимо изнутри.
Meso-Xanthin F199™ (Мезоксантин) — инъекционный препарат медицинского назначения для эксклюзивной детоксикации клеток кожи на эпигенетическом уровне за счет уникального активного компонента – каротонида Fucoxanthin F199 (Фукоксантин), полученного с помощью биотрансформирующей технологии и оказывающего научно доказанный терапевтический эффект на генетический материал клеток эпидермиса и дермы, способствует самовосстановлению «поврежденных» клеток кожи, обеспечивает противовоспалительный эффект, «защищает» от воздействия агрессивных факторов окружающей среды.
В чем уникальность Meso-Xanthin F199™?
Со временем способность клетки распознавать повреждения на уровне ДНК снижается, в результате чего нарушается и замедляется процесс клеточного деления.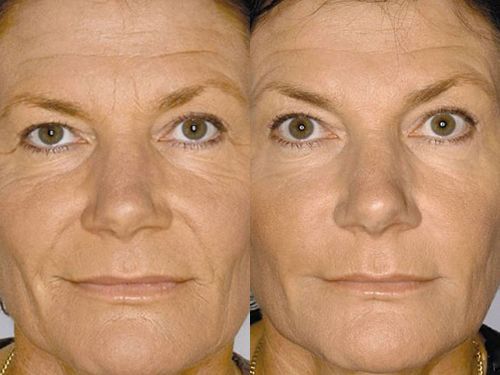 За счет уникального состава, главным компонентом которого является мощный антиоксидант Fucoxanthin F199, инъекционный препарат защищает и стабилизирует структуру ДНК клеток кожи, оптимизирует восстановительные процессы, защищает кожу от негативного воздействия окружающей среды и безопасно «очищает» ее изнутри. Таким образом, пациент получает идеальный рельеф и качество кожи без воспаление и акне.
За счет уникального состава, главным компонентом которого является мощный антиоксидант Fucoxanthin F199, инъекционный препарат защищает и стабилизирует структуру ДНК клеток кожи, оптимизирует восстановительные процессы, защищает кожу от негативного воздействия окружающей среды и безопасно «очищает» ее изнутри. Таким образом, пациент получает идеальный рельеф и качество кожи без воспаление и акне.
Для какого типа старения наиболее оптимально подходит?
Из-за особенностей строения и старения кожи лица наиболее подходит для деформационно-отечного и мускульного типов старения.
6 причин приобрести Meso-Xanthin F199™
1. Единственный препарат, который комплексно решает как дерматологические, так и косметологические проблемы, и, как следствие, кожа «светится здоровьем изнутри»
2. Уникальный антиоксидант второго поколения Fucoxantin восстанавливает правильную работу клетки с помощью эпигенетических механизмов и оказывает противовоспалительный эффект.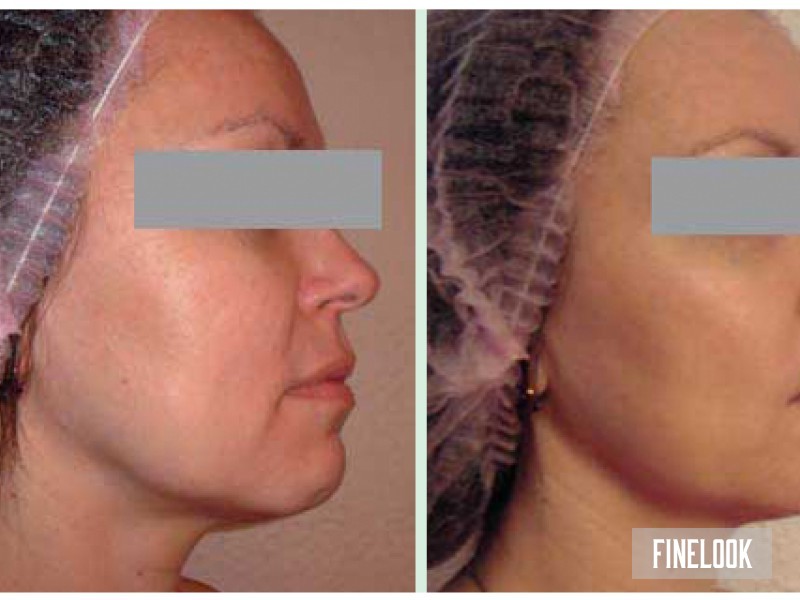
2. «Очищение» клеток кожи от вредных веществ и повреждений (тканевая детоксикация)
3. Защита от агрессивных факторов окружающей среды и устранение воспаления
4. Останавливает процессы «увядания» кожи
5. Не требует постоянных инъекций
6. Запатентованный препарат, прошедший многочисленные клинические исследования
Meso-Xanthin F199™ — секрет идеальной кожи!
Результатом применения препарата является значительное улучшение качества кожи с накопительным эффектом, таким образом для сохранения устойчивого результата будет достаточно поддерживающего курса инъекций 1 раз в год.
Сегодня пациенты все чаще делают выбор в пользу эстетических методов, позволяющих выглядеть естественно и обеспечивающих результат с минимальной агрессией. Мезоксантин — это уникальная технология, полностью соответствующая этой тенденции.
Первые результаты действия препарата можно заметить уже после первой процедуры! Необходимый и полный эффект будет достигнут после курса процедур, назначенного врачом-косметологом.
Попробуйте Meso-Xanthin F199™ и ощутите кожу, которая «светится здоровьем»!
Предназначен для профессионального использования врачами, прошедшими специальный курс обучения!
Эмет™ эксклюзивно представляет Meso-Xanthin F199™ в Украине и странах СНГ.
Мезоксантин — препарат для биоревитализации: показания и преимущества
Биоревитализация Мезоксантин
С возрастом состояние кожи человека только ухудшается. Этому способствует и экологическая обстановка, и процессы старения, а также современный напряженный уровень жизни с обилием стрессов. Ученые во всем мире постоянно работают в деле предотвращения старения, его замедления и возвращения молодости кожи. Одной из такой разработок является препарат Мезоксантин.
О процедуре
Биоревитализация Мезоксантин – это своего рода тренд в косметологии. Инновационный препарат, воздействие которого на кожу запускает регенеративный процесс в тканях, способствует более быстрому восстановлению эпидермиса (по сравнению с действием привычных уже препаратов для возвращения молодости, использующихся повсеместно).
Мезоксантин (Meso-Xanthin F199) – активное вещество, действующее на генную структуру клеток. Препарат позволяет держать под контролем активность клеток, усиливая ее по мере необходимости.
Мезоксантин является старшим братом Мезовартона (а он уже успел завоевать заслуженную популярность среди пациентов). Но в отличие от него Мезоксантин можно использовать у пациентов от 25-30 лет. Оба препарата хорошо сочетаются друг с другом и могут использоваться в комплексной терапии для омоложения.
Какие проблемы решает
Биоревитализация Meso Xanthin эффективно устраняет такие проблемы, как:
- Возрастные изменения на коже (снижение упругости, тургора, возникновение морщин, деформированный контур лица, сухость кожи)
- Гипермигментирование
- Реабилитация после пластических операций
- Восстановление после глубинных и срединных пилингов, дермабразии с помощью лазера
- Фотостарение после загара (солярия)
Благодаря воздействию препарата на клеточную систему в фибропластах кожи увеличивается экспрессия генов и белков (интегринов), которые обеспечивают процессы межклеточного матрикса и играют важную роль в восстановлении поврежденной ДНК.
Как проходит процедура
Процедура заключается во введении инъекций препарата под кожу пациента. Процесс занимает не более 40 минут. Врач-косметолог на предварительной консультации вместе с пациентом определяют проблемные зоны и области для коррекции, выясняют, нет ли у клиента противопоказаний для процедуры.
Препарат поставляется в индивидуальной упаковке, врач вскрывает ее непосредственно на сеансе перед пациентом. Внутри упаковки находятся специальные стикеры, подтверждающие оригинальное происхождение медикамента и являющиеся защитой от подделок.
Волосы пациента убирают под шапочку, кожа обрабатывается раствором хлоргексидина, и врач приступает к инъекциям. Введение препарата не ощущается, пациент может только почувствовать сам укол, но игла очень тоненькая, поэтому укол почти не ощущается.
На коже после процедуры могут образовываться небольшие папулы, которые проходят в течение 1-3 дней. Пациенты Центра «Cleo line» (Москва) любят мезоксантин за отсутствие побочных эффектов и ярко-выраженный результат.
Пациенты Центра «Cleo line» (Москва) любят мезоксантин за отсутствие побочных эффектов и ярко-выраженный результат.
Противопоказания
Есть и противопоказания у процедуры, они являются общими и схожи с остальными противопоказаниями при выполнении инъекционных методов омоложения:
- Заболевания аутоиммунные
- Аллергические реакции
- Обострения хронических заболеваний
- Эпилепсия
- Гематологические патологии
- Период вынашивания ребенка и ГВ
Чтобы узнать подходит ли процедура лично вам, лучше проконсультироваться со своим лечащим врачом.
Количество процедур и периодичность
Потребность в сеансах, а вернее в их периодичности, зависит от возраста пациента, но это не менее 4-6 процедур. Они могут проводиться в комплексе с Мезовартоном. Эффект сохраняется около 12 месяцев, затем следует повторить «инъекции молодости».
На консультации наш врач-косметолог проведет осмотр кожи пациента и даст необходимые рекомендации о требующемся количестве процедур и скажет, когда стоит выполнить повторный курс инъекций.
Результат
Благодаря уникальному составу Мезоксантина он способен оказывать действие на клеточную ДНК и возвратить лицу утраченную молодость и привлекательность. Препарат действует на только на те гены, которые отвечают за состояние кожи. Его успешно используют для профилактики старения и для биорепарации.
В результате процедуры пациент сможет избавиться:
- От пигментированной кожи и постакне
- От лишнего жира на лице
- От морщин, вялости и сухости кожи
Препарат также эффективен для восстановления кожи после таких процедур, как лазерная шлифовка и пилинг.
Препарат
Биоревитализант Meso-Xanthin – инновационный продукт, призванный решать проблемы старения кожи у пациентов от 25 лет и старше. Его механизм объясняется в запуске процессов регенерации и оказываемым влиянием на стволовые клетки.
Препарат выделен из морских водорослей, это пигмент из группы каротиноидов. Также в составе:
- гиалуроновая кислота
- незаменимые аминокислоты
- регуляторные пептиды
- коэнзимы
- витамины
- нуклеиновые кислоты
Выпускают Мезоксантин в одноразовом шприце дозировкой в 1. 5 мл.
5 мл.
Почему мы
Предлагаем пройти курс процедур биоревитализации Мезоксантина в Центре Cleo Line в Москве.
Почему стоит пройти процедуру у нас:
- Клиника работает с 2010 года – за это время мы обрели заслуженную репутацию в сфере косметологии;
- Сертифицированные препараты и оборудование обеспечивают эффективность процедур и гарантируют безопасность нашим клиентам;
- Высокий уровень наших специалистов – вы можете убедиться, посмотрев видео и фото наших пациентов с результатами после проведения сеансов;
- Доступные цены – стоимость процедур в нашем Центре средняя по Москве, а качество всегда на высоте;
- В Cleo Line есть уникальные, которые редко встречаются в других клиниках.
В штате нашего Центра опытные, профессиональные врачи-косметологи, которые способны вернуть молодость вашей коже и ее красоту.
Биоревитализация Мезоксантин в Москве — цена, подготовка к процедуре
Каждому человеку, к сожалению, приходится сталкиваться со старением кожи. Возрастные изменения нельзя отменить, но с помощью современной косметологии их возможно замедлить так, что вы будете выглядеть значительно моложе, и результат сохранится на долгие годы. Например, с помощью биоревитализации препаратом Мезоксантин (Meso Xanthin F199). Процедура интенсивно увлажняет и питает кожу, устраняет покраснения и высыпания, возвращает здоровый свежий цвет лица.
Возрастные изменения нельзя отменить, но с помощью современной косметологии их возможно замедлить так, что вы будете выглядеть значительно моложе, и результат сохранится на долгие годы. Например, с помощью биоревитализации препаратом Мезоксантин (Meso Xanthin F199). Процедура интенсивно увлажняет и питает кожу, устраняет покраснения и высыпания, возвращает здоровый свежий цвет лица.
В чем преимущество Meso Xanthin F199
В отличие от большинства препаратов, Meso Xanthin F199 действует на клеточном уровне. Он стимулирует деление стволовых клеток и благотворно влияет на ДНК эпидермиса благодаря действию каротиноида F199.
Входящие в состав средства пептиды (тиреодоксин и пептид меди) снимают воспаления, гиалуроновая кислота — интенсивно увлажняет кожу и восстанавливает ее эластичность. Витамин А омолаживает, С — убирает лишнюю пигментацию, Е — защищает от свободных радикалов и предотвращает преждевременное старение. Еще один активный компонент препарата — нуклеиновая кислота — стимулирует синтез коллагена и эластина, которые отвечают за упругость и молодость кожи.
Показания к биоревитализации
Биоревитализация Meso Xanthin F199 эффективно устраняет такие проблемы, как:
- пигментация;
- глубокие мимические морщины;
- акне 1-2 стадии;
- сухость и стянутость, потеря эластичности кожи;
- повышенная жирность кожи;
- нарушения текстуры эпидермиса;
- себорейный дерматит, при котором появляются новые высыпания;
- нечеткий овал лица;
- ярко выраженный второй подбородок.
Биоревитализация Мезоксантин эффективна как для профилактики старения, так и для омоложения кожи.
Как подготовиться к процедуре
Особой подготовки к биоревитализации не требуется. Единственная рекомендация — отказаться от посещения бань и саун за 2 недели до и после процедуры. Это необходимо для того, чтобы кожа не подвергалась повышенным нагрузкам. Если вы принимаете какие-либо препараты, предупредите об этом врача-косметолога на предварительной консультации.
Как проходит биоревитализация
Сеанс инъекций Мезоксантин занимает около 40 минут. Процедура включает несколько этапов:
Процедура включает несколько этапов:
- Демакияж и антисептическая обработка кожи.
- Местная анестезия с помощью специального крема или укола.
- Разметка линий, по которым будут вводить препарат.
- Введение препарата по выбранной врачом методике.
- Противовоспалительная, успокаивающая обработка кожи.
После сеанса в карточку пациента вносят данные о серии и номере введенного препарата.
Цена процедуры Мезоксантин в клинике «BL»
Цена процедуры Мезоксантин зависит от количества ампул и сеансов, которое необходимо пациенту для достижения желаемого результата. Точную стоимость процедур вам рассчитает врач-косметолог на предварительной консультации. На нашем сайте указаны начальные расценки на биоревитализацию. В стоимость включены ампула препарата объемом 1,5 мл, использование инструментов и работа косметолога.
Реабилитационный период
После инъекции Мезоксантин на коже могут появиться небольшие покраснения, микросинячки отеки. Бояться этих симптомов не нужно, они пройдут сами спустя 5-7 дней. Сразу после биоревитализации не стоит умываться и пользоваться косметикой. Первые 1,5-2 недели после процедуры — воздержаться от солнечных ванн и солярия, сауны и бани, физических нагрузок, плавания в водоемах и бассейнах.
Благодаря высокой эффективности и уникальному комплексному действию биоревитализация Meso Xanthin не только омолаживает, но и лечит кожу. В клинике косметологии и дерматологии «BL» эту процедуру выполняют специалисты с медицинским образованием. Запишитесь на консультацию, и наши врачи-косметологи помогут сделать вашу кожу красивой и здоровой.
Популярные вопросы
1. Достаточно ли одной процедуры для омоложения?
Если вы хотите добиться стойкого долгосрочного эффекта, то биоревитализацию лучше проводить курсами. Оптимальное количество процедур с использованием Мезоксантина – 4-6 с перерывом 1-2 недели.
2. Хватит одной ампулы для нескольких процедур?
Для выполнения каждой новой процедуры косметолог использует отдельный стерильный шприц с препаратом. Это необходимо для того, чтобы препарат был свежим, стерильным и эффективным. Вы можете не беспокоиться по поводу экономии, так как за один сеанс косметолог может обрабатывать несколько зон – область декольте, лицо, шею, а результат биоревитализации превосходит эффект от применения множества дорогостоящих кремов.
3. Можно делать биоревитализацию летом?
Да, лето – наиболее подходящий сезон для процедуры. Инъекции Мезоксантин даже рекомендуется делать в летнее время, так как они лечат и восстанавливают кожу, подготавливая ее к солнечным ваннам и загару.
Биоревитализация Мезоксантин — курс мезоксантина в Москве, коррекция возрастных изменений кожи, Meso Xanthin f199
Молодую кожу характеризует свежесть и сияние, упругость и отсутствие пигментных пятен. Однако современный образ жизни, вредные привычки могут не лучшим образом отражаться на ее состоянии. Биоревитализация Мезоксантин не только вернет коже здоровый внешний вид, но и защитит от вредных факторов окружающей среды, замедлив процессы старения.
Как работает
Meso Xanthin f199 – препарат нового поколения для подкожного введения, содержащий гиалуроновую кислоту и комплекс активных компонентов, которые, работая в синергизме, усиливают результат процедуры биоревитализации.
Механизм действия
- Гиалуроновая кислота. Высокомолекулярное соединение, которое восстанавливает упругость кожи, насыщает ее влагой, а также регулирует синтез фибробластов и улучшает транспорт питательных веществ в коже;
- Регуляторные пептиды. Тиоредоксин защищает клеточную мембрану от повреждения, контролирует выработку меланина. Пептид меди улучшает микроциркуляцию, купирует воспалительные процессы, активизирует синтез собственного коллагена;
- Фукоксантин. Каротиноид, полученный из водорослей, является мощнейшим антиоксидантом, защищающим клетки кожи от повреждающих факторов окружающей среды.
- Инсулиноподобный, эпидермальный факторы роста. Вещества, регулирующие скорость деления и обновления клеток эпидермиса и дермы;
- Аминокислоты, антиоксиданты, витамины, нуклеиновые кислоты – основные структурные компоненты для правильного протекания процесса «сборки» волокон коллагена и эластина, а также для обеспечения биосинтетических процессов основных клеток кожи.
Meso Xanthin f199 – идеальный препарат для пациентов 30-35 лет, однако при раннем появлении признаков старения, процедура выполняется и более молодым пациентам.
Процедура биоревитализации Мезоксантин является курсовой — для получения максимального эффекта рекомендовано проведение 4-6 процедур с интервалом 10-14 дней.
Преимущества препарата
Высокая эффективность за счет сбалансированного состава: в отличие от классических биоревитализантов, содержащих только гиалуроновую кислоту, в состав препарата Мезоксантин входит целый комплекс дополнительных компонентов, повышающих эффективность терапии
Низкий риск аллергических реакций – в состав коктейля входят высокоочищенные компоненты
Заметный результат. Первые изменения можно заметить уже через 2-3 процедуры. Полноценный эффект достигается после курса, состоящего из 4-7 сеансов
Сочетаемость с другими процедурами. Препарат может использоваться как в моновиде, так и в рамках сочетанного протокола, повышая результативность аппаратных процедур
Показания к применению препарата
Коррекция первых признаков старения: сниженный тургор, дряблость и обезвоженность кожи
Комплексное восстановление кожи в послеродовом периоде
Комплексная коррекция гиперпигментации
Тусклый, серый цвет лица, уставшая кожа
Процедура выбора для защиты кожи в условиях повышенной инсоляции (перед и после отпуска в жарких странах)
Кожа курильщиков
Профилактика процессов старения кожи
Подготовка к проведению лазерной шлифовки, термолифтинга, фотоомоложения, химических пилингов
Биоревитализация Мезоксантин проводится в зоне лица, шеи, декольте, кистей рук
Для каких процедур применяется Мезоксантин (Meso Xanthin f199) — препарат для биоревитализации
Код молодости Meso-Wharton P199 и Мeso-Xanthin F199!
Код молодости Meso-Wharton P199 и Мeso-Xanthin F199!
Биорепаранты Мезовартон (Meso-Wharton) и мезоксантин (Мeso-Xanthin) можно назвать усовершенствованным биоревитализантами. Дело в том, что гиалуроновая кислота, которая выступает основой препаратов, модифицирована по уникальной методике. К каждой её молекуле прикреплены активные вещества: аминокислоты, витамины, микроэлементы, пептиды, это позволяет продлить существование молекулы гиалуроновой кислоты, тем самым спровоцировать запуск процессов омоложения. В отличие от биревитализантов и мезопрепаратов, модифицированная гиалуроновая кислота бирепарантов находится в тканях гораздо дольше, это позволяет организму сформировать запас полезных элементов и использовать их в дальнейшем постепенно, запуская механизм обновления кожи.
МЕЗОВАРТОН P199.
Мезовартон провоцирует интенсивное восстановление клеток кожи, но главное его свойство – это увеличению количества собственных стволовых клеток.
Помимо витаминов, аминокислот, факторов роста и высокомолекулярной гиалуроновой кислоты в состав Мезовартона входит полипептид « Wharton Jelly Peptide P199 », который был открыт в ходе сложных операций на плоде в утробе матери. Послеоперационное заживление тканей у плода происходит достаточно быстро, при этом рубцы не образуются. Благодаря исследованиям, удалось вывести полипептид из пупочного канатика. Именно этот полипептид запускает процессы обновления в клетках. Синтетический аналог этого полипетида и входит в состав препарата.
Действие препарата Мезовартон.
Кожа увлажняется, возвращается тонус и упругость, происходит насыщение витаминами и микроэлементами. Но самое главное – запускаются процессы омоложения, собственные клетки кожи активно обновляются.
Показания к применению препарата Мезовартон.
Мезовартон показан при возрастных изменениях кожи после 40-45 лет: морщины, потеря четкости овала лица, вялая не эластичная кожа, тусклый цвет лица. Мезовартон показан при восстановлении после ожогов и химических пиллингов, а также после перенесенных пластических операций.
МЕЗОКСАНТИН F199.
В отличие от Мезовартона, биорепарант Мезокснатин разработан специально для молодой кожи с первыми признаками старения (25-30 лет). Мезоксантин продлевает и сохраняет молодость кожи, оказывает защитные действия ДНК клетки.
По составу Мезоксантин схож с Мезовартоном, но помимо высокомолекулярной гиалуроновой кислоты, аминокислот, витаминов и факторов роста, в препарате присутствует каротиноид Фукоксантин. Этот ключевой компонент, полученный из морских водорослей, обладает мощным омолаживающим действием.
Действие и эффект от применения ппрепарата Мезоксантин.
Мезоксантин работает с собственным стволовыми клетками пациента, закладывая в них информацию молодой и здоровой клетки, тем самым активизируя регенерацию и обновление тканей. Тургор кожи повышается, появляется эффект подтяжки, цвет лица улучшается, кожа сияет здоровьем и молодостью. Мезоксантин также существенно снижает видимость пигментных пятен и сосудистых рисунков. Но главным эффектом от применения препарата является торможение старения клетки.
Показания к применению Мезоксантина:
- первые признаки старения кожи;
- подготовка или восстановление после пластической операции;
- гиперпигментация;
- ожоги разного происхождения;
- перенесённые глубокие пилинги и лазерные шлифовки.
Биорепарация Meso Xanthin и Meso Wharton
Биорепаранты Мезовартон (Meso-Wharton) и мезоксантин (Мeso-Xanthin) можно назвать усовершенствованным биоревитализантами. Дело в том, что гиалуроновая кислота, которая выступает основой препаратов, модифицирована по уникальной методике. К каждой её молекуле прикреплены активные вещества: аминокислоты, витамины, микроэлементы, пептиды, это позволяет продлить существование молекулы гиалуроновой кислоты, тем самым спровоцировать запуск процессов омоложения.
В отличие от биоревитализантов и мезопрепаратов, модифицированная гиалуроновая кислота биорепарантов находится в тканях гораздо дольше, это позволяет организму сформировать запас полезных элементов и использовать их в дальнейшем постепенно, запуская механизм обновления кожи.
Мезовартон в клинике в Москве
Мезовартон провоцирует интенсивное восстановление клеток кожи, но главное его свойство – это увеличению количества собственных стволовых клеток.
Помимо витаминов, аминокислот, факторов роста и высокомолекулярной гиалуроновой кислоты в состав Мезовартона входит полипептид “Wharton Jelly Peptide P199”, который был открыт в ходе сложных операций на плоде в утробе матери. Послеоперационное заживление тканей у плода происходит достаточно быстро, при этом рубцы не образуются. Благодаря исследованиям, удалось вывести полипептид из пупочного канатика. Именно этот полипептид запускает процессы обновления в клетках. Синтетический аналог этого полипетида и входит в состав препарата.
- Повышает активность клеток и синтез собственного коллагена, эластина и гиалуроновой кислоты, улучшает текстуру кожи (повышает её плотность)
- участвует в регуляции заживления и восстановления кожи, нормализует микроциркуляцию.
- оказывает влияние на внутриклеточный метаболизм, стимулирует рост клеток.
- сильнейший антиоксидант, моделирует выработку меланина.
- является мощным противовоспалительным агентом
Открытие полипептида «Wharton Jelly Peptide Р199» связано с деятельностью известного хирурга акушера-гинеколога, доктора Медицины, профессора Бориса Петриковского. Доктор Петриковский обратил внимание, что заживление тканей у плода всегда протекает эффективно и без образования рубца, и установил, что такой процесс заживления обусловлен высокой пролифиративной активностью эмбриональных стволовых клеток в желеобразной эмбриональной субстанции пупочного канатика «Wharton’s Jelly».
В результате исследований был выделен полипептид, стимулирующий деление клеток. Совместно с лабораторией University Medical Center, Long Island, N. Y,. профессором Петриковским создан синтетический аналог этого пептида, который получил название «Wharton Jelly Peptide P199». На протяжении четырех лет российскими врачами совместно с институтом « Fijie» (представителями Мeso-Wharton P199), институтом биологии развития им. Кольцова, РАН, получены результаты не только омоложения кожи, но и лечения купероза, восстановления кожи после лазерных процедур.
Показания к применению:
В косметологии:
- Профилактика и терапия «увядания» кожи.
- Коррекция возрастных изменений (морщины, потеря тонуса и эластичности, гравитационный птоз I-II степени)
- Синдром обезвоженной кожи.
- Подготовка кожи к пластическим операциям.
- Реабилитация кожи в послеоперационном периоде.
- Восстановление кожи после срединных и глубоких пилингов, лазерных шлифовок и других инвазивных процедур.
- Комплексная терапия дисхромий.
В дерматологии:
- Синдром постакне.
- Синдром фенотипически жирной кожи.
- Синдром кожи курильщика.
- Акне 1-2 стадии, вне обострения.
- Розацеа (все формы).
- Розацеаподобный демодекоз.
- Фотодерматиты, сопровождающиеся образованием меланогенетических пятен.
- Себорейный дерматит.
- Ксероз кожи.
Лучший омолаживающий эффект определен у категории пациентов 35-48 лет. Помимо синтетического аналога эмбрионального пептида в состав препарата Мeso-Wharton P199 входит биосинтетическая высокомолекулярная гиалуроновая кислота, которая создает гидрорезерв в межклеточном матриксе, а также комплекс из аминокислот, витаминов, факторов роста, инкапсулированных в наносомы: все то, что необходимо для непосредственного омоложения клеток кожи и обеспечивает видимый эффект лифтинга.
Действие препарата Мезовартон
Кожа увлажняется, возвращается тонус и упругость, происходит насыщение витаминами и микроэлементами. Но самое главное – запускаются процессы омоложения, собственные клетки кожи активно обновляются.
Показания к применению препарата Мезовартон
Мезовартон показан при возрастных изменениях кожи после 40 лет: морщины, потеря четкости овала лица, вялая не эластичная кожа, тусклый цвет лица. Мезовартон показан при восстановлении после ожогов и химических пиллингов, а также после перенесенных пластических операций.
Мезоксантин в клинике в Москве
В отличие от Мезовартона, биорепарант Мезокснатин разработан специально для молодой кожи с первыми признаками старения (28-30 лет). Мезоксантин продлевает и сохраняет молодость кожи, оказывает защитные действия ДНК клетки.
По составу Мезоксантин схож с Мезовартоном, но помимо высокомолекулярной гиалуроновой кислоты, аминокислот, витаминов и факторов роста, в препарате присутствует каротиноид Фукоксантин. Этот ключевой компонент, полученный из морских водорослей, обладает мощным омолаживающим действием.
Действие и эффект от применения ппрепарата Мезоксантин
Мезоксантин работает с собственным стволовыми клетками пациента, закладывая в них информацию молодой и здоровой клетки, тем самым активизируя регенерацию и обновление тканей. Тургор кожи повышается, появляется эффект подтяжки, цвет лица улучшается, кожа сияет здоровьем и молодостью. Мезоксантин также существенно снижает видимость пигментных пятен и сосудистых рисунков. Но главным эффектом от применения препарата является торможение старения клетки.
Показания к применению Мезоксантина
первые признаки старения кожи;
подготовка или восстановление после пластической операции;
гиперпигментация;
ожоги разного происхождения;
перенесённые глубокие пиллинги и лазерные шлифовки.
Стоимость процедуры биореперация в клинике “Доктора Гришкяна” в Москве
Запись на прием
Реакция пигмента желтого пятна на добавку, содержащую мезозеаксантин, лютеин и зеаксантин
Nutr Metab (Лондон). 2007; 4: 12.
, 1 , 2 , 2 , 3 и 2
Ричард А Боун
1 Департамент физики, Международный университет Флориды, 11200 SW 8th Street, Майами , FL 33199, США
John T. Landrum
2 Департамент химии и биохимии, Международный университет Флориды, 11200 SW 8th Street, Майами, Флорида 33199, США
Yisi Cao
2 Департамент химии и биохимии , Международный университет Флориды, 11200 SW 8th Street, Майами, Флорида 33199, США
Алан Н. Ховард
3 Даунинг-колледж, Кембриджский университет, Кембридж CB2 1DQ, Великобритания
Франческа Альварес-Кальдерон
2 Департамент химии и биохимии, Международный университет Флориды, 11200 SW 8th Street, Майами, Флорида 33199, США
1 Физический факультет Международного университета Флориды, 11200 SW 8th Street, Майами, Флорида 33199, США
2 Департамент химии и биохимии, Международный университет Флориды, 11200 SW 8th Street, Майами, Флорида 33199, США
3 Даунинг-колледж, Кембриджский университет, Кембридж CB2 1DQ, UK
Автор, ответственный за переписку.
Поступило 9 февраля 2007 г .; Принято 11 мая 2007 г.
Copyright © 2007 Bone et al; лицензиат BioMed Central Ltd.
Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License (http://creativecommons.org/licenses/by/2.0), которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе. при условии правильного цитирования оригинала.
Эта статья цитируется в других статьях в PMC.
Abstract
Предпосылки
Возрастная дегенерация желтого пятна (AMD) — это заболевание с множеством факторов риска, многие из которых связаны с окислительным стрессом.Считается, что макулярный пигмент с его антиоксидантными и светозащитными свойствами защищает от AMD. Результатом стало появление диетических добавок, содержащих макулярные каротиноиды, лютеин и зеаксантин. Совсем недавно на рынке появилась добавка, содержащая, кроме того, третий главный каротиноид макулярного пигмента, мезозеаксантин. Целью исследования было определить эффективность такой добавки в повышении плотности макулярного пигмента у людей.
Методы
Было проведено 120-дневное исследование добавок, в котором 10 субъектов получали гелевые капсулы, которые обеспечивали 20 мг / день преимущественно мезозеаксантина с меньшими количествами лютеина и зеаксантина.Второй группе из 9 субъектов давали гелевые колпачки, содержащие плацебо, в течение того же 120-дневного периода. До и во время периода приема добавок образцы сыворотки крови анализировали с помощью высокоэффективной жидкостной хроматографии на содержание каротиноидов. Точно так же оптическую плотность макулярного пигмента измеряли с помощью фотометрии гетерохроматического мерцания. Различия в ответе между группами добавок и плацебо были проверены на значимость с использованием t-критерия Стьюдента.
Результаты
Во время приема каротиноидов образцы крови показали присутствие всех трех каротиноидов.Оптическая плотность макулярного пигмента, измеренная при 460 нм, увеличивалась в среднем на 0,59 ± 0,79 миллиабсорбционных единиц / день у 10 субъектов, получавших добавки. Это значительно отличалось от группы плацебо (9 субъектов), для которой средняя скорость составляла -0,17 ± 0,42 миллиабсорбционных единиц / день.
Заключение
Мы впервые показали, что мезозеаксантин всасывается в сыворотку после приема внутрь. Данные показывают, что добавка, содержащая преимущественно мезозеаксантин, обычно эффективна для повышения плотности макулярного пигмента и может оказаться полезным дополнением к защите от AMD.
Предпосылки
Макулярный пигмент (MP), впервые идентифицированный в середине 1980-х как комбинация лютеина и зеаксантина [1-3], впоследствии было показано, что он характеризуется наличием определенных стереоизомеров этих двух каротиноидов [4] . Хотя лютеин (L) присутствует в виде одного стереоизомера, [(3R, 3’R, 6’R) -β, ε-каротин-3,3′-диол], зеаксантин встречается в основном в виде смеси [(3R, 3’R) -β, β-каротин-3,3′-диол] и [(3R, 3’S) -β, β-каротин-3,3′-диол] с гораздо меньшим количеством [(3S, 3’S) -β, β-каротин-3,3′-диол].Первые два преобладающих изомера зеаксантина называются зеаксантином (Z) и мезо -зеаксантин (MZ) соответственно. Из этих каротиноидов только L и Z обычно потребляются в соотношении примерно семь к одному [5], тогда как MZ является необычным и, следовательно, редким изомером в рационе. MZ присутствует в значительных количествах в промышленных цыплятах и яйцах в Мексике, где его обычно добавляют в корм для достижения желаемой окраски этих продуктов. С этой целью ежегодно продается около 3000 кг МЗ [6].В популяции США L и Z в изобилии присутствуют в сыворотке, но MZ обычно не может быть обнаружен в сыворотке. Это наблюдение привело к гипотезе, что MZ образуется в сетчатке как продукт преобразования L [4,7]. In vitro превращение L в MZ легко достигается в реакции, катализируемой основанием [4], и это является основой промышленного процесса его синтеза и использования в кормах для домашней птицы. Гипотеза конверсии подтверждается распределением отдельных каротиноидов в сетчатке. В центральных 10 ° больше MZ и меньше L относительно Z, тогда как на периферии (эксцентриситет> 35 °) ситуация обратная [8].Это говорит о том, что постулируемый процесс преобразования работает с большей эффективностью в фовеальном центре по сравнению с периферической сетчаткой. Обезьяны, выращенные на бескаротиноидной диете, а затем добавленные только L, впоследствии показали как L, так и MZ в MP. Те, к которым добавлялся Z, не показали MZ в их MP, только Z. Эти данные являются убедительным доказательством в поддержку гипотезы L-to-MZ конверсии [9].
Абсолютная конфигурация гидроксильных групп, расположенных на 3 и 3 ‘атомах углерода каротиноидных концевых групп, идентична в молекулах L и MZ.Таким образом, преобразование L в MZ должно включать только сдвиг одной двойной углерод-углеродной связи в ε-кольце L, тем самым увеличивая конъюгацию (см. Рис.). Альтернативный механизм образования MZ предполагает, что метаболит, дегидролютеин, вызывает MZ посредством ферментативного пути восстановления [10]. Действительно, кето-каротиноид кантаксантин действительно подвергается редукции в сетчатке человека и приматов, что подтверждает эту возможность [11]. Однако в плазме дегидролютеин образуется как из L [12], так и из Z [13].Если эти процессы также происходят в глазу и MZ образуется из этого метаболита, он должен был быть обнаружен у обезьян, принимающих Z- и L-добавки. Какой бы путь ни был задействован, он, вероятно, будет включать ферментативный контроль, чтобы соответствовать наблюдениям, что доля MZ в сетчатке зависит от местоположения.
Структуры основных компонентов пигмента желтого пятна.
На этом этапе мы можем порассуждать о возможных преимуществах, которые такое преобразование может дать глазу.Было высказано предположение, что МП защищает макулу двумя процессами [14]. Его присутствие в аксонах фоторецепторов [15] вместе с диапазоном спектрального поглощения (~ 400-500 нм) обеспечивает MP способность защищать задние ткани, такие как внешние сегменты фоторецепторов и RPE, от актинического синего света. Кроме того, его присутствие во внешних сегментах и RPE [16,17] может смягчить фотоокислительное повреждение, вызванное синим светом [18], благодаря его антиоксидантным свойствам и улавливанию свободных радикалов.Эксперименты in vitro показывают, что Z является более сильным антиоксидантом, чем L [18]. В одном исследовании тушение синглетного кислорода Z было примерно в два раза эффективнее тушения L [19]. Причина, по-видимому, связана, по крайней мере частично, с расширенной конъюгацией Z по сравнению с L. MZ разделяет эту электронную функцию с Z и, следовательно, должен обладать тем же антиоксидантным потенциалом, что и Z. Также сообщалось, что в сочетании с зеаксантином Связывающий белок, пи-изоформа глутатион-S-трансферазы, MZ обеспечивает немного лучшую защиту от окисления липидной мембраны, чем Z [20].Без связывающего белка ситуация обратная. Таким образом, для макулы может быть выгодно увеличить отношение общего зеаксантина (Z + MZ) к L. В сыворотке отношение Z к L составляет примерно 1: 4. Второстепенным преимуществом может быть скромный, но значительный сдвиг в сторону более длинных волн Z-хромофора по сравнению с L, что приводит к увеличению диапазона длин волн экранирования синего света по сравнению с тем, который был бы обеспечен, если бы МП состоял преимущественно из L. Третье преимущество может возникнуть из фактического размещения молекул каротиноидов.Наблюдения показывают, что L и Z могут присутствовать внутри клеточных мембран [21,22]. Z, по-видимому, охватывает мембрану в перпендикулярной ориентации, тогда как L имеет тенденцию лежать близко к поверхности мембраны [23]. Эти конфигурации размещают защитные участки окисления Z ближе к легко окисляемым цепям полиненасыщенных жирных кислот внутри мембраны.
Целью исследования было изучить способность проглоченного MZ в сочетании с L и Z увеличивать оптическую плотность MP.Исследование было мотивировано недавним появлением диетических добавок, содержащих значительные количества MZ в дополнение к L и Z.
Методы
Субъекты
Восемь мужчин и 2 женщины были набраны из университетского сообщества для исследования добавок. Их возраст колебался от 21 до 58 лет (в среднем 30,5 ± 10,9 года). Для более детального анализа каротиноидов сыворотки крови были привлечены еще двое испытуемых. Их возраст был 51 и 61 год. Впоследствии для получения плацебо была набрана группа сравнения (плацебо стало доступно только после того, как исследование было начато).Группа состояла из 5 мужчин и 4 женщин в возрасте от 19 до 31 года (в среднем 22,1 ± 3,6 года). Хотя наше исследование не соответствовало стандартному двойному слепому плацебо-контролируемому исследованию, в котором субъектов случайным образом распределяли в группы лечения и плацебо, оно действительно предлагало возможность отличить изменения MP, вызванные добавками, от изменений, которые могли произойти при более длительной терапии. случайная основа. Следует также отметить, что исследование проводилось в Южной Флориде, где диета, как правило, не является сезонной из-за постоянной доступности обычно потребляемых фруктов и овощей.Поэтому мы считаем, что отказ от одновременного использования групп добавок и плацебо не приведет к искажению результатов. Кроме того, хотя разница в среднем возрасте групп была просто значительной (p <0,05), мы не знаем о каких-либо возрастных различиях в способности людей изменять свой МП с помощью добавок.
Критериями исключения для потенциальных субъектов были: 1) курение или курение в течение предыдущих 12 месяцев, 2) любая визуальная патология, 3) неспособность во время практических занятий обеспечить приемлемые измерения оптической плотности MP (MPOD) и 4) использование пероральных добавок, содержащих значительную (> 0.25 мг / день) количества L и / или Z. Помимо последнего ограничения, субъекты могли свободно следовать своей обычной диете. Субъекты подписали форму информированного согласия в соответствии с требованиями Институционального наблюдательного совета, и исследование соответствовало принципам Хельсинкской декларации. Каждый испытуемый прошел обучение гетерохроматической фликкер-фотометрии, методу, используемому для определения MPOD. Официальное включение в исследование последовало за периодом практики, в течение которого от субъектов требовалось достичь приемлемых измерений MPOD (стандартная ошибка среднего значения на основе набора из 5 центральных и 5 периферийных настроек ≤ 0.020 единиц поглощения. См. ниже.).
Добавка
Субъектам в группе добавок дали запасы гелевых капсул, содержащих неэтерифицированные каротиноиды: 14,9 мг MZ, 5,5 мг L и 1,4 мг Z в виде суспензии в соевом масле, и проинформировали о содержимом. Состав гелевых крышек определяли с помощью ВЭЖХ (см. Ниже). Смесь каротиноидов была произведена Industrial Orgánica SA (Монтеррей, Мексика) путем катализируемой основанием реакции каротиноидов (~ 93% L, 7% Z), экстрагированных из бархатцев (Targetes sp.). Безопасность MZ была подтверждена в недавнем исследовании токсичности. На основании исследования уровень отсутствия наблюдаемых побочных эффектов (NOAEL) MZ у крыс составлял> 200 мг / кг / день [24]. Продукт также был протестирован на мутагенность с помощью теста Эймса с отрицательными результатами [25].
Субъектам в группе плацебо давали гелевые колпачки, содержащие только небольшое количество растительного масла. В отличие от группы приема добавок, группа плацебо была слепой, получив информацию о том, что гелевые колпачки содержат либо каротиноиды, либо плацебо.Субъекты в обеих группах были проинструктированы принимать гелевые капсулы ежедневно во время еды в течение 120 дней.
MPOD измерений
MPOD было определено для каждого объекта методом гетерохроматической фликкер-фотометрии (HFP) [26]. Испытуемые наблюдали стимул под углом 1,5 °, который чередовался между 460 и 540 нм, и регулировали интенсивность первого до минимума мерцания. Пять повторных корректировок были сделаны при просмотре стимула в центре (частота 30 Гц), и 5 повторных эталонных корректировок были сделаны при просмотре стимула периферически с эксцентриситетом 8 ° (частота 22 Гц).После каждой настройки клиновому фильтру, регулирующему интенсивность 460 нм, автоматически давалось случайное смещение. Логарифмическое соотношение средних значений двух наборов измерений интенсивности равно разнице в MPOD при 460 нм между фовеа и периферическим референсным участком. Предполагая, что MPOD незначительно на периферии, процедура по существу обеспечивает средний MPOD в пределах 1,5 ° центрального [27]. Однако это может быть не так для субъектов, получающих высокие дозы каротиноидов. Родригес-Кармона и др.обнаружили, что после приема 20 мг L и / или Z в день, наклон распределения MPOD оставался конечным даже до эксцентриситета 8 ° [28], что означает, что нельзя предполагать, что MPOD равняется нулю в этом месте. Таким образом, центральный MPOD может быть немного недооценен HFP в конце исследования добавок, даже если в процедуре используется эталонный участок до 8 °. Кроме того, в парафовеа (эксцентриситет 5,5 °) MPOD может, согласно одному исследованию [29], увеличиваться с возрастом, и это по той же причине может вызывать очевидное снижение центрального MPOD с возрастом при использовании 5.5 ° или, возможно, 8 °, ориентир.
Измерения MPOD проводились по крайней мере 4 раза до приема добавок, затем дважды в неделю в течение 120-дневного периода приема добавок и в течение 4-недельного периода после приема добавок. (Делались поправки на праздники и т. Д., Что приводило к случайным пропускам в данных.) Следует отметить, что эти измерения представляют собой тест, проводимый самостоятельно, без вмешательства оператора. Субъекты записывают каждую настройку клина, нажимая кнопку, и микропроцессор автоматически вычисляет их MPOD и соответствующую стандартную ошибку в среднем.Это эффективно устраняет любую предвзятость оператора или субъекта, которая в противном случае могла бы по-разному влиять на результаты либо группы MZ, либо группы плацебо.
Анализ каротиноидов в сыворотке
Образцы сыворотки были получены от каждого субъекта для отслеживания изменений в концентрации L и Z. Анализ проводился ассистентом, который не знал происхождения образцов сыворотки (MZ или плацебо). Два образца были взяты перед добавлением, чтобы установить исходный уровень.Во время приема добавки образцы сыворотки брали каждые 2 недели. Каротиноиды экстрагировали из сыворотки с помощью методов, которые были описаны ранее [30], и включали добавление до экстракции известного количества внутреннего стандарта (монопентиллютеинового эфира) на каждый миллилитр сыворотки. ВЭЖХ экстрактов проводили на обращенно-фазовой системе с использованием колонки Ultracarb ODS 3 мкм 250 × 4,6 мм (Phenomenex, Torrance CA). Подвижная фаза представляла собой ацетонитрил / метанол (85:15) при 1 мл / мин с 0.Добавлен 1% триэтиламин для ингибирования разложения каротиноидов во время элюирования.
Эта система способна производить базовое разделение L и объединенных стереоизомеров зеаксантина, но не отделяет Z от MZ. Чтобы определить, всасывается ли MZ в сыворотку вместе с L и Z, образцы сыворотки были взяты у 2 дополнительных субъектов, A и B, до приема и после 6 недель приема добавок. Каротиноиды, экстрагированные из этих образцов, анализировали с помощью ВЭЖХ на 250 × 4.Колонка Chiralpak AD диаметром 6 мм, состоящая из носителя из диоксида кремния, модифицированного хиральным полисахаридом (Daicel Chemical Industries, Осака, Япония), и подвижной фазы, состоящей из гексана и изопропилового спирта. Элюирование проводили при скорости потока 0,8 мл / мин, начиная с 90% гексана и 10% изопропилового спирта и увеличивая до 100% гексана в течение 55-минутного градиента. Стереоизомеры идентифицировали путем сравнения с порядком элюирования известных стандартов.
Те же системы использовались для анализа каротиноидов в добавке.
Результаты
Присутствие в сыворотке MZ в дополнение к L и Z, полученное в результате приема добавок, было подтверждено у двух субъектов, A и B, которые участвовали в этой части исследования. Перед добавлением сывороточные концентрации L, Z и MZ составляли 22,9, 4,4 и 0,0 нмоль / дл и 14,8, 2,1 и 0,0 нмоль / дл для субъектов A и B соответственно. После 6 недель приема эти значения составили 23,9, 8,7 и 4,4 нмоль / дл для субъекта A и 45,4, 15,4 и 14,5 нмоль / дл для субъекта B.
Для остальных 10 субъектов в исследовании добавок (субъекты № 1–10) мы определили увеличение L и комбинированного Z + MZ в сыворотке путем усреднения значений каждого субъекта до приема добавок, а также значений, полученных за неделю. 6 до конца периода приема добавок. На последнее среднее значение не повлияло повышение концентрации каротиноидов в сыворотке, которое обычно происходит на ранней стадии приема добавок [31]. Результаты представлены в таблице. До приема добавок средняя концентрация для 10 субъектов составляла 30.5 ± 12,5 (диапазон от 16,4 до 54,2) нмоль / дл для L и 9,7 ± 4,8 (диапазон от 3,6 до 19,0) нмоль / дл для Z + MZ. Во время приема добавок (т.е. с 6 недели до конца приема) эти значения выросли до 38,0 ± 12,0 (диапазон от 24,2 до 62,3) нмоль / дл для L и 26,4 ± 6,5 (диапазон от 13,6 до 35,0) нмоль / дл для Z + MZ. .
Таблица 1
Сывороточные ответы для 10 субъектов в группе добавок. Исходные значения и значения плато относятся к средним значениям, полученным до приема и с 6 недели до конца приема, соответственно.
| Номер субъекта | Исходная концентрация L ± стандартное отклонение (нмоль / дл) | Концентрация L на плато ± стандартное отклонение (нмоль / дл) | Исходная концентрация Z + MZ ± стандартное отклонение (нмоль / дл) | Плато Z + Концентрация MZ ± стандартное отклонение (нмоль / дл) | ||||
| 1 | 36,9 ± 17,8 | 42,4 ± 6,7 | 5,6 ± 0,4 | 25,1 ± 5,2 | ||||
| 2 | 16,4 ± 1,9 12,3 | 7,4 ± 1.6 | 34,9 ± 15,4 | |||||
| 3 | 22,6 ± 3,5 | 26,3 ± 2,7 | 8,7 ± 1,1 | 22,9 ± 3,7 | ||||
| 4 | 35,8 ± 1,8 | 36,4 5,6 | 29,6 ± 8,8 | |||||
| 5 | 18,2 ± 1,4 | 25,5 ± 5,8 | 6,1 ± 0,4 | 22,1 ± 5,7 | ||||
| 6 | 42,7 ± 0,9 | 62,3 3,0 | 35.0 ± 9,3 | |||||
| 7 | 16,7 ± 3,3 | 24,2 ± 4,9 | 7,3 ± 0,9 | 13,6 ± 3,5 | ||||
| 8 | 54,2 ± 5,2 | 45,2 ± 10,6 | 45,2 ± 10,6 | 30,4 ± 0,8 | ||||
| 9 | 34,0 ± 6,8 | 49,1 ± 4,2 | 14,0 ± 3,8 | 27,0 ± 1,2 | ||||
| 10 | 27,1 ± 3,8 | 34,6 ± 1,2 | ||||||
| Среднее ± стандартное отклонение | 30,5 ± 12,5 | 38,0 ± 12,0 | 9,7 ± 4,8 | 9014 ± 6,5 для группы |
субъекты № 11–19), средний уровень L в сыворотке пациентов изменился с 19,5 ± 6,4 (диапазон от 4,6 до 27,9) до приема плацебо до 30,7 ± 22,8 (диапазон от 6,4 до 79,1) нмоль / дл с 6 недели до конца. из «добавок». Для Z значение изменилось с 7.От 6 ± 3,4 (диапазон от 2,1 до 10,0) до 15,8 ± 15,3 (диапазон от 2,9 до 50,3) нмоль / дл. Ни одно из этих средних изменений, которое могло быть связано с изменениями в питании, не было значимым согласно двустороннему t-критерию (p = 0,14 для L, p = 0,13 для Z), равно как и какие-либо индивидуальные изменения.
Ответ на
MPOD у каждого субъекта был определен количественно путем расчета средней скорости изменения MPOD, измеренной в миллиабсорбционных единицах в день (мАЕ / день), и соответствующей стандартной ошибки (SE) для каждого глаза каждого субъекта в течение периода исследования.Данные для левого глаза субъекта № 1 (группа добавок), у которого был особенно устойчивый ответ и небольшой разброс в измерениях MPOD, и для правого глаза субъекта № 6 (группа добавок), у которого не было значительных изменений в MPOD в совокупности. с большим разбросом, показаны на рис. Кратковременная изменчивость от сеанса к сеансу типична для данных, полученных с помощью HFP, и, вероятно, является артефактом измерения. Скорость изменения MPOD для каждого глаза каждого субъекта рассчитывалась с использованием всех измерений MPOD для этого глаза с нулевого дня (начало приема добавок) и далее.Основываясь на наблюдении, что некоторые субъекты (например, субъекты 2, 4, 9) имели значительно разные начальные MPOD в их левом и правом глазах, мы рассматривали ответы в каждом глазу субъекта как независимые наблюдения. Полные результаты для группы добавок представлены в таблице. Таблица включает p-значения, основанные на двустороннем t-тесте, которые показывают, были ли измеренные скорости изменения MPOD значительно отличаться от нуля. Значительные темпы увеличения MPOD наблюдались в 12 глазах, никаких значительных изменений не произошло в 7 глазах и, что удивительно, значительное снижение произошло в одном глазу.
Таблица 2
Ответ оптической плотности макулярного пигмента (MPOD) на добавку. Данные MPOD для группы добавок, полученные до приема, вместе со скоростью изменения MPOD во время приема. Значения p показывают, значительно ли отличаются эти показатели от нуля. (AU = единица поглощения)
| Субъект / глаз | MPOD pre AU | SD pre AU | Скорость изменения MPOD ± SE, mAU / день | p | Значимость скорости изменения |
| 1 / л | 0.421 | 0,016 | 2,22 ± 0,11 | <0,0001 | Сигн. увеличение |
| 1 / R | 0,446 | 0,025 | 2,01 ± 0,06 | <0,0001 | Signif. увеличение |
| 2 / L | 0,779 | 0,015 | -0,18 ± 0,30 | 0,57 | Без знач. изменение |
| 2 / R | 0,679 | 0,016 | 0,17 ± 0,38 | 0.66 | Без знач. изменение |
| 3 / L | 0,286 | 0,018 | 0,27 ± 0,10 | 0,012 | Signif. увеличение |
| 3 / R | 0,306 | 0,011 | -0,04 ± 0,09 | 0,69 | Без знач. изменение |
| 4 / L | 0,468 | 0,019 | 1,23 ± 0,21 | <0,0001 | Signif. прибавка |
| 4 / R | 0.355 | 0,022 | 1,58 ± 0,28 | <0,0001 | Сигн. увеличение |
| 5 / л | 0,254 | 0,018 | 0,51 ± 0,14 | 0,0009 | Signif. увеличение |
| 5 / R | 0,265 | 0,027 | -0,46 ± 0,18 | 0,016 | Signif. уменьшение |
| 6 / л | 0,351 | 0,019 | -0,22 ± 0,16 | 0.18 | Без знач. изменение |
| 6 / R | 0,362 | 0,014 | 0,02 ± 0,21 | 0,94 | Без знач. изменение |
| 7 / L | 0,335 | 0,017 | 0,92 ± 0,34 | 0,015 | Signif. увеличение |
| 7 / R | 0,304 | 0,02 | -0,57 ± 0,35 | 0,12 | Без знач. изменить |
| 8 / л | 0.718 | 0,013 | 0,65 ± 0,25 | 0,016 | Знач. увеличение |
| 8 / R | 0,722 | 0,014 | 0,44 ± 0,32 | 0,17 | Без знач. изменение |
| 9 / L | 0,344 | 0,012 | 1,07 ± 0,29 | 0,0009 | Signif. увеличение |
| 9 / R | 0,421 | 0,011 | 1,33 ± 0,35 | 0,0008 | Signif.увеличение |
| 10 / л | 0,96 | 0,008 | 0,43 ± 0,05 | <0,0001 | Signif. увеличение |
| 10 / R | 0,854 | 0,008 | 0,41 ± 0,04 | <0,0001 | Signif. увеличение |
Ответ оптической плотности макулярного пигмента (MPOD) на добавку в левом глазу субъекта № 1 (темные кружки) и в правом глазу субъекта № 6 (светлые кружки).Прием добавок начался в нулевой день.
Результаты MPOD для группы плацебо показаны в том же формате в таблице. У одного человека наблюдалось значительное снижение MPOD на обоих глазах, а у другого — только на один глаз. Никаких значительных изменений MPOD не наблюдалось ни в одном глазу другого субъекта в группе плацебо.
Таблица 3
Ответ оптической плотности макулярного пигмента (MPOD) на плацебо. См. Подробности в таблице 2.
| Субъект / глаз | MPOD до AU | SD до AU | Скорость изменения MPOD ± SE, mAU / день | p | Значимость скорости изменения |
| 0.244 | 0,034 | 0,01 ± 0,43 | 0,99 | Без знач. изменение | |
| 11 / R | 0,246 | 0,055 | -0,20 ± 0,26 | 0,46 | Без знач. изменение |
| 12 / L | 0,570 | 0,043 | -0,99 ± 0,23 | 0,0001 | Signif. уменьшение |
| 12 / R | 0,551 | 0,105 | -0,10 ± 0,22 | 0,65 | Без знач.изменение |
| 13 / L | 0,473 | 0,065 | 0,00 ± 0,30 | 0,99 | Без знач. изменение |
| 13 / R | 0,397 | 0,077 | 0,66 ± 0,41 | 0,12 | Без знач. изменение |
| 14 / L | 0,825 | 0,067 | 0,03 ± 0,94 | 0,98 | Без знач. сдача |
| 14 / R | 0,922 | 0.186 | 0,36 ± 0,33 | 0,30 | Без знач. изменение |
| 15 / L | 0,328 | 0,050 | 0,14 ± 0,22 | 0,53 | Без знач. изменение |
| 15 / R | 0,334 | 0,058 | -0,11 ± 0,24 | 0,66 | Без знач. изменение |
| 16 / L | 0,492 | 0,048 | -0,72 ± 0,16 | <0,0001 | Signif.уменьшение |
| 16 / R | 0,527 | 0,022 | -0,60 ± 0,18 | 0,0020 | Signif. уменьшение |
| 17 / L | 0,579 | 0,036 | -0,64 ± 0,87 | 0,48 | Без знач. изменение |
| 17 / R | 0,482 | 0,054 | -0,32 ± 0,49 | 0,52 | Без знач. изменить |
| 18 / L | 0,628 | 0.041 | -0,28 ± 0,30 | 0,36 | Без знач. изменение |
| 18 / R | 0,625 | 0,057 | 0,43 ± 0,28 | 0,13 | Без знач. изменение |
| 19 / L | 0,739 | 0,143 | -0,44 ± 0,33 | 0,19 | Без знач. изменение |
| 19 / R | 0,693 | 0,076 | -0,30 ± 0,36 | 0,41 | Без знач.change |
Обсуждение
Данные субъектов A и B впервые указывают на то, что MZ, хотя и не является важным компонентом нормальной диеты, тем не менее всасывается в сыворотку. Испытуемые не соблюдали контролируемую диету, и этим можно было объяснить, по крайней мере частично, очень разные ответы, которые наблюдались. L, Z и MZ в добавке были в соотношении 1,0: 0,3: 2,7, в то время как в сыворотке увеличение этих каротиноидов в результате приема было в соотношении 1.0: 4,3: 4,4 для субъекта A и 1,0: 0,43: 0,47 для субъекта B. Таким образом, сывороточные ответы для этих двух субъектов не выявили общей картины, и относительная эффективность, с которой L, Z и MZ всасываются в сыворотку, не может быть оценена. предложили без пользы более крупное исследование с участием большего числа субъектов и подробного знания их индивидуальных диет. Данные анализа обращенно-фазовой ВЭЖХ сыворотки L и комбинированного Z + MZ у других 10 субъектов в группе добавок в достаточной степени соответствовали ожиданиям, основанным на составе добавки.В приложении соотношение L: Z + MZ составляло 1,0: 3,0. В сыворотке, усредненной для всех 10 субъектов, увеличение L и Z + MZ в результате приема добавок было в соотношении 1,0: 2,2. Наблюдалась небольшая тенденция к большему увеличению L и Z + MZ у субъектов, у которых уровни этих каротиноидов перед добавлением были ниже, но не на уровне статистической значимости.
Величины среднего увеличения L и Z + MZ у субъектов, получавших добавку, были довольно скромными по сравнению с теми, о которых сообщалось у субъектов, получавших сравнимые количества только L или только Z.Например, сообщалось о среднем ~ 3-кратном увеличении сывороточного L у субъектов, принимавших 5 мг L в день в течение 6 месяцев [32]. В другом 6-месячном исследовании субъекты получали суточную дозу 10 мг L, 10 мг Z или 10 мг L в сочетании с 10 мг Z [33]. Среднее увеличение L в сыворотке было ~ 7 раз для группы L, среднее увеличение Z в сыворотке было ~ 27 раз для группы Z, а среднее увеличение L и Z в сыворотке было ~ 4 и 14 раз соответственно для группа, получающая как L, так и Z. Вероятным фактором, влияющим на биодоступность каротиноида, является состав добавки.Имеются также некоторые свидетельства конкуренции каротиноидов за их захват сывороткой при введении в комбинации [34]. Оба эти фактора могли повлиять на данное исследование.
В соответствии с другими исследованиями L- и Z-добавок [30,31], ответы MP варьировались с точки зрения увеличения MPOD среди 10 субъектов в группе добавок. У четырех субъектов наблюдались значительные темпы увеличения MPOD на обоих глазах, а у 4 других наблюдались значительные темпы увеличения только на одном глазу.Средняя частота ± стандартное отклонение для группы составила 0,59 ± 0,79 мАЕ / день. Для группы плацебо не было значительных темпов увеличения, и среднее значение ± стандартное отклонение составило -0,17 ± 0,42 мАЕ / день. Согласно двустороннему t-критерию средние значения для 2 групп значительно различались (p <0,002). Результаты, полученные для группы добавок, можно сравнить с нашими более ранними исследованиями, в которых мы сообщили о результатах, в среднем 1,13 ± 0,10 мАЕ / день для исследования 30 мг / день L с использованием 2 субъектов [31] и 0,48 ± 0,16 мАЕ / день для 30 человек. исследование Z в мг / день, снова с участием 2 человек [30].В пересчете на миллиграмм средняя скорость увеличения MPOD, полученная в текущем исследовании, очень похожа на полученную в исследовании L и примерно вдвое превышает значение, полученное в исследовании Z. Однако суждение при проведении этих сравнений должно быть предварительным, исходя из небольшого числа субъектов в более ранних исследованиях.
Для этого небольшого исследования мы не обнаружили корреляции между скоростью увеличения ОПМР у субъектов, принимавших добавки, и ни концентрацией плато (с 6 недели до конца приема), ни изменением концентрации L или Z + MZ.Однако, когда мы ограничили наш анализ теми испытуемыми, которые были более опытны в HFP, судя по разбросу их данных, возникла интересная тенденция. Для субъектов, у которых скорость изменения ОПРОД сопровождалась стандартной ошибкой ≤ 0,21 мАЕ / день, эти показатели положительно коррелировали с увеличением сывороточного Z + MZ (R 2 = 0,31), хотя и не полностью достигали уровня статистических данных. значимость (р = 0,078). Следовательно, возможно, что ответы МП, которые мы наблюдали у наших испытуемых, были в значительной степени связаны с присутствием основного компонента добавки, MZ, который был в ~ 10 раз больше, чем Z.Однако окончательный вывод должен дождаться тестирования добавки, содержащей только MZ.
Субъект № 5 в группе добавок показал аномальный результат, состоящий из значительных темпов увеличения и уменьшения MPOD в левом и правом глазах соответственно. Если предположить, что этот субъект предоставил надежные данные, уменьшение, наблюдаемое в правом глазу, могло быть связано с более быстрым нарастанием МП при эксцентриситете 8 ° по сравнению с фовеа, как обсуждалось ранее. Значительное снижение MPOD в группе плацебо могло быть связано с изменением диеты во время периода исследования.
Данные текущего и предыдущих исследований ограничены размером выборки, что затрудняет аргументацию в пользу любого из трех каротиноидов, L, Z или MZ, как предпочтительного средства повышения плотности MP. С другой стороны, мы знаем, что значительная часть L в центральной сетчатке преобразуется в MZ. В центре сетчатки отношение MZ к L самое высокое и приближается к 1: 1. Это наблюдение предполагает, что эффективность преобразования L в MZ обычно ниже 50%. Кроме того, возможно, что процесс преобразования может включать в себя чистое разрушение каротиноида.В качестве доказательства данные вскрытия глаз показывают, что соотношение (L + MZ): Z изменяется по всей сетчатке от ~ 2: 1 в центре, где происходит большая часть конверсии, до ~ 3: 1 на периферии [7]. . Таким образом, может быть преимущество в обеспечении MZ в добавке за счет L, если цель состоит в том, чтобы повысить общий уровень зеаксантина и потенциально улучшить степень защиты сетчатки.
Заключение
Наше исследование показывает, что добавка, содержащая макулярные каротиноиды, L, Z и MZ, но в основном MZ, эффективна для повышения MPOD у большинства пациентов.Повышение MPOD может быть эффективным средством защиты стареющего населения от AMD.
Конкурирующие интересы
Трое из авторов, RAB, JTL и ANH, имеют собственный интерес в использовании MZ для повышения MPOD и лечения макулярных заболеваний.
Вклад авторов
RAB, JTL и ANH выступили инициаторами исследования. ANH предоставила капсулы MZ для исследования. Компания RAB разработала мерцающий фотометр, обучила испытуемых его использованию и проанализировала данные. JTL контролировала анализ сыворотки крови и анализировала данные.YC и FA-C провели анализ образцов сыворотки крови методом ВЭЖХ. RAB и JTL подготовили рукопись.
Благодарности
Данное исследование было поддержано грантом Фонда Говарда, Кембридж, Великобритания. Капсулы были предоставлены Quantum Nutritionals, Walled Lake MI 48390 и содержали продукт, произведенный Industrial Orgánica SA, Монтеррей, Мексика.
Ссылки
- Bone RA, Landrum JT, Fernandez L, Tarsis SL. Анализ макулярного пигмента с помощью ВЭЖХ: распределение по сетчатке и возрастное исследование.Инвестируйте Ophthalmol Vis Sci. 1988; 29: 843–849. [PubMed] [Google Scholar]
- Bone RA, Landrum JT, Tarsis SL. Предварительная идентификация макулярного пигмента человека. Vision Res. 1985; 25: 1531–1535. DOI: 10.1016 / 0042-6989 (85)
-3. [PubMed] [CrossRef] [Google Scholar]
- Handelman GJ, Dratz EA, Reay CC, van Kuijk FJGM. Каротиноиды в желтом пятне человека и всей сетчатке глаза. Инвестируйте Ophthalmol Vis Sci. 1988. 29: 850–855. [PubMed] [Google Scholar]
- Bone RA, Landrum JT, Hime GW, Cains A, Zamor J.Стереохимия макулярных каротиноидов человека. Инвестируйте Ophthalmol Vis Sci. 1993; 34: 2033–2040. [PubMed] [Google Scholar]
- Müller H. Die tägliche Aufnahme von Carotinoiden (Carotine und Xanthophylle) aus Gesamtnahrungsproben und die Carotinoidgehalte ausgewählter Gemüse- und Obstarten. Zeitschrift für Ernährungswissenschaft. 1996; 35: 45–50. DOI: 10.1007 / BF01612027. [PubMed] [CrossRef] [Google Scholar]
- Torres JA. Личное общение. 2007.
- Bone RA, Landrum JT, Friedes LM, Gomez CM, Kilburn MD, Menendez E, Vidal I., Wang W.Распределение стереоизомеров лютеина и зеаксантина в сетчатке человека. Exp Eye Res. 1997. 64: 211–218. DOI: 10.1006 / exer.1996.0210. [PubMed] [CrossRef] [Google Scholar]
- Ландрам Дж. Т., Боун Р. А., Мур Л. Л., Гомес К. М.. Анализ распределения зеаксантина в индивидуальных сетчатках человека. В: Пакер Л., редактор. Методы Энзимол. Vol. 299. Сан-Диего, Academic Press; 1999. С. 457–467. [PubMed] [Google Scholar]
- Джонсон Э. Дж., Нойрингер М., Рассел Р. М., Шальч В., Сноддерли Д. М.. Манипуляции с питанием сетчатки приматов, III Влияние добавок лютеина или зеаксантина на жировую ткань и сетчатку обезьян без ксантофилла.Инвестируйте Ophthalmol Vis Sci. 2005; 46: 692–702. DOI: 10.1167 / iovs.02-1192. [PubMed] [CrossRef] [Google Scholar]
- Landrum JT, Bone RA. Механические доказательства глазных болезней и каротиноидов. В кн .: Кринский Н.И., редактор. Каротиноиды в здоровье и болезнях. Нью-Йорк, Марсель Деккер, Инк; 2004. С. 445–472. [Google Scholar]
- Goralczyk R, Buser S, Bausch J, Bee W., Zühlke U, Barker FM. Возникновение двулучепреломляющих включений сетчатки у Cynomolgus обезьян после высоких доз кантаксантина. Инвестируйте Ophthalmol Vis Sci.1997; 38: 741–752. [PubMed] [Google Scholar]
- Thurmann PA, Schalch W., Aebischer JC, Tenter U, Cohn W. Кинетика лютеина, зеаксантина и 3-дегидро-лютеина в плазме после многократных пероральных доз лютеиновой добавки. Американский журнал клинического питания. 2005; 82: 88–97. [PubMed] [Google Scholar]
- Хартманн Д., Турманн П.А., Спитцер В., Скалч В., Маннер Б., Кон В. Кинетика плазмы зеаксантина и 3′-дегидро-лютеина после многократных пероральных доз синтетического зеаксантина. Американский журнал клинического питания.2004. 79: 410–417. [PubMed] [Google Scholar]
- Битти С., Ко Х. Х., Фил М., Хенсон Д., Бултон М. Роль оксидантного стресса в патогенезе возрастной дегенерации желтого пятна. Surv Ophthalmol. 2000. 45: 115–134. DOI: 10.1016 / S0039-6257 (00) 00140-5. [PubMed] [CrossRef] [Google Scholar]
- Сноддерли Д.М., Аурон Д.Д., Делори ФК. Макулярный пигмент. II. Пространственное распределение сетчатки приматов. Инвестируйте Ophthalmol Vis Sci. 1984. 25: 674–685. [PubMed] [Google Scholar]
- Рапп Л.М., Сима С.С., Чой Дж. Х.Концентрации лютеина и зеаксантина в мембранах наружных сегментов палочек перифовеальной и периферической сетчатки человека. Инвестируйте Ophthalmol Vis Sci. 2000. 41: 1200–1209. [PubMed] [Google Scholar]
- Sommerburg OG, Siems WG, Hurst JS, Lewis JW, Kliger DS, van Kuijk FJGM. Лютеин и зеаксантин связаны с фоторецепторами сетчатки глаза человека. Curr Eye Res. 1999; 19: 491–495. DOI: 10.1076 / ceyr.19.6.491.5276. [PubMed] [CrossRef] [Google Scholar]
- Ким С.Р., Наканиши К., Итагаки Ю., Воробей-младший.Фотоокисление A2-PE, флуорофора внешнего сегмента фоторецептора, и защита лютеином и зеаксантином. Экспериментальные исследования глаз. 2006; 82: 828–839. DOI: 10.1016 / j.exer.2005.10.004. [PubMed] [CrossRef] [Google Scholar]
- Кантрелл А., МакГарви Д.Д., Траскотт Т.Г., Ранкан Ф., Бом Ф. Тушение синглетного кислорода с помощью пищевых каротиноидов в модельной мембранной среде. Arch Biochem Biophys. 2003; 412: 47–54. DOI: 10.1016 / S0003-9861 (03) 00014-6. [PubMed] [CrossRef] [Google Scholar]
- Bhosale P, Bernstein PS.Синергетические эффекты зеаксантина и его связывающего белка в предотвращении окисления липидной мембраны. Biochim Biophys Acta. 2005; 1740: 116–121. [PubMed] [Google Scholar]
- Bone RA, Landrum JT. Макулярный пигмент в мембранах из волокон Генле — модель для кистей Хайдингера. Vision Res. 1984. 24: 103–108. DOI: 10.1016 / 0042-6989 (84)
-4. [PubMed] [CrossRef] [Google Scholar]
- Bone RA, Landrum JT, Cains A. Спектры оптической плотности макулярного пигмента in vivo и in vitro. Vision Res.1992. 32: 105–110. DOI: 10.1016 / 0042-6989 (92)
-3. [PubMed] [CrossRef] [Google Scholar]
- Sujak A, Okulski W, Gruszecki WI. Организация пигментов ксантофилла лютеина и зеаксантина в липидных мембранах, образованных дипальмитоилфосфатидилхолином. Biochim Biophys Acta. 2000; 1509: 255–263. DOI: 10.1016 / S0005-2736 (00) 00299-6. [PubMed] [CrossRef] [Google Scholar]
- Gene Logic Inc: номер испытания (1567-04370). Тринадцатинедельная пероральная (через желудочный зонд) токсичность мезозеаксантина у крыс Han Wister с 4-недельным выздоровлением.610 Professional Drive, Гейтерсбург, Мэриленд 20879. 2006.
- Проект № 26471-0-4090OECD. Covance Laboratories, 9200 Leesburh Pike, Вена, VA22182-1699. 2006.
- Bone RA, Landrum JT. Гетерохроматическая фликкер-фотометрия. Arch Biochem Biophys. 2004. 430: 137–142. DOI: 10.1016 / j.abb.2004.04.003. [PubMed] [CrossRef] [Google Scholar]
- Bone RA, Landrum JT, Gibert JC. Макулярный пигмент и краевая гипотеза фликкер-фотометрии. Исследование зрения. 2004; 44: 3045–3051. DOI: 10.1016 / j.visres.2004.07.008. [PubMed] [CrossRef] [Google Scholar]
- Родригес-Кармона М., Квансакул Дж., Харлоу Дж. А., Копке В., Шальч В., Барбур Дж. Л. Влияние добавок лютеина и / или зеаксантина на плотность макулярного пигмента человека и цветовое зрение. Офтальмологическая и физиологическая оптика. 2006. 26: 137–147. DOI: 10.1111 / j.1475-1313.2006.00386.x. [PubMed] [CrossRef] [Google Scholar]
- Berendschot TTJM, ван Норрен Д. О возрастной зависимости оптической плотности макулярного пигмента.Экспериментальные исследования глаз. 2005. 81: 602–609. DOI: 10.1016 / j.exer.2005.03.019. [PubMed] [CrossRef] [Google Scholar]
- Bone RA, Landrum JT, Guerra L., H., Ruiz CA. Пищевые добавки с лютеином и зеаксантином повышают плотность макулярных пигментов и концентрацию этих каротиноидов в сыворотке крови. J Nutr. 2003; 133: 992–998. [PubMed] [Google Scholar]
- Ландрам Дж. Т., Боун Р. А., Джоа Х., Килберн М. Д., Мур Л. Л., Спраг К. Э. Годовое исследование макулярного пигмента: эффект 140 дней приема лютеиновой добавки.Exp Eye Res. 1997. 65: 57–62. DOI: 10.1006 / exer.1997.0309. [PubMed] [CrossRef] [Google Scholar]
- Khachik F, de Moura FF, Chew EY, Douglass LW, Ferris III FL, Kim J, Thompson DJS. Влияние добавок лютеина и зеаксантина на метаболиты этих каротиноидов в сыворотке крови людей в возрасте 60 лет и старше. Инвестируйте Ophthalmol Vis Sci. 2006; 47: 5234–5242. DOI: 10.1167 / iovs.06-0504. [PubMed] [CrossRef] [Google Scholar]
- Шальч В., Кон В., Баркер Ф.М., Кёпке В., Меллерио Дж., Берд А.С., Робсон А.Г., Фитцке Ф.Ф., Ван Куийк FJGM.Накопление ксантофилла в сетчатке человека во время приема лютеина или зеаксантина — исследование LUXEA (LUtein Xanthophyll Eye Contemporary). Arch Biochem Biophys. 2007. 458: 128–135. DOI: 10.1016 / j.abb.2006.09.032. [PubMed] [CrossRef] [Google Scholar]
- Kostic D, White WS, Olson JA. Кишечная абсорбция, клиренс сыворотки и взаимодействие между лютеином и бета-каротином при введении взрослым людям в отдельных или комбинированных пероральных дозах. Am J Clin Nutr. 1995; 62: 604–610. [PubMed] [Google Scholar]
Реакция пигмента желтого пятна на добавку, содержащую мезозеаксантин, лютеин и зеаксантин
Nutr Metab (Лондон).2007; 4: 12.
, 1 , 2 , 2 , 3 и 2
Ричард А Боун
1 Департамент физики, Международный университет Флориды, 11200 SW 8th Street, Майами , FL 33199, США
John T. Landrum
2 Департамент химии и биохимии, Международный университет Флориды, 11200 SW 8th Street, Майами, Флорида 33199, США
Yisi Cao
2 Департамент химии и биохимии , Международный университет Флориды, 11200 SW 8th Street, Майами, Флорида 33199, США
Алан Н. Ховард
3 Даунинг-колледж, Кембриджский университет, Кембридж CB2 1DQ, Великобритания
Франческа Альварес-Кальдерон
2 Департамент химии и биохимии, Международный университет Флориды, 11200 SW 8th Street, Майами, Флорида 33199, США
1 Физический факультет Международного университета Флориды, 11200 SW 8th Street, Майами, Флорида 33199, США
2 Департамент химии и биохимии, Международный университет Флориды, 11200 SW 8th Street, Майами, Флорида 33199, США
3 Даунинг-колледж, Кембриджский университет, Кембридж CB2 1DQ, UK
Автор, ответственный за переписку.
Поступило 9 февраля 2007 г .; Принято 11 мая 2007 г.
Copyright © 2007 Bone et al; лицензиат BioMed Central Ltd.
Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License (http://creativecommons.org/licenses/by/2.0), которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе. при условии правильного цитирования оригинала.
Эта статья цитируется в других статьях в PMC.
Abstract
Предпосылки
Возрастная дегенерация желтого пятна (AMD) — это заболевание с множеством факторов риска, многие из которых связаны с окислительным стрессом.Считается, что макулярный пигмент с его антиоксидантными и светозащитными свойствами защищает от AMD. Результатом стало появление диетических добавок, содержащих макулярные каротиноиды, лютеин и зеаксантин. Совсем недавно на рынке появилась добавка, содержащая, кроме того, третий главный каротиноид макулярного пигмента, мезозеаксантин. Целью исследования было определить эффективность такой добавки в повышении плотности макулярного пигмента у людей.
Методы
Было проведено 120-дневное исследование добавок, в котором 10 субъектов получали гелевые капсулы, которые обеспечивали 20 мг / день преимущественно мезозеаксантина с меньшими количествами лютеина и зеаксантина.Второй группе из 9 субъектов давали гелевые колпачки, содержащие плацебо, в течение того же 120-дневного периода. До и во время периода приема добавок образцы сыворотки крови анализировали с помощью высокоэффективной жидкостной хроматографии на содержание каротиноидов. Точно так же оптическую плотность макулярного пигмента измеряли с помощью фотометрии гетерохроматического мерцания. Различия в ответе между группами добавок и плацебо были проверены на значимость с использованием t-критерия Стьюдента.
Результаты
Во время приема каротиноидов образцы крови показали присутствие всех трех каротиноидов.Оптическая плотность макулярного пигмента, измеренная при 460 нм, увеличивалась в среднем на 0,59 ± 0,79 миллиабсорбционных единиц / день у 10 субъектов, получавших добавки. Это значительно отличалось от группы плацебо (9 субъектов), для которой средняя скорость составляла -0,17 ± 0,42 миллиабсорбционных единиц / день.
Заключение
Мы впервые показали, что мезозеаксантин всасывается в сыворотку после приема внутрь. Данные показывают, что добавка, содержащая преимущественно мезозеаксантин, обычно эффективна для повышения плотности макулярного пигмента и может оказаться полезным дополнением к защите от AMD.
Предпосылки
Макулярный пигмент (MP), впервые идентифицированный в середине 1980-х как комбинация лютеина и зеаксантина [1-3], впоследствии было показано, что он характеризуется наличием определенных стереоизомеров этих двух каротиноидов [4] . Хотя лютеин (L) присутствует в виде одного стереоизомера, [(3R, 3’R, 6’R) -β, ε-каротин-3,3′-диол], зеаксантин встречается в основном в виде смеси [(3R, 3’R) -β, β-каротин-3,3′-диол] и [(3R, 3’S) -β, β-каротин-3,3′-диол] с гораздо меньшим количеством [(3S, 3’S) -β, β-каротин-3,3′-диол].Первые два преобладающих изомера зеаксантина называются зеаксантином (Z) и мезо -зеаксантин (MZ) соответственно. Из этих каротиноидов только L и Z обычно потребляются в соотношении примерно семь к одному [5], тогда как MZ является необычным и, следовательно, редким изомером в рационе. MZ присутствует в значительных количествах в промышленных цыплятах и яйцах в Мексике, где его обычно добавляют в корм для достижения желаемой окраски этих продуктов. С этой целью ежегодно продается около 3000 кг МЗ [6].В популяции США L и Z в изобилии присутствуют в сыворотке, но MZ обычно не может быть обнаружен в сыворотке. Это наблюдение привело к гипотезе, что MZ образуется в сетчатке как продукт преобразования L [4,7]. In vitro превращение L в MZ легко достигается в реакции, катализируемой основанием [4], и это является основой промышленного процесса его синтеза и использования в кормах для домашней птицы. Гипотеза конверсии подтверждается распределением отдельных каротиноидов в сетчатке. В центральных 10 ° больше MZ и меньше L относительно Z, тогда как на периферии (эксцентриситет> 35 °) ситуация обратная [8].Это говорит о том, что постулируемый процесс преобразования работает с большей эффективностью в фовеальном центре по сравнению с периферической сетчаткой. Обезьяны, выращенные на бескаротиноидной диете, а затем добавленные только L, впоследствии показали как L, так и MZ в MP. Те, к которым добавлялся Z, не показали MZ в их MP, только Z. Эти данные являются убедительным доказательством в поддержку гипотезы L-to-MZ конверсии [9].
Абсолютная конфигурация гидроксильных групп, расположенных на 3 и 3 ‘атомах углерода каротиноидных концевых групп, идентична в молекулах L и MZ.Таким образом, преобразование L в MZ должно включать только сдвиг одной двойной углерод-углеродной связи в ε-кольце L, тем самым увеличивая конъюгацию (см. Рис.). Альтернативный механизм образования MZ предполагает, что метаболит, дегидролютеин, вызывает MZ посредством ферментативного пути восстановления [10]. Действительно, кето-каротиноид кантаксантин действительно подвергается редукции в сетчатке человека и приматов, что подтверждает эту возможность [11]. Однако в плазме дегидролютеин образуется как из L [12], так и из Z [13].Если эти процессы также происходят в глазу и MZ образуется из этого метаболита, он должен был быть обнаружен у обезьян, принимающих Z- и L-добавки. Какой бы путь ни был задействован, он, вероятно, будет включать ферментативный контроль, чтобы соответствовать наблюдениям, что доля MZ в сетчатке зависит от местоположения.
Структуры основных компонентов пигмента желтого пятна.
На этом этапе мы можем порассуждать о возможных преимуществах, которые такое преобразование может дать глазу.Было высказано предположение, что МП защищает макулу двумя процессами [14]. Его присутствие в аксонах фоторецепторов [15] вместе с диапазоном спектрального поглощения (~ 400-500 нм) обеспечивает MP способность защищать задние ткани, такие как внешние сегменты фоторецепторов и RPE, от актинического синего света. Кроме того, его присутствие во внешних сегментах и RPE [16,17] может смягчить фотоокислительное повреждение, вызванное синим светом [18], благодаря его антиоксидантным свойствам и улавливанию свободных радикалов.Эксперименты in vitro показывают, что Z является более сильным антиоксидантом, чем L [18]. В одном исследовании тушение синглетного кислорода Z было примерно в два раза эффективнее тушения L [19]. Причина, по-видимому, связана, по крайней мере частично, с расширенной конъюгацией Z по сравнению с L. MZ разделяет эту электронную функцию с Z и, следовательно, должен обладать тем же антиоксидантным потенциалом, что и Z. Также сообщалось, что в сочетании с зеаксантином Связывающий белок, пи-изоформа глутатион-S-трансферазы, MZ обеспечивает немного лучшую защиту от окисления липидной мембраны, чем Z [20].Без связывающего белка ситуация обратная. Таким образом, для макулы может быть выгодно увеличить отношение общего зеаксантина (Z + MZ) к L. В сыворотке отношение Z к L составляет примерно 1: 4. Второстепенным преимуществом может быть скромный, но значительный сдвиг в сторону более длинных волн Z-хромофора по сравнению с L, что приводит к увеличению диапазона длин волн экранирования синего света по сравнению с тем, который был бы обеспечен, если бы МП состоял преимущественно из L. Третье преимущество может возникнуть из фактического размещения молекул каротиноидов.Наблюдения показывают, что L и Z могут присутствовать внутри клеточных мембран [21,22]. Z, по-видимому, охватывает мембрану в перпендикулярной ориентации, тогда как L имеет тенденцию лежать близко к поверхности мембраны [23]. Эти конфигурации размещают защитные участки окисления Z ближе к легко окисляемым цепям полиненасыщенных жирных кислот внутри мембраны.
Целью исследования было изучить способность проглоченного MZ в сочетании с L и Z увеличивать оптическую плотность MP.Исследование было мотивировано недавним появлением диетических добавок, содержащих значительные количества MZ в дополнение к L и Z.
Методы
Субъекты
Восемь мужчин и 2 женщины были набраны из университетского сообщества для исследования добавок. Их возраст колебался от 21 до 58 лет (в среднем 30,5 ± 10,9 года). Для более детального анализа каротиноидов сыворотки крови были привлечены еще двое испытуемых. Их возраст был 51 и 61 год. Впоследствии для получения плацебо была набрана группа сравнения (плацебо стало доступно только после того, как исследование было начато).Группа состояла из 5 мужчин и 4 женщин в возрасте от 19 до 31 года (в среднем 22,1 ± 3,6 года). Хотя наше исследование не соответствовало стандартному двойному слепому плацебо-контролируемому исследованию, в котором субъектов случайным образом распределяли в группы лечения и плацебо, оно действительно предлагало возможность отличить изменения MP, вызванные добавками, от изменений, которые могли произойти при более длительной терапии. случайная основа. Следует также отметить, что исследование проводилось в Южной Флориде, где диета, как правило, не является сезонной из-за постоянной доступности обычно потребляемых фруктов и овощей.Поэтому мы считаем, что отказ от одновременного использования групп добавок и плацебо не приведет к искажению результатов. Кроме того, хотя разница в среднем возрасте групп была просто значительной (p <0,05), мы не знаем о каких-либо возрастных различиях в способности людей изменять свой МП с помощью добавок.
Критериями исключения для потенциальных субъектов были: 1) курение или курение в течение предыдущих 12 месяцев, 2) любая визуальная патология, 3) неспособность во время практических занятий обеспечить приемлемые измерения оптической плотности MP (MPOD) и 4) использование пероральных добавок, содержащих значительную (> 0.25 мг / день) количества L и / или Z. Помимо последнего ограничения, субъекты могли свободно следовать своей обычной диете. Субъекты подписали форму информированного согласия в соответствии с требованиями Институционального наблюдательного совета, и исследование соответствовало принципам Хельсинкской декларации. Каждый испытуемый прошел обучение гетерохроматической фликкер-фотометрии, методу, используемому для определения MPOD. Официальное включение в исследование последовало за периодом практики, в течение которого от субъектов требовалось достичь приемлемых измерений MPOD (стандартная ошибка среднего значения на основе набора из 5 центральных и 5 периферийных настроек ≤ 0.020 единиц поглощения. См. ниже.).
Добавка
Субъектам в группе добавок дали запасы гелевых капсул, содержащих неэтерифицированные каротиноиды: 14,9 мг MZ, 5,5 мг L и 1,4 мг Z в виде суспензии в соевом масле, и проинформировали о содержимом. Состав гелевых крышек определяли с помощью ВЭЖХ (см. Ниже). Смесь каротиноидов была произведена Industrial Orgánica SA (Монтеррей, Мексика) путем катализируемой основанием реакции каротиноидов (~ 93% L, 7% Z), экстрагированных из бархатцев (Targetes sp.). Безопасность MZ была подтверждена в недавнем исследовании токсичности. На основании исследования уровень отсутствия наблюдаемых побочных эффектов (NOAEL) MZ у крыс составлял> 200 мг / кг / день [24]. Продукт также был протестирован на мутагенность с помощью теста Эймса с отрицательными результатами [25].
Субъектам в группе плацебо давали гелевые колпачки, содержащие только небольшое количество растительного масла. В отличие от группы приема добавок, группа плацебо была слепой, получив информацию о том, что гелевые колпачки содержат либо каротиноиды, либо плацебо.Субъекты в обеих группах были проинструктированы принимать гелевые капсулы ежедневно во время еды в течение 120 дней.
MPOD измерений
MPOD было определено для каждого объекта методом гетерохроматической фликкер-фотометрии (HFP) [26]. Испытуемые наблюдали стимул под углом 1,5 °, который чередовался между 460 и 540 нм, и регулировали интенсивность первого до минимума мерцания. Пять повторных корректировок были сделаны при просмотре стимула в центре (частота 30 Гц), и 5 повторных эталонных корректировок были сделаны при просмотре стимула периферически с эксцентриситетом 8 ° (частота 22 Гц).После каждой настройки клиновому фильтру, регулирующему интенсивность 460 нм, автоматически давалось случайное смещение. Логарифмическое соотношение средних значений двух наборов измерений интенсивности равно разнице в MPOD при 460 нм между фовеа и периферическим референсным участком. Предполагая, что MPOD незначительно на периферии, процедура по существу обеспечивает средний MPOD в пределах 1,5 ° центрального [27]. Однако это может быть не так для субъектов, получающих высокие дозы каротиноидов. Родригес-Кармона и др.обнаружили, что после приема 20 мг L и / или Z в день, наклон распределения MPOD оставался конечным даже до эксцентриситета 8 ° [28], что означает, что нельзя предполагать, что MPOD равняется нулю в этом месте. Таким образом, центральный MPOD может быть немного недооценен HFP в конце исследования добавок, даже если в процедуре используется эталонный участок до 8 °. Кроме того, в парафовеа (эксцентриситет 5,5 °) MPOD может, согласно одному исследованию [29], увеличиваться с возрастом, и это по той же причине может вызывать очевидное снижение центрального MPOD с возрастом при использовании 5.5 ° или, возможно, 8 °, ориентир.
Измерения MPOD проводились по крайней мере 4 раза до приема добавок, затем дважды в неделю в течение 120-дневного периода приема добавок и в течение 4-недельного периода после приема добавок. (Делались поправки на праздники и т. Д., Что приводило к случайным пропускам в данных.) Следует отметить, что эти измерения представляют собой тест, проводимый самостоятельно, без вмешательства оператора. Субъекты записывают каждую настройку клина, нажимая кнопку, и микропроцессор автоматически вычисляет их MPOD и соответствующую стандартную ошибку в среднем.Это эффективно устраняет любую предвзятость оператора или субъекта, которая в противном случае могла бы по-разному влиять на результаты либо группы MZ, либо группы плацебо.
Анализ каротиноидов в сыворотке
Образцы сыворотки были получены от каждого субъекта для отслеживания изменений в концентрации L и Z. Анализ проводился ассистентом, который не знал происхождения образцов сыворотки (MZ или плацебо). Два образца были взяты перед добавлением, чтобы установить исходный уровень.Во время приема добавки образцы сыворотки брали каждые 2 недели. Каротиноиды экстрагировали из сыворотки с помощью методов, которые были описаны ранее [30], и включали добавление до экстракции известного количества внутреннего стандарта (монопентиллютеинового эфира) на каждый миллилитр сыворотки. ВЭЖХ экстрактов проводили на обращенно-фазовой системе с использованием колонки Ultracarb ODS 3 мкм 250 × 4,6 мм (Phenomenex, Torrance CA). Подвижная фаза представляла собой ацетонитрил / метанол (85:15) при 1 мл / мин с 0.Добавлен 1% триэтиламин для ингибирования разложения каротиноидов во время элюирования.
Эта система способна производить базовое разделение L и объединенных стереоизомеров зеаксантина, но не отделяет Z от MZ. Чтобы определить, всасывается ли MZ в сыворотку вместе с L и Z, образцы сыворотки были взяты у 2 дополнительных субъектов, A и B, до приема и после 6 недель приема добавок. Каротиноиды, экстрагированные из этих образцов, анализировали с помощью ВЭЖХ на 250 × 4.Колонка Chiralpak AD диаметром 6 мм, состоящая из носителя из диоксида кремния, модифицированного хиральным полисахаридом (Daicel Chemical Industries, Осака, Япония), и подвижной фазы, состоящей из гексана и изопропилового спирта. Элюирование проводили при скорости потока 0,8 мл / мин, начиная с 90% гексана и 10% изопропилового спирта и увеличивая до 100% гексана в течение 55-минутного градиента. Стереоизомеры идентифицировали путем сравнения с порядком элюирования известных стандартов.
Те же системы использовались для анализа каротиноидов в добавке.
Результаты
Присутствие в сыворотке MZ в дополнение к L и Z, полученное в результате приема добавок, было подтверждено у двух субъектов, A и B, которые участвовали в этой части исследования. Перед добавлением сывороточные концентрации L, Z и MZ составляли 22,9, 4,4 и 0,0 нмоль / дл и 14,8, 2,1 и 0,0 нмоль / дл для субъектов A и B соответственно. После 6 недель приема эти значения составили 23,9, 8,7 и 4,4 нмоль / дл для субъекта A и 45,4, 15,4 и 14,5 нмоль / дл для субъекта B.
Для остальных 10 субъектов в исследовании добавок (субъекты № 1–10) мы определили увеличение L и комбинированного Z + MZ в сыворотке путем усреднения значений каждого субъекта до приема добавок, а также значений, полученных за неделю. 6 до конца периода приема добавок. На последнее среднее значение не повлияло повышение концентрации каротиноидов в сыворотке, которое обычно происходит на ранней стадии приема добавок [31]. Результаты представлены в таблице. До приема добавок средняя концентрация для 10 субъектов составляла 30.5 ± 12,5 (диапазон от 16,4 до 54,2) нмоль / дл для L и 9,7 ± 4,8 (диапазон от 3,6 до 19,0) нмоль / дл для Z + MZ. Во время приема добавок (т.е. с 6 недели до конца приема) эти значения выросли до 38,0 ± 12,0 (диапазон от 24,2 до 62,3) нмоль / дл для L и 26,4 ± 6,5 (диапазон от 13,6 до 35,0) нмоль / дл для Z + MZ. .
Таблица 1
Сывороточные ответы для 10 субъектов в группе добавок. Исходные значения и значения плато относятся к средним значениям, полученным до приема и с 6 недели до конца приема, соответственно.
| Номер субъекта | Исходная концентрация L ± стандартное отклонение (нмоль / дл) | Концентрация L на плато ± стандартное отклонение (нмоль / дл) | Исходная концентрация Z + MZ ± стандартное отклонение (нмоль / дл) | Плато Z + Концентрация MZ ± стандартное отклонение (нмоль / дл) | ||||
| 1 | 36,9 ± 17,8 | 42,4 ± 6,7 | 5,6 ± 0,4 | 25,1 ± 5,2 | ||||
| 2 | 16,4 ± 1,9 12,3 | 7,4 ± 1.6 | 34,9 ± 15,4 | |||||
| 3 | 22,6 ± 3,5 | 26,3 ± 2,7 | 8,7 ± 1,1 | 22,9 ± 3,7 | ||||
| 4 | 35,8 ± 1,8 | 36,4 5,6 | 29,6 ± 8,8 | |||||
| 5 | 18,2 ± 1,4 | 25,5 ± 5,8 | 6,1 ± 0,4 | 22,1 ± 5,7 | ||||
| 6 | 42,7 ± 0,9 | 62,3 3,0 | 35.0 ± 9,3 | |||||
| 7 | 16,7 ± 3,3 | 24,2 ± 4,9 | 7,3 ± 0,9 | 13,6 ± 3,5 | ||||
| 8 | 54,2 ± 5,2 | 45,2 ± 10,6 | 45,2 ± 10,6 | 30,4 ± 0,8 | ||||
| 9 | 34,0 ± 6,8 | 49,1 ± 4,2 | 14,0 ± 3,8 | 27,0 ± 1,2 | ||||
| 10 | 27,1 ± 3,8 | 34,6 ± 1,2 | ||||||
| Среднее ± стандартное отклонение | 30,5 ± 12,5 | 38,0 ± 12,0 | 9,7 ± 4,8 | 9014 ± 6,5 для группы |
субъекты № 11–19), средний уровень L в сыворотке пациентов изменился с 19,5 ± 6,4 (диапазон от 4,6 до 27,9) до приема плацебо до 30,7 ± 22,8 (диапазон от 6,4 до 79,1) нмоль / дл с 6 недели до конца. из «добавок». Для Z значение изменилось с 7.От 6 ± 3,4 (диапазон от 2,1 до 10,0) до 15,8 ± 15,3 (диапазон от 2,9 до 50,3) нмоль / дл. Ни одно из этих средних изменений, которое могло быть связано с изменениями в питании, не было значимым согласно двустороннему t-критерию (p = 0,14 для L, p = 0,13 для Z), равно как и какие-либо индивидуальные изменения.
Ответ на
MPOD у каждого субъекта был определен количественно путем расчета средней скорости изменения MPOD, измеренной в миллиабсорбционных единицах в день (мАЕ / день), и соответствующей стандартной ошибки (SE) для каждого глаза каждого субъекта в течение периода исследования.Данные для левого глаза субъекта № 1 (группа добавок), у которого был особенно устойчивый ответ и небольшой разброс в измерениях MPOD, и для правого глаза субъекта № 6 (группа добавок), у которого не было значительных изменений в MPOD в совокупности. с большим разбросом, показаны на рис. Кратковременная изменчивость от сеанса к сеансу типична для данных, полученных с помощью HFP, и, вероятно, является артефактом измерения. Скорость изменения MPOD для каждого глаза каждого субъекта рассчитывалась с использованием всех измерений MPOD для этого глаза с нулевого дня (начало приема добавок) и далее.Основываясь на наблюдении, что некоторые субъекты (например, субъекты 2, 4, 9) имели значительно разные начальные MPOD в их левом и правом глазах, мы рассматривали ответы в каждом глазу субъекта как независимые наблюдения. Полные результаты для группы добавок представлены в таблице. Таблица включает p-значения, основанные на двустороннем t-тесте, которые показывают, были ли измеренные скорости изменения MPOD значительно отличаться от нуля. Значительные темпы увеличения MPOD наблюдались в 12 глазах, никаких значительных изменений не произошло в 7 глазах и, что удивительно, значительное снижение произошло в одном глазу.
Таблица 2
Ответ оптической плотности макулярного пигмента (MPOD) на добавку. Данные MPOD для группы добавок, полученные до приема, вместе со скоростью изменения MPOD во время приема. Значения p показывают, значительно ли отличаются эти показатели от нуля. (AU = единица поглощения)
| Субъект / глаз | MPOD pre AU | SD pre AU | Скорость изменения MPOD ± SE, mAU / день | p | Значимость скорости изменения |
| 1 / л | 0.421 | 0,016 | 2,22 ± 0,11 | <0,0001 | Сигн. увеличение |
| 1 / R | 0,446 | 0,025 | 2,01 ± 0,06 | <0,0001 | Signif. увеличение |
| 2 / L | 0,779 | 0,015 | -0,18 ± 0,30 | 0,57 | Без знач. изменение |
| 2 / R | 0,679 | 0,016 | 0,17 ± 0,38 | 0.66 | Без знач. изменение |
| 3 / L | 0,286 | 0,018 | 0,27 ± 0,10 | 0,012 | Signif. увеличение |
| 3 / R | 0,306 | 0,011 | -0,04 ± 0,09 | 0,69 | Без знач. изменение |
| 4 / L | 0,468 | 0,019 | 1,23 ± 0,21 | <0,0001 | Signif. прибавка |
| 4 / R | 0.355 | 0,022 | 1,58 ± 0,28 | <0,0001 | Сигн. увеличение |
| 5 / л | 0,254 | 0,018 | 0,51 ± 0,14 | 0,0009 | Signif. увеличение |
| 5 / R | 0,265 | 0,027 | -0,46 ± 0,18 | 0,016 | Signif. уменьшение |
| 6 / л | 0,351 | 0,019 | -0,22 ± 0,16 | 0.18 | Без знач. изменение |
| 6 / R | 0,362 | 0,014 | 0,02 ± 0,21 | 0,94 | Без знач. изменение |
| 7 / L | 0,335 | 0,017 | 0,92 ± 0,34 | 0,015 | Signif. увеличение |
| 7 / R | 0,304 | 0,02 | -0,57 ± 0,35 | 0,12 | Без знач. изменить |
| 8 / л | 0.718 | 0,013 | 0,65 ± 0,25 | 0,016 | Знач. увеличение |
| 8 / R | 0,722 | 0,014 | 0,44 ± 0,32 | 0,17 | Без знач. изменение |
| 9 / L | 0,344 | 0,012 | 1,07 ± 0,29 | 0,0009 | Signif. увеличение |
| 9 / R | 0,421 | 0,011 | 1,33 ± 0,35 | 0,0008 | Signif.увеличение |
| 10 / л | 0,96 | 0,008 | 0,43 ± 0,05 | <0,0001 | Signif. увеличение |
| 10 / R | 0,854 | 0,008 | 0,41 ± 0,04 | <0,0001 | Signif. увеличение |
Ответ оптической плотности макулярного пигмента (MPOD) на добавку в левом глазу субъекта № 1 (темные кружки) и в правом глазу субъекта № 6 (светлые кружки).Прием добавок начался в нулевой день.
Результаты MPOD для группы плацебо показаны в том же формате в таблице. У одного человека наблюдалось значительное снижение MPOD на обоих глазах, а у другого — только на один глаз. Никаких значительных изменений MPOD не наблюдалось ни в одном глазу другого субъекта в группе плацебо.
Таблица 3
Ответ оптической плотности макулярного пигмента (MPOD) на плацебо. См. Подробности в таблице 2.
| Субъект / глаз | MPOD до AU | SD до AU | Скорость изменения MPOD ± SE, mAU / день | p | Значимость скорости изменения |
| 0.244 | 0,034 | 0,01 ± 0,43 | 0,99 | Без знач. изменение | |
| 11 / R | 0,246 | 0,055 | -0,20 ± 0,26 | 0,46 | Без знач. изменение |
| 12 / L | 0,570 | 0,043 | -0,99 ± 0,23 | 0,0001 | Signif. уменьшение |
| 12 / R | 0,551 | 0,105 | -0,10 ± 0,22 | 0,65 | Без знач.изменение |
| 13 / L | 0,473 | 0,065 | 0,00 ± 0,30 | 0,99 | Без знач. изменение |
| 13 / R | 0,397 | 0,077 | 0,66 ± 0,41 | 0,12 | Без знач. изменение |
| 14 / L | 0,825 | 0,067 | 0,03 ± 0,94 | 0,98 | Без знач. сдача |
| 14 / R | 0,922 | 0.186 | 0,36 ± 0,33 | 0,30 | Без знач. изменение |
| 15 / L | 0,328 | 0,050 | 0,14 ± 0,22 | 0,53 | Без знач. изменение |
| 15 / R | 0,334 | 0,058 | -0,11 ± 0,24 | 0,66 | Без знач. изменение |
| 16 / L | 0,492 | 0,048 | -0,72 ± 0,16 | <0,0001 | Signif.уменьшение |
| 16 / R | 0,527 | 0,022 | -0,60 ± 0,18 | 0,0020 | Signif. уменьшение |
| 17 / L | 0,579 | 0,036 | -0,64 ± 0,87 | 0,48 | Без знач. изменение |
| 17 / R | 0,482 | 0,054 | -0,32 ± 0,49 | 0,52 | Без знач. изменить |
| 18 / L | 0,628 | 0.041 | -0,28 ± 0,30 | 0,36 | Без знач. изменение |
| 18 / R | 0,625 | 0,057 | 0,43 ± 0,28 | 0,13 | Без знач. изменение |
| 19 / L | 0,739 | 0,143 | -0,44 ± 0,33 | 0,19 | Без знач. изменение |
| 19 / R | 0,693 | 0,076 | -0,30 ± 0,36 | 0,41 | Без знач.change |
Обсуждение
Данные субъектов A и B впервые указывают на то, что MZ, хотя и не является важным компонентом нормальной диеты, тем не менее всасывается в сыворотку. Испытуемые не соблюдали контролируемую диету, и этим можно было объяснить, по крайней мере частично, очень разные ответы, которые наблюдались. L, Z и MZ в добавке были в соотношении 1,0: 0,3: 2,7, в то время как в сыворотке увеличение этих каротиноидов в результате приема было в соотношении 1.0: 4,3: 4,4 для субъекта A и 1,0: 0,43: 0,47 для субъекта B. Таким образом, сывороточные ответы для этих двух субъектов не выявили общей картины, и относительная эффективность, с которой L, Z и MZ всасываются в сыворотку, не может быть оценена. предложили без пользы более крупное исследование с участием большего числа субъектов и подробного знания их индивидуальных диет. Данные анализа обращенно-фазовой ВЭЖХ сыворотки L и комбинированного Z + MZ у других 10 субъектов в группе добавок в достаточной степени соответствовали ожиданиям, основанным на составе добавки.В приложении соотношение L: Z + MZ составляло 1,0: 3,0. В сыворотке, усредненной для всех 10 субъектов, увеличение L и Z + MZ в результате приема добавок было в соотношении 1,0: 2,2. Наблюдалась небольшая тенденция к большему увеличению L и Z + MZ у субъектов, у которых уровни этих каротиноидов перед добавлением были ниже, но не на уровне статистической значимости.
Величины среднего увеличения L и Z + MZ у субъектов, получавших добавку, были довольно скромными по сравнению с теми, о которых сообщалось у субъектов, получавших сравнимые количества только L или только Z.Например, сообщалось о среднем ~ 3-кратном увеличении сывороточного L у субъектов, принимавших 5 мг L в день в течение 6 месяцев [32]. В другом 6-месячном исследовании субъекты получали суточную дозу 10 мг L, 10 мг Z или 10 мг L в сочетании с 10 мг Z [33]. Среднее увеличение L в сыворотке было ~ 7 раз для группы L, среднее увеличение Z в сыворотке было ~ 27 раз для группы Z, а среднее увеличение L и Z в сыворотке было ~ 4 и 14 раз соответственно для группа, получающая как L, так и Z. Вероятным фактором, влияющим на биодоступность каротиноида, является состав добавки.Имеются также некоторые свидетельства конкуренции каротиноидов за их захват сывороткой при введении в комбинации [34]. Оба эти фактора могли повлиять на данное исследование.
В соответствии с другими исследованиями L- и Z-добавок [30,31], ответы MP варьировались с точки зрения увеличения MPOD среди 10 субъектов в группе добавок. У четырех субъектов наблюдались значительные темпы увеличения MPOD на обоих глазах, а у 4 других наблюдались значительные темпы увеличения только на одном глазу.Средняя частота ± стандартное отклонение для группы составила 0,59 ± 0,79 мАЕ / день. Для группы плацебо не было значительных темпов увеличения, и среднее значение ± стандартное отклонение составило -0,17 ± 0,42 мАЕ / день. Согласно двустороннему t-критерию средние значения для 2 групп значительно различались (p <0,002). Результаты, полученные для группы добавок, можно сравнить с нашими более ранними исследованиями, в которых мы сообщили о результатах, в среднем 1,13 ± 0,10 мАЕ / день для исследования 30 мг / день L с использованием 2 субъектов [31] и 0,48 ± 0,16 мАЕ / день для 30 человек. исследование Z в мг / день, снова с участием 2 человек [30].В пересчете на миллиграмм средняя скорость увеличения MPOD, полученная в текущем исследовании, очень похожа на полученную в исследовании L и примерно вдвое превышает значение, полученное в исследовании Z. Однако суждение при проведении этих сравнений должно быть предварительным, исходя из небольшого числа субъектов в более ранних исследованиях.
Для этого небольшого исследования мы не обнаружили корреляции между скоростью увеличения ОПМР у субъектов, принимавших добавки, и ни концентрацией плато (с 6 недели до конца приема), ни изменением концентрации L или Z + MZ.Однако, когда мы ограничили наш анализ теми испытуемыми, которые были более опытны в HFP, судя по разбросу их данных, возникла интересная тенденция. Для субъектов, у которых скорость изменения ОПРОД сопровождалась стандартной ошибкой ≤ 0,21 мАЕ / день, эти показатели положительно коррелировали с увеличением сывороточного Z + MZ (R 2 = 0,31), хотя и не полностью достигали уровня статистических данных. значимость (р = 0,078). Следовательно, возможно, что ответы МП, которые мы наблюдали у наших испытуемых, были в значительной степени связаны с присутствием основного компонента добавки, MZ, который был в ~ 10 раз больше, чем Z.Однако окончательный вывод должен дождаться тестирования добавки, содержащей только MZ.
Субъект № 5 в группе добавок показал аномальный результат, состоящий из значительных темпов увеличения и уменьшения MPOD в левом и правом глазах соответственно. Если предположить, что этот субъект предоставил надежные данные, уменьшение, наблюдаемое в правом глазу, могло быть связано с более быстрым нарастанием МП при эксцентриситете 8 ° по сравнению с фовеа, как обсуждалось ранее. Значительное снижение MPOD в группе плацебо могло быть связано с изменением диеты во время периода исследования.
Данные текущего и предыдущих исследований ограничены размером выборки, что затрудняет аргументацию в пользу любого из трех каротиноидов, L, Z или MZ, как предпочтительного средства повышения плотности MP. С другой стороны, мы знаем, что значительная часть L в центральной сетчатке преобразуется в MZ. В центре сетчатки отношение MZ к L самое высокое и приближается к 1: 1. Это наблюдение предполагает, что эффективность преобразования L в MZ обычно ниже 50%. Кроме того, возможно, что процесс преобразования может включать в себя чистое разрушение каротиноида.В качестве доказательства данные вскрытия глаз показывают, что соотношение (L + MZ): Z изменяется по всей сетчатке от ~ 2: 1 в центре, где происходит большая часть конверсии, до ~ 3: 1 на периферии [7]. . Таким образом, может быть преимущество в обеспечении MZ в добавке за счет L, если цель состоит в том, чтобы повысить общий уровень зеаксантина и потенциально улучшить степень защиты сетчатки.
Заключение
Наше исследование показывает, что добавка, содержащая макулярные каротиноиды, L, Z и MZ, но в основном MZ, эффективна для повышения MPOD у большинства пациентов.Повышение MPOD может быть эффективным средством защиты стареющего населения от AMD.
Конкурирующие интересы
Трое из авторов, RAB, JTL и ANH, имеют собственный интерес в использовании MZ для повышения MPOD и лечения макулярных заболеваний.
Вклад авторов
RAB, JTL и ANH выступили инициаторами исследования. ANH предоставила капсулы MZ для исследования. Компания RAB разработала мерцающий фотометр, обучила испытуемых его использованию и проанализировала данные. JTL контролировала анализ сыворотки крови и анализировала данные.YC и FA-C провели анализ образцов сыворотки крови методом ВЭЖХ. RAB и JTL подготовили рукопись.
Благодарности
Данное исследование было поддержано грантом Фонда Говарда, Кембридж, Великобритания. Капсулы были предоставлены Quantum Nutritionals, Walled Lake MI 48390 и содержали продукт, произведенный Industrial Orgánica SA, Монтеррей, Мексика.
Ссылки
- Bone RA, Landrum JT, Fernandez L, Tarsis SL. Анализ макулярного пигмента с помощью ВЭЖХ: распределение по сетчатке и возрастное исследование.Инвестируйте Ophthalmol Vis Sci. 1988; 29: 843–849. [PubMed] [Google Scholar]
- Bone RA, Landrum JT, Tarsis SL. Предварительная идентификация макулярного пигмента человека. Vision Res. 1985; 25: 1531–1535. DOI: 10.1016 / 0042-6989 (85)
-3. [PubMed] [CrossRef] [Google Scholar]
- Handelman GJ, Dratz EA, Reay CC, van Kuijk FJGM. Каротиноиды в желтом пятне человека и всей сетчатке глаза. Инвестируйте Ophthalmol Vis Sci. 1988. 29: 850–855. [PubMed] [Google Scholar]
- Bone RA, Landrum JT, Hime GW, Cains A, Zamor J.Стереохимия макулярных каротиноидов человека. Инвестируйте Ophthalmol Vis Sci. 1993; 34: 2033–2040. [PubMed] [Google Scholar]
- Müller H. Die tägliche Aufnahme von Carotinoiden (Carotine und Xanthophylle) aus Gesamtnahrungsproben und die Carotinoidgehalte ausgewählter Gemüse- und Obstarten. Zeitschrift für Ernährungswissenschaft. 1996; 35: 45–50. DOI: 10.1007 / BF01612027. [PubMed] [CrossRef] [Google Scholar]
- Torres JA. Личное общение. 2007.
- Bone RA, Landrum JT, Friedes LM, Gomez CM, Kilburn MD, Menendez E, Vidal I., Wang W.Распределение стереоизомеров лютеина и зеаксантина в сетчатке человека. Exp Eye Res. 1997. 64: 211–218. DOI: 10.1006 / exer.1996.0210. [PubMed] [CrossRef] [Google Scholar]
- Ландрам Дж. Т., Боун Р. А., Мур Л. Л., Гомес К. М.. Анализ распределения зеаксантина в индивидуальных сетчатках человека. В: Пакер Л., редактор. Методы Энзимол. Vol. 299. Сан-Диего, Academic Press; 1999. С. 457–467. [PubMed] [Google Scholar]
- Джонсон Э. Дж., Нойрингер М., Рассел Р. М., Шальч В., Сноддерли Д. М.. Манипуляции с питанием сетчатки приматов, III Влияние добавок лютеина или зеаксантина на жировую ткань и сетчатку обезьян без ксантофилла.Инвестируйте Ophthalmol Vis Sci. 2005; 46: 692–702. DOI: 10.1167 / iovs.02-1192. [PubMed] [CrossRef] [Google Scholar]
- Landrum JT, Bone RA. Механические доказательства глазных болезней и каротиноидов. В кн .: Кринский Н.И., редактор. Каротиноиды в здоровье и болезнях. Нью-Йорк, Марсель Деккер, Инк; 2004. С. 445–472. [Google Scholar]
- Goralczyk R, Buser S, Bausch J, Bee W., Zühlke U, Barker FM. Возникновение двулучепреломляющих включений сетчатки у Cynomolgus обезьян после высоких доз кантаксантина. Инвестируйте Ophthalmol Vis Sci.1997; 38: 741–752. [PubMed] [Google Scholar]
- Thurmann PA, Schalch W., Aebischer JC, Tenter U, Cohn W. Кинетика лютеина, зеаксантина и 3-дегидро-лютеина в плазме после многократных пероральных доз лютеиновой добавки. Американский журнал клинического питания. 2005; 82: 88–97. [PubMed] [Google Scholar]
- Хартманн Д., Турманн П.А., Спитцер В., Скалч В., Маннер Б., Кон В. Кинетика плазмы зеаксантина и 3′-дегидро-лютеина после многократных пероральных доз синтетического зеаксантина. Американский журнал клинического питания.2004. 79: 410–417. [PubMed] [Google Scholar]
- Битти С., Ко Х. Х., Фил М., Хенсон Д., Бултон М. Роль оксидантного стресса в патогенезе возрастной дегенерации желтого пятна. Surv Ophthalmol. 2000. 45: 115–134. DOI: 10.1016 / S0039-6257 (00) 00140-5. [PubMed] [CrossRef] [Google Scholar]
- Сноддерли Д.М., Аурон Д.Д., Делори ФК. Макулярный пигмент. II. Пространственное распределение сетчатки приматов. Инвестируйте Ophthalmol Vis Sci. 1984. 25: 674–685. [PubMed] [Google Scholar]
- Рапп Л.М., Сима С.С., Чой Дж. Х.Концентрации лютеина и зеаксантина в мембранах наружных сегментов палочек перифовеальной и периферической сетчатки человека. Инвестируйте Ophthalmol Vis Sci. 2000. 41: 1200–1209. [PubMed] [Google Scholar]
- Sommerburg OG, Siems WG, Hurst JS, Lewis JW, Kliger DS, van Kuijk FJGM. Лютеин и зеаксантин связаны с фоторецепторами сетчатки глаза человека. Curr Eye Res. 1999; 19: 491–495. DOI: 10.1076 / ceyr.19.6.491.5276. [PubMed] [CrossRef] [Google Scholar]
- Ким С.Р., Наканиши К., Итагаки Ю., Воробей-младший.Фотоокисление A2-PE, флуорофора внешнего сегмента фоторецептора, и защита лютеином и зеаксантином. Экспериментальные исследования глаз. 2006; 82: 828–839. DOI: 10.1016 / j.exer.2005.10.004. [PubMed] [CrossRef] [Google Scholar]
- Кантрелл А., МакГарви Д.Д., Траскотт Т.Г., Ранкан Ф., Бом Ф. Тушение синглетного кислорода с помощью пищевых каротиноидов в модельной мембранной среде. Arch Biochem Biophys. 2003; 412: 47–54. DOI: 10.1016 / S0003-9861 (03) 00014-6. [PubMed] [CrossRef] [Google Scholar]
- Bhosale P, Bernstein PS.Синергетические эффекты зеаксантина и его связывающего белка в предотвращении окисления липидной мембраны. Biochim Biophys Acta. 2005; 1740: 116–121. [PubMed] [Google Scholar]
- Bone RA, Landrum JT. Макулярный пигмент в мембранах из волокон Генле — модель для кистей Хайдингера. Vision Res. 1984. 24: 103–108. DOI: 10.1016 / 0042-6989 (84)
-4. [PubMed] [CrossRef] [Google Scholar]
- Bone RA, Landrum JT, Cains A. Спектры оптической плотности макулярного пигмента in vivo и in vitro. Vision Res.1992. 32: 105–110. DOI: 10.1016 / 0042-6989 (92)
-3. [PubMed] [CrossRef] [Google Scholar]
- Sujak A, Okulski W, Gruszecki WI. Организация пигментов ксантофилла лютеина и зеаксантина в липидных мембранах, образованных дипальмитоилфосфатидилхолином. Biochim Biophys Acta. 2000; 1509: 255–263. DOI: 10.1016 / S0005-2736 (00) 00299-6. [PubMed] [CrossRef] [Google Scholar]
- Gene Logic Inc: номер испытания (1567-04370). Тринадцатинедельная пероральная (через желудочный зонд) токсичность мезозеаксантина у крыс Han Wister с 4-недельным выздоровлением.610 Professional Drive, Гейтерсбург, Мэриленд 20879. 2006.
- Проект № 26471-0-4090OECD. Covance Laboratories, 9200 Leesburh Pike, Вена, VA22182-1699. 2006.
- Bone RA, Landrum JT. Гетерохроматическая фликкер-фотометрия. Arch Biochem Biophys. 2004. 430: 137–142. DOI: 10.1016 / j.abb.2004.04.003. [PubMed] [CrossRef] [Google Scholar]
- Bone RA, Landrum JT, Gibert JC. Макулярный пигмент и краевая гипотеза фликкер-фотометрии. Исследование зрения. 2004; 44: 3045–3051. DOI: 10.1016 / j.visres.2004.07.008. [PubMed] [CrossRef] [Google Scholar]
- Родригес-Кармона М., Квансакул Дж., Харлоу Дж. А., Копке В., Шальч В., Барбур Дж. Л. Влияние добавок лютеина и / или зеаксантина на плотность макулярного пигмента человека и цветовое зрение. Офтальмологическая и физиологическая оптика. 2006. 26: 137–147. DOI: 10.1111 / j.1475-1313.2006.00386.x. [PubMed] [CrossRef] [Google Scholar]
- Berendschot TTJM, ван Норрен Д. О возрастной зависимости оптической плотности макулярного пигмента.Экспериментальные исследования глаз. 2005. 81: 602–609. DOI: 10.1016 / j.exer.2005.03.019. [PubMed] [CrossRef] [Google Scholar]
- Bone RA, Landrum JT, Guerra L., H., Ruiz CA. Пищевые добавки с лютеином и зеаксантином повышают плотность макулярных пигментов и концентрацию этих каротиноидов в сыворотке крови. J Nutr. 2003; 133: 992–998. [PubMed] [Google Scholar]
- Ландрам Дж. Т., Боун Р. А., Джоа Х., Килберн М. Д., Мур Л. Л., Спраг К. Э. Годовое исследование макулярного пигмента: эффект 140 дней приема лютеиновой добавки.Exp Eye Res. 1997. 65: 57–62. DOI: 10.1006 / exer.1997.0309. [PubMed] [CrossRef] [Google Scholar]
- Khachik F, de Moura FF, Chew EY, Douglass LW, Ferris III FL, Kim J, Thompson DJS. Влияние добавок лютеина и зеаксантина на метаболиты этих каротиноидов в сыворотке крови людей в возрасте 60 лет и старше. Инвестируйте Ophthalmol Vis Sci. 2006; 47: 5234–5242. DOI: 10.1167 / iovs.06-0504. [PubMed] [CrossRef] [Google Scholar]
- Шальч В., Кон В., Баркер Ф.М., Кёпке В., Меллерио Дж., Берд А.С., Робсон А.Г., Фитцке Ф.Ф., Ван Куийк FJGM.Накопление ксантофилла в сетчатке человека во время приема лютеина или зеаксантина — исследование LUXEA (LUtein Xanthophyll Eye Contemporary). Arch Biochem Biophys. 2007. 458: 128–135. DOI: 10.1016 / j.abb.2006.09.032. [PubMed] [CrossRef] [Google Scholar]
- Kostic D, White WS, Olson JA. Кишечная абсорбция, клиренс сыворотки и взаимодействие между лютеином и бета-каротином при введении взрослым людям в отдельных или комбинированных пероральных дозах. Am J Clin Nutr. 1995; 62: 604–610. [PubMed] [Google Scholar]
Преимущества лютеина и зеаксантина для глаз
HomeEye CareEye NutritionКак лютеин и зеаксантин могут помочь вашим глазам | En Español
Один-два удара для здоровья глаз и зрения
Лютеин и зеаксантин — это два типа каротиноидов, пигменты от желтого до красного, широко встречающиеся в овощах и других растениях.Хотя лютеин считается желтым пигментом, в высоких концентрациях он кажется оранжево-красным.
В природе лютеин (LOO-teen) и зеаксантин (zee-ah-ZAN-thin), по-видимому, поглощают избыточную световую энергию, чтобы предотвратить повреждение растений от слишком большого количества солнечного света, особенно от высокоэнергетических световых лучей, называемых синим светом.
Вареный шпинат — один из лучших натуральных источников лютеина и зеаксантина.
Лютеин и зеаксантин не только содержатся во многих зеленых листовых растениях, а также в ярких фруктах и овощах, но и в высоких концентрациях в желтоватом цвете глаза человека.Фактически, макула также называется «желтым пятном» (от латинского macula , что означает «пятно», и lutea , что означает «желтый»).
Недавние исследования обнаружили третий каротиноид в желтом пятне. Этот пигмент, называемый мезозеаксантином, не содержится в пищевых продуктах и, по-видимому, создается в сетчатке из лютеина.
Лютеин и зеаксантин, по-видимому, выполняют важные антиоксидантные функции в организме. Наряду с другими природными антиоксидантами, включая витамин C, бета-каротин и витамин E, эти важные пигменты защищают организм от разрушительного воздействия свободных радикалов, которые являются нестабильными молекулами, которые могут разрушать клетки и играть роль во многих заболеваниях.
Помимо важных преимуществ для глаз и зрения, лютеин может помочь защитить от атеросклероза (накопление жировых отложений в артериях), болезни, которая приводит к большинству сердечных приступов.
Преимущества лютеина и зеаксантина для глаз
Считается, что лютеин, зеаксантин и мезозеаксантин в макуле блокируют попадание синего света на нижележащие структуры сетчатки, тем самым снижая риск вызванного светом окислительного повреждения, которое может привести к дегенерация желтого пятна (AMD).
Ряд исследований показал, что лютеин и зеаксантин либо помогают предотвратить AMD, либо могут замедлить прогрессирование заболевания:
Исследование, опубликованное в Nutrition & Metabolism , показало, что пищевая добавка, содержащая мезозеаксантин, лютеин и зеаксантин, эффективно увеличила оптическую плотность макулярного пигмента в глазах большинства людей. Считается, что пигмент желтого пятна обеспечивает защиту от развития дегенерации желтого пятна.
Исследования, опубликованные в American Journal of Epidemiology , Ophthalmology и Archives of Ophthalmology , обнаружили, что более высокие уровни лютеина и зеаксантина в рационе связаны с более низкой частотой случаев AMD.
В двух исследованиях, опубликованных в журнале Investigative Ophthalmology and Visual Science , было обнаружено, что глаза с более высоким уровнем пигментов желтого пятна с меньшей вероятностью имеют или развивают дегенерацию желтого пятна.
В исследовании, опубликованном в Archives of Biochemistry and Biophysics , авторы исследования пришли к выводу, что лютеин, зеаксантин и мезозеаксантин фильтруют коротковолновый свет и предотвращают или уменьшают образование свободных радикалов в пигментном эпителии сетчатки и сосудистой оболочке.Они также предполагают, что смесь этих каротиноидов более эффективна, чем любой из отдельных каротиноидов при той же общей концентрации.
В исследовании, опубликованном в журнале Optometry , участники с ранней AMD, которые потребляли 8 мг зеаксантина в день в течение одного года, улучшили свое ночное вождение, а их острота зрения улучшилась в среднем на 1,5 линии на глазной карте.
В мае 2013 года были опубликованы долгожданные результаты второго крупномасштабного исследования возрастных заболеваний глаз (AREDS2), спонсируемого Национальным институтом глаз.
AREDS2 был продолжением оригинального 5-летнего исследования AREDS, опубликованного в 2001 году, в котором было обнаружено, что ежедневное использование антиоксидантных добавок, содержащих бета-каротин, витамин C, витамин E, цинк и медь, снижает риск прогрессирования AMD на 25%. процент среди участников с ранней и средней дегенерацией желтого пятна.
Целью AREDS2 было оценить влияние других питательных веществ, включая лютеин и зеаксантин, на профилактику AMD и других возрастных заболеваний глаз. AREDS2 также исследовал эффект удаления бета-каротина из добавки AREDS, поскольку добавление этого предшественника витамина А было связано с повышенным риском некоторых видов рака среди курильщиков и курильщиков в прошлом.
Результаты AREDS2 выявили участников исследования с ранними признаками дегенерации желтого пятна, которые принимали модификацию исходной пищевой добавки AREDS, которая содержала 10 мг лютеина и 2 мг зеаксантина (без бета-каротина) каждый день в течение 5-летнего периода исследования. снижение риска прогрессирования AMD на 10-25%. Участники исследования, чьи диеты содержали наименьшее количество продуктов, содержащих натуральный лютеин и зеаксантин, испытали наибольшее снижение риска AMD от приема ежедневных пищевых добавок.
Хотя AREDS2 и другие исследования предоставляют доказательства того, что лютеин и зеаксантин могут играть роль в предотвращении дегенерации желтого пятна (или, по крайней мере, в снижении риска прогрессирования AMD), менее ясно, помогают ли эти каротиноиды предотвращать катаракту.
Исследование, опубликованное в Archives of Ophthalmology , предполагает, что женщины, в рацион которых входит большое количество здоровой пищи, содержащей лютеин, зеаксантин и другие каротиноиды, имеют более низкий риск катаракты, чем женщины, в рационе которых содержится меньшее количество этих питательных веществ.
Однако в AREDS2 дополнительный прием лютеина и зеаксантина не повлиял на риск или прогрессирование катаракты.
Продукты, содержащие лютеин и зеаксантин
Лучшими натуральными источниками лютеина и зеаксантина являются зеленые листовые овощи и другие зеленые или желтые овощи. По данным Министерства сельского хозяйства США (USDA), среди них вареная капуста и приготовленный шпинат возглавляют список.
Невегетарианские источники лютеина и зеаксантина включают яичные желтки. Но если у вас высокий уровень холестерина, вам будет гораздо лучше получать большую часть этих желтых питательных веществ из фруктов и овощей.
Попробуйте эти простые рецепты — все они содержат лютеин и зеаксантин:
Добавки лютеина и зеаксантина
Продукты с лютеином и зеаксантином.
Из-за очевидных преимуществ лютеина и зеаксантина для глаз и сердечно-сосудистой системы, многие компании, производящие пищевые продукты, добавили эти каротиноиды в свои формулы с множеством витаминов. Другие ввели специальные витамины для глаз, которые в основном состоят из лютеина и зеаксантина.
В настоящее время не существует Рекомендуемой диетической нормы (RDA) или Рекомендуемой суточной дозы (RDI) для лютеина или зеаксантина, но некоторые эксперты говорят, что вам следует принимать не менее 6 миллиграммов (мг) лютеина в день для положительного эффекта.
Остается неясным, сколько лютеина и зеаксантина необходимо ежедневно для адекватной защиты глаз и зрения. Кроме того, в настоящее время неизвестно, обладают ли добавки таким же действием, как лютеин и зеаксантин, полученные из пищевых источников.
Нет известных побочных токсических эффектов при приеме слишком большого количества лютеина или зеаксантина. В некоторых случаях у людей, которые едят большое количество моркови или желтых и зеленых цитрусовых, может развиться безвредное пожелтение кожи, называемое каротинемией. Хотя внешний вид этого состояния может вызывать тревогу и его можно спутать с желтухой, желтое изменение цвета исчезает при сокращении потребления этих богатых каротиноидами продуктов.(Каротинемия также может быть связана с чрезмерным потреблением пищевых добавок, богатых каротиноидами.)
Популярные добавки с лютеином и зеаксантином включают:
MacuHealth с LMZ3 (MacuHealth LLC)
Zeavanthis
ICaps Eye Vitamin Lutein & Zeaxanthin Formula (Alcon)
Macula Complete (Biosyntrx)
MacularProtect Complete (ScienceBased Health)
MaxiVision Ocular Formula (
909ard)
Окувит (Bausch + Lomb)
Источником лютеина во многих добавках лютеина являются цветки календулы, а зеаксантина — красный перец.Если вы выбираете добавку лютеина и зеаксантина, убедитесь, что это высококачественный продукт от уважаемой компании по производству пищевых добавок.
Помните, что прием пищевых добавок не заменяет здоровое питание. Хорошо сбалансированная диета, включающая большое количество фруктов и овощей, обычно является лучшим способом получить необходимые вам питательные вещества для глаз.
Если у вас низкий уровень макулярного пигмента и вы чувствительны к свету, спросите своего офтальмолога о фотохромных линзах.Эти линзы для очков защищают ваши глаза от ультрафиолета и видимого синего света высокой энергии, который может повредить ткань сетчатки, и они автоматически темнеют на солнечном свете, чтобы снизить светочувствительность.
Также помните, что люди иногда по-разному реагируют на определенные добавки, что может иметь непредвиденные эффекты, такие как побочные реакции на лекарства. Прежде чем принимать какие-либо добавки для зрения, проконсультируйтесь с врачом или окулистом.
Исследование на животных показывает, что пищевые добавки снижают риск диабетической ретинопатии
Пищевые добавки, содержащие лютеин и зеаксантин, липоевую кислоту и омега-3 жирные кислоты, эффективны в предотвращении развития ретинопатии у диабетических крыс, согласно исследованию.
Исследователи из Kresge Eye Institute в Детройте исследовали влияние добавок, содержащих каротиноиды, на окислительный стресс и воспаление сетчатки, а также на развитие диабетической ретинопатии.
Диабет был индуцирован и подтвержден у всех крыс в исследовании, а затем некоторым крысам давали диету, которая включала пищевые добавки, в то время как другим давали ту же пищу, но без добавок. Через 11 месяцев сетчатку крыс оценивали на предмет изменений кровеносных сосудов, клеточного повреждения и других изменений сетчатки, характерных для диабетической ретинопатии.
У крыс, не получавших пищевые добавки, вызванное диабетом повреждение кровеносных сосудов сетчатки было в три-четыре раза больше, чем у крыс, получавших добавленные питательные вещества.
Авторы исследования пришли к выводу, что пищевые добавки, использованные в этом исследовании, предотвращали диабетическую ретинопатию и сохраняли нормальное функционирование сетчатки. Они также сказали, что, хотя для подтверждения требуется тестирование на людях, эти добавки «могут представлять собой достижимую и недорогую дополнительную терапию» для подавления диабетической ретинопатии у людей с диабетом.
Полный отчет об исследовании был опубликован в Интернете в январе 2014 года на сайте Nutrition & Metabolism .
ПОДРОБНЕЕ: Новости питания глаз
Шерин Джегтвиг, CNS, также внесла свой вклад в эту статью.
Примечания и ссылки
Лютеин + зеаксантин и омега-3 жирные кислоты для возрастной дегенерации желтого пятна: рандомизированное клиническое испытание Age-Related Eye Disease Study 2 (AREDS2). JAMA. Опубликовано в мае 2013 года.
Исследование
NIH дает ясность в отношении добавок для защиты от слепоты глаз. Пресс-релиз Национального института глаз (NEI) выпущен в мае 2013 года.
Противовоспалительное действие лютеина при ишемическом / гипоксическом поражении сетчатки: исследования in vivo и in vitro. Исследовательская офтальмология и визуализация . Опубликовано в Интернете в августе 2012 года.
Исследования механизма поглощения синглетного кислорода макулярным пигментом человека. Архив биохимии и биофизики . Август 2010.
Здоровое питание и последующая распространенность ядерной катаракты у женщин. Архив офтальмологии . Июнь 2010 г.
Связь между возрастной ядерной катарактой и лютеином и зеаксантином в пище и сыворотке крови в каротиноидах в исследовании возрастных глазных болезней (CAREDS), дополнительном исследовании Инициативы по охране здоровья женщин. Архив офтальмологии . Март 2008 г.
Диетические антиоксиданты и долгосрочная частота возрастной дегенерации желтого пятна: исследование глаз Голубых гор. Офтальмология . Февраль 2008 г.
Каротиноиды в пище, витамины С и Е и риск катаракты у женщин. Архив офтальмологии . Январь 2008 г.
Реакция пигмента желтого пятна на добавку, содержащую мезозеаксантин, лютеин и зеаксантин. Питание и обмен веществ . May 2007.
Связь между промежуточной возрастной дегенерацией желтого пятна и лютеином и зеаксантином в каротиноидах в исследовании возрастных глазных болезней (CAREDS). Архив офтальмологии . Август 2006 г.
Оксигенированный каротиноид лютеин и прогрессирование раннего атеросклероза: исследование атеросклероза в Лос-Анджелесе. Тираж . Июнь 2001 г.
Лютеин и зеаксантин в диете и сыворотке и их связь с возрастной макулопатией в Третьем национальном обзоре по вопросам здоровья и питания. Американский журнал эпидемиологии . March 2001.
Пигмент желтого пятна и риск возрастной дегенерации желтого пятна у субъектов из Северной Европы. Исследовательская офтальмология и визуализация . Февраль 2001.
Макулярный пигмент в глазах доноров с ВМД и без ВМД: исследование случай-контроль. Исследовательская офтальмология и визуализация . Январь 2001г.
Страница опубликована в феврале 2019 г.
Страница обновлена в июне 2021 г.
Марганец (iii) мезо-тетракис (орто-N-алкилпиридил) порфирины. Синтез, характеристика и катализ дисмутации O2˙–
Серия орто изомеров мезо -тетракис ( N -алкилпиридил) порфиринов (алкил представляет собой метил, этил, н-пропил, н-бутил, н-гексил и н-октил) и их Mn ( III ) комплексы были синтезированы и охарактеризованы методами элементного анализа, УФ / видимой спектроскопии, масс-спектрометрии с ионизацией электрораспылением и электрохимии.Увеличение числа атомов углерода в алкильных цепях с 1 до 8 сопровождается увеличением: (а) липофильности, измеренной с помощью хроматографического фактора удерживания, R f ; (b) металлоцентрированный окислительно-восстановительный потенциал, E 1/2 от +220 до +367 мВ по сравнению с NHE, и (c) константа диссоциации протона, p K a2 от С 10.9 по 13.2. Была обнаружена линейная корреляция между порфиринами Mn ( III ) E 1/2 и R f и между p K a2 и R f безметалловых соединений.Как порфирины
становятся все более липофильными, уменьшение гидратации препятствует созданию заряда, одновременно усиливая электроноакцепторный эффект положительно заряженных атомов пиридильного азота. Следовательно, E 1/2 линейно возрастает с увеличением p K a2 , тенденция основности порфирина противоположна той, о которой мы ранее сообщали для другого водорастворимого Mn ( III ) порфирины. Все эти порфирины Mn ( III ) являются мощными катализаторами дисмутации супероксида (диспропорционирования).Несмотря на благоприятное увеличение E 1/2 с увеличением длины цепи, каталитическая константа скорости уменьшается от метила (log k cat
= 7,79) до н-бутила, а затем увеличивается так, что н-октил является таким же сильным имитатором SOD, как и метиловые и этильные соединения. Наблюдаемое поведение возникает из-за взаимодействия гидратации и стерических эффектов, которые модулируют электронные эффекты.
Одноразовые амперометрические биосенсоры на основе ксантиноксидазы, иммобилизованной в трехэлектродной системе с модифицированной трафаретной печатью «берлинский синий»
Lindberg D, Grimes C.Влияние глобализации торговли на безопасность пищевых продуктов. Sensor Lett , 2004, 2: 161–163
Артикул
Google Scholar
Hu S, Xu C, Luo J, Luo J, Cui D. Биосенсор для обнаружения гипоксантина на основе ксантиноксидазы, иммобилизованный на электроде из химически модифицированной угольной пасты. Anal Chim Acta , 2000, 412: 55–61
CAS
Статья
Google Scholar
Sugase S, Цуда Т.Определение молочной кислоты, мочевой кислоты, ксантина и тирозина в человеческом поте с помощью ВЭЖХ и изменение концентрации молочной кислоты в нем после употребления вина. Бунсеки Кагаку , 2002, 51: 429–435
CAS
Статья
Google Scholar
Саманиду В.Ф., Метакса А.С., Пападояннис И.Н. Прямое одновременное определение уремических токсинов: креатина, креатинина, мочевой кислоты и ксантина в биологических жидкостях человека с помощью ВЭЖХ. J Liq Chromatogr Relat Technol , 2002, 25: 43–57
CAS
Статья
Google Scholar
Чан СТ, Яо MWY, Вонг YC, Вонг Т, Мок CS, Sin DWM.Оценка химических индикаторов для контроля свежести кормов и определения летучих аминов в рыбе методами твердофазной микроэкстракции и газовой хроматографии-масс-спектрометрии. Eur Food Res Technol , 2006, 224: 67–74
CAS
Статья
Google Scholar
Олафсдоттир Г., Мартинсдоттир Э., Охеленшлагер Дж. Методы оценки свежести рыбы в научных исследованиях и в промышленности. Trends Food Sci Technol , 1997, 8: 258–265
CAS
Статья
Google Scholar
Armenta S, Coelho NMM, Roda R, Garrigues S, de la Guardia M.Определение свежести морепродуктов с помощью инфракрасной спектроскопии с преобразованием Фурье в паровой фазе. Anal Chim Acta , 2006, 580: 216–222
CAS
Статья
Google Scholar
Смулевич Г., Дрогетти Э., Фокарди С., Колетта М., Чаччо С., Ночентини М. Экспресс-спектроскопический метод для обнаружения мошенничества с обработкой тунца угарным газом. Food Chem , 2007, 101: 1071–1077
CAS
Статья
Google Scholar
Chen XM, Lin ZJ, Chen DJ, Jia TT, Cai ZM, Wang XR, Chen X, Chen GN, Oyama M.Неферментативное амперометрическое определение глюкозы с помощью наночастиц палладия, нанесенных на функциональные углеродные нанотрубки. Biosens Bioelectron , 2010, 25: 1803–1808
CAS
Статья
Google Scholar
Yuan JH, Wang K, Xia XH. Высокоупорядоченные массивы платиновых нанотрубок для амперометрического определения глюкозы. Adv Func Mater , 2005, 15: 803–809
CAS
Статья
Google Scholar
Венугопал В.Биосенсоры в рыбоводстве и контроле качества. Biosens Bioelectron , 2002, 17: 147–157
CAS
Статья
Google Scholar
Киргоз О.А., Тимур С., Ван Дж., Телефонку А. Электрод из стеклоуглеродистой пасты, модифицированный ксантиноксидазой. Electrochem Commun , 2004, 6: 913–916
Статья
Google Scholar
Хоши Т., Ногучи Т., Анзай Дж.Изготовление амперометрических ксантиновых сенсоров на основе многослойных тонких пленок, содержащих ксантиноксидазу. Mater Sci Eng C , 2006, 26: 100–103
CAS
Статья
Google Scholar
Кубукку М., Тимур С., Аник У. Исследование характеристик электрода из стеклоуглеродной пасты, модифицированного наночастицами золота и ксантиноксидазой, для обнаружения ксантина и гипоксантина. Таланта , 2007, 74: 434–439
CAS
Статья
Google Scholar
Ли XH, Xie ZH, Min H, Xian YZ, Jin LT.Амперометрический биосенсор на гипоксантин на основе иммобилизованной ксантиноксидазы на стеклоуглеродном электроде, модифицированном наночастицами мезо-тетрафенилпорфирина железа (III). Anal Lett , 2008, 41: 456–468
CAS
Статья
Google Scholar
Zhang M, Li L, Du Z, Xu S, Li C, Chen X, Zhang T, Wang T. Амперометрический биосенсор с быстрым откликом для H 2 O 2 Обнаружение на основе пероксидазы хрена / диоксид титана-нанопроволоки / стеклоуглеродный электрод, модифицированный хитозаном. Sensor Lett , 2009 г., 7: 543–549
CAS
Статья
Google Scholar
Игнатов С., Шишниашвили Д., Ге Б., Шеллер Ф. В., Лисдат Ф. Амперометрический биосенсор на основе функционализированного золотого электрода для обнаружения антиоксидантов. Biosens Bioelectron , 2002, 17: 191–199
CAS
Статья
Google Scholar
Ван К., Чен Дж. Х., Чен Дж., Лю А. Л., Ли Г. В., Ло Х. Б., Линь XH, Чен Ю. З.Электрохимический биосенсор типа сэндвич для обнаружения гена слияния bcr / abl с использованием заблокированных нуклеиновых кислот на золотом электроде. Электроанал , 2009 г., 21: 1159–1166
КАС
Статья
Google Scholar
Сан В., Гао Р., Цзяо К. Электрохимия и электрокатализ гемоглобина в пленке нафион / нано-СаСО 3 на новом электроде из углеродной пасты, модифицированной ионной жидкостью BPPF6. J Phys Chem B , 2007, 111: 4560–4567
CAS
Статья
Google Scholar
Машхадизаде М.Х., Талакеш М., Песте М., Момени А., Хамидиан Х., Мазлум М.Новый электрод из модифицированной угольной пасты для потенциометрического определения иона ртути (II). Электроанализ , 2006, 18: 2174
CAS
Статья
Google Scholar
Сюэ MH, Xu Q, Zhou M, Zhu JJ. In situ иммобилизация глюкозооксидазы в гибридной пленке хитозан-золотые наночастицы на электроде, модифицированном берлинской лазурью, для высокочувствительного определения глюкозы. Electrochem Commun , 2006, 8: 1468–1474
CAS
Статья
Google Scholar
Чен Х.Л., Чжао Л., Чен Х, Чжуан ZX, Ван XR.Разработка амперометрического биосенсора глюкозы на основе иммобилизации глюкозооксидазы в матрице ормосил-ПВС на модифицированном электроде берлинской синей. Sci China Ser-B: Chem , 2009, 52: 1128–1135
CAS
Статья
Google Scholar
Suprun E, Evtugyn G, Budnikov H, Ricci F, Moscone D, Palleschi G. Датчик ацетилхолинэстеразы на основе угольного электрода с трафаретной печатью, модифицированного берлинской лазурью. Anal Bioanal Chem , 2005, 383: 597–604
CAS
Статья
Google Scholar
Lowinsohn D, Bertotti M. Поточный инъекционный анализ l-лактата крови с использованием биосенсора на основе берлинского синего в качестве амперометрического детектора. Anal Biochem , 2007, 365: 260–265
CAS
Статья
Google Scholar
Карякин А.А., Гительмахер О.В., Карякина Е.Е.Биосенсор первого поколения на основе берлинской голубой. Чувствительный амперометрический электрод для глюкозы. Anal Chem , 1995, 67: 2419–2423
CAS
Google Scholar
Ван Дж., Педреро М., Сакслунд Х., Хаммерих О., Пингаррон Дж. Электрохимическая активация углеродных полос с трафаретной печатью. Аналитик , 1996, 121: 345–350
CAS
Статья
Google Scholar
де Маттос ИЛ, Гортон Л, Лаурелл Т, Малинаускас А, Карякин АА.Разработка биосенсоров на основе гексацианоферратов. Таланта , 2000, 52: 791–799
Артикул
Google Scholar
de Mattos IL, Gorton L, Ruzgas T. Сенсор и биосенсор на основе электродов с нанесенным методом трафаретной печати из золота и платины, модифицированного берлинской синью. Biosens Bioelectron , 2003, 18: 193–200
Статья
Google Scholar
Li M, Zhao G, Yue Z, Huang S.Датчик следов перекиси водорода с использованием электрода, модифицированного многослойными углеродными нанотрубками, коллоидом золото-хитозан и берлинской лазурью. Microchimica Acta , 2009 г., 167: 167–172
CAS
Статья
Google Scholar
Aymard C, Belarbi A. Кинетика термической дезактивации ферментов: простая трехпараметрическая феноменологическая модель может описать спад активности фермента, независимо от механизма. Enzyme Microb Technol , 2000, 27: 612–618
CAS
Статья
Google Scholar
Вильялонга Р., Матос М., Као Р. Создание амперометрического биосенсора для определения ксантина через супрамолекулярные ассоциации Electrochem Commun , 2007, 9: 454–458
CAS
Статья
Google Scholar
Liu Y, Nie L, Tao W, Yao S. Амперометрическое исследование Au-коллоидной функции на ксантиновом биосенсоре на основе ксантиноксидазы, иммобилизованной в слое полипиррола. Электроанализ , 2004, 16: 1271–1278
Статья
Google Scholar
Shan D, Wang YN, Xue HG, Cosnier S, Ding SN. Наночастицы ксантиноксидазы / лапонита, иммобилизованные на стеклоуглеродном электроде: прямой перенос электронов и мультиэлектрокатализ. Biosens Bioelectron , 2009, 24: 3556–3561
CAS
Статья
Google Scholar
Астаксантин: обзор литературы
Список литературы
1 Андерсен, Л.П., Холк, С., Купчинскас, Л., Киуделис, Г., Йонайтис, Л., Янчаускас, Д., Пермин, Х. и Вадстром, Т. Маркеры воспаления желудка и интерлейкины у пациентов с функциональной диспепсией, получавших лечение астаксантин. FEMS Immunol.Med Microbiol. 2007; 50 (2): 244-248.
2 Белькаро, Г., Сезароне, М. Р., Корнелли, У. и Дугал, М. М. Ф. Афрагил (справа) в лечении 34 симптомов менопаузы: пилотное исследование. Панминерва Мед . 2010; 52 (2 Дополнение 1): 49-54.
3 Comhaire, F.H., El Garem, Y., Mahmoud, A., Eertmans, F., and Schoonjans, F. Комбинированное традиционное / антиоксидантное «астаксантинное» лечение мужского бесплодия: двойное слепое рандомизированное исследование. Азиатский Дж. Андрол . 2005; 7 (3): 257-262.
4 Фассет, Р. Г. и Кумбс, Дж. С. Астаксантин: потенциальное терапевтическое средство при сердечно-сосудистых заболеваниях. Мар. Лекарства . 2011; 9 (3): 447-465.
5 Хори, С., Окуда, К., Ямасита, Т., Ватанабе, К., Курамоти, К., Хосокава, М., Такеучи, Т., Какуда, М., Мияшита, К., Сугавара, Ф. ., Yoshida, H., and Mizushina, Y. Очищенный лютеин канолы избирательно ингибирует определенные изоформы ДНК-полимераз млекопитающих и снижает воспалительный ответ. Липиды. 2010; 45 (8): 713-721.
6 Купчинскас, Л., Лафоли, П., Лигнелл, А., Киуделис, Г., Йонайтис, Л., Адамонис, К., Андерсен, Л. П., и Вадстром, Т. Эффективность природного антиоксиданта астаксантина в лечении функциональной диспепсии у пациентов с инфекцией Helicobacter pylori или без нее: проспективное, рандомизированное, двойное слепое и плацебо-контролируемое исследование. Фитомедицина . 2008; 15 (6-7): 391-399.
7 Lignell, Å. Лекарство для увеличения продолжительности мышечной функции или лечения мышечных расстройств или заболеваний. 1999; заявка на патентную кооперацию № 9
8. Лю, X. и Осава, Т. Астаксантин защищает нейрональные клетки от окислительного повреждения и является мощным кандидатом в пищу для мозга. Форум Нутр . 2009; 61: 129-135.
9 Накагава К., Кико Т., Миядзава Т., Карпентеро, Бурдеос Г., Кимура Ф., Сато А. и Миядзава Т.Антиоксидантный эффект астаксантина на перекисное окисление фосфолипидов в эритроцитах человека. Бр Дж Нутрь . 2011; 105 (11): 1563-1571.
10 Паризи, В., Тедески, М., Галлинаро, Г., Варано, М., Савиано, С., и Пьермарокки, С. Каротиноиды и антиоксиданты в итальянском исследовании возрастной макулопатии: модификации мультифокальной электроретинограммы через 1 год. Офтальмология . 2008; 115 (2): 324-333.
11 Пашков, Ф. Дж., Ватумулл, Д. Г., и Кэмпбелл, К. Л. Астаксантин: новое потенциальное лечение окислительного стресса и воспаления при сердечно-сосудистых заболеваниях. Ам Дж. Кардиол . 5-22-2008; 101 (10А): 58D-68D.
12 Серебряный, В., Малинин, А., Гудин, Т., и Пашков, Ф. Влияние ксанкора, синтетического производного астаксантина, in vitro на гемостатические биомаркеры у субъектов, не получавших аспирин, и получавших аспирин с множественными факторами риска при сосудистых заболеваниях. Am J Ther . 2010; 17 (2): 125-132.
13 Ямасита Э. Влияние пищевой добавки, содержащей астаксантин, на состояние кожи. Каротиноидная наука . 2006; 10: 91-95.
14 Йошида, Х., Yanai, H., Ito, K., Tomono, Y., Koikeda, T., Tsukahara, H., and Tada, N. Введение природного астаксантина увеличивает сывороточный холестерин HDL и адипонектин у субъектов с легкой гиперлипидемией. Атеросклероз. 2010; 209 (2): 520-523.
15 Юань, Дж. П., Пэн, Дж., Инь, К., и Ван, Дж. Х. Потенциальные оздоровительные эффекты астаксантина: ценный каротиноид, главным образом из микроводорослей. Мол Нутр Пищевой Рес . 2011; 55 (1): 150-165.
% PDF-1.7
%
371 0 объект
>
эндобдж
xref
371 143
0000000016 00000 н.
0000003781 00000 п.
0000004010 00000 н.
0000004052 00000 н.
0000004088 00000 н.
0000004714 00000 н.
0000004822 00000 н.
0000004931 00000 н.
0000005040 00000 н.
0000005149 00000 п.
0000005259 00000 н.
0000005368 00000 н.
0000005478 00000 п.
0000005587 00000 н.
0000005698 00000 п.
0000005808 00000 п.
0000005917 00000 н.
0000006027 00000 н.
0000006136 00000 н.
0000006247 00000 н.
0000006358 00000 п.
0000006468 00000 н.
0000006579 00000 п.
0000006689 00000 н.
0000006799 00000 н.
0000006906 00000 н.
0000007011 00000 п.
0000007115 00000 н.
0000007223 00000 н.
0000007303 00000 н.
0000007383 00000 п.
0000007460 00000 н.
0000007539 00000 н.
0000007617 00000 н.
0000007697 00000 н.
0000007776 00000 н.
0000007856 00000 н.
0000007935 00000 п.
0000008013 00000 н.
0000008090 00000 н.
0000008168 00000 п.
0000008246 00000 н.
0000008325 00000 н.
0000008405 00000 н.
0000008485 00000 н.
0000008565 00000 н.
0000008645 00000 н.
0000008725 00000 н.
0000008805 00000 н.
0000008885 00000 н.
0000008965 00000 н.
0000009046 00000 н.
0000009127 00000 н.
0000009208 00000 н.
0000009289 00000 н.
0000009370 00000 п.
0000009450 00000 н.
0000009530 00000 н.
0000009610 00000 п.
0000009691 00000 п.
0000009771 00000 п.
0000009852 00000 н.
0000009932 00000 н.
0000010012 00000 п.
0000010093 00000 п.
0000010173 00000 п.
0000010287 00000 п.
0000010345 00000 п.
0000010478 00000 п.
0000010524 00000 п.
0000010558 00000 п.
0000010636 00000 п.
0000011941 00000 п.
0000012163 00000 п.
0000012377 00000 п.
0000012809 00000 п.
0000013179 00000 п.
0000013619 00000 п.
0000013689 00000 п.
0000013985 00000 п.
0000014193 00000 п.
0000014496 00000 п.
0000015180 00000 п.
0000015712 00000 п.
0000017330 00000 п.
0000017909 00000 п.
0000018115 00000 п.
0000018409 00000 п.
0000018478 00000 п.
0000018656 00000 п.
0000020392 00000 п.
0000020760 00000 п.
0000021036 00000 п.
0000021192 00000 п.
0000021364 00000 н.
0000021565 00000 п.
0000021726 00000 п.
0000021917 00000 п.
0000023586 00000 п.
0000024195 00000 п.
0000024402 00000 п.
0000024695 00000 п.
0000024762 00000 п.
0000024940 00000 п.
0000026746 00000 н.
0000028510 00000 п.
0000028866 00000 п.
0000029121 00000 п.
0000030919 00000 п.
0000032659 00000 п.
0000042144 00000 п.
0000044352 00000 п.
0000051741 00000 п.
0000053497 00000 п.
0000057423 00000 п.
0000057653 00000 п.
0000057881 00000 п.
0000061420 00000 п.
0000088010 00000 п.
0000129996 00000 н.
0000130537 00000 п.
0000130671 00000 н.
0000149370 00000 н.
0000149409 00000 н.
0000149521 00000 н.
0000149598 00000 н.
0000149651 00000 п.
0000149728 00000 н.
0000149815 00000 н.
0000149873 00000 н.
0000150086 00000 н.
0000150188 00000 н.
0000150284 00000 н.
0000150403 00000 н.
0000150514 00000 н.
0000150619 00000 н.
0000150787 00000 н.
0000150967 00000 н.
0000151089 00000 н.
0000151206 00000 н.
0000151365 00000 н.
0000151564 00000 н.
0000003156 00000 н.
трейлер
] >>
startxref
0
%% EOF
513 0 объект
> поток
x ڔ RkQjƋ`f7 & QHEͯ, m # I H ۄ (FACv_hERP ** AE
.
