Гиалуроновая кислота и алкоголь: Алкоголь после увеличения губ: сколько нельзя пить после процедуры, можно ли употреблять пиво, спиртное
Алкоголь после увеличения губ: можно ли пить?
Алкоголь после увеличения губ принимать не желательно. Эту рекомендацию дают все косметологи. Но не преувеличена ли опасность? Чтобы знать это наверняка, необходимо изучить вопрос всесторонне. Подробную информацию на эту тему можно найти на площадке Plastichno.
Увеличение губ гиалуроновой кислотой
Гиалуроновая кислота – вещество, которое вырабатывается самим организмом и имеет высокомолекулярную структуру. Она входит в состав нервной, соединительной и эпителиальной ткани.
С возрастом этой кислоты вырабатывается организмом все меньше. Но так как гиалуронка хорошо переносится организмом, то при правильном введении и соблюдении всех мер, она не вызывает побочных эффектов.
Используется гиалуронка в косметологии как средство заполнения морщин, для улучшения состояния кожи лица и для увеличения губ. Филлеры с гиалуроновой кислотой, введенные в них, полностью застывают за несколько дней. В течение этого времени организм требует бережного к себе отношения.
Гиалуронка и спирт
Для того чтобы понять, какой результат может ожидать при совмещении процедуры красоты и приеме алкоголя, нужно проанализировать его воздействие на организм. Прием спиртосодержащих напитков приводит к обезвоживанию. В результате появляются отеки, кожа быстрее стареет, образуются морщины.
Вводимая в губы гиалуроновая кислота способствует их увлажнению на длительное время. Это связано с тем, что каждая молекула способна притягивать к себе и удерживать несколько сотен молекул воды.
Но при одновременном присутствии филлера и спирта, эффект от гиалуронки меняется. В результате:
- Гиалуроновая кислота начинает быстро разрушаться и впитываться в соседние ткани, переходя в межклеточную жидкость.
- Наблюдается пересыхание кожи, в том числе в местах проколов. В итоге могут появляться трещины, проникать инфекция.
- Спирт обладает свойством повышать давление и стимулировать работу кровотока. Но это не желательно при косметологических процедурах, так как может спровоцировать образование гематом.

Алкоголь после увеличения губ
После прохождения процедуры введения филлеров в губы, от употребления алкоголя рекомендуется воздержаться на несколько недель. Соблюдение этого простого правила позволит избежать осложнений и побочек, а также не допустить того, чтобы гиалуронка полностью всосалась, не дав результата.
Строгий запрет на прием спиртосодержащих напитков накладывается на первые сутки. Но желательно воздержаться от употребления еще как минимум на 5 дней.
Замедление восстановления
Утрата жидкости при попадании в организм алкоголя приводит к замедлению процесса регенерации тканей. При этом меняются показатели крови, повышается риск тромбов.
Кровеносные сосуды под действием спирта переносят большую нагрузку – они сначала расширяются, а потом сужаются. На этом фоне происходят скачки давления и нарушение всего процесса кровообращения, которое затронет, в том числе зону губ, подвергшуюся введению филлера. Из-за этого ткани не будут получать необходимый кислород и полезные вещества.
Из-за этого ткани не будут получать необходимый кислород и полезные вещества.
Несмотря на то, что инъекции гиалуронкой – малотравматичная процедура, которая, как правило, хорошо переносится, присутствие алкоголя в организме может спровоцировать побочные эффекты и замедлить восстановление.
Отечность
Употребление спиртосодержащих напитков приводит к интенсивному выведению жидкости из организма. О необходимости восполнения водного баланса говорит сильная жажда. В результате человек начинает пить много воды, которая задерживается в организме и вызывает отеки.
Инфицирование
Алкоголь также негативно сказывается на иммунитете. После процедуры по коррекции губ, очень важно, чтобы в организм не проникла инфекция. Но пересушенные участки с образовавшимися корочками, становятся открытыми воротами для попадания инфекции.
Неэстетичный эффект
Введенный в губы гель с гиалуроновой кислотой при присутствии спирта в организме может, как полностью рассосаться, так и неравномерно застыть. При этом могут появиться на контуре рта пятна, которые будут отличаться по плотности и цвету от естественной поверхности губ.
При этом могут появиться на контуре рта пятна, которые будут отличаться по плотности и цвету от естественной поверхности губ.
Такой эффект не представляет опасности для здоровья, но выглядит неэстетично. Устранить его поможет косметолог, введя в губы средство для нейтрализации гиалуронки.
Когда будет «можно» алкоголь?
Для того чтобы быть уверенной в результативности процедуры по введению филлеров и свести к минимуму неудачные последствия, от алкогольных напитков желательно воздерживаться дней на 5, а лучше – на пару недель после процедуры. Такое ограничение относится не только к крепким напиткам, но и к слабоалкогольным.
Запрет на алкоголь – не единственное требование после введения гиалуронки. Обо всех нюансах использования декоративной и ухаживающей косметики, а также приема лекарств рекомендуется консультироваться у косметолога.
Прием спиртосодержащих напитков до введения гиалуронки
Косметологи, работающие с гиалуроновой кислотой, рекомендуют воздержаться от приема крепких напитков не только после процедуры, но и за несколько дней до нее. Это обстоятельство также влияет на результативность процедуры и прохождение периода восстановления.
Это обстоятельство также влияет на результативность процедуры и прохождение периода восстановления.
Кроме спиртосодержащих напитков, под запрет попадают продукты, которые могут вызывать аллергическую реакцию или приводить к обезвоживанию. Например, копчености, соленые и перченые блюда.
Рекомендуется не принимать алкогольные напитки на протяжении 3-4 дней перед процедурой.
Алкоголь после увеличения губ повышает риск побочных эффектов. Для того чтобы результат введения филлеров был хороший, необходимо воздержаться от принятия спиртного и соблюдать все рекомендации специалиста.
Отзывы людей
- Юлия, 33 года: Увеличить губы – это была моя мечта. Меня поймут девушки, у которых они настолько не объемные, что крась или не крась помадой – эффекта нет. Перед тем как решиться на инъекции гиалуронки, я изучила много отзывов на тематических форумах. Основная рекомендация – четко соблюдать все требования, которые озвучивает косметолог.
 А самого косметолога тоже нужно выбирать очень тщательно, ведь ему доверяешь свою внешность.
А самого косметолога тоже нужно выбирать очень тщательно, ведь ему доверяешь свою внешность. - Татьяна, 36 лет: Насчет алкоголя – запрет не случайный. Моя подруга его нарушила, и у нее весь гиалурон просто рассосался, как будто и не вводили. Ей было очень обидно – вложить деньги, и все впустую. Но она сама виновата – шампанское через несколько часов после филлеров было явно лишнее.
Материалы взяты с Plastichno.com
Алкоголь после биоревитализации | Швейцарская клиника омоложения Versua
При всем своем положительном эффекте на кожу биоревитализация — это все-таки стресс, после которого хочется расслабиться, позволив себе каплю алкоголя. Однако многие косметологи утверждают, что употребление спиртных напитков разрушает действие процедуры, а значит, время и деньги на профессиональное омоложение будут выброшены на ветер. Такой точки зрения придерживаются и врачи VERSUA Clinic. Потому что мы можем ее доказать.
Такой точки зрения придерживаются и врачи VERSUA Clinic. Потому что мы можем ее доказать.
Три причины не пить алкоголь после биоревитализации
- Любой спиртной напиток, даже легкое вино, ускоряет процесс выведения жидкости из организма. То же самое касается и гиалуроновой кислоты — основного компонента препарата для микроинъекций. А значит, эффект от процедуры станет значительно меньше, чем мог бы быть, так как кожа снова будет обезвоживаться, то есть вернется к своему исходному состоянию.
- Гиалуроновая кислота не только увлажняет ткани, но и расширяет сосуды. Такое же действие оказывает на капилляры и алкоголь. А значит, после употребления спиртных напитков они еще больше увеличатся в диаметре, что может привести к непредсказуемым последствиям.
- После микроинъекций всегда появляются небольшие отеки, вызванные подкожным введением препарата. Как правило, на следующий день после процедуры они проходят, однако если вы решите отпраздновать посещение косметолога, продолжительность изменений тканей лица увеличится.
 Отек «задержится», при этом он может распространиться на все тело.
Отек «задержится», при этом он может распространиться на все тело.
Когда спиртное не навредит?
Если употребление алкоголя планируется через 3-4 дня после биоревитализации. К этому времени не только сойдет отек, но и исчезнут папулы — объемные кожные образования, спровоцированные микроинъекциями. Однако конкретный срок должен определить специалист исходя из особенностей вашей кожи и ее реакции на препарат.
А вот употреблять любые спиртосодержащие напитки за 1-2 дня до проведения процедуры не рекомендуется, поэтому если на это время вы планируете банкет, его лучше перенести. Или же ограничить себя в реализации желаний.
Алкоголь после филлеров | Я КОСМЕТОЛОГ
Алкоголь после филлеров: можно ли совмещать спиртное с омолаживающими уколами?
Каких только страхов не написано в интернете по поводу сочетания горячительных напитков и инъекционных косметологических процедур. После прочтения многих таких статей можно прийти к выводу, что достаточно выпить бокал вина – и все, «совсем мертвый станешь».
Мы ни в коем случае не призываем употреблять алкоголь после инъекций филлеров гиалуроновой кислоты, равно как и до визита к косметологу. В то же время, именно спиртное многие считают причиной развития осложнений и/или отсутствия эффекта от процедуры – это неверно, поскольку никаких научных подтверждений подобным тезисам нет. Существенного вреда от небольшого количества спиртного, употребленного до процедуры или в раннем восстановительном периоде, не будет.
Почему же тогда косметологи призывают пациентов отказаться от «градусов» хотя бы на несколько первых дней после увеличения губ и заполнения морщин? Можно ли использовать этанол в качестве анестетика перед уколами? Правда ли, что из-за бокала вина филлер может в тот же день выйти из организма, не оказав никакого эффекта?
Как спиртное взаимодействует с гиалуроновой кислотой
При употреблении алкогольных напитков в нашем организме происходят следующие значимые изменения:
- В нервной системе – снижается чувствительность к боли и физическому дискомфорту, появляется многословность, раскрепощенность в движениях.
 При более высоких дозах возбуждение сменяется расслаблением, замедлением мышления и безразличием.
При более высоких дозах возбуждение сменяется расслаблением, замедлением мышления и безразличием. - Физически – учащается пульс, расширяются сосуды, что приводит к ускорению кровотока. Немного снижается мышечный тонус. По мере повышения концентрации этанола, происходит отток крови от кожных покровов, мышцы еще более расслабляются, мимика становится менее выразительной. Спустя несколько часов появляется умеренная отечность, которая достаточно быстро уходит.
Напрямую ни один из этих моментов не влияет ни на свойства вводимой гиалуроновой кислоты, ни на то, как именно наш организм «примет» филлер. Тем не менее, косметологи обычно рекомендуют воздержаться от алкоголя в день процедуры и еще 2-3 дня после нее. Этому есть вполне разумное объяснение.
Во-первых, в тех случаях, когда напитки «с градусом» употребляют непосредственно перед уколами, чтобы уменьшить возможные дискомфортные ощущения и психологически расслабиться:
- косметолог получает суетливую и многословную пациентку, работать с которой куда сложнее, чем со спокойной и сдержанной.
 При этом сами обезболивающие свойства алкоголя сильно переоценены – ни в какое сравнение со стандартным кремом-анестетиком они не идут;
При этом сами обезболивающие свойства алкоголя сильно переоценены – ни в какое сравнение со стандартным кремом-анестетиком они не идут; - временное снижение тонуса мимических мышц, характерное даже для легкого опьянения, мешает врачу оценить реальное состояние лица пациентки. В результате он может недоколоть или, наоборот, поставить немного больше филлера, чем требуется – это не приведет к сколько-нибудь серьезным последствиям, но и не даст получить максимально хороший результат.
Во-вторых, тем, кто планирует выпить сразу после процедуры и/или в течение нескольких ближайших дней, следует помнить, что:
- Этанол ускоряет ток крови, а значит неизбежные синяки и гематомы от инъекций могут быть крупнее, чем при полном отказе от алкоголя. Этот момент особенно важен при увеличении губ, поскольку именно в ходе этой процедуры травмируется максимальное количество сосудов.
- Средние и большие дозы спиртного приводят к обезвоживанию и последующему излишнему застою жидкости в тканях.
 Такой эффект заметно усилит ту отечность, которая в норме возникает после введения гиалуроновой кислотыиз-за повреждения тканей иглой – и лицо в течение 1-2 дней может выглядеть крайне непрезентабельно.
Такой эффект заметно усилит ту отечность, которая в норме возникает после введения гиалуроновой кислотыиз-за повреждения тканей иглой – и лицо в течение 1-2 дней может выглядеть крайне непрезентабельно. - Иногда излишне расслабленное состояние после спиртного мешает соблюдать стандартные правила, разработанные для снижения вероятности осложнений и закрепления эффекта от процедуры. Так, первые пару дней пациенту рекомендуется спать исключительно на спине, чтобы не было лишнего давления на только что вставший филлер – а с алкоголем контролировать себя ночью будет уже не так просто, как без него.
- Хуже всего, если речь идет не об 1-2 бокалах вина или пива за ужином после процедуры, а о более масштабных мероприятиях, когда помимо обильных «возлияний» предполагается посещение сауны или бани, а также употребление большого количества жирной, жареной, соленой и пряной пищи. От подобного времяпрепровождения в первые пару дней желательно отказаться, поскольку здесь речь идет о нарушении уже не одного, а сразу нескольких важных послепроцедурных ограничений.

Может ли употребление алкоголя после контурной пластики привести к осложнениям?
Косметологи склонны перекладывать ответственность за любые нежелательные последствия «уколов красоты» на пациентов. Однако, ни слабые, ни крепкие спиртные напитки не повышают вероятность появления каких либо побочек от инъекций гиалуроновых филлеров, кроме отечности и гематом. Все остальное, будь то фиброз, комкование геля, отсутствие результата процедуры и т.п. всегда имеет свои конкретные причины, никак не связанные с горячительными напитками:
- Если препарат «простоял» в тканях меньше, чем должен был. За включение гиалуроновой, полимолочной кислот, коллагена и прочих активных компонентов дермальных наполнителей в обмен веществ и, как следствие, их вывод из организма, отвечают ферменты. Для ГК, например, это гиалуронидаза. Активность этих ферментов определяется целым рядом условий, таких как возраст человека, состояние его здоровья, качество филлера, влияние повреждающих факторов среды (которых помимо алкоголя великое множество) и проч.
 Оценивать действие каждого из них по отдельности большого смысла нет, потому связывать подозрительно недолгий эффект инъекционного препарата только лишь с употреблением спиртного не стоит. Кратковременное повышение кровотока в тканях, вызываемое опьянением, тоже не имеет существенного влияния на скорость обменных процессов: расширение сосудов лица происходит по многу раз в течение дня, не только после спиртного, но и как реакция на эмоции, физическую нагрузку, изменение температуры и влажности воздуха и т.п.
Оценивать действие каждого из них по отдельности большого смысла нет, потому связывать подозрительно недолгий эффект инъекционного препарата только лишь с употреблением спиртного не стоит. Кратковременное повышение кровотока в тканях, вызываемое опьянением, тоже не имеет существенного влияния на скорость обменных процессов: расширение сосудов лица происходит по многу раз в течение дня, не только после спиртного, но и как реакция на эмоции, физическую нагрузку, изменение температуры и влажности воздуха и т.п. - Если эффекта не было вообще. Не секрет, что можно ввести под красную кайму губ 2 мл филлера, а спустя 1-2 дня не увидеть в зеркале практически никаких изменений. Но, скорее всего, в данном случае речь идет о поддельном или низкокачественном препарате. Винить в этом алкоголь будет неправильно: этиловый спирт никак не взаимодействует с компонентами геля, потому «рассосать» такое большое количество ГК он просто не в состоянии.
- Если появился фиброз. Гиалуроновая кислота обладает способностью активировать развитие соединительной ткани.
 Это происходит благодаря стимуляции деления клеток с увеличением числа фибробластов и активного синтеза коллагена и эластина. В умеренном количестве это дает омолаживающий лифтинговый эффект, в избыточном – приводит к рубцеванию, появлению под кожей плотных шишек. Спровоцировать чересчур активное развитие соединительной ткани могут инфекция, нарушение процессов заживления в результате недостатка кислорода (гипоксия), внешние воздействия. Спиртное в связи с кратковременным нахождением этилового спирта в организме оказать подобного влияния не в состоянии. Чуть более опасная в этом плане привычка – курение, так как помимо хронической интоксикации, никотин нарушает процесс насыщения тканей кислородом.
Это происходит благодаря стимуляции деления клеток с увеличением числа фибробластов и активного синтеза коллагена и эластина. В умеренном количестве это дает омолаживающий лифтинговый эффект, в избыточном – приводит к рубцеванию, появлению под кожей плотных шишек. Спровоцировать чересчур активное развитие соединительной ткани могут инфекция, нарушение процессов заживления в результате недостатка кислорода (гипоксия), внешние воздействия. Спиртное в связи с кратковременным нахождением этилового спирта в организме оказать подобного влияния не в состоянии. Чуть более опасная в этом плане привычка – курение, так как помимо хронической интоксикации, никотин нарушает процесс насыщения тканей кислородом.
При введении филлеров для увеличения губ, заполнения морщин и т.п., существует лишь одно ограничение, связанное с употреблением горячительных напитков: нельзя приходить на саму процедуру в нетрезвом виде, поскольку даже легкая степень опьянения станет серьезной помехой для косметолога. А вот употребление вина, шампанского, пива и даже чего-то покрепче за день и более до визита в клинику или салон – совсем не повод переносить сеанс на другую дату.
А вот употребление вина, шампанского, пива и даже чего-то покрепче за день и более до визита в клинику или салон – совсем не повод переносить сеанс на другую дату.
Точно также, нет оснований отказываться от употребления спиртного после «уколов красоты». Но тут нужно знать меру и учитывать индивидуальные особенности своего организма:
- не сочетать «градусы» с другими напитками и продуктами, которые могут способствовать задержке жидкости в тканях и усиливать отеки;
- не пить, если в ходе сеанса травмировано большое количество сосудов и есть риск формирования гематом.
В то же время, нет ни одного осложнения, которое вызывалось бы именно алкоголем. В тех случаях, когда результат процедуры оказался неудовлетворительным, искать причины необходимо с учетом всех факторов, которые могли повлиять на конечный результат: и качества дермального наполнителя, и техники введения, и профессионализма врача, выполнявшего инъекции. Не стоит валить все на бокал красного вина, если пациенту вводился контрафактный препарат сомнительного происхождения или просто у косметолога руки «не из того места растут».
можно ли пить до и после биоревитализации и мезотерапии
Главный «маяк», который направляет усилия разработчиков косметических процедур и препаратов, — красота. С момента создания синтетической гиалуроновой кислоты, мезотерапии и биоревитализации, красота перестала быть синонимом молодости. Эти инвазивные процедуры продемонстрировали, что сохранять ее можно в любом возрасте. И так же легко в любом возрасте ее потерять – если имеет место регулярное употребление алкоголя. Поэтому салонные омолаживающие процедуры находятся в постоянном противостоянии со спиртными напитками. Не имеет значения, чем наполнен бокал, разливным пивом или элитным коньяком, — гиалуроновая кислота и алкоголь не могут сосуществовать. Давайте разберемся почему.
Чем опасен алкоголь при инвазивных процедурах?
Изобретено много наружных средств, состав и действие которых сходится с составом коктейлей для мезотерапии, но их введение в структурные слои кожи оказалось более результативным. Наряду с тем – более рискованным. Тысячи клиенток, столкнувшихся с мезотерапией впервые, верят, что станут красавицами в первый же день после процедуры. Забыв, что обычная внутримышечная инъекция требует периода заживления, не говоря о манипуляциях с кожей лица.
Наряду с тем – более рискованным. Тысячи клиенток, столкнувшихся с мезотерапией впервые, верят, что станут красавицами в первый же день после процедуры. Забыв, что обычная внутримышечная инъекция требует периода заживления, не говоря о манипуляциях с кожей лица.
Отечность и припухлости, мелкие синячки вокруг точек введения иглы проходят быстро и рассасываются бесследно при нормальном образе жизни. Если принимать гомеопатические препараты, процесс заживления ускорится. Если принимать алкоголь после биоревитализации, посттравматическое состояние кожи может усугубиться. Много проколов – много точек риска. Даже терапевты, выписывающие пациентам курс инъекций лекарственных препаратов, запрещают пациентам пить крепкие напитки, не говоря о косметологах.
Инъекции с алкоголем несовместимы
Омолаживающих процедур, предполагающих инвазивное воздействие на кожу, немало: инъекции ботокса или диспорта, биоревитализация, биоармирование, мезотерапия и т.д. У каждой из них свой период вето на спиртные напитки. Длительность периода воздержания от приема спиртного установлена клинически, и для всех примерно одинакова. Но, учитывая образ жизни клиентки, врач-косметолог может внести свои коррективы.
Длительность периода воздержания от приема спиртного установлена клинически, и для всех примерно одинакова. Но, учитывая образ жизни клиентки, врач-косметолог может внести свои коррективы.
Вернуться к оглавлению
Алкоголь до и после мезотерапии
Мезотерапия предполагает множество микроинъекций со специальным витаминным коктейлем. Каждая лаборатория предлагает свой эффективный рецепт мезококтейля, но все они включают такие компоненты:
- сосудорасширяющие средства;
- витамины;
- гиалуроновая кислота;
- гликолевая кислота.
Ни один из перечисленных ингредиентов не «дружит» со спиртным. Алкоголь тоже расширяет сосуды, а это дополнительное усиление кровотока и еще большее расширение сосудов. И мезококтейль, во-первых, будет свободно циркулировать в дерме, а во-вторых, не в том направлении, которое нужно для эстетической коррекции лица.
Витамины под действием алкоголя разрушаются, и не оказывают исцеляющего воздействия. Их наличие в мезококтейлях неслучайно: они помогают усваиваться другим компонентам, обеспечивают глубокое питание кожи и стимулируют быстрое восстановление после процедуры. Последствия их нейтрализации или других способов взаимодействия с алкоголем предсказать невозможно.
Последствия их нейтрализации или других способов взаимодействия с алкоголем предсказать невозможно.
Гиалуроновая кислота, которая является ключевым компонентом любого препарата для омолаживающих инъекционных операций, во-первых, выводится быстрее, и эффект от процедуры не будет продолжителен. Во-вторых, она вводится только в области, обозначенные косметологом заранее. Значит, именно там кожа разрушается под действием возрастных изменений в ее структуре, потеряла упругость и т.д. Доза гиалуроновой кислоты в других зонах может оказаться неуместной, тем не менее, по расширенным сосудам она попадет в непредусмотренные области кожи.
Из-за алкоголя гиалуроновая кислота может попасть в непредусмотренные места
Мезотерапия и алкоголь несовместимы! Лучше не принимать алкогольных напитков на протяжении 2-3 суток перед процедурой и в течение минимум 3-4 суток после. Четких временных границ косметологи не дают, но если клиент хочет стойкого результата, 5-7 суток без спиртного отлично способствуют этому.
Вернуться к оглавлению
Биоревитализация и алкоголь
Механизм действия и ход проведения процедуры делают ее похожей на мезотерапию. Биоревитализация представляет собой инъекционную методику омолаживания кожи и запуска в ней естественного синтеза волокон, необходимых для предотвращения старения. Препарат, основанный на гиалуроновой кислоте вводится в структурные слои кожи с помощью тонкой иглы.
От гиалуроновой кислоты во многом зависит состояние внешних слоев кожи. Она обеспечивает гидратацию кожи, притягивая молекулы воды. Спиртные напитки, мягко говоря, не способствуют увлажнению кожи, поэтому лучше не пытаться совместить гиалуроновую кислоту с ними.
Кроме того, как было сказано, расширенные сосуды препятствуют фиксации гиалуроновой кислоты в зоне инъекций. Усиление кровотока некстати и до, и после сеансов процедуры, поэтому посещение сауны, прием алкогольных напитков и пребывание под ультрафиолетовыми лучами придется исключить.
Можно ли принимать алкоголь после биоревитализации? Сразу – нельзя, это может стать причиной сильных отеков. Некоторые косметологи утверждают, что употреблять спиртное позволительно через 6-8 часов после сеанса, но зная о процессах, спровоцированных алкоголем, лучше повременить хотя бы 1-2 суток.
Некоторые косметологи утверждают, что употреблять спиртное позволительно через 6-8 часов после сеанса, но зная о процессах, спровоцированных алкоголем, лучше повременить хотя бы 1-2 суток.
Алкоголь сам по себе, без посторонних факторов, провоцирует отечность. Достаточно вспомнить, какое лицо утром у людей, у которых накануне была вечеринка. Инъекционные методики тоже имеют отечность в числе побочных явлений в реабилитационный период. Не нужно усложнять ситуацию, чтобы потом сомневаться в профессионализме врачей, эффективности препаратов и обвинять всех вокруг в случае нежелательных последствий.
Поделитесь статьей с друзьями:
Можно ли пить алкоголь перед процедурой увеличения губ?
Содержание статьи
Решившись стать обладательницами соблазнительных пухлых губок, некоторые представительницы прекрасного пола не задумываются о том, можно ли перед этой манипуляцией употреблять спиртное. И напрасно не задумываются.
И напрасно не задумываются.
Несмотря на то, что инъекции «гиалуронки» по мнению специалистов в области эстет-медицины считаются минимально травматичными, стоит обратить внимание на слово «инъекция». Любой укол это, все-таки, травмирование кожного покрова, к тому же, введенная в ткани гиалуроновая кислота первое время будет рассматриваться организмом очаровательной барышни как некий чужеродный агент. Так зачем усугублять ситуацию еще и градусами?
Если вам кажется, что ничего страшного от пары бокалов Мартини или рюмочки элитного Hennessy, выпитых накануне похода в косметологический салон, не случится, то вы однозначно ошибаетесь. Думаете, что алкоголь может выступать в роли анестезии? Увы, все это скорее на уровне самовнушения: на самом деле толку от такого лже-обезболивания не будет, а вот навредить ожидаемому от процедуры результату и увеличить продолжительность восстановительного этапа принятое спиртное очень даже способно.
Почему категоричное «нет»?
Этанол имеет свойство приводить к обезвоживанию (дегидратации) организма. Естественно, чем внушительнее концентрация спирта, тем больше вы теряете жидкости. Покажется удивительным, но наравне с обезвоживанием, прием алко может спровоцировать и задержку жидкости — отсюда чрезмерные отеки, повышение АД и прочие «прелести», которые совершенно вам не нужны в дополнение к некоторому дискомфорту, который и так возникнет в процессе увеличения губ «гиалуронкой».
Временные синячки, припухлость и покраснение в местах проколов вам, к сожалению, и без спиртного обеспечены, но после употребления алкоголя эти неэстетичные проявления будут выражены еще ярче и острее.
За сколько нужно прекратить прием алкоголя
Обычно косметологи, выполняющие биоревитализацию (ИНЪЕКЦИИ), рекомендуют женщинам отказаться от приема крепких напитков за 3-4 дня до процедуры, со слабым алкоголем милым дамам придется «завязать» не менее чем за 24 часа, а лучше за полтора суток до предстоящих инъекций гиалуроновой кислоты.
Чтобы точнее определиться с содержанием в крови этанола, не будет лишним прибегнуть к более точным расчетам, связанным с дозой последнего приема спиртного и собственным весом. Не думайте, что это очень сложно — есть масса способов сделать это по специальным формулам или таблицам. Один из эффективных способов определить «уровень градуса» в организме — воспользоваться довольно простой формулой, которую вывел именитый химик из Швеции Эрик Видмарк.
С = А/(m*r) – вот он, этот вполне удобный алко-калькулятор, который вы можете применить на практике для достаточно верных расчетов. Здесь С будет итоговым показателем концентрации алкоголя в крови (в промилле), A — масса выпитого спиртного (в гр), m — масса вашего тела (в кг), r — коэффициент распределения по Видмарку (для дам он составляет 0,6). Как видите, сложностей никаких нет, формула реально элементарная, но дает вполне точный результат.
При необходимости вы можете использовать другие варианты подсчета, например, таблицы, где указывается вес/рост, количество «принятого на грудь» и примерное время выведения этанола из крови. Единственное, что можно сказать однозначно, пить перед походом к мастеру сферы бьюти-индустрии не стоит. Красота, хоть и требует жертв, но приносить ей в виде агнца свое здоровье из-за принятой рюмочки не нужно.
Единственное, что можно сказать однозначно, пить перед походом к мастеру сферы бьюти-индустрии не стоит. Красота, хоть и требует жертв, но приносить ей в виде агнца свое здоровье из-за принятой рюмочки не нужно.
По материалам косметологической клиники BeBeauty Clinic в г. Симферополь.
совместимость, почему нельзя пить спиртное
Процедура и этанол
Процедура воздействия на клетки кожи и межклеточное пространство с помощью гиалурона нередко провоцирует побочные проявления. Независимо от того, каким способом проводится биоревитализация, организм реагирует на адаптацию введенного полисахарида общими и местными реакциями, вплоть до отторжения введенного материала.
Виды процедур
Косметологи проводят курс восстановления контура лица и упругости кожи двумя основными способами:
- введением полисахарида с помощью инъекции;
- проведением молекул гиалурона в подкожную зону воздействием инфракрасных лучей.

Эффект от первого и второго способов одинаковый, рекомендации косметологов после курсов также одни и те же: главное – это запрет на алкоголь до и после процедуры с применением Гиалуроновой кислоты.
Влияние этила на кожу
Воздействие этанола на кожный покров зависит от качества и количества, а также частоты потребления напитка, содержащего спирт. Считается, что один или два бокала качественного вина не воздействуют на кожу, но крепкие напитки, особенно если принимать их часто и в больших количествах, способны провоцировать существенное изменение внешности.
- Уменьшается количество жидкости в подкожном эпителии, тем самым провоцируется обезвоживание на клеточном уровне. Как следствие, появление мелких и мимических морщин.
- Этанол способен уничтожать важные витамины С и Е, которые напрямую участвуют в процессах производства коллагена. Алкоголь вместе с Гиалуроновой кислотой способен полностью аннулировать эффект от курса процедур.

- Употребление спиртных напитков провоцирует вывод жидкости в пространство между клеток, отечность тканей лица. Аллергический отек, возникающий в результате инъекций гиалурона, провоцирует увеличение проявлений побочного эффекта и аллергического ответа на препарат.
Совместимость молекул этанола и белков гиалурона практически нулевая, потому часто они вступают в конфликт между собой при одновременном попадании в организм.
Механизмы противодействия
Спиртное с Гиалуроновой кислотой не просто отказывается взаимодействовать, но, зачастую, вступает в противодействие. Состав вещества, вводимого под кожу содержит не только Гиалуроновую кислоту, но также и витаминные комплексы, другие кислоты и вспомогательные вещества. Специалисты обращают внимание на то, что ни один ингредиент «омолаживающего коктейля» не желает «дружить» с этанолами в силу ряда причин:
- Спирт способен разрушать витаминные компоненты, в том числе и те, которые добавляют в состав Гиалуронового коктейля.

- Период выведения активного вещества под воздействием алкоголя значительно сокращается, уменьшая тем самым время продолжительность качественного эффекта от курса.
- Способность этанола расширять сосуды, увеличивая тем самым их проницаемость, способствует тому, что вместе с действенными компонентами в сосуды проникают одновременно и несовместимые вещества. Возможен также и эффект наоборот: Гиалуроновая кислота проникнет в области, не предназначенные для коррекции.
Категорически нельзя также и после введения Гиалуроновой кислоты пить алкоголь в любых количествах, даже незначительных. Реакция, которая последует в организме после «встречи» этих несовместимых веществ, может привести к непростым последствиям: сложные отеки в зоне коррекции, некроз тканей в обработанной области, гематомы и посинение губы, окологубной зоны.
Пить алкоголь разрешено не ранее, чем спустя неделю после курса процедур или за 10 дней перед тем, как делать биоревитализацию.
Источник:
РЛС: https://www.rlsnet.ru/mnn_index_id_2664.htm
Нашли ошибку? Выделите ее и нажмите Ctrl + Enter
ГИАЛУРОНОВАЯ КИСЛОТА ИНЪЕКЦИИ И АЛКОГОЛЬ. Ивантеевка. Узнать стоимость
Это значит, что препарат может не усвоиться и процедуру, возможно, придется проводить раз за разом не наблюдая эффекта. К сожалению, это далеко не самое неприятное последствие приема алкоголя в сочетании с гиалуроновой кислотой. Если Вы выбрали инъекционный метод введения, то помните, что побочным эффектом часто становится возникновение гематом, отеков и покраснений. Если учесть, что после приема даже небольшого количества алкоголя на следующее утро отечность повышается, нетрудно представить, как она усилится если совмещать алкоголь и гиалуроновую кислоту. Инъекционное вмешательство влечет за собой полный запрет на спиртное независимо, какое вещество вводится в организм.
ГИАЛУРОНОВАЯ КИСЛОТА ИНЪЕКЦИИ И АЛКОГОЛЬ
Образуя, при введении вязкую гелеобразную массу, гиалуронат распределяется в проблемных зонах и из водных запасов и начинает интенсивно питать и увлажнять кожу. Благодаря способности к активному увлажнению это вещество противостоит старению и увяданию кожных покровов. Алкоголь после гиалуроновой кислоты иссушает и обезвоживает, что сводит увлажняющий эффект на нет.
Благодаря способности к активному увлажнению это вещество противостоит старению и увяданию кожных покровов. Алкоголь после гиалуроновой кислоты иссушает и обезвоживает, что сводит увлажняющий эффект на нет.
В результате могут получиться не только обширные гематомы, но и неприятное осложнение как выход препарата за пределы инъекционной зоны. Таким образом, можно получить не только видимые невооруженным взглядом бугорки и неровности, но и явную асимметрию лица. Если вовремя не обратиться в клинику, то все это может повлечь за собой осложнения: некроз, абсцесс, фиброз. В этом случае не избежать хирургического вмешательства. Лучшим решением будет не принимать алкоголь за 5–7 дней до и после уколов или других косметологических процедур, связанных с гиалуроновой кислотой. Помните, что «безопасных укольчиков для лица» не существует, и любое вмешательство должно сопровождаться соблюдением всех правил безопасности.
Совместимость алкоголя и гиалуроновой кислоты. Гиалуроновая кислота, это источник молодости и красоты нашей кожи.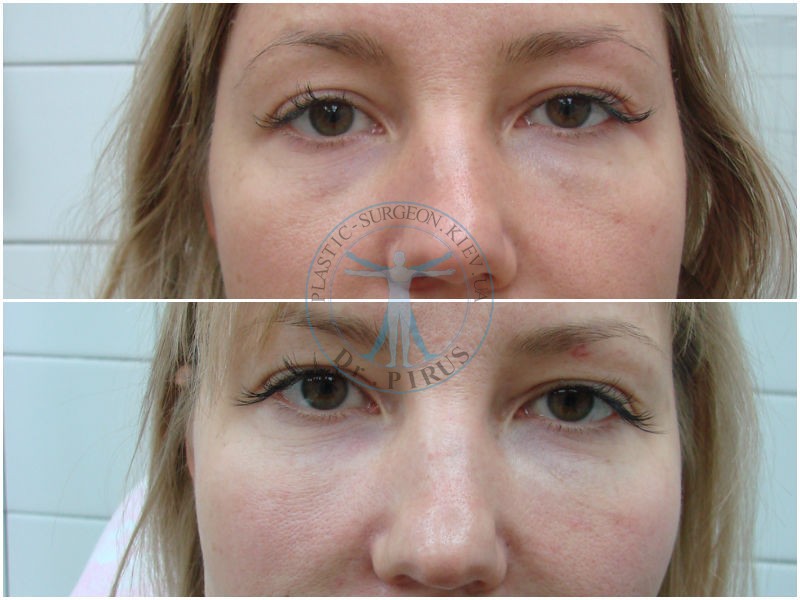 Существует огромное количество косметических средств на ее основе. Сюда входят и крема, и сыворотки, и маски. Но нельзя отрицать что стойкий и выраженный эффект применения гиалуроновой кислоты достигается в случае, если имеется возможность прибегнуть к салонным процедурам. Существуют инъекционные и безинъекционные способы попадания гиалуронки в эпидермис, где образуются запасы питательной жидкости, которые стимулируют процессы омоложения.
Существует огромное количество косметических средств на ее основе. Сюда входят и крема, и сыворотки, и маски. Но нельзя отрицать что стойкий и выраженный эффект применения гиалуроновой кислоты достигается в случае, если имеется возможность прибегнуть к салонным процедурам. Существуют инъекционные и безинъекционные способы попадания гиалуронки в эпидермис, где образуются запасы питательной жидкости, которые стимулируют процессы омоложения.
К инъекционным методам относят мезотерапию и биоревитализацию. Главным отличием между ними считается состав вещества, вводимого под кожу. При биоревитализации это чистая гиалуроновая кислота, иногда с добавлением обезболивающего препарата. Для мезотерапии используются лечебно-косметические гели, в состав которых кроме гиалуроната входят различные питательные вещества, в зависимости от производителя и цели использования. Для того чтобы удостовериться, что инъекции гиалуроновой кислоты вам подходят необходимо проходить соответствующие анализы на аллергические реакции.
Кроме этого, алкоголь обладает выраженным сосудорасширяющим эффектом, в том числе если употреблять его до начала сеанса. Это приведет к самым непредсказуемым реакциям организма, поскольку сосуды, расширяясь, могут влиять на распределение вещества в эпидермисе. Четко обозначенные зоны инъекции предполагают, что гиалуроновая кислота займет именно то место, где имеются проблемы и где ее присутствие не будет нежелательным.
Методы введения препарата. К безинъекционным методам относится внедрение гиалуроновой кислоты при помощи различных специализированных аппаратов, таких как: Электропорация. Под воздействием электрических импульсов вещество проникает в эпидермис через микроканалы, Лазерная гиалуронопластика влияет через потовые железы при помощи излучения, Ионофорез отличается от лазерной методики только оборудованием и осуществляется с помощью стабильного гальванического тока, Криомезотерапия — это сочетанием двух методов: электропорации и охлаждения, Аквафорез-комбинацией и включает в себя лазерную, лимфодренажную терапию, и электромиостимуляцию. Магнитофорез, ультрафонофорез предполагают воздействие путем магнитных и ультразвуковых волн.
Магнитофорез, ультрафонофорез предполагают воздействие путем магнитных и ультразвуковых волн.
Далее следует подготовка кожи к процедурам. После каждого сеанса необходим восстановительный период, поскольку инвазивный метод предполагает наличие микроповреждений на коже. В этот момент очень важно последовательно выполнять все рекомендации косметолога, даже если они кажутся вам излишне требовательными. Довольно часто помимо прочих вопросов пациентов волнует можно ли пить спиртное после того как процедура была выполнена? В этом случае необходимо представлять себе каким образом воздействуют на наш организм гиалуроновая кислота и алкоголь, поскольку механизмы их совершенно противоположны и совместимость стремится к нулю. Эффективность и побочные действия. Молекулы гиалуроновой кислоты притягивают и удерживают воду достигая соотношения 1 к 500 или даже 1 к 1000.
ГИАЛУРОНОВАЯ КИСЛОТА ИНЪЕКЦИИ
При условии, что вы остановили свой выбор на квалифицированном и добросовестном специалисте, перед проведением сеанса он соберет данные о вашем анамнезе, образе жизни и вредных привычках. Пациенту будет озвучен список того, что нельзя делать во избежание усиления побочных эффектов или возникновения осложнений.
Пациенту будет озвучен список того, что нельзя делать во избежание усиления побочных эффектов или возникновения осложнений.
Смотрите также
Гиалуроновая кислота отменяет этанол-зависимое ингибирование биосинтеза коллагена в культивируемых фибробластах человека
Drug Des Devel Ther. 2015; 9: 6225–6233.
Магдалена Донейко
1 Кафедра эстетической медицины, Медицинский университет Белостока, Белосток, Польша
Анджей Пржилипяк
1 Кафедра эстетической медицины, Медицинский университет Белостока
, Белосток, Польша
2 Кафедра медицинской химии, Медицинский университет Белостока, Белосток, Польша
Войцех Милтык
3 Кафедра фармацевтического анализа, Фармацевтический факультет, Медицинский университет Белостока, Белосток, Белосток
Кафедра эстетической медицины, Медицинский университет Белостока, Белосток, Польша
Ежи Пжилипяк
4 Медицинский офис, Белосток, Польша
Илона Заремба
2 ł Кафедра медицинской химии Беловостокского медицинского университета Польша
Аркадиуш Суразиньс ki
2 Кафедра медицинской химии Белостокского медицинского университета, Белосток, Польша
1 Кафедра эстетической медицины Белостокского медицинского университета, Белосток, Польша
2 Кафедра медицинской химии медицинского университета Белосток, Белосток, Польша
3 Кафедра фармацевтического анализа, Фармацевтический факультет, Белостокский медицинский университет, Белосток, Польша
4 Медицинский офис, Белосток, Польша
Переписка: Магдалена, Медицинский факультет, Эстонский факультет of Pharmacy, Медицинский университет Белостока, улица Академицкая 3, 15-267 Белосток, Польша, Email moc. liamg @ okjenod Авторские права © 2015 Donejko et al. Эта работа опубликована Dove Medical Press Limited и находится под лицензией Creative Commons Attribution — Non Commercial (unported, v3.0) License. Полные условия лицензии доступны по адресу http://creativecommons.org/licenses/by-nc/3.0 /. Некоммерческое использование работы разрешено без какого-либо разрешения Dove Medical Press Limited при условии правильной ссылки на эту статью. Эта статья цитируется в других статьях PMC.
liamg @ okjenod Авторские права © 2015 Donejko et al. Эта работа опубликована Dove Medical Press Limited и находится под лицензией Creative Commons Attribution — Non Commercial (unported, v3.0) License. Полные условия лицензии доступны по адресу http://creativecommons.org/licenses/by-nc/3.0 /. Некоммерческое использование работы разрешено без какого-либо разрешения Dove Medical Press Limited при условии правильной ссылки на эту статью. Эта статья цитируется в других статьях PMC.
Abstract
Введение
Целью исследования было оценить влияние этанола на биосинтез коллагена в культивируемых фибробластах кожи человека и роль гиалуроновой кислоты (HA) в этом процессе.Что касается механизма действия этанола на фибробласты кожи человека, мы исследовали: экспрессию интегрина β 1 и рецептора инсулиноподобного фактора роста 1 (IGF-IR), экспрессию белков сигнального пути: митоген-активированные протеинкиназы (MAPK), протеинкиназы. B (Akt), ядерный фактор, каппа B (NF-κB), фактор транскрипции, анализ цитотоксичности и апоптоза, активность металлопротеиназы, а также влияние HA на эти процессы.
Материалы и методы
Биосинтез коллагена, активность пролидазы, биосинтез ДНК и цитотоксичность были измерены в конфлюэнтных культурах фибробластов кожи человека, обработанных 25, 50 и 100 мМ этанолом, этанолом и 500 мкг / мл HA.Вестерн-блот-анализ и зимография были выполнены для оценки экспрессии коллагена типа I, рецептора интегрина β 1 , IGF-IR, белка NF-κB, белка фосфо-Akt, киназы MAPK, активности каспазы 9 и матриксных металлопротеиназ (MMP-9). и ММП-2).
Результаты
Дозозависимый этанол приводит к нарушению биосинтеза коллагена в культурах фибробластов за счет снижения активности пролидазы и экспрессии интегрина β 1 и IGF-IR. Это сопровождалось повышенной цитотоксичностью, апоптозом и снижением экспрессии белков сигнального пути, индуцированных интегрином β 1 и IGF-IR, то есть киназами MAPK (ERK 1/2 ).Пониженное количество синтезированного коллагена и нарушение активности пролидазы также может быть связано с активацией фактора транскрипции NF-κB, который подавляет экспрессию гена коллагена. Это предполагает, что снижение продукции коллагена фибробластами может быть вызвано нарушением его биосинтеза, но не деградацией. Применение ГК оказывает защитное действие на нарушения, вызванные исследуемыми веществами. По-видимому, регуляторный механизм индуцированной этанолом аберрации коллагена имеет место на уровне биосинтеза коллагена, поскольку не было обнаружено влияния этанола и ГК на процесс деградации коллагена ММП-2 и ММП-9.
Это предполагает, что снижение продукции коллагена фибробластами может быть вызвано нарушением его биосинтеза, но не деградацией. Применение ГК оказывает защитное действие на нарушения, вызванные исследуемыми веществами. По-видимому, регуляторный механизм индуцированной этанолом аберрации коллагена имеет место на уровне биосинтеза коллагена, поскольку не было обнаружено влияния этанола и ГК на процесс деградации коллагена ММП-2 и ММП-9.
Заключение
Это исследование предоставляет доказательства того, что этанол нарушает метаболизм коллагена в фибробластах кожи человека, что приводит к значительному снижению количества продуцируемого белка. Этот механизм, вероятно, связан с подавлением активности пролидазы, экспрессии интегрина β 1 и рецепторов IGF-IR, а также белков сигнального пути, индуцированных этими рецепторами.
Ключевые слова: коллаген , этанол, гиалуроновая кислота, фибробласты
Введение
Воздействие этанола (этилового спирта) может вызывать множество местных и систематических нарушений. Органы, которые особенно страдают от интоксикации этанолом, — это легкие, почки и печень.1 Было показано, что интоксикация этанолом вызывает окислительный стресс, что приводит к модуляции экспрессии металлопротеиназ и тканевых ингибиторов матриксных металлопротеиназ (ММП) в клетках сердца и печени, способствующих развитию изменения клеточного фенотипа на фибробластоподобные с дальнейшими последствиями в накоплении тканевого коллагена и фиброзе.2,3 В нескольких исследованиях задокументировано этанол-зависимое окислительное повреждение в печени.Было обнаружено, что механизм этого процесса может включать функцию митохондрий и выживаемость клеток.1 Таким образом, цитотоксичность этанола может способствовать апоптозу клеток или может вызывать провоспалительные цитокины.4 Было обнаружено, что алкоголь ингибирует рост клеток карциномы молочной железы человека MCF-7 в vitro.5
Органы, которые особенно страдают от интоксикации этанолом, — это легкие, почки и печень.1 Было показано, что интоксикация этанолом вызывает окислительный стресс, что приводит к модуляции экспрессии металлопротеиназ и тканевых ингибиторов матриксных металлопротеиназ (ММП) в клетках сердца и печени, способствующих развитию изменения клеточного фенотипа на фибробластоподобные с дальнейшими последствиями в накоплении тканевого коллагена и фиброзе.2,3 В нескольких исследованиях задокументировано этанол-зависимое окислительное повреждение в печени.Было обнаружено, что механизм этого процесса может включать функцию митохондрий и выживаемость клеток.1 Таким образом, цитотоксичность этанола может способствовать апоптозу клеток или может вызывать провоспалительные цитокины.4 Было обнаружено, что алкоголь ингибирует рост клеток карциномы молочной железы человека MCF-7 в vitro.5
Кажется, что этанол особенно влияет на биосинтез коллагена I типа. Этот процесс происходит в основном в клетках печени, но также наблюдается и в клетках кожи. Воздействие этанола на кожу привело к появлению многих дерматологических аномалий, таких как ладонная эритема, полнокровие, инфекции и приливы.6 Биопсии, полученные с кожи доноров, злоупотребляющих алкоголем, подтвердили аномалию структуры ткани, а изолированные фибробласты вызвали длительное время пролиферации.6 Некоторые данные предполагают, что этанол может влиять на заживление ран, вмешиваясь в биосинтез коллагена I и III.7 Этанол обычно используется в косметике, фармацевтика и дезинфицирующие средства.8,9 Большое количество спиртов используется в качестве разбавителей, консервантов, ингредиентов увлажняющих веществ или ароматизаторов в косметических средствах, наносимых на кожу.9,10 Концентрация этанола в продукте для типичного применения может варьироваться от менее чем От 1% до 96.9%.
Воздействие этанола на кожу привело к появлению многих дерматологических аномалий, таких как ладонная эритема, полнокровие, инфекции и приливы.6 Биопсии, полученные с кожи доноров, злоупотребляющих алкоголем, подтвердили аномалию структуры ткани, а изолированные фибробласты вызвали длительное время пролиферации.6 Некоторые данные предполагают, что этанол может влиять на заживление ран, вмешиваясь в биосинтез коллагена I и III.7 Этанол обычно используется в косметике, фармацевтика и дезинфицирующие средства.8,9 Большое количество спиртов используется в качестве разбавителей, консервантов, ингредиентов увлажняющих веществ или ароматизаторов в косметических средствах, наносимых на кожу.9,10 Концентрация этанола в продукте для типичного применения может варьироваться от менее чем От 1% до 96.9%.
Гиалуроновая кислота (ГК) оказалась полезным средством при заживлении ран и воспалительных процессах. Это подтверждено исследованиями in vivo и in vitro.11,12 Примерно половина продуцируемого гиалуронана синтезируется фибробластами и находится во внеклеточном матриксе кожи. Связывание HA с кластером дифференцировки 44 (CD44) и рецептором для подвижности, опосредованной гиалуроновой кислотой (RHAMM) на фибробластах, может влиять на передачу сигналов, тем самым регулируя рост, дифференцировку, адгезию и синтез коллагена клеток.13 Синтез коллагена в фибробластах может запускаться разными способами, одним из которых является пролидаза-зависимый механизм. 12
Связывание HA с кластером дифференцировки 44 (CD44) и рецептором для подвижности, опосредованной гиалуроновой кислотой (RHAMM) на фибробластах, может влиять на передачу сигналов, тем самым регулируя рост, дифференцировку, адгезию и синтез коллагена клеток.13 Синтез коллагена в фибробластах может запускаться разными способами, одним из которых является пролидаза-зависимый механизм. 12
Механизм защитного действия ГК в отношении нарушений метаболизма коллагена при воздействии этанола неизвестен. Поэтому мы сосредоточились на механизме индуцированного этанолом подавления биосинтеза коллагена и роли ГК в этом процессе. Чтобы изучить и охарактеризовать потенциальные негативные последствия воздействия этанола на фибробласты кожи, мы исследовали его влияние на экспрессию коллагена I типа, интегрина β 1 и рецептора инсулиноподобного фактора роста 1 (IGF-IR), фосфорилированных митоген-активируемых. протеинкиназы (MAPKs: ERK 1 / ERK 2 ), протеинкиназа B (Akt), ядерный фактор, усиливающий легкую каппа-цепь активированных B-клеток (NF-κB), каспаза 9 и активность пролидазы в культивированные фибробласты кожи человека.
Материалы и методы
Культура клеток
Первичный дермальный фибробласт: нормальный, человек, взрослый ATCC ® PCS-201-012 ™ был приобретен в ATCC (Манассас, Вирджиния, США), а натриевая соль HA H5542 была приобретена у Sigma -Олдрич (Сент-Луис, Миссури, США). Клетки поддерживали в среде Игла, модифицированной Дульбекко, с добавлением 10% фетальной бычьей сыворотки (HyClone Laboratories, Логан, Юта, США), 2 мМ глутамина, 50 Ед / мл пенициллина и 50 мкг / мл стрептомицина при 37 ° C в 5 % CO 2 инкубатор.Клетки использовали между пассажами 10 и 14 для всех экспериментов. Получено этическое разрешение Белостокского медицинского университета на использование линий клеток человека.
Синтез коллагена
Включение радиоактивного предшественника в белки измеряли после мечения конфлюэнтных фибробластов, культивируемых в питательной среде с различными концентрациями этанола и HA 500 мкг / мл в течение 24 часов в бессывороточной среде с 5 [ 3 H] пролин (5 мкКи / мл, 28 Ки / ммоль). Количество включенной метки в коллаген определяли путем переваривания белков очищенной коллагеназой Clostridium histolyticum по методу Петеркофски и Дигельмана.14
Количество включенной метки в коллаген определяли путем переваривания белков очищенной коллагеназой Clostridium histolyticum по методу Петеркофски и Дигельмана.14
Определение активности пролидазы
Активность пролидазы измеряли с использованием метода, описанного Myara et al. Концентрацию белка измеряли методом Lowry et al.16. Клетки собирали перед центрифугированием при 200 × g в течение 15 минут. От супернатанта отказались.Затем осадок ресуспендировали в (4- (2-гидроксиэтил) -1-пиперазинэтансульфоновой кислоте (HEPES) (50 мМ, pH 7,8) и разрушали ультразвуком (3 × 10 секунд при температуре 0 ° C). После этого следовало центрифугирование при 12000 × г в течение 30 минут при 4 ° C, и белок был определен в супернатанте, и была проанализирована активность пролидазы. Затем 100 мкл пробы супернатанта клеточного экстракта были смешаны с HEPES (100 мкл, 50 мМ, pH 7,8. ), который содержал MnCl 2 (для достижения конечной концентрации 1 мМ MnCl 2 ). Образцы инкубировали при 37 ° C в течение 24 часов перед тем, как инициировать введение 100 мкл 94 мМ глицилпролина (Gly-Pro) для достижения 47 мМ конечной концентрации Gly-Pro. Затем образцы инкубировали при 7 ° C в течение 60 минут и реакцию останавливали добавлением 0,45 М трихлоруксусной кислоты (TCA) (порция 1 мл). TCA добавляли в параллельные неиспользованные пробирки в «нулевой момент». Затем следовало центрифугирование образцов в течение 15 минут при 10,000 × g . Определение пролина происходило путем добавления TCA / супернатанта (0.5 мл) к смеси (1: 1) ледяной уксусной кислоты / реактива Чинарда. Затем все инкубировали при 90 ° C в течение 10 минут. Колориметрию (поглощение при 515 нм) использовали для определения пролина по отношению к стандартам пролина. Результаты выражали в наномолях пролина, высвобождаемого в минуту на миллиграмм белка.
Образцы инкубировали при 37 ° C в течение 24 часов перед тем, как инициировать введение 100 мкл 94 мМ глицилпролина (Gly-Pro) для достижения 47 мМ конечной концентрации Gly-Pro. Затем образцы инкубировали при 7 ° C в течение 60 минут и реакцию останавливали добавлением 0,45 М трихлоруксусной кислоты (TCA) (порция 1 мл). TCA добавляли в параллельные неиспользованные пробирки в «нулевой момент». Затем следовало центрифугирование образцов в течение 15 минут при 10,000 × g . Определение пролина происходило путем добавления TCA / супернатанта (0.5 мл) к смеси (1: 1) ледяной уксусной кислоты / реактива Чинарда. Затем все инкубировали при 90 ° C в течение 10 минут. Колориметрию (поглощение при 515 нм) использовали для определения пролина по отношению к стандартам пролина. Результаты выражали в наномолях пролина, высвобождаемого в минуту на миллиграмм белка.
Биосинтез ДНК
Изучено влияние исследуемых веществ на включение фибробластов [ 3 H] -тимидина. В 24-луночные чашки для культур ткани клетки высевали из расчета 1 × 10 5 клеток / лунку, используя 1 мл ростовой среды в каждой лунке. Через 48 часов (1,6 ± 0,1 × 10 5 клеток / лунку) в лунки для культивирования добавляли различные концентрации этанола с 500 мкг / мл гиалуронана или без него на 24 часа при 37 ° C. После этого в лунки добавляли 0,5 мкКи [ 3 H] -тимидина (6,7 Ки / ммоль) и культуры инкубировали при 37 ° C в течение 4 часов. Затем клетки промывали трижды 1 мл 0,05 М трис-HCl и дважды 5% ТХК. После этого проводили лизис клеток в 1 мл 0,1 М NaOH, содержащем 1% додецилсульфат натрия (SDS).Затем добавляли 4 мл сцинтилляционной жидкости и измеряли радиоактивность на сцинтилляционном счетчике.
Через 48 часов (1,6 ± 0,1 × 10 5 клеток / лунку) в лунки для культивирования добавляли различные концентрации этанола с 500 мкг / мл гиалуронана или без него на 24 часа при 37 ° C. После этого в лунки добавляли 0,5 мкКи [ 3 H] -тимидина (6,7 Ки / ммоль) и культуры инкубировали при 37 ° C в течение 4 часов. Затем клетки промывали трижды 1 мл 0,05 М трис-HCl и дважды 5% ТХК. После этого проводили лизис клеток в 1 мл 0,1 М NaOH, содержащем 1% додецилсульфат натрия (SDS).Затем добавляли 4 мл сцинтилляционной жидкости и измеряли радиоактивность на сцинтилляционном счетчике.
Анализ цитотоксичности
Жизнеспособность клеток оценивали с помощью анализа метилтиазолилтетразолия (МТТ), который основан на превращении желтого тетразолийбромида МТТ в пурпурное производное формазана митохондриальным ферментом сукцинатдегидрогеназой в жизнеспособных клетках. В конце инкубационного периода среду переносили в 96-луночные планшеты для определения цитокинов.Клетки промывали 0,2 мл фосфатно-солевого буфера и анализировали на цитотоксичность в том же лотке. Для обработанных клеток токсичность выражали в процентах.
Для обработанных клеток токсичность выражали в процентах.
SDS-PAGE
Метод Лэммли использовали для проведения электрофореза в пластинчатом 10% -ном додецилсульфат-полиакриламидном геле (SDS-PAGE). Анализировали образцы клеточных супернатантов (20 мкг белка). В качестве стандартов использовали: миозин (200 кДа), галактозидазу (116,2 кДа), фосфорилазу b (97,4 кДа), бычий сывороточный альбумин (66.2 кДа) и овальбумин (45 кДа) (Bio-Rad, Беркли, Калифорния, США).
Вестерн-блот-анализ
Метод Лэммли использовали для проведения электрофореза в пластинчатом SDS-PAGE. Анализировали равные порции клеточных супернатантов (20 мкг белка). Мы конденсировали десятикратную культуральную среду с использованием центриконов (отсечка 3 кДа), смешанных с буфером для образцов Лэммли (содержащим 2,5% SDS, без восстановителя). Электрофорез проводили с равными порциями (100 мкг) белка. После электрофореза клетки уравновешивали в 25 мМ Трис с 0.2 М глицин в 20% метаноле (об. / Об. ) В течение 5 минут. Образцы переносили в поры нитроцеллюлозы размером 0,2 мкм при 100 мА в течение 1 часа. Для этой процедуры использовалась система электрофореза LKB 2117 Multiphor II Multiphor (GE Healthcare Bio-Sciences AB, Упсала, Швеция). Мы инкубировали нитроцеллюлозу в течение 1 часа с моноклональными антителами против коллагена I (концентрация 1: 1000), моноклональными антителами против фосфо-Akt (концентрация 1: 1000), поликлональными антителами против NF-κB (концентрация 1: 1000), моноклональное антитело против фосфо-MAPK (ERK 1/2 ) (концентрация 1: 1000), моноклональное антитело против каспазы 9 (концентрация 1: 1000).Антитела растворяли в растворе, содержащем 5% сухого молока, в трис-буферном физиологическом растворе с Tween 20 (TBS-T) (20 ммоль / л буфера Tris – HCl, pH 7,4, содержащего 150 ммоль / л NaCl и 0,05% Tween 20). . Для анализа фосфо-MAPK (ERK 1 / ERK / 2 ) и фосфо-AKT добавляли конъюгат щелочной фосфатазы против мышиного IgG (цельная молекула) в концентрации 1: 5000 в TBS-T.
) В течение 5 минут. Образцы переносили в поры нитроцеллюлозы размером 0,2 мкм при 100 мА в течение 1 часа. Для этой процедуры использовалась система электрофореза LKB 2117 Multiphor II Multiphor (GE Healthcare Bio-Sciences AB, Упсала, Швеция). Мы инкубировали нитроцеллюлозу в течение 1 часа с моноклональными антителами против коллагена I (концентрация 1: 1000), моноклональными антителами против фосфо-Akt (концентрация 1: 1000), поликлональными антителами против NF-κB (концентрация 1: 1000), моноклональное антитело против фосфо-MAPK (ERK 1/2 ) (концентрация 1: 1000), моноклональное антитело против каспазы 9 (концентрация 1: 1000).Антитела растворяли в растворе, содержащем 5% сухого молока, в трис-буферном физиологическом растворе с Tween 20 (TBS-T) (20 ммоль / л буфера Tris – HCl, pH 7,4, содержащего 150 ммоль / л NaCl и 0,05% Tween 20). . Для анализа фосфо-MAPK (ERK 1 / ERK / 2 ) и фосфо-AKT добавляли конъюгат щелочной фосфатазы против мышиного IgG (цельная молекула) в концентрации 1: 5000 в TBS-T. Для анализа NF-κB и каспазы-9, конъюгированного вторым антителом к щелочной фосфатазе, добавляли антикроличий IgG (целая молекула) в концентрации 1: 5000 в TBS-T.Для анализа коллагена типа I и конъюгированного второго антитела β-актина и щелочной фосфатазы добавляли анти-козий IgG (целая молекула) в концентрации 1: 5000 в TBS-T. Всю смесь инкубировали 30 минут при медленном встряхивании. После этого нитроцеллюлозу промывали TBS-T (5 × 5 минут) и обрабатывали реагентом жидкого субстрата 5-бром-4-хлор-3-индолилфосфат / нитросиний тетразолий. Интенсивность полос определяли количественно с помощью денситометрического анализа.
Для анализа NF-κB и каспазы-9, конъюгированного вторым антителом к щелочной фосфатазе, добавляли антикроличий IgG (целая молекула) в концентрации 1: 5000 в TBS-T.Для анализа коллагена типа I и конъюгированного второго антитела β-актина и щелочной фосфатазы добавляли анти-козий IgG (целая молекула) в концентрации 1: 5000 в TBS-T. Всю смесь инкубировали 30 минут при медленном встряхивании. После этого нитроцеллюлозу промывали TBS-T (5 × 5 минут) и обрабатывали реагентом жидкого субстрата 5-бром-4-хлор-3-индолилфосфат / нитросиний тетразолий. Интенсивность полос определяли количественно с помощью денситометрического анализа.
Зимография
Желатинолитическую активность измеряли с использованием метода Unemori и Werb.18 Мы конденсировали десятикратную культуральную среду с использованием центриконов (отсечка 3 кДа), смешанных с буфером для образцов (содержащим 2,5% SDS, без восстановителя). Электрофорез проводили с равными количествами белка (20 мкг) на полиакриламидных гелях (10%) в невосстанавливающих условиях. Гели пропитывали желатином (1 мг / мл). Инкубацию геля после электрофореза для удаления SDS проводили в течение 30 минут в 2% Triton X-100. После этого следовала инкубация в буфере, содержащем 50 мМ Трис – HCl, pH 8 с CaCl 2 5 мМ (субстратный буфер) в течение 18–24 часов при 37 ° C.После этого для окрашивания использовали кумасси бриллиантовый синий R250 (Thermo Fisher Scientific, Уолтем, Массачусетс, США).
Гели пропитывали желатином (1 мг / мл). Инкубацию геля после электрофореза для удаления SDS проводили в течение 30 минут в 2% Triton X-100. После этого следовала инкубация в буфере, содержащем 50 мМ Трис – HCl, pH 8 с CaCl 2 5 мМ (субстратный буфер) в течение 18–24 часов при 37 ° C.После этого для окрашивания использовали кумасси бриллиантовый синий R250 (Thermo Fisher Scientific, Уолтем, Массачусетс, США).
Статистические методы
Средние значения по крайней мере для трех анализов ± стандартное отклонение (± SD) были рассчитаны во всех соответствующих экспериментах. Статистический анализ проводился с применением двустороннего непарного критерия Стьюдента t и дисперсионного анализа. Использовалась программа IBM SPSS 22.0 Statstics Genericom (IBM Corporation, Армонк, Нью-Йорк, США). П <0.05 и P <0,01 признан статистически значимым.
Результаты
Чтобы оценить активность этанола в синтезе коллагена в фибробластах кожи человека, клетки инкубировали в течение 24 часов в 25, 50 и 100 мМ этанола, а также в этаноле с HA в концентрации 500 мкг. / мл. Было показано, что этанол вызывает снижение синтеза коллагена дозозависимым образом (и). Воздействие на фибробласты различных концентраций этанола способствует ингибированию биосинтеза коллагена на 58.08% (2,39% ± стандартное отклонение; n = 3), 76,23% (3,52% ± стандартное отклонение; n = 3), 83,15% (4,03% ± стандартное отклонение; n = 3) P <0,05, P <0,01, соответственно по сравнению с контрольным значением. Однако в присутствии HA в концентрации 500 мкг / мл эффективность этанола по ингибированию биосинтеза коллагена была намного ниже. ГК, добавленный только к клеткам, не оказывал значительного влияния на биосинтез коллагена в контрольных клетках. Представленные результаты свидетельствуют о том, что этанол оказывает ингибирующее действие на синтез коллагена в сливающихся фибробластах кожи человека, а ГК противодействует этому процессу (и).
/ мл. Было показано, что этанол вызывает снижение синтеза коллагена дозозависимым образом (и). Воздействие на фибробласты различных концентраций этанола способствует ингибированию биосинтеза коллагена на 58.08% (2,39% ± стандартное отклонение; n = 3), 76,23% (3,52% ± стандартное отклонение; n = 3), 83,15% (4,03% ± стандартное отклонение; n = 3) P <0,05, P <0,01, соответственно по сравнению с контрольным значением. Однако в присутствии HA в концентрации 500 мкг / мл эффективность этанола по ингибированию биосинтеза коллагена была намного ниже. ГК, добавленный только к клеткам, не оказывал значительного влияния на биосинтез коллагена в контрольных клетках. Представленные результаты свидетельствуют о том, что этанол оказывает ингибирующее действие на синтез коллагена в сливающихся фибробластах кожи человека, а ГК противодействует этому процессу (и).
Биосинтез коллагена, измеренный как включение 5 [ 3 H] -пролина в белки, чувствительные к действию бактериальной коллагеназы, в сливающихся фибробластах кожи человека, инкубированных в течение 24 часов с различными концентрациями этанола и HA.
Примечания: Тест ANOVA: ** P <0,01. Планки погрешностей представляют собой ± стандартное отклонение; п = 3.
Сокращения: ANOVA, дисперсионный анализ; HA, гиалуроновая кислота; ДМСО, диметилсульфоксид; dpm, распадов в минуту.
Вестерн-иммуноблот-анализ коллагена типа I в субконфлюэнтных фибробластах кожи человека (контроль), клетках, обработанных с или без HA в течение 24 часов. Интенсивность окрашивания полос определяли количественно с помощью денситометрического анализа. Тест Стьюдента t -тест, * P <0,05 и ** P <0,01.
Примечания: 1, контроль; 2, этанол 25 мМ; 3, этанол 50 мМ; 4, этанол 100 мМ; 5, НА; 6, этанол 25 мМ и НА; 7, этанол 50 мМ и НА; 8, этанол 100 мМ и НА.Образцы, используемые для электрофореза, состояли из 20 мкг белка объединенных экстрактов клеток.
Сокращения: AU, условные единицы; HA, гиалуроновая кислота.
Фермент, ответственный за рециклинг пролина для ресинтеза коллагена, — пролидаза и ММП. Добавление этанола в концентрациях 25, 50 и 100 мМ к культурам клеток способствовало снижению активности пролидазы на 29,05% (4,55% ± стандартное отклонение; n = 3), 56,15% (3,82% ± стандартное отклонение; n = 3), и 88,18% (1,16% ± стандартное отклонение; n = 3). Добавление НА оказало значительный защитный эффект на активность пролидазы в фибробластах, инкубированных с этанолом.ГК восстанавливала активность пролидазы в клетках, инкубированных с этанолом, до контрольного уровня ().
Добавление этанола в концентрациях 25, 50 и 100 мМ к культурам клеток способствовало снижению активности пролидазы на 29,05% (4,55% ± стандартное отклонение; n = 3), 56,15% (3,82% ± стандартное отклонение; n = 3), и 88,18% (1,16% ± стандартное отклонение; n = 3). Добавление НА оказало значительный защитный эффект на активность пролидазы в фибробластах, инкубированных с этанолом.ГК восстанавливала активность пролидазы в клетках, инкубированных с этанолом, до контрольного уровня ().
Активность пролидазы в конфлюэнтных фибробластах кожи человека, инкубированных в течение 24 часов с различными концентрациями этанола и НА.
Примечания: Тест ANOVA: * P <0,05, ** P <0,01. Планки погрешностей представляют собой ± стандартное отклонение; п = 3.
Сокращения: ANOVA, дисперсионный анализ; HA, гиалуроновая кислота.
Проведенные исследования доказывают, что этанол нарушает метаболизм коллагена в фибробластах кожи человека, что приводит к значительному снижению синтеза ДНК. Распад за минуту [ 3 H] тимидина, включенного в ДНК этих клеток, был принят за 100%. Это было эталонное значение. Мы оценили эффект этанола в присутствии или в отсутствие ГК (500 мг / мл). Воздействие на фибробласты этанола различных концентраций способствовало ингибированию синтеза ДНК на 21,06% (7,08% ± стандартное отклонение; n = 3), 44,15% (5,06% ± стандартное отклонение; n = 3), 56,27% (4,26% ± стандартное отклонение; n = 3), 50,16% (4,56% ± стандартное отклонение; n = 3) P <0,05, P <0,01, соответственно, по сравнению с контрольным значением.ГК оказывает защитное влияние на процессы, вызванные этанолом ().
Распад за минуту [ 3 H] тимидина, включенного в ДНК этих клеток, был принят за 100%. Это было эталонное значение. Мы оценили эффект этанола в присутствии или в отсутствие ГК (500 мг / мл). Воздействие на фибробласты этанола различных концентраций способствовало ингибированию синтеза ДНК на 21,06% (7,08% ± стандартное отклонение; n = 3), 44,15% (5,06% ± стандартное отклонение; n = 3), 56,27% (4,26% ± стандартное отклонение; n = 3), 50,16% (4,56% ± стандартное отклонение; n = 3) P <0,05, P <0,01, соответственно, по сравнению с контрольным значением.ГК оказывает защитное влияние на процессы, вызванные этанолом ().
Биосинтез ДНК, измеренный по включению [ 3 H] -тимидина в ДНК в фибробластах кожи человека (контроль), инкубированных в течение 24 часов с различными концентрациями этанола и НА.
Примечания: Тест ANOVA: * P <0,05, ** P <0,01. Планки погрешностей представляют собой ± стандартное отклонение; п = 3.
Сокращения: ANOVA, дисперсионный анализ; HA, гиалуроновая кислота.
Эффективность HA в снижении цитотоксичности 25, 50 и 100 мМ этанола показана на рисунке. Было показано, что этанол вызывает цитотоксичность дозозависимым образом. Наличие этанола ингибирования выживаемости клеток 20,16% (4,05% ± стандартное отклонение; n = 3), 35,18% (3,63% ± стандартное отклонение; n = 3), 56,03% (2,53% ± стандартное отклонение; n = 3) P < 0,01 соответственно по сравнению с контрольным значением. Рецептор интегрина β 1 играет ключевую роль в контроле биосинтеза коллагена и активности пролидазы. В этом исследовании мы обнаружили, что этанол снижает экспрессию рецептора интегрина β 1 дозозависимым образом.В культивируемых клетках, инкубированных с HA и этанолом, этот эффект исчез. Было обнаружено, что экспрессия рецептора интегрина в клетках, обработанных различными концентрациями этанола и HA, была такой же, как и в контрольных клетках ().
Цитотоксичность фибробластов кожи человека (контроль), инкубированных в течение 24 часов с различными концентрациями этанола и НА.
Примечания: Тест ANOVA: * P <0,05, ** P <0,01. Планки погрешностей представляют собой ± стандартное отклонение; п = 3.
Сокращения: ANOVA, дисперсионный анализ; HA, гиалуроновая кислота.
Вестерн-иммуноблот-анализ для β 1 интегрина ( A ), рецептора инсулиноподобного фактора роста I ( B ), ERK 1/2 ( C ), киназы Akt ( D ), каспаза 9 ( E ) и β-актин ( F ) в субконфлюэнтных фибробластах кожи человека (контроль), клетках, обработанных с или без HA в течение 24 часов. Интенсивность окрашивания полос определяли количественно с помощью денситометрического анализа.
Примечания: Студенческий тест t -тест: * P <0,05, ** P <0,01. 1, контроль; 2, этанол 25 мМ; 3, этанол 50 мМ; 4, этанол 100 мМ; 5, НА; 6, этанол 25 мМ и НА; 7, этанол 50 мМ и НА; 8, этанол 100 мМ и НА. Образцы, используемые для электрофореза, состояли из 20 мкг белка объединенных экстрактов клеток.
1, контроль; 2, этанол 25 мМ; 3, этанол 50 мМ; 4, этанол 100 мМ; 5, НА; 6, этанол 25 мМ и НА; 7, этанол 50 мМ и НА; 8, этанол 100 мМ и НА. Образцы, используемые для электрофореза, состояли из 20 мкг белка объединенных экстрактов клеток.
Сокращения: AU, условные единицы; ERK, киназа, регулируемая внеклеточными сигналами; HA, гиалуроновая кислота.
Известно, что перекрестное взаимодействие между рецептором интегрина β 1 и рецептором IGF-IR играет ключевую роль в активации экспрессии гена коллагена и активности пролидазы.Этанол, как и в случае рецептора интегрина, вызывал снижение экспрессии IGF-IR (дозозависимым образом). ГК также оказывает защитное действие на уровень экспрессии этого рецептора (). В этом случае экспрессия рецептора IGF-IR в клетках, инкубированных с этанолом и HA, была близка к контролю.
Сигнал, передаваемый стимулированным IGF-IR и β 1 рецептором интегрина, приводит к активации MAPK (ERK 1/2 ) и Akt. 14,15. Как видно на фибробластах, обработанных этанолом, экспрессия MAPK (фосфо-ERK 1/2 ) снижалось дозозависимым образом.Добавление HA к клеткам, обработанным этанолом, оказало защитное действие на зависимое от этанола снижение экспрессии фосфо-ERK 1/2 . Этанол и этанол с HA, добавленные к культивированным фибробластам, не влияли на экспрессию фосфо-AKT киназ (). Различные концентрации этанола оказывают цитотоксическое действие на фибробласты кожи человека, что приводит к индукции апоптоза, что приводит к наблюдаемому увеличению экспрессии каспазы 9 (). Более того, применение ГК оказывает защитное действие на нарушения пролиферации клеток, вызванные этанолом.Более того, экспрессия β-актина не изменялась в клетках при обработке этанолом в присутствии или в отсутствие НА ().
14,15. Как видно на фибробластах, обработанных этанолом, экспрессия MAPK (фосфо-ERK 1/2 ) снижалось дозозависимым образом.Добавление HA к клеткам, обработанным этанолом, оказало защитное действие на зависимое от этанола снижение экспрессии фосфо-ERK 1/2 . Этанол и этанол с HA, добавленные к культивированным фибробластам, не влияли на экспрессию фосфо-AKT киназ (). Различные концентрации этанола оказывают цитотоксическое действие на фибробласты кожи человека, что приводит к индукции апоптоза, что приводит к наблюдаемому увеличению экспрессии каспазы 9 (). Более того, применение ГК оказывает защитное действие на нарушения пролиферации клеток, вызванные этанолом.Более того, экспрессия β-актина не изменялась в клетках при обработке этанолом в присутствии или в отсутствие НА ().
Некоторые данные свидетельствуют о том, что пролидаза-зависимая регуляция биосинтеза коллагена может иметь место на уровне транскрипции, в зависимости от экспрессии NF-κB. NF-κB — это фактор транскрипции, который действует как ингибитор экспрессии альфа 1 и альфа 2 субъединиц коллагена типа I. 19,20 Мы обнаружили повышенную экспрессию NF-κB в фибробластах, обработанных этанолом ().Добавление НА к клеткам, обработанным этанолом, способствовало снижению экспрессии этого транскрипционного фактора до контрольного уровня. Более того, экспрессия β-актина не изменялась в клетках при обработке этанолом в присутствии или в отсутствие НА (). Похоже, что регуляторный механизм индуцированной этанолом аберрации коллагена имеет место в точке биосинтеза коллагена, поскольку не было обнаружено влияния этанола и ГК на процесс деградации коллагена ММП-2 и ММП-9 ().
19,20 Мы обнаружили повышенную экспрессию NF-κB в фибробластах, обработанных этанолом ().Добавление НА к клеткам, обработанным этанолом, способствовало снижению экспрессии этого транскрипционного фактора до контрольного уровня. Более того, экспрессия β-актина не изменялась в клетках при обработке этанолом в присутствии или в отсутствие НА (). Похоже, что регуляторный механизм индуцированной этанолом аберрации коллагена имеет место в точке биосинтеза коллагена, поскольку не было обнаружено влияния этанола и ГК на процесс деградации коллагена ММП-2 и ММП-9 ().
Вестерн-иммуноблот-анализ белка p65 NF-κB ( A ) и β-актина ( B ) в субконфлюэнтных фибробластах кожи человека (контроль), клетках, обработанных с или без HA в течение 24 часов.Интенсивность окрашивания полос определяли количественно с помощью денситометрического анализа.
Примечания: Студенческий тест t -тест: ** P <0,01. 1, контроль; 2, этанол 25 мМ; 3, этанол 50 мМ; 4, этанол 100 мМ; 5, НА; 6, этанол 25 мМ и НА; 7, этанол 50 мМ и НА; 8, этанол 100 мМ и НА. Образцы, используемые для электрофореза, состояли из 20 мкг белка объединенных экстрактов клеток.
Образцы, используемые для электрофореза, состояли из 20 мкг белка объединенных экстрактов клеток.
Сокращения: AU, условные единицы; HA, гиалуроновая кислота.
Зимография для MMP-9 (92 кДа) и MMP-2 (72 кДа) в субконфлюэнтных фибробластах кожи человека (контроль), клетках, обработанных с или без HA в течение 24 часов.
Примечания: Интенсивность окрашивания полос количественно определяли с помощью денситометрического анализа. 1, контроль; 2, этанол 25 мМ; 3, этанол 50 мМ; 4, этанол 100 мМ; 5, НА; 6, этанол 25 мМ и НА; 7, этанол 50 мМ и НА; 8, этанол 100 мМ и НА. Образцы, используемые для электрофореза, состояли из 20 мкг белка объединенных экстрактов клеток.
Сокращения: AU, условные единицы; HA, гиалуроновая кислота; ММП, матричная металлопротеиназа.
Обсуждение
Хотя цитотоксичность этанола хорошо известна, механизм ее воздействия на метаболизм коллагена в тканях до конца не изучен. Похоже, что аномалии метаболизма коллагена, вызванные этанолом, тканеспецифичны. В печени он может способствовать стимуляции биосинтеза коллагена с последствием фиброза тканей, в то время как в коже может происходить противоположный процесс с последствием заживления ран.
Похоже, что аномалии метаболизма коллагена, вызванные этанолом, тканеспецифичны. В печени он может способствовать стимуляции биосинтеза коллагена с последствием фиброза тканей, в то время как в коже может происходить противоположный процесс с последствием заживления ран.
В этом исследовании мы предоставили доказательства того, что этанол подавляет метаболизм коллагена в фибробластах кожи посредством нескольких уровней регуляции этого белка. Сначала это влияет на активность пролидазы, фермента, который играет важную роль в биосинтезе коллагена.Фермент отвечает за рециркуляцию пролина для ресинтеза коллагена, тем самым определяя выработку коллагена. Пептидные связи между пролином и другими аминокислотами могут быть расщеплены также другой пептидазой, пролиназой, которой необходим пролин в N-концевом положении.21 Пролидаза — вторая иминопептидаза, которая расщепляет дипептиды С-концевым пролином для сбора свободного пролина. Фермент переваривает как эндогенные, так и диетические дипептиды Xaa-Pro. 21
21
Другой уровень регуляции метаболизма коллагена в обработанных этанолом фибробластах был обнаружен при β 1 интегрина и IGF-IR.Ранее мы обнаружили, что перекрестные помехи между рецепторами способствуют усилению биосинтеза коллагена. 22 В настоящем исследовании мы обнаружили, что этанол способствует подавлению экспрессии обоих рецепторов. Одновременно мы обнаружили повышение транскрипционной активности NF-κB, известного ингибитора коллагена типа I, который субъединиц экспрессии гена.20 В результате проведенных исследований был сделан вывод, что этанол приводит к нарушению биосинтеза коллагена в фибробластах. культур за счет снижения активности пролидазы и экспрессии интегрина β 1 и IGF-IR.Это сопровождалось пониженной экспрессией белков сигнального пути, индуцированной интегрином β 1 и IGF-IR, то есть киназами MAPK (ERK 1/2 ). Пониженное количество синтезированного коллагена и нарушение активности пролидазы также может быть связано с активацией фактора транскрипции NF-κB, который подавляет экспрессию гена коллагена. Применение ГК в концентрации 500 мкг / мл оказывает защитное действие на нарушения, вызванные исследуемыми веществами. Совокупность процессов, на которые влияет этанол, объясняет механизм индуцированного этанолом подавления биосинтеза коллагена.Основываясь на наших предыдущих исследованиях, мы рассматривали ГК как средство, противодействующее вызванной этанолом дерегуляции метаболизма коллагена в фибробластах.11 Фактически, мы обнаружили, что ГК устраняет все изученные дефекты метаболизма коллагена, вызванные этанолом. В нашей предыдущей статье мы не наблюдали отменяющего эффекта ГК, когда кофеин подавлял синтез коллагена.23 Различные концентрации этанола оказывают цитотоксическое действие на фибробласты кожи человека, что приводит к снижению выживаемости, ингибированию биосинтеза ДНК и индукции апоптоза, что приводит к в наблюдаемом повышении экспрессии каспазы 9.Более того, применение ГК оказывает защитное действие на дефект пролиферации клеток, вызванный этанолом.
Применение ГК в концентрации 500 мкг / мл оказывает защитное действие на нарушения, вызванные исследуемыми веществами. Совокупность процессов, на которые влияет этанол, объясняет механизм индуцированного этанолом подавления биосинтеза коллагена.Основываясь на наших предыдущих исследованиях, мы рассматривали ГК как средство, противодействующее вызванной этанолом дерегуляции метаболизма коллагена в фибробластах.11 Фактически, мы обнаружили, что ГК устраняет все изученные дефекты метаболизма коллагена, вызванные этанолом. В нашей предыдущей статье мы не наблюдали отменяющего эффекта ГК, когда кофеин подавлял синтез коллагена.23 Различные концентрации этанола оказывают цитотоксическое действие на фибробласты кожи человека, что приводит к снижению выживаемости, ингибированию биосинтеза ДНК и индукции апоптоза, что приводит к в наблюдаемом повышении экспрессии каспазы 9.Более того, применение ГК оказывает защитное действие на дефект пролиферации клеток, вызванный этанолом.
HA играет важную роль в поддержании внеклеточного матрикса и вызывает защитное действие на структуру коллагена. 24,25 HA — это искусство гликозаминогликанов, где d-глюкуроновая кислота связана с частицей N -ацетилглюкозамина через гликозидные связи26. , 27 Клетка окружена слоем гиалуронана, который отвечает за форму, адгезию и миграцию клетки.24 Кожа содержит примерно 50% всей гиалуроновой кислоты в организме. ГК улучшает процессы заживления при некоторых патологических состояниях, таких как венозные язвы или повреждения мембран. Данные литературы показывают, что ГК играет полезную роль в регенеративных процессах, связанных с дисфункцией синтеза коллагена.28 Мы можем предположить, что ГК защищает от нарушений, вызванных этанолом. Этот защитный эффект можно контролировать посредством взаимодействия гиалуронана с его рецепторами CD44 и / или RHAMM.29 По крайней мере, в эндотелиальных клетках этот механизм способствует стимуляции выработки коллагена.30 Вопрос о том, играют ли рецепторы CD44 и RHAMM важную роль в механизме НА-зависимого противодействия токсичности этанола, требует дальнейшего изучения.
24,25 HA — это искусство гликозаминогликанов, где d-глюкуроновая кислота связана с частицей N -ацетилглюкозамина через гликозидные связи26. , 27 Клетка окружена слоем гиалуронана, который отвечает за форму, адгезию и миграцию клетки.24 Кожа содержит примерно 50% всей гиалуроновой кислоты в организме. ГК улучшает процессы заживления при некоторых патологических состояниях, таких как венозные язвы или повреждения мембран. Данные литературы показывают, что ГК играет полезную роль в регенеративных процессах, связанных с дисфункцией синтеза коллагена.28 Мы можем предположить, что ГК защищает от нарушений, вызванных этанолом. Этот защитный эффект можно контролировать посредством взаимодействия гиалуронана с его рецепторами CD44 и / или RHAMM.29 По крайней мере, в эндотелиальных клетках этот механизм способствует стимуляции выработки коллагена.30 Вопрос о том, играют ли рецепторы CD44 и RHAMM важную роль в механизме НА-зависимого противодействия токсичности этанола, требует дальнейшего изучения.
Данные, представленные в этой статье, могут иметь определенное социальное значение. Они предполагают, что фибробласты особенно чувствительны к этанолу и реагируют на это соединение путем ингибирования биосинтеза коллагена. Этот процесс способствует старению кожи, что представляет особый интерес для косметологии. Принимая во внимание приведенные выше данные и тот факт, что этанол обычно используется в косметологии, можно предположить, что этанол можно заменить в косметике другим растворителем или консервантами.Также можно рассматривать включение ГК в косметические препараты, содержащие этанол.
Выражение признательности
MD является научным сотрудником в области проектных исследований, исследований, коммерциализации: программа поддержки докторантов UMB, подмера 8.2.1 Операционная программа человеческого капитала, софинансируемая Европейским союзом в рамках Европейского социального фонда. Работа частично поддержана грантами Белостокского медицинского университета (143-14749F, 143-30730F, 144-30828F).
Сноски
Раскрытие информации
Авторы сообщают об отсутствии конфликта интересов в этой работе.
Ссылки
1. Сид Б., Верракс Дж., Кальдерон ПБ. Роль активации AMPK в окислительном повреждении клеток: последствия для алкогольной болезни печени. Biochem Pharmacol. 2013. 86 (2): 200–209. [PubMed] [Google Scholar] 2. Эль-Хадж Э.С., Эль-Хадж М.К., Волошенюк Т.Г. и др. Алкогольная модуляция металлопротеиназ сердечного матрикса (ММП) и тканевых ингибиторов ММП способствует накоплению коллагена. Alcohol Clin Exp Res. 2014. 38 (2): 448–456. [Бесплатная статья PMC] [PubMed] [Google Scholar] 3. Xu GF, Li PT, Wang XY и др.Динамические изменения экспрессии матриксных металлопротеиназ и их ингибиторов, TIMP, во время фиброза печени, вызванного алкоголем у крыс. Мир Дж. Гастроэнтерол. 2004. 10 (24): 3621–3627. [Бесплатная статья PMC] [PubMed] [Google Scholar] 4. Neuman MG, Nanau RM, Oruña L, Coto G. Противовоспалительные эффекты гиалуроновой кислоты in vitro при повреждении клеток кожи, вызванном этанолом. J. Pharm. Pharm. Sci. 2011. 14 (3): 425–437. [PubMed] [Google Scholar] 5. Пржилипиак А., Рабе Т., Хафнер Дж., Пржилипиак М., Руннебаум Б.Влияние этанола на рост in vitro клеточной линии карциномы молочной железы человека MCF-7. Arch Gynecol Obstet. 1996. 258 (3): 137–140. [PubMed] [Google Scholar] 6. Джонен Ч., Хартманн Б., Штеффен И. и др. Выделение и размножение клеток кожи для трансплантации клеток ограничено у пациентов, употребляющих табак, алкоголь или страдающих сахарным диабетом. Бернс. 2006. 32 (2): 194–200. [PubMed] [Google Scholar] 7. Ранзер MJ, Чен Л., ДиПьетро Л.А. При острой интоксикации этанолом нарушается функция фибробластов и прочность на разрыв раны.Alcohol Clin Exp Res. 2011; 35 (1): 83–90. [Бесплатная статья PMC] [PubMed] [Google Scholar] 8. Бойс Дж. М.. Обновите информацию о гигиене рук. Am J Infect Control. 2013. 41 (5): 94–96. [PubMed] [Google Scholar] 9. Ким И-Ч, Пак Джей-Х, Людовице П.Дж., Праусниц MR. Синергетическое усиление проницаемости кожи N-лауроилсаркозином и этанолом.
J. Pharm. Pharm. Sci. 2011. 14 (3): 425–437. [PubMed] [Google Scholar] 5. Пржилипиак А., Рабе Т., Хафнер Дж., Пржилипиак М., Руннебаум Б.Влияние этанола на рост in vitro клеточной линии карциномы молочной железы человека MCF-7. Arch Gynecol Obstet. 1996. 258 (3): 137–140. [PubMed] [Google Scholar] 6. Джонен Ч., Хартманн Б., Штеффен И. и др. Выделение и размножение клеток кожи для трансплантации клеток ограничено у пациентов, употребляющих табак, алкоголь или страдающих сахарным диабетом. Бернс. 2006. 32 (2): 194–200. [PubMed] [Google Scholar] 7. Ранзер MJ, Чен Л., ДиПьетро Л.А. При острой интоксикации этанолом нарушается функция фибробластов и прочность на разрыв раны.Alcohol Clin Exp Res. 2011; 35 (1): 83–90. [Бесплатная статья PMC] [PubMed] [Google Scholar] 8. Бойс Дж. М.. Обновите информацию о гигиене рук. Am J Infect Control. 2013. 41 (5): 94–96. [PubMed] [Google Scholar] 9. Ким И-Ч, Пак Джей-Х, Людовице П.Дж., Праусниц MR. Синергетическое усиление проницаемости кожи N-лауроилсаркозином и этанолом. Int J Pharmaceutics. 2008. 352 (1–2): 129–138. [PubMed] [Google Scholar] 10. Pendlington RU, Whittle E, Robinson JA, Howes D. Судьба этанола, наносимого на кожу местно. Food Chem Toxicol. 2001. 39 (2): 169–174.[PubMed] [Google Scholar] 11. Surazynski A, Miltyk W, Czarnomysy R, Grabowska J, Palka J. Гиалуроновая кислота отменяет зависимую от оксида азота стимуляцию деградации коллагена в культивируемых хондроцитах человека. Pharmacol Res. 2009. 60 (1): 46–49. [PubMed] [Google Scholar] 12. Гази К., Денг-Пичон У., Варнет Дж.М., Крыса П. Фрагменты гиалуроновой кислоты улучшают заживление ран на кожной модели in vitro за счет базовой активации пуринорецептора P2X7: роль молекулярной массы. PLoS One. 2012; 7 (11): e48351. [Бесплатная статья PMC] [PubMed] [Google Scholar] 13.Nawrat P, Surazynski A, Karna E, Pałka JA. Влияние гиалуроновой кислоты на индуцированное интерлейкином-1 нарушение регуляции метаболизма коллагена в культивируемых фибробластах кожи человека. Pharmacol Res. 2005. 51 (5): 473–477.
Int J Pharmaceutics. 2008. 352 (1–2): 129–138. [PubMed] [Google Scholar] 10. Pendlington RU, Whittle E, Robinson JA, Howes D. Судьба этанола, наносимого на кожу местно. Food Chem Toxicol. 2001. 39 (2): 169–174.[PubMed] [Google Scholar] 11. Surazynski A, Miltyk W, Czarnomysy R, Grabowska J, Palka J. Гиалуроновая кислота отменяет зависимую от оксида азота стимуляцию деградации коллагена в культивируемых хондроцитах человека. Pharmacol Res. 2009. 60 (1): 46–49. [PubMed] [Google Scholar] 12. Гази К., Денг-Пичон У., Варнет Дж.М., Крыса П. Фрагменты гиалуроновой кислоты улучшают заживление ран на кожной модели in vitro за счет базовой активации пуринорецептора P2X7: роль молекулярной массы. PLoS One. 2012; 7 (11): e48351. [Бесплатная статья PMC] [PubMed] [Google Scholar] 13.Nawrat P, Surazynski A, Karna E, Pałka JA. Влияние гиалуроновой кислоты на индуцированное интерлейкином-1 нарушение регуляции метаболизма коллагена в культивируемых фибробластах кожи человека. Pharmacol Res. 2005. 51 (5): 473–477. [PubMed] [Google Scholar] 14. Петеркофский Б., Дигельманн Р. Использование смеси коллагеназ, свободных от протеиназ, для специфического анализа радиоактивного коллагена в присутствии других белков. Биохимия. 1971; 10 (6): 988–994. [PubMed] [Google Scholar] 15. Myara I, Charpentier C, Lemonnier A. Оптимальные условия для анализа пролидазы колориметрическим определением пролина: применение к иминодипептидурии.Clin Chim Acta. 1982; 125 (2): 193–205. [PubMed] [Google Scholar] 16. Лоури Н., Розенбро Н., Фарр Л., Рэндалл Р. Измерение белка с реагентом фолин-фенол. J Biol Chem. 1951; 193 (1): 265–275. [PubMed] [Google Scholar] 17. Laemmli UK. Расщепление структурных белков при сборке головки бактериофага Т4. Природа. 1970. 227 (5259): 680–685. [PubMed] [Google Scholar] 18. Unemori E, Werb Z. Реорганизация полимеризованного актина: возможный спусковой механизм для индукции проколлагеназы в фибробластах, культивируемых в коллагеновых гелях и на них.J Cell Biol. 1986. 103 (3): 1021–1031. [Бесплатная статья PMC] [PubMed] [Google Scholar] 19.
[PubMed] [Google Scholar] 14. Петеркофский Б., Дигельманн Р. Использование смеси коллагеназ, свободных от протеиназ, для специфического анализа радиоактивного коллагена в присутствии других белков. Биохимия. 1971; 10 (6): 988–994. [PubMed] [Google Scholar] 15. Myara I, Charpentier C, Lemonnier A. Оптимальные условия для анализа пролидазы колориметрическим определением пролина: применение к иминодипептидурии.Clin Chim Acta. 1982; 125 (2): 193–205. [PubMed] [Google Scholar] 16. Лоури Н., Розенбро Н., Фарр Л., Рэндалл Р. Измерение белка с реагентом фолин-фенол. J Biol Chem. 1951; 193 (1): 265–275. [PubMed] [Google Scholar] 17. Laemmli UK. Расщепление структурных белков при сборке головки бактериофага Т4. Природа. 1970. 227 (5259): 680–685. [PubMed] [Google Scholar] 18. Unemori E, Werb Z. Реорганизация полимеризованного актина: возможный спусковой механизм для индукции проколлагеназы в фибробластах, культивируемых в коллагеновых гелях и на них.J Cell Biol. 1986. 103 (3): 1021–1031. [Бесплатная статья PMC] [PubMed] [Google Scholar] 19. Коуба Д., Чунг К.-Й, Нишияма Т. и др. Ядерный фактор-κB опосредует ингибирующее действие TNF-α на транскрипцию гена коллагена α2 (I) (COL1A2) в дермальных фибробластах человека. J Immunol. 1999. 162 (7): 4226–4234. [PubMed] [Google Scholar] 20. Miltyk W, Karna E, Palka J. Независимый от пролидазы механизм камптотецина-индуцированного ингибирования биосинтеза коллагена в культивируемых фибробластах кожи человека. J Biochem. 2007. 141 (2): 287–292.[PubMed] [Google Scholar] 21. Китченер Р.Л., Грюнден А.М. Функция пролидазы в метаболизме пролина и ее медицинские и биотехнологические применения. J Appl Microbiol. 2012. 113 (2): 233–247. [PubMed] [Google Scholar] 22. Surazynski A, Miltyk W, Prokop I, Palka J. Пролидазозависимая регуляция экспрессии рецепторов TGF и TGF β в фибробластах кожи человека. Eur J Pharmacol. 2010. 649 (1–3): 115–119. [PubMed] [Google Scholar] 23. Донейко М., Пржилипиак А., Рысяк Э., Глушук К., Суразинский А. Влияние кофеина и гиалуроновой кислоты на биосинтез коллагена в фибробластах кожи человека.
Коуба Д., Чунг К.-Й, Нишияма Т. и др. Ядерный фактор-κB опосредует ингибирующее действие TNF-α на транскрипцию гена коллагена α2 (I) (COL1A2) в дермальных фибробластах человека. J Immunol. 1999. 162 (7): 4226–4234. [PubMed] [Google Scholar] 20. Miltyk W, Karna E, Palka J. Независимый от пролидазы механизм камптотецина-индуцированного ингибирования биосинтеза коллагена в культивируемых фибробластах кожи человека. J Biochem. 2007. 141 (2): 287–292.[PubMed] [Google Scholar] 21. Китченер Р.Л., Грюнден А.М. Функция пролидазы в метаболизме пролина и ее медицинские и биотехнологические применения. J Appl Microbiol. 2012. 113 (2): 233–247. [PubMed] [Google Scholar] 22. Surazynski A, Miltyk W, Prokop I, Palka J. Пролидазозависимая регуляция экспрессии рецепторов TGF и TGF β в фибробластах кожи человека. Eur J Pharmacol. 2010. 649 (1–3): 115–119. [PubMed] [Google Scholar] 23. Донейко М., Пржилипиак А., Рысяк Э., Глушук К., Суразинский А. Влияние кофеина и гиалуроновой кислоты на биосинтез коллагена в фибробластах кожи человека. Drug Des Devel Ther. 2014; 8: 1923–1928. [Бесплатная статья PMC] [PubMed] [Google Scholar] 25. Karna E, Miltyk W, Surazyński A, Pałka JA. Защитный эффект гиалуроновой кислоты на индуцированную интерлейкином-1 дерегуляцию передачи сигналов рецептора бета1-интегрина и инсулиноподобного фактора роста-I и биосинтез коллагена в культивируемых хондроцитах человека. Mol Cell Biochem. 2008. 308 (1–2): 57–64. [PubMed] [Google Scholar] 26. Гириш К.С., Кемпараджу К. Волшебный клей гиалуронан и его ластик гиалуронидаза: биологический обзор.Life Sci. 2007. 80 (21): 1921–1943. [PubMed] [Google Scholar] 27. Шефер Л, Шефер РМ. Протеогликаны: от структурных соединений до сигнальных молекул. Cell Tissue Res. 2010. 339 (1): 237–246. [PubMed] [Google Scholar] 28. Суразинский А., Милтык В., Палка Дж., Панг Дж. М.. Пролидазозависимая регуляция биосинтеза коллагена. Аминокислоты. 2008. 35 (4): 731–738. [PubMed] [Google Scholar] 29. Aruffo A, Stamenkovic I, Melnick M, Underhill CB, Seed B. CD44 является основным рецептором гиалуроната на клеточной поверхности.
Drug Des Devel Ther. 2014; 8: 1923–1928. [Бесплатная статья PMC] [PubMed] [Google Scholar] 25. Karna E, Miltyk W, Surazyński A, Pałka JA. Защитный эффект гиалуроновой кислоты на индуцированную интерлейкином-1 дерегуляцию передачи сигналов рецептора бета1-интегрина и инсулиноподобного фактора роста-I и биосинтез коллагена в культивируемых хондроцитах человека. Mol Cell Biochem. 2008. 308 (1–2): 57–64. [PubMed] [Google Scholar] 26. Гириш К.С., Кемпараджу К. Волшебный клей гиалуронан и его ластик гиалуронидаза: биологический обзор.Life Sci. 2007. 80 (21): 1921–1943. [PubMed] [Google Scholar] 27. Шефер Л, Шефер РМ. Протеогликаны: от структурных соединений до сигнальных молекул. Cell Tissue Res. 2010. 339 (1): 237–246. [PubMed] [Google Scholar] 28. Суразинский А., Милтык В., Палка Дж., Панг Дж. М.. Пролидазозависимая регуляция биосинтеза коллагена. Аминокислоты. 2008. 35 (4): 731–738. [PubMed] [Google Scholar] 29. Aruffo A, Stamenkovic I, Melnick M, Underhill CB, Seed B. CD44 является основным рецептором гиалуроната на клеточной поверхности. Клетка.1990. 61 (7): 1303–1313. [PubMed] [Google Scholar] 30. Руни П., Ван М., Кумар П., Кумар С. Ангиогенные олигосахариды гиалуронана увеличивают выработку коллагенов эндотелиальными клетками. J Cell Sci. 1993. 105 (1): 213–218. [PubMed] [Google Scholar]
Клетка.1990. 61 (7): 1303–1313. [PubMed] [Google Scholar] 30. Руни П., Ван М., Кумар П., Кумар С. Ангиогенные олигосахариды гиалуронана увеличивают выработку коллагенов эндотелиальными клетками. J Cell Sci. 1993. 105 (1): 213–218. [PubMed] [Google Scholar]
Гиалуроновая кислота отменяет этанол-зависимое ингибирование биосинтеза коллагена в культивируемых фибробластах человека
Drug Des Devel Ther. 2015; 9: 6225–6233.
Магдалена Донейко
1 Кафедра эстетической медицины, Медицинский университет Белостока, Белосток, Польша
Анджей Пржилипяк
1 Кафедра эстетической медицины, Медицинский университет Белостока
, Белосток, Польша
2 Кафедра медицинской химии, Медицинский университет Белостока, Белосток, Польша
Войцех Милтык
3 Кафедра фармацевтического анализа, Фармацевтический факультет, Медицинский университет Белостока, Белосток, Белосток
Кафедра эстетической медицины, Медицинский университет Белостока, Белосток, Польша
Ежи Пжилипяк
4 Медицинский офис, Белосток, Польша
Илона Заремба
2 ł Кафедра медицинской химии Беловостокского медицинского университета Польша
Аркадиуш Суразиньс ki
2 Кафедра медицинской химии Белостокского медицинского университета, Белосток, Польша
1 Кафедра эстетической медицины Белостокского медицинского университета, Белосток, Польша
2 Кафедра медицинской химии медицинского университета Белосток, Белосток, Польша
3 Кафедра фармацевтического анализа, Фармацевтический факультет, Белостокский медицинский университет, Белосток, Польша
4 Медицинский офис, Белосток, Польша
Переписка: Магдалена, Медицинский факультет, Эстонский факультет of Pharmacy, Медицинский университет Белостока, улица Академицкая 3, 15-267 Белосток, Польша, Email moc. liamg @ okjenod Авторские права © 2015 Donejko et al. Эта работа опубликована Dove Medical Press Limited и находится под лицензией Creative Commons Attribution — Non Commercial (unported, v3.0) License. Полные условия лицензии доступны по адресу http://creativecommons.org/licenses/by-nc/3.0 /. Некоммерческое использование работы разрешено без какого-либо разрешения Dove Medical Press Limited при условии правильной ссылки на эту статью. Эта статья цитируется в других статьях PMC.
liamg @ okjenod Авторские права © 2015 Donejko et al. Эта работа опубликована Dove Medical Press Limited и находится под лицензией Creative Commons Attribution — Non Commercial (unported, v3.0) License. Полные условия лицензии доступны по адресу http://creativecommons.org/licenses/by-nc/3.0 /. Некоммерческое использование работы разрешено без какого-либо разрешения Dove Medical Press Limited при условии правильной ссылки на эту статью. Эта статья цитируется в других статьях PMC.
Abstract
Введение
Целью исследования было оценить влияние этанола на биосинтез коллагена в культивируемых фибробластах кожи человека и роль гиалуроновой кислоты (HA) в этом процессе.Что касается механизма действия этанола на фибробласты кожи человека, мы исследовали: экспрессию интегрина β 1 и рецептора инсулиноподобного фактора роста 1 (IGF-IR), экспрессию белков сигнального пути: митоген-активированные протеинкиназы (MAPK), протеинкиназы. B (Akt), ядерный фактор, каппа B (NF-κB), фактор транскрипции, анализ цитотоксичности и апоптоза, активность металлопротеиназы, а также влияние HA на эти процессы.
Материалы и методы
Биосинтез коллагена, активность пролидазы, биосинтез ДНК и цитотоксичность были измерены в конфлюэнтных культурах фибробластов кожи человека, обработанных 25, 50 и 100 мМ этанолом, этанолом и 500 мкг / мл HA.Вестерн-блот-анализ и зимография были выполнены для оценки экспрессии коллагена типа I, рецептора интегрина β 1 , IGF-IR, белка NF-κB, белка фосфо-Akt, киназы MAPK, активности каспазы 9 и матриксных металлопротеиназ (MMP-9). и ММП-2).
Результаты
Дозозависимый этанол приводит к нарушению биосинтеза коллагена в культурах фибробластов за счет снижения активности пролидазы и экспрессии интегрина β 1 и IGF-IR. Это сопровождалось повышенной цитотоксичностью, апоптозом и снижением экспрессии белков сигнального пути, индуцированных интегрином β 1 и IGF-IR, то есть киназами MAPK (ERK 1/2 ).Пониженное количество синтезированного коллагена и нарушение активности пролидазы также может быть связано с активацией фактора транскрипции NF-κB, который подавляет экспрессию гена коллагена.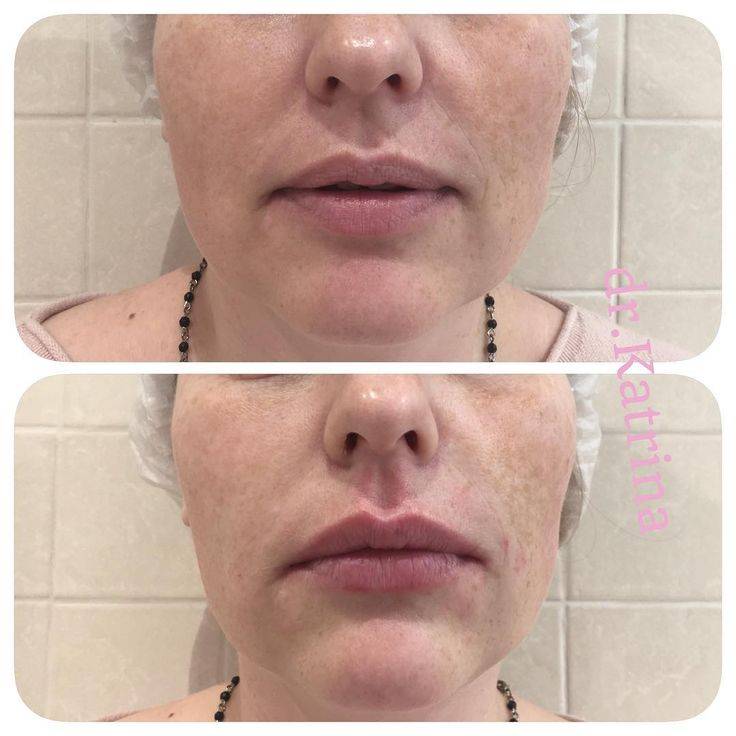 Это предполагает, что снижение продукции коллагена фибробластами может быть вызвано нарушением его биосинтеза, но не деградацией. Применение ГК оказывает защитное действие на нарушения, вызванные исследуемыми веществами. По-видимому, регуляторный механизм индуцированной этанолом аберрации коллагена имеет место на уровне биосинтеза коллагена, поскольку не было обнаружено влияния этанола и ГК на процесс деградации коллагена ММП-2 и ММП-9.
Это предполагает, что снижение продукции коллагена фибробластами может быть вызвано нарушением его биосинтеза, но не деградацией. Применение ГК оказывает защитное действие на нарушения, вызванные исследуемыми веществами. По-видимому, регуляторный механизм индуцированной этанолом аберрации коллагена имеет место на уровне биосинтеза коллагена, поскольку не было обнаружено влияния этанола и ГК на процесс деградации коллагена ММП-2 и ММП-9.
Заключение
Это исследование предоставляет доказательства того, что этанол нарушает метаболизм коллагена в фибробластах кожи человека, что приводит к значительному снижению количества продуцируемого белка. Этот механизм, вероятно, связан с подавлением активности пролидазы, экспрессии интегрина β 1 и рецепторов IGF-IR, а также белков сигнального пути, индуцированных этими рецепторами.
Ключевые слова: коллаген , этанол, гиалуроновая кислота, фибробласты
Введение
Воздействие этанола (этилового спирта) может вызывать множество местных и систематических нарушений. Органы, которые особенно страдают от интоксикации этанолом, — это легкие, почки и печень.1 Было показано, что интоксикация этанолом вызывает окислительный стресс, что приводит к модуляции экспрессии металлопротеиназ и тканевых ингибиторов матриксных металлопротеиназ (ММП) в клетках сердца и печени, способствующих развитию изменения клеточного фенотипа на фибробластоподобные с дальнейшими последствиями в накоплении тканевого коллагена и фиброзе.2,3 В нескольких исследованиях задокументировано этанол-зависимое окислительное повреждение в печени.Было обнаружено, что механизм этого процесса может включать функцию митохондрий и выживаемость клеток.1 Таким образом, цитотоксичность этанола может способствовать апоптозу клеток или может вызывать провоспалительные цитокины.4 Было обнаружено, что алкоголь ингибирует рост клеток карциномы молочной железы человека MCF-7 в vitro.5
Органы, которые особенно страдают от интоксикации этанолом, — это легкие, почки и печень.1 Было показано, что интоксикация этанолом вызывает окислительный стресс, что приводит к модуляции экспрессии металлопротеиназ и тканевых ингибиторов матриксных металлопротеиназ (ММП) в клетках сердца и печени, способствующих развитию изменения клеточного фенотипа на фибробластоподобные с дальнейшими последствиями в накоплении тканевого коллагена и фиброзе.2,3 В нескольких исследованиях задокументировано этанол-зависимое окислительное повреждение в печени.Было обнаружено, что механизм этого процесса может включать функцию митохондрий и выживаемость клеток.1 Таким образом, цитотоксичность этанола может способствовать апоптозу клеток или может вызывать провоспалительные цитокины.4 Было обнаружено, что алкоголь ингибирует рост клеток карциномы молочной железы человека MCF-7 в vitro.5
Кажется, что этанол особенно влияет на биосинтез коллагена I типа. Этот процесс происходит в основном в клетках печени, но также наблюдается и в клетках кожи. Воздействие этанола на кожу привело к появлению многих дерматологических аномалий, таких как ладонная эритема, полнокровие, инфекции и приливы.6 Биопсии, полученные с кожи доноров, злоупотребляющих алкоголем, подтвердили аномалию структуры ткани, а изолированные фибробласты вызвали длительное время пролиферации.6 Некоторые данные предполагают, что этанол может влиять на заживление ран, вмешиваясь в биосинтез коллагена I и III.7 Этанол обычно используется в косметике, фармацевтика и дезинфицирующие средства.8,9 Большое количество спиртов используется в качестве разбавителей, консервантов, ингредиентов увлажняющих веществ или ароматизаторов в косметических средствах, наносимых на кожу.9,10 Концентрация этанола в продукте для типичного применения может варьироваться от менее чем От 1% до 96.9%.
Воздействие этанола на кожу привело к появлению многих дерматологических аномалий, таких как ладонная эритема, полнокровие, инфекции и приливы.6 Биопсии, полученные с кожи доноров, злоупотребляющих алкоголем, подтвердили аномалию структуры ткани, а изолированные фибробласты вызвали длительное время пролиферации.6 Некоторые данные предполагают, что этанол может влиять на заживление ран, вмешиваясь в биосинтез коллагена I и III.7 Этанол обычно используется в косметике, фармацевтика и дезинфицирующие средства.8,9 Большое количество спиртов используется в качестве разбавителей, консервантов, ингредиентов увлажняющих веществ или ароматизаторов в косметических средствах, наносимых на кожу.9,10 Концентрация этанола в продукте для типичного применения может варьироваться от менее чем От 1% до 96.9%.
Гиалуроновая кислота (ГК) оказалась полезным средством при заживлении ран и воспалительных процессах. Это подтверждено исследованиями in vivo и in vitro.11,12 Примерно половина продуцируемого гиалуронана синтезируется фибробластами и находится во внеклеточном матриксе кожи. Связывание HA с кластером дифференцировки 44 (CD44) и рецептором для подвижности, опосредованной гиалуроновой кислотой (RHAMM) на фибробластах, может влиять на передачу сигналов, тем самым регулируя рост, дифференцировку, адгезию и синтез коллагена клеток.13 Синтез коллагена в фибробластах может запускаться разными способами, одним из которых является пролидаза-зависимый механизм. 12
Механизм защитного действия ГК в отношении нарушений метаболизма коллагена при воздействии этанола неизвестен. Поэтому мы сосредоточились на механизме индуцированного этанолом подавления биосинтеза коллагена и роли ГК в этом процессе. Чтобы изучить и охарактеризовать потенциальные негативные последствия воздействия этанола на фибробласты кожи, мы исследовали его влияние на экспрессию коллагена I типа, интегрина β 1 и рецептора инсулиноподобного фактора роста 1 (IGF-IR), фосфорилированных митоген-активируемых. протеинкиназы (MAPKs: ERK 1 / ERK 2 ), протеинкиназа B (Akt), ядерный фактор, усиливающий легкую каппа-цепь активированных B-клеток (NF-κB), каспаза 9 и активность пролидазы в культивированные фибробласты кожи человека.
Материалы и методы
Культура клеток
Первичный дермальный фибробласт: нормальный, человек, взрослый ATCC ® PCS-201-012 ™ был приобретен в ATCC (Манассас, Вирджиния, США), а натриевая соль HA H5542 была приобретена у Sigma -Олдрич (Сент-Луис, Миссури, США). Клетки поддерживали в среде Игла, модифицированной Дульбекко, с добавлением 10% фетальной бычьей сыворотки (HyClone Laboratories, Логан, Юта, США), 2 мМ глутамина, 50 Ед / мл пенициллина и 50 мкг / мл стрептомицина при 37 ° C в 5 % CO 2 инкубатор.Клетки использовали между пассажами 10 и 14 для всех экспериментов. Получено этическое разрешение Белостокского медицинского университета на использование линий клеток человека.
Синтез коллагена
Включение радиоактивного предшественника в белки измеряли после мечения конфлюэнтных фибробластов, культивируемых в питательной среде с различными концентрациями этанола и HA 500 мкг / мл в течение 24 часов в бессывороточной среде с 5 [ 3 H] пролин (5 мкКи / мл, 28 Ки / ммоль).Количество включенной метки в коллаген определяли путем переваривания белков очищенной коллагеназой Clostridium histolyticum по методу Петеркофски и Дигельмана.14
Определение активности пролидазы
Активность пролидазы измеряли с использованием метода, описанного Myara et al. Концентрацию белка измеряли методом Lowry et al.16. Клетки собирали перед центрифугированием при 200 × g в течение 15 минут. От супернатанта отказались.Затем осадок ресуспендировали в (4- (2-гидроксиэтил) -1-пиперазинэтансульфоновой кислоте (HEPES) (50 мМ, pH 7,8) и разрушали ультразвуком (3 × 10 секунд при температуре 0 ° C). После этого следовало центрифугирование при 12000 × г в течение 30 минут при 4 ° C, и белок был определен в супернатанте, и была проанализирована активность пролидазы. Затем 100 мкл пробы супернатанта клеточного экстракта были смешаны с HEPES (100 мкл, 50 мМ, pH 7,8. ), который содержал MnCl 2 (для достижения конечной концентрации 1 мМ MnCl 2 ).Образцы инкубировали при 37 ° C в течение 24 часов перед тем, как инициировать введение 100 мкл 94 мМ глицилпролина (Gly-Pro) для достижения 47 мМ конечной концентрации Gly-Pro. Затем образцы инкубировали при 7 ° C в течение 60 минут и реакцию останавливали добавлением 0,45 М трихлоруксусной кислоты (TCA) (порция 1 мл). TCA добавляли в параллельные неиспользованные пробирки в «нулевой момент». Затем следовало центрифугирование образцов в течение 15 минут при 10,000 × g . Определение пролина происходило путем добавления TCA / супернатанта (0.5 мл) к смеси (1: 1) ледяной уксусной кислоты / реактива Чинарда. Затем все инкубировали при 90 ° C в течение 10 минут. Колориметрию (поглощение при 515 нм) использовали для определения пролина по отношению к стандартам пролина. Результаты выражали в наномолях пролина, высвобождаемого в минуту на миллиграмм белка.
Биосинтез ДНК
Изучено влияние исследуемых веществ на включение фибробластов [ 3 H] -тимидина. В 24-луночные чашки для культур ткани клетки высевали из расчета 1 × 10 5 клеток / лунку, используя 1 мл ростовой среды в каждой лунке.Через 48 часов (1,6 ± 0,1 × 10 5 клеток / лунку) в лунки для культивирования добавляли различные концентрации этанола с 500 мкг / мл гиалуронана или без него на 24 часа при 37 ° C. После этого в лунки добавляли 0,5 мкКи [ 3 H] -тимидина (6,7 Ки / ммоль) и культуры инкубировали при 37 ° C в течение 4 часов. Затем клетки промывали трижды 1 мл 0,05 М трис-HCl и дважды 5% ТХК. После этого проводили лизис клеток в 1 мл 0,1 М NaOH, содержащем 1% додецилсульфат натрия (SDS).Затем добавляли 4 мл сцинтилляционной жидкости и измеряли радиоактивность на сцинтилляционном счетчике.
Анализ цитотоксичности
Жизнеспособность клеток оценивали с помощью анализа метилтиазолилтетразолия (МТТ), который основан на превращении желтого тетразолийбромида МТТ в пурпурное производное формазана митохондриальным ферментом сукцинатдегидрогеназой в жизнеспособных клетках. В конце инкубационного периода среду переносили в 96-луночные планшеты для определения цитокинов.Клетки промывали 0,2 мл фосфатно-солевого буфера и анализировали на цитотоксичность в том же лотке. Для обработанных клеток токсичность выражали в процентах.
SDS-PAGE
Метод Лэммли использовали для проведения электрофореза в пластинчатом 10% -ном додецилсульфат-полиакриламидном геле (SDS-PAGE). Анализировали образцы клеточных супернатантов (20 мкг белка). В качестве стандартов использовали: миозин (200 кДа), галактозидазу (116,2 кДа), фосфорилазу b (97,4 кДа), бычий сывороточный альбумин (66.2 кДа) и овальбумин (45 кДа) (Bio-Rad, Беркли, Калифорния, США).
Вестерн-блот-анализ
Метод Лэммли использовали для проведения электрофореза в пластинчатом SDS-PAGE. Анализировали равные порции клеточных супернатантов (20 мкг белка). Мы конденсировали десятикратную культуральную среду с использованием центриконов (отсечка 3 кДа), смешанных с буфером для образцов Лэммли (содержащим 2,5% SDS, без восстановителя). Электрофорез проводили с равными порциями (100 мкг) белка. После электрофореза клетки уравновешивали в 25 мМ Трис с 0.2 М глицин в 20% метаноле (об. / Об.) В течение 5 минут. Образцы переносили в поры нитроцеллюлозы размером 0,2 мкм при 100 мА в течение 1 часа. Для этой процедуры использовалась система электрофореза LKB 2117 Multiphor II Multiphor (GE Healthcare Bio-Sciences AB, Упсала, Швеция). Мы инкубировали нитроцеллюлозу в течение 1 часа с моноклональными антителами против коллагена I (концентрация 1: 1000), моноклональными антителами против фосфо-Akt (концентрация 1: 1000), поликлональными антителами против NF-κB (концентрация 1: 1000), моноклональное антитело против фосфо-MAPK (ERK 1/2 ) (концентрация 1: 1000), моноклональное антитело против каспазы 9 (концентрация 1: 1000).Антитела растворяли в растворе, содержащем 5% сухого молока, в трис-буферном физиологическом растворе с Tween 20 (TBS-T) (20 ммоль / л буфера Tris – HCl, pH 7,4, содержащего 150 ммоль / л NaCl и 0,05% Tween 20). . Для анализа фосфо-MAPK (ERK 1 / ERK / 2 ) и фосфо-AKT добавляли конъюгат щелочной фосфатазы против мышиного IgG (цельная молекула) в концентрации 1: 5000 в TBS-T. Для анализа NF-κB и каспазы-9, конъюгированного вторым антителом к щелочной фосфатазе, добавляли антикроличий IgG (целая молекула) в концентрации 1: 5000 в TBS-T.Для анализа коллагена типа I и конъюгированного второго антитела β-актина и щелочной фосфатазы добавляли анти-козий IgG (целая молекула) в концентрации 1: 5000 в TBS-T. Всю смесь инкубировали 30 минут при медленном встряхивании. После этого нитроцеллюлозу промывали TBS-T (5 × 5 минут) и обрабатывали реагентом жидкого субстрата 5-бром-4-хлор-3-индолилфосфат / нитросиний тетразолий. Интенсивность полос определяли количественно с помощью денситометрического анализа.
Зимография
Желатинолитическую активность измеряли с использованием метода Unemori и Werb.18 Мы конденсировали десятикратную культуральную среду с использованием центриконов (отсечка 3 кДа), смешанных с буфером для образцов (содержащим 2,5% SDS, без восстановителя). Электрофорез проводили с равными количествами белка (20 мкг) на полиакриламидных гелях (10%) в невосстанавливающих условиях. Гели пропитывали желатином (1 мг / мл). Инкубацию геля после электрофореза для удаления SDS проводили в течение 30 минут в 2% Triton X-100. После этого следовала инкубация в буфере, содержащем 50 мМ Трис – HCl, pH 8 с CaCl 2 5 мМ (субстратный буфер) в течение 18–24 часов при 37 ° C.После этого для окрашивания использовали кумасси бриллиантовый синий R250 (Thermo Fisher Scientific, Уолтем, Массачусетс, США).
Статистические методы
Средние значения по крайней мере для трех анализов ± стандартное отклонение (± SD) были рассчитаны во всех соответствующих экспериментах. Статистический анализ проводился с применением двустороннего непарного критерия Стьюдента t и дисперсионного анализа. Использовалась программа IBM SPSS 22.0 Statstics Genericom (IBM Corporation, Армонк, Нью-Йорк, США). П <0.05 и P <0,01 признан статистически значимым.
Результаты
Чтобы оценить активность этанола в синтезе коллагена в фибробластах кожи человека, клетки инкубировали в течение 24 часов в 25, 50 и 100 мМ этанола, а также в этаноле с HA в концентрации 500 мкг. / мл. Было показано, что этанол вызывает снижение синтеза коллагена дозозависимым образом (и). Воздействие на фибробласты различных концентраций этанола способствует ингибированию биосинтеза коллагена на 58.08% (2,39% ± стандартное отклонение; n = 3), 76,23% (3,52% ± стандартное отклонение; n = 3), 83,15% (4,03% ± стандартное отклонение; n = 3) P <0,05, P <0,01, соответственно по сравнению с контрольным значением. Однако в присутствии HA в концентрации 500 мкг / мл эффективность этанола по ингибированию биосинтеза коллагена была намного ниже. ГК, добавленный только к клеткам, не оказывал значительного влияния на биосинтез коллагена в контрольных клетках. Представленные результаты свидетельствуют о том, что этанол оказывает ингибирующее действие на синтез коллагена в сливающихся фибробластах кожи человека, а ГК противодействует этому процессу (и).
Биосинтез коллагена, измеренный как включение 5 [ 3 H] -пролина в белки, чувствительные к действию бактериальной коллагеназы, в сливающихся фибробластах кожи человека, инкубированных в течение 24 часов с различными концентрациями этанола и HA.
Примечания: Тест ANOVA: ** P <0,01. Планки погрешностей представляют собой ± стандартное отклонение; п = 3.
Сокращения: ANOVA, дисперсионный анализ; HA, гиалуроновая кислота; ДМСО, диметилсульфоксид; dpm, распадов в минуту.
Вестерн-иммуноблот-анализ коллагена типа I в субконфлюэнтных фибробластах кожи человека (контроль), клетках, обработанных с или без HA в течение 24 часов. Интенсивность окрашивания полос определяли количественно с помощью денситометрического анализа. Тест Стьюдента t -тест, * P <0,05 и ** P <0,01.
Примечания: 1, контроль; 2, этанол 25 мМ; 3, этанол 50 мМ; 4, этанол 100 мМ; 5, НА; 6, этанол 25 мМ и НА; 7, этанол 50 мМ и НА; 8, этанол 100 мМ и НА.Образцы, используемые для электрофореза, состояли из 20 мкг белка объединенных экстрактов клеток.
Сокращения: AU, условные единицы; HA, гиалуроновая кислота.
Фермент, ответственный за рециклинг пролина для ресинтеза коллагена, — пролидаза и ММП. Добавление этанола в концентрациях 25, 50 и 100 мМ к культурам клеток способствовало снижению активности пролидазы на 29,05% (4,55% ± стандартное отклонение; n = 3), 56,15% (3,82% ± стандартное отклонение; n = 3), и 88,18% (1,16% ± стандартное отклонение; n = 3). Добавление НА оказало значительный защитный эффект на активность пролидазы в фибробластах, инкубированных с этанолом.ГК восстанавливала активность пролидазы в клетках, инкубированных с этанолом, до контрольного уровня ().
Активность пролидазы в конфлюэнтных фибробластах кожи человека, инкубированных в течение 24 часов с различными концентрациями этанола и НА.
Примечания: Тест ANOVA: * P <0,05, ** P <0,01. Планки погрешностей представляют собой ± стандартное отклонение; п = 3.
Сокращения: ANOVA, дисперсионный анализ; HA, гиалуроновая кислота.
Проведенные исследования доказывают, что этанол нарушает метаболизм коллагена в фибробластах кожи человека, что приводит к значительному снижению синтеза ДНК.Распад за минуту [ 3 H] тимидина, включенного в ДНК этих клеток, был принят за 100%. Это было эталонное значение. Мы оценили эффект этанола в присутствии или в отсутствие ГК (500 мг / мл). Воздействие на фибробласты этанола различных концентраций способствовало ингибированию синтеза ДНК на 21,06% (7,08% ± стандартное отклонение; n = 3), 44,15% (5,06% ± стандартное отклонение; n = 3), 56,27% (4,26% ± стандартное отклонение; n = 3), 50,16% (4,56% ± стандартное отклонение; n = 3) P <0,05, P <0,01, соответственно, по сравнению с контрольным значением.ГК оказывает защитное влияние на процессы, вызванные этанолом ().
Биосинтез ДНК, измеренный по включению [ 3 H] -тимидина в ДНК в фибробластах кожи человека (контроль), инкубированных в течение 24 часов с различными концентрациями этанола и НА.
Примечания: Тест ANOVA: * P <0,05, ** P <0,01. Планки погрешностей представляют собой ± стандартное отклонение; п = 3.
Сокращения: ANOVA, дисперсионный анализ; HA, гиалуроновая кислота.
Эффективность HA в снижении цитотоксичности 25, 50 и 100 мМ этанола показана на рисунке. Было показано, что этанол вызывает цитотоксичность дозозависимым образом. Наличие этанола ингибирования выживаемости клеток 20,16% (4,05% ± стандартное отклонение; n = 3), 35,18% (3,63% ± стандартное отклонение; n = 3), 56,03% (2,53% ± стандартное отклонение; n = 3) P < 0,01 соответственно по сравнению с контрольным значением. Рецептор интегрина β 1 играет ключевую роль в контроле биосинтеза коллагена и активности пролидазы. В этом исследовании мы обнаружили, что этанол снижает экспрессию рецептора интегрина β 1 дозозависимым образом.В культивируемых клетках, инкубированных с HA и этанолом, этот эффект исчез. Было обнаружено, что экспрессия рецептора интегрина в клетках, обработанных различными концентрациями этанола и HA, была такой же, как и в контрольных клетках ().
Цитотоксичность фибробластов кожи человека (контроль), инкубированных в течение 24 часов с различными концентрациями этанола и НА.
Примечания: Тест ANOVA: * P <0,05, ** P <0,01. Планки погрешностей представляют собой ± стандартное отклонение; п = 3.
Сокращения: ANOVA, дисперсионный анализ; HA, гиалуроновая кислота.
Вестерн-иммуноблот-анализ для β 1 интегрина ( A ), рецептора инсулиноподобного фактора роста I ( B ), ERK 1/2 ( C ), киназы Akt ( D ), каспаза 9 ( E ) и β-актин ( F ) в субконфлюэнтных фибробластах кожи человека (контроль), клетках, обработанных с или без HA в течение 24 часов. Интенсивность окрашивания полос определяли количественно с помощью денситометрического анализа.
Примечания: Студенческий тест t -тест: * P <0,05, ** P <0,01. 1, контроль; 2, этанол 25 мМ; 3, этанол 50 мМ; 4, этанол 100 мМ; 5, НА; 6, этанол 25 мМ и НА; 7, этанол 50 мМ и НА; 8, этанол 100 мМ и НА. Образцы, используемые для электрофореза, состояли из 20 мкг белка объединенных экстрактов клеток.
Сокращения: AU, условные единицы; ERK, киназа, регулируемая внеклеточными сигналами; HA, гиалуроновая кислота.
Известно, что перекрестное взаимодействие между рецептором интегрина β 1 и рецептором IGF-IR играет ключевую роль в активации экспрессии гена коллагена и активности пролидазы.Этанол, как и в случае рецептора интегрина, вызывал снижение экспрессии IGF-IR (дозозависимым образом). ГК также оказывает защитное действие на уровень экспрессии этого рецептора (). В этом случае экспрессия рецептора IGF-IR в клетках, инкубированных с этанолом и HA, была близка к контролю.
Сигнал, передаваемый стимулированным IGF-IR и β 1 рецептором интегрина, приводит к активации MAPK (ERK 1/2 ) и Akt.14,15. Как видно на фибробластах, обработанных этанолом, экспрессия MAPK (фосфо-ERK 1/2 ) снижалось дозозависимым образом.Добавление HA к клеткам, обработанным этанолом, оказало защитное действие на зависимое от этанола снижение экспрессии фосфо-ERK 1/2 . Этанол и этанол с HA, добавленные к культивированным фибробластам, не влияли на экспрессию фосфо-AKT киназ (). Различные концентрации этанола оказывают цитотоксическое действие на фибробласты кожи человека, что приводит к индукции апоптоза, что приводит к наблюдаемому увеличению экспрессии каспазы 9 (). Более того, применение ГК оказывает защитное действие на нарушения пролиферации клеток, вызванные этанолом.Более того, экспрессия β-актина не изменялась в клетках при обработке этанолом в присутствии или в отсутствие НА ().
Некоторые данные свидетельствуют о том, что пролидаза-зависимая регуляция биосинтеза коллагена может иметь место на уровне транскрипции, в зависимости от экспрессии NF-κB. NF-κB — это фактор транскрипции, который действует как ингибитор экспрессии альфа 1 и альфа 2 субъединиц коллагена типа I. 19,20 Мы обнаружили повышенную экспрессию NF-κB в фибробластах, обработанных этанолом ().Добавление НА к клеткам, обработанным этанолом, способствовало снижению экспрессии этого транскрипционного фактора до контрольного уровня. Более того, экспрессия β-актина не изменялась в клетках при обработке этанолом в присутствии или в отсутствие НА (). Похоже, что регуляторный механизм индуцированной этанолом аберрации коллагена имеет место в точке биосинтеза коллагена, поскольку не было обнаружено влияния этанола и ГК на процесс деградации коллагена ММП-2 и ММП-9 ().
Вестерн-иммуноблот-анализ белка p65 NF-κB ( A ) и β-актина ( B ) в субконфлюэнтных фибробластах кожи человека (контроль), клетках, обработанных с или без HA в течение 24 часов.Интенсивность окрашивания полос определяли количественно с помощью денситометрического анализа.
Примечания: Студенческий тест t -тест: ** P <0,01. 1, контроль; 2, этанол 25 мМ; 3, этанол 50 мМ; 4, этанол 100 мМ; 5, НА; 6, этанол 25 мМ и НА; 7, этанол 50 мМ и НА; 8, этанол 100 мМ и НА. Образцы, используемые для электрофореза, состояли из 20 мкг белка объединенных экстрактов клеток.
Сокращения: AU, условные единицы; HA, гиалуроновая кислота.
Зимография для MMP-9 (92 кДа) и MMP-2 (72 кДа) в субконфлюэнтных фибробластах кожи человека (контроль), клетках, обработанных с или без HA в течение 24 часов.
Примечания: Интенсивность окрашивания полос количественно определяли с помощью денситометрического анализа. 1, контроль; 2, этанол 25 мМ; 3, этанол 50 мМ; 4, этанол 100 мМ; 5, НА; 6, этанол 25 мМ и НА; 7, этанол 50 мМ и НА; 8, этанол 100 мМ и НА. Образцы, используемые для электрофореза, состояли из 20 мкг белка объединенных экстрактов клеток.
Сокращения: AU, условные единицы; HA, гиалуроновая кислота; ММП, матричная металлопротеиназа.
Обсуждение
Хотя цитотоксичность этанола хорошо известна, механизм ее воздействия на метаболизм коллагена в тканях до конца не изучен.Похоже, что аномалии метаболизма коллагена, вызванные этанолом, тканеспецифичны. В печени он может способствовать стимуляции биосинтеза коллагена с последствием фиброза тканей, в то время как в коже может происходить противоположный процесс с последствием заживления ран.
В этом исследовании мы предоставили доказательства того, что этанол подавляет метаболизм коллагена в фибробластах кожи посредством нескольких уровней регуляции этого белка. Сначала это влияет на активность пролидазы, фермента, который играет важную роль в биосинтезе коллагена.Фермент отвечает за рециркуляцию пролина для ресинтеза коллагена, тем самым определяя выработку коллагена. Пептидные связи между пролином и другими аминокислотами могут быть расщеплены также другой пептидазой, пролиназой, которой необходим пролин в N-концевом положении.21 Пролидаза — вторая иминопептидаза, которая расщепляет дипептиды С-концевым пролином для сбора свободного пролина. Фермент переваривает как эндогенные, так и диетические дипептиды Xaa-Pro.21
Другой уровень регуляции метаболизма коллагена в обработанных этанолом фибробластах был обнаружен при β 1 интегрина и IGF-IR.Ранее мы обнаружили, что перекрестные помехи между рецепторами способствуют усилению биосинтеза коллагена. 22 В настоящем исследовании мы обнаружили, что этанол способствует подавлению экспрессии обоих рецепторов. Одновременно мы обнаружили повышение транскрипционной активности NF-κB, известного ингибитора коллагена типа I, который субъединиц экспрессии гена.20 В результате проведенных исследований был сделан вывод, что этанол приводит к нарушению биосинтеза коллагена в фибробластах. культур за счет снижения активности пролидазы и экспрессии интегрина β 1 и IGF-IR.Это сопровождалось пониженной экспрессией белков сигнального пути, индуцированной интегрином β 1 и IGF-IR, то есть киназами MAPK (ERK 1/2 ). Пониженное количество синтезированного коллагена и нарушение активности пролидазы также может быть связано с активацией фактора транскрипции NF-κB, который подавляет экспрессию гена коллагена. Применение ГК в концентрации 500 мкг / мл оказывает защитное действие на нарушения, вызванные исследуемыми веществами. Совокупность процессов, на которые влияет этанол, объясняет механизм индуцированного этанолом подавления биосинтеза коллагена.Основываясь на наших предыдущих исследованиях, мы рассматривали ГК как средство, противодействующее вызванной этанолом дерегуляции метаболизма коллагена в фибробластах.11 Фактически, мы обнаружили, что ГК устраняет все изученные дефекты метаболизма коллагена, вызванные этанолом. В нашей предыдущей статье мы не наблюдали отменяющего эффекта ГК, когда кофеин подавлял синтез коллагена.23 Различные концентрации этанола оказывают цитотоксическое действие на фибробласты кожи человека, что приводит к снижению выживаемости, ингибированию биосинтеза ДНК и индукции апоптоза, что приводит к в наблюдаемом повышении экспрессии каспазы 9.Более того, применение ГК оказывает защитное действие на дефект пролиферации клеток, вызванный этанолом.
HA играет важную роль в поддержании внеклеточного матрикса и вызывает защитное действие на структуру коллагена. 24,25 HA — это искусство гликозаминогликанов, где d-глюкуроновая кислота связана с частицей N -ацетилглюкозамина через гликозидные связи26. , 27 Клетка окружена слоем гиалуронана, который отвечает за форму, адгезию и миграцию клетки.24 Кожа содержит примерно 50% всей гиалуроновой кислоты в организме. ГК улучшает процессы заживления при некоторых патологических состояниях, таких как венозные язвы или повреждения мембран. Данные литературы показывают, что ГК играет полезную роль в регенеративных процессах, связанных с дисфункцией синтеза коллагена.28 Мы можем предположить, что ГК защищает от нарушений, вызванных этанолом. Этот защитный эффект можно контролировать посредством взаимодействия гиалуронана с его рецепторами CD44 и / или RHAMM.29 По крайней мере, в эндотелиальных клетках этот механизм способствует стимуляции выработки коллагена.30 Вопрос о том, играют ли рецепторы CD44 и RHAMM важную роль в механизме НА-зависимого противодействия токсичности этанола, требует дальнейшего изучения.
Данные, представленные в этой статье, могут иметь определенное социальное значение. Они предполагают, что фибробласты особенно чувствительны к этанолу и реагируют на это соединение путем ингибирования биосинтеза коллагена. Этот процесс способствует старению кожи, что представляет особый интерес для косметологии. Принимая во внимание приведенные выше данные и тот факт, что этанол обычно используется в косметологии, можно предположить, что этанол можно заменить в косметике другим растворителем или консервантами.Также можно рассматривать включение ГК в косметические препараты, содержащие этанол.
Выражение признательности
MD является научным сотрудником в области проектных исследований, исследований, коммерциализации: программа поддержки докторантов UMB, подмера 8.2.1 Операционная программа человеческого капитала, софинансируемая Европейским союзом в рамках Европейского социального фонда. Работа частично поддержана грантами Белостокского медицинского университета (143-14749F, 143-30730F, 144-30828F).
Сноски
Раскрытие информации
Авторы сообщают об отсутствии конфликта интересов в этой работе.
Ссылки
1. Сид Б., Верракс Дж., Кальдерон ПБ. Роль активации AMPK в окислительном повреждении клеток: последствия для алкогольной болезни печени. Biochem Pharmacol. 2013. 86 (2): 200–209. [PubMed] [Google Scholar] 2. Эль-Хадж Э.С., Эль-Хадж М.К., Волошенюк Т.Г. и др. Алкогольная модуляция металлопротеиназ сердечного матрикса (ММП) и тканевых ингибиторов ММП способствует накоплению коллагена. Alcohol Clin Exp Res. 2014. 38 (2): 448–456. [Бесплатная статья PMC] [PubMed] [Google Scholar] 3. Xu GF, Li PT, Wang XY и др.Динамические изменения экспрессии матриксных металлопротеиназ и их ингибиторов, TIMP, во время фиброза печени, вызванного алкоголем у крыс. Мир Дж. Гастроэнтерол. 2004. 10 (24): 3621–3627. [Бесплатная статья PMC] [PubMed] [Google Scholar] 4. Neuman MG, Nanau RM, Oruña L, Coto G. Противовоспалительные эффекты гиалуроновой кислоты in vitro при повреждении клеток кожи, вызванном этанолом. J. Pharm. Pharm. Sci. 2011. 14 (3): 425–437. [PubMed] [Google Scholar] 5. Пржилипиак А., Рабе Т., Хафнер Дж., Пржилипиак М., Руннебаум Б.Влияние этанола на рост in vitro клеточной линии карциномы молочной железы человека MCF-7. Arch Gynecol Obstet. 1996. 258 (3): 137–140. [PubMed] [Google Scholar] 6. Джонен Ч., Хартманн Б., Штеффен И. и др. Выделение и размножение клеток кожи для трансплантации клеток ограничено у пациентов, употребляющих табак, алкоголь или страдающих сахарным диабетом. Бернс. 2006. 32 (2): 194–200. [PubMed] [Google Scholar] 7. Ранзер MJ, Чен Л., ДиПьетро Л.А. При острой интоксикации этанолом нарушается функция фибробластов и прочность на разрыв раны.Alcohol Clin Exp Res. 2011; 35 (1): 83–90. [Бесплатная статья PMC] [PubMed] [Google Scholar] 8. Бойс Дж. М.. Обновите информацию о гигиене рук. Am J Infect Control. 2013. 41 (5): 94–96. [PubMed] [Google Scholar] 9. Ким И-Ч, Пак Джей-Х, Людовице П.Дж., Праусниц MR. Синергетическое усиление проницаемости кожи N-лауроилсаркозином и этанолом. Int J Pharmaceutics. 2008. 352 (1–2): 129–138. [PubMed] [Google Scholar] 10. Pendlington RU, Whittle E, Robinson JA, Howes D. Судьба этанола, наносимого на кожу местно. Food Chem Toxicol. 2001. 39 (2): 169–174.[PubMed] [Google Scholar] 11. Surazynski A, Miltyk W, Czarnomysy R, Grabowska J, Palka J. Гиалуроновая кислота отменяет зависимую от оксида азота стимуляцию деградации коллагена в культивируемых хондроцитах человека. Pharmacol Res. 2009. 60 (1): 46–49. [PubMed] [Google Scholar] 12. Гази К., Денг-Пичон У., Варнет Дж.М., Крыса П. Фрагменты гиалуроновой кислоты улучшают заживление ран на кожной модели in vitro за счет базовой активации пуринорецептора P2X7: роль молекулярной массы. PLoS One. 2012; 7 (11): e48351. [Бесплатная статья PMC] [PubMed] [Google Scholar] 13.Nawrat P, Surazynski A, Karna E, Pałka JA. Влияние гиалуроновой кислоты на индуцированное интерлейкином-1 нарушение регуляции метаболизма коллагена в культивируемых фибробластах кожи человека. Pharmacol Res. 2005. 51 (5): 473–477. [PubMed] [Google Scholar] 14. Петеркофский Б., Дигельманн Р. Использование смеси коллагеназ, свободных от протеиназ, для специфического анализа радиоактивного коллагена в присутствии других белков. Биохимия. 1971; 10 (6): 988–994. [PubMed] [Google Scholar] 15. Myara I, Charpentier C, Lemonnier A. Оптимальные условия для анализа пролидазы колориметрическим определением пролина: применение к иминодипептидурии.Clin Chim Acta. 1982; 125 (2): 193–205. [PubMed] [Google Scholar] 16. Лоури Н., Розенбро Н., Фарр Л., Рэндалл Р. Измерение белка с реагентом фолин-фенол. J Biol Chem. 1951; 193 (1): 265–275. [PubMed] [Google Scholar] 17. Laemmli UK. Расщепление структурных белков при сборке головки бактериофага Т4. Природа. 1970. 227 (5259): 680–685. [PubMed] [Google Scholar] 18. Unemori E, Werb Z. Реорганизация полимеризованного актина: возможный спусковой механизм для индукции проколлагеназы в фибробластах, культивируемых в коллагеновых гелях и на них.J Cell Biol. 1986. 103 (3): 1021–1031. [Бесплатная статья PMC] [PubMed] [Google Scholar] 19. Коуба Д., Чунг К.-Й, Нишияма Т. и др. Ядерный фактор-κB опосредует ингибирующее действие TNF-α на транскрипцию гена коллагена α2 (I) (COL1A2) в дермальных фибробластах человека. J Immunol. 1999. 162 (7): 4226–4234. [PubMed] [Google Scholar] 20. Miltyk W, Karna E, Palka J. Независимый от пролидазы механизм камптотецина-индуцированного ингибирования биосинтеза коллагена в культивируемых фибробластах кожи человека. J Biochem. 2007. 141 (2): 287–292.[PubMed] [Google Scholar] 21. Китченер Р.Л., Грюнден А.М. Функция пролидазы в метаболизме пролина и ее медицинские и биотехнологические применения. J Appl Microbiol. 2012. 113 (2): 233–247. [PubMed] [Google Scholar] 22. Surazynski A, Miltyk W, Prokop I, Palka J. Пролидазозависимая регуляция экспрессии рецепторов TGF и TGF β в фибробластах кожи человека. Eur J Pharmacol. 2010. 649 (1–3): 115–119. [PubMed] [Google Scholar] 23. Донейко М., Пржилипиак А., Рысяк Э., Глушук К., Суразинский А. Влияние кофеина и гиалуроновой кислоты на биосинтез коллагена в фибробластах кожи человека.Drug Des Devel Ther. 2014; 8: 1923–1928. [Бесплатная статья PMC] [PubMed] [Google Scholar] 25. Karna E, Miltyk W, Surazyński A, Pałka JA. Защитный эффект гиалуроновой кислоты на индуцированную интерлейкином-1 дерегуляцию передачи сигналов рецептора бета1-интегрина и инсулиноподобного фактора роста-I и биосинтез коллагена в культивируемых хондроцитах человека. Mol Cell Biochem. 2008. 308 (1–2): 57–64. [PubMed] [Google Scholar] 26. Гириш К.С., Кемпараджу К. Волшебный клей гиалуронан и его ластик гиалуронидаза: биологический обзор.Life Sci. 2007. 80 (21): 1921–1943. [PubMed] [Google Scholar] 27. Шефер Л, Шефер РМ. Протеогликаны: от структурных соединений до сигнальных молекул. Cell Tissue Res. 2010. 339 (1): 237–246. [PubMed] [Google Scholar] 28. Суразинский А., Милтык В., Палка Дж., Панг Дж. М.. Пролидазозависимая регуляция биосинтеза коллагена. Аминокислоты. 2008. 35 (4): 731–738. [PubMed] [Google Scholar] 29. Aruffo A, Stamenkovic I, Melnick M, Underhill CB, Seed B. CD44 является основным рецептором гиалуроната на клеточной поверхности. Клетка.1990. 61 (7): 1303–1313. [PubMed] [Google Scholar] 30. Руни П., Ван М., Кумар П., Кумар С. Ангиогенные олигосахариды гиалуронана увеличивают выработку коллагенов эндотелиальными клетками. J Cell Sci. 1993. 105 (1): 213–218. [PubMed] [Google Scholar]
Гиалуроновая кислота отменяет этанол-зависимое ингибирование биосинтеза коллагена в культивируемых фибробластах человека
Drug Des Devel Ther. 2015; 9: 6225–6233.
Магдалена Донейко
1 Кафедра эстетической медицины, Медицинский университет Белостока, Белосток, Польша
Анджей Пржилипяк
1 Кафедра эстетической медицины, Медицинский университет Белостока
, Белосток, Польша
2 Кафедра медицинской химии, Медицинский университет Белостока, Белосток, Польша
Войцех Милтык
3 Кафедра фармацевтического анализа, Фармацевтический факультет, Медицинский университет Белостока, Белосток, Белосток
Кафедра эстетической медицины, Медицинский университет Белостока, Белосток, Польша
Ежи Пжилипяк
4 Медицинский офис, Белосток, Польша
Илона Заремба
2 ł Кафедра медицинской химии Беловостокского медицинского университета Польша
Аркадиуш Суразиньс ki
2 Кафедра медицинской химии Белостокского медицинского университета, Белосток, Польша
1 Кафедра эстетической медицины Белостокского медицинского университета, Белосток, Польша
2 Кафедра медицинской химии медицинского университета Белосток, Белосток, Польша
3 Кафедра фармацевтического анализа, Фармацевтический факультет, Белостокский медицинский университет, Белосток, Польша
4 Медицинский офис, Белосток, Польша
Переписка: Магдалена, Медицинский факультет, Эстонский факультет of Pharmacy, Медицинский университет Белостока, улица Академицкая 3, 15-267 Белосток, Польша, Email moc.liamg @ okjenod Авторские права © 2015 Donejko et al. Эта работа опубликована Dove Medical Press Limited и находится под лицензией Creative Commons Attribution — Non Commercial (unported, v3.0) License. Полные условия лицензии доступны по адресу http://creativecommons.org/licenses/by-nc/3.0 /. Некоммерческое использование работы разрешено без какого-либо разрешения Dove Medical Press Limited при условии правильной ссылки на эту статью. Эта статья цитируется в других статьях PMC.
Abstract
Введение
Целью исследования было оценить влияние этанола на биосинтез коллагена в культивируемых фибробластах кожи человека и роль гиалуроновой кислоты (HA) в этом процессе.Что касается механизма действия этанола на фибробласты кожи человека, мы исследовали: экспрессию интегрина β 1 и рецептора инсулиноподобного фактора роста 1 (IGF-IR), экспрессию белков сигнального пути: митоген-активированные протеинкиназы (MAPK), протеинкиназы. B (Akt), ядерный фактор, каппа B (NF-κB), фактор транскрипции, анализ цитотоксичности и апоптоза, активность металлопротеиназы, а также влияние HA на эти процессы.
Материалы и методы
Биосинтез коллагена, активность пролидазы, биосинтез ДНК и цитотоксичность были измерены в конфлюэнтных культурах фибробластов кожи человека, обработанных 25, 50 и 100 мМ этанолом, этанолом и 500 мкг / мл HA.Вестерн-блот-анализ и зимография были выполнены для оценки экспрессии коллагена типа I, рецептора интегрина β 1 , IGF-IR, белка NF-κB, белка фосфо-Akt, киназы MAPK, активности каспазы 9 и матриксных металлопротеиназ (MMP-9). и ММП-2).
Результаты
Дозозависимый этанол приводит к нарушению биосинтеза коллагена в культурах фибробластов за счет снижения активности пролидазы и экспрессии интегрина β 1 и IGF-IR. Это сопровождалось повышенной цитотоксичностью, апоптозом и снижением экспрессии белков сигнального пути, индуцированных интегрином β 1 и IGF-IR, то есть киназами MAPK (ERK 1/2 ).Пониженное количество синтезированного коллагена и нарушение активности пролидазы также может быть связано с активацией фактора транскрипции NF-κB, который подавляет экспрессию гена коллагена. Это предполагает, что снижение продукции коллагена фибробластами может быть вызвано нарушением его биосинтеза, но не деградацией. Применение ГК оказывает защитное действие на нарушения, вызванные исследуемыми веществами. По-видимому, регуляторный механизм индуцированной этанолом аберрации коллагена имеет место на уровне биосинтеза коллагена, поскольку не было обнаружено влияния этанола и ГК на процесс деградации коллагена ММП-2 и ММП-9.
Заключение
Это исследование предоставляет доказательства того, что этанол нарушает метаболизм коллагена в фибробластах кожи человека, что приводит к значительному снижению количества продуцируемого белка. Этот механизм, вероятно, связан с подавлением активности пролидазы, экспрессии интегрина β 1 и рецепторов IGF-IR, а также белков сигнального пути, индуцированных этими рецепторами.
Ключевые слова: коллаген , этанол, гиалуроновая кислота, фибробласты
Введение
Воздействие этанола (этилового спирта) может вызывать множество местных и систематических нарушений.Органы, которые особенно страдают от интоксикации этанолом, — это легкие, почки и печень.1 Было показано, что интоксикация этанолом вызывает окислительный стресс, что приводит к модуляции экспрессии металлопротеиназ и тканевых ингибиторов матриксных металлопротеиназ (ММП) в клетках сердца и печени, способствующих развитию изменения клеточного фенотипа на фибробластоподобные с дальнейшими последствиями в накоплении тканевого коллагена и фиброзе.2,3 В нескольких исследованиях задокументировано этанол-зависимое окислительное повреждение в печени.Было обнаружено, что механизм этого процесса может включать функцию митохондрий и выживаемость клеток.1 Таким образом, цитотоксичность этанола может способствовать апоптозу клеток или может вызывать провоспалительные цитокины.4 Было обнаружено, что алкоголь ингибирует рост клеток карциномы молочной железы человека MCF-7 в vitro.5
Кажется, что этанол особенно влияет на биосинтез коллагена I типа. Этот процесс происходит в основном в клетках печени, но также наблюдается и в клетках кожи. Воздействие этанола на кожу привело к появлению многих дерматологических аномалий, таких как ладонная эритема, полнокровие, инфекции и приливы.6 Биопсии, полученные с кожи доноров, злоупотребляющих алкоголем, подтвердили аномалию структуры ткани, а изолированные фибробласты вызвали длительное время пролиферации.6 Некоторые данные предполагают, что этанол может влиять на заживление ран, вмешиваясь в биосинтез коллагена I и III.7 Этанол обычно используется в косметике, фармацевтика и дезинфицирующие средства.8,9 Большое количество спиртов используется в качестве разбавителей, консервантов, ингредиентов увлажняющих веществ или ароматизаторов в косметических средствах, наносимых на кожу.9,10 Концентрация этанола в продукте для типичного применения может варьироваться от менее чем От 1% до 96.9%.
Гиалуроновая кислота (ГК) оказалась полезным средством при заживлении ран и воспалительных процессах. Это подтверждено исследованиями in vivo и in vitro.11,12 Примерно половина продуцируемого гиалуронана синтезируется фибробластами и находится во внеклеточном матриксе кожи. Связывание HA с кластером дифференцировки 44 (CD44) и рецептором для подвижности, опосредованной гиалуроновой кислотой (RHAMM) на фибробластах, может влиять на передачу сигналов, тем самым регулируя рост, дифференцировку, адгезию и синтез коллагена клеток.13 Синтез коллагена в фибробластах может запускаться разными способами, одним из которых является пролидаза-зависимый механизм. 12
Механизм защитного действия ГК в отношении нарушений метаболизма коллагена при воздействии этанола неизвестен. Поэтому мы сосредоточились на механизме индуцированного этанолом подавления биосинтеза коллагена и роли ГК в этом процессе. Чтобы изучить и охарактеризовать потенциальные негативные последствия воздействия этанола на фибробласты кожи, мы исследовали его влияние на экспрессию коллагена I типа, интегрина β 1 и рецептора инсулиноподобного фактора роста 1 (IGF-IR), фосфорилированных митоген-активируемых. протеинкиназы (MAPKs: ERK 1 / ERK 2 ), протеинкиназа B (Akt), ядерный фактор, усиливающий легкую каппа-цепь активированных B-клеток (NF-κB), каспаза 9 и активность пролидазы в культивированные фибробласты кожи человека.
Материалы и методы
Культура клеток
Первичный дермальный фибробласт: нормальный, человек, взрослый ATCC ® PCS-201-012 ™ был приобретен в ATCC (Манассас, Вирджиния, США), а натриевая соль HA H5542 была приобретена у Sigma -Олдрич (Сент-Луис, Миссури, США). Клетки поддерживали в среде Игла, модифицированной Дульбекко, с добавлением 10% фетальной бычьей сыворотки (HyClone Laboratories, Логан, Юта, США), 2 мМ глутамина, 50 Ед / мл пенициллина и 50 мкг / мл стрептомицина при 37 ° C в 5 % CO 2 инкубатор.Клетки использовали между пассажами 10 и 14 для всех экспериментов. Получено этическое разрешение Белостокского медицинского университета на использование линий клеток человека.
Синтез коллагена
Включение радиоактивного предшественника в белки измеряли после мечения конфлюэнтных фибробластов, культивируемых в питательной среде с различными концентрациями этанола и HA 500 мкг / мл в течение 24 часов в бессывороточной среде с 5 [ 3 H] пролин (5 мкКи / мл, 28 Ки / ммоль).Количество включенной метки в коллаген определяли путем переваривания белков очищенной коллагеназой Clostridium histolyticum по методу Петеркофски и Дигельмана.14
Определение активности пролидазы
Активность пролидазы измеряли с использованием метода, описанного Myara et al. Концентрацию белка измеряли методом Lowry et al.16. Клетки собирали перед центрифугированием при 200 × g в течение 15 минут. От супернатанта отказались.Затем осадок ресуспендировали в (4- (2-гидроксиэтил) -1-пиперазинэтансульфоновой кислоте (HEPES) (50 мМ, pH 7,8) и разрушали ультразвуком (3 × 10 секунд при температуре 0 ° C). После этого следовало центрифугирование при 12000 × г в течение 30 минут при 4 ° C, и белок был определен в супернатанте, и была проанализирована активность пролидазы. Затем 100 мкл пробы супернатанта клеточного экстракта были смешаны с HEPES (100 мкл, 50 мМ, pH 7,8. ), который содержал MnCl 2 (для достижения конечной концентрации 1 мМ MnCl 2 ).Образцы инкубировали при 37 ° C в течение 24 часов перед тем, как инициировать введение 100 мкл 94 мМ глицилпролина (Gly-Pro) для достижения 47 мМ конечной концентрации Gly-Pro. Затем образцы инкубировали при 7 ° C в течение 60 минут и реакцию останавливали добавлением 0,45 М трихлоруксусной кислоты (TCA) (порция 1 мл). TCA добавляли в параллельные неиспользованные пробирки в «нулевой момент». Затем следовало центрифугирование образцов в течение 15 минут при 10,000 × g . Определение пролина происходило путем добавления TCA / супернатанта (0.5 мл) к смеси (1: 1) ледяной уксусной кислоты / реактива Чинарда. Затем все инкубировали при 90 ° C в течение 10 минут. Колориметрию (поглощение при 515 нм) использовали для определения пролина по отношению к стандартам пролина. Результаты выражали в наномолях пролина, высвобождаемого в минуту на миллиграмм белка.
Биосинтез ДНК
Изучено влияние исследуемых веществ на включение фибробластов [ 3 H] -тимидина. В 24-луночные чашки для культур ткани клетки высевали из расчета 1 × 10 5 клеток / лунку, используя 1 мл ростовой среды в каждой лунке.Через 48 часов (1,6 ± 0,1 × 10 5 клеток / лунку) в лунки для культивирования добавляли различные концентрации этанола с 500 мкг / мл гиалуронана или без него на 24 часа при 37 ° C. После этого в лунки добавляли 0,5 мкКи [ 3 H] -тимидина (6,7 Ки / ммоль) и культуры инкубировали при 37 ° C в течение 4 часов. Затем клетки промывали трижды 1 мл 0,05 М трис-HCl и дважды 5% ТХК. После этого проводили лизис клеток в 1 мл 0,1 М NaOH, содержащем 1% додецилсульфат натрия (SDS).Затем добавляли 4 мл сцинтилляционной жидкости и измеряли радиоактивность на сцинтилляционном счетчике.
Анализ цитотоксичности
Жизнеспособность клеток оценивали с помощью анализа метилтиазолилтетразолия (МТТ), который основан на превращении желтого тетразолийбромида МТТ в пурпурное производное формазана митохондриальным ферментом сукцинатдегидрогеназой в жизнеспособных клетках. В конце инкубационного периода среду переносили в 96-луночные планшеты для определения цитокинов.Клетки промывали 0,2 мл фосфатно-солевого буфера и анализировали на цитотоксичность в том же лотке. Для обработанных клеток токсичность выражали в процентах.
SDS-PAGE
Метод Лэммли использовали для проведения электрофореза в пластинчатом 10% -ном додецилсульфат-полиакриламидном геле (SDS-PAGE). Анализировали образцы клеточных супернатантов (20 мкг белка). В качестве стандартов использовали: миозин (200 кДа), галактозидазу (116,2 кДа), фосфорилазу b (97,4 кДа), бычий сывороточный альбумин (66.2 кДа) и овальбумин (45 кДа) (Bio-Rad, Беркли, Калифорния, США).
Вестерн-блот-анализ
Метод Лэммли использовали для проведения электрофореза в пластинчатом SDS-PAGE. Анализировали равные порции клеточных супернатантов (20 мкг белка). Мы конденсировали десятикратную культуральную среду с использованием центриконов (отсечка 3 кДа), смешанных с буфером для образцов Лэммли (содержащим 2,5% SDS, без восстановителя). Электрофорез проводили с равными порциями (100 мкг) белка. После электрофореза клетки уравновешивали в 25 мМ Трис с 0.2 М глицин в 20% метаноле (об. / Об.) В течение 5 минут. Образцы переносили в поры нитроцеллюлозы размером 0,2 мкм при 100 мА в течение 1 часа. Для этой процедуры использовалась система электрофореза LKB 2117 Multiphor II Multiphor (GE Healthcare Bio-Sciences AB, Упсала, Швеция). Мы инкубировали нитроцеллюлозу в течение 1 часа с моноклональными антителами против коллагена I (концентрация 1: 1000), моноклональными антителами против фосфо-Akt (концентрация 1: 1000), поликлональными антителами против NF-κB (концентрация 1: 1000), моноклональное антитело против фосфо-MAPK (ERK 1/2 ) (концентрация 1: 1000), моноклональное антитело против каспазы 9 (концентрация 1: 1000).Антитела растворяли в растворе, содержащем 5% сухого молока, в трис-буферном физиологическом растворе с Tween 20 (TBS-T) (20 ммоль / л буфера Tris – HCl, pH 7,4, содержащего 150 ммоль / л NaCl и 0,05% Tween 20). . Для анализа фосфо-MAPK (ERK 1 / ERK / 2 ) и фосфо-AKT добавляли конъюгат щелочной фосфатазы против мышиного IgG (цельная молекула) в концентрации 1: 5000 в TBS-T. Для анализа NF-κB и каспазы-9, конъюгированного вторым антителом к щелочной фосфатазе, добавляли антикроличий IgG (целая молекула) в концентрации 1: 5000 в TBS-T.Для анализа коллагена типа I и конъюгированного второго антитела β-актина и щелочной фосфатазы добавляли анти-козий IgG (целая молекула) в концентрации 1: 5000 в TBS-T. Всю смесь инкубировали 30 минут при медленном встряхивании. После этого нитроцеллюлозу промывали TBS-T (5 × 5 минут) и обрабатывали реагентом жидкого субстрата 5-бром-4-хлор-3-индолилфосфат / нитросиний тетразолий. Интенсивность полос определяли количественно с помощью денситометрического анализа.
Зимография
Желатинолитическую активность измеряли с использованием метода Unemori и Werb.18 Мы конденсировали десятикратную культуральную среду с использованием центриконов (отсечка 3 кДа), смешанных с буфером для образцов (содержащим 2,5% SDS, без восстановителя). Электрофорез проводили с равными количествами белка (20 мкг) на полиакриламидных гелях (10%) в невосстанавливающих условиях. Гели пропитывали желатином (1 мг / мл). Инкубацию геля после электрофореза для удаления SDS проводили в течение 30 минут в 2% Triton X-100. После этого следовала инкубация в буфере, содержащем 50 мМ Трис – HCl, pH 8 с CaCl 2 5 мМ (субстратный буфер) в течение 18–24 часов при 37 ° C.После этого для окрашивания использовали кумасси бриллиантовый синий R250 (Thermo Fisher Scientific, Уолтем, Массачусетс, США).
Статистические методы
Средние значения по крайней мере для трех анализов ± стандартное отклонение (± SD) были рассчитаны во всех соответствующих экспериментах. Статистический анализ проводился с применением двустороннего непарного критерия Стьюдента t и дисперсионного анализа. Использовалась программа IBM SPSS 22.0 Statstics Genericom (IBM Corporation, Армонк, Нью-Йорк, США). П <0.05 и P <0,01 признан статистически значимым.
Результаты
Чтобы оценить активность этанола в синтезе коллагена в фибробластах кожи человека, клетки инкубировали в течение 24 часов в 25, 50 и 100 мМ этанола, а также в этаноле с HA в концентрации 500 мкг. / мл. Было показано, что этанол вызывает снижение синтеза коллагена дозозависимым образом (и). Воздействие на фибробласты различных концентраций этанола способствует ингибированию биосинтеза коллагена на 58.08% (2,39% ± стандартное отклонение; n = 3), 76,23% (3,52% ± стандартное отклонение; n = 3), 83,15% (4,03% ± стандартное отклонение; n = 3) P <0,05, P <0,01, соответственно по сравнению с контрольным значением. Однако в присутствии HA в концентрации 500 мкг / мл эффективность этанола по ингибированию биосинтеза коллагена была намного ниже. ГК, добавленный только к клеткам, не оказывал значительного влияния на биосинтез коллагена в контрольных клетках. Представленные результаты свидетельствуют о том, что этанол оказывает ингибирующее действие на синтез коллагена в сливающихся фибробластах кожи человека, а ГК противодействует этому процессу (и).
Биосинтез коллагена, измеренный как включение 5 [ 3 H] -пролина в белки, чувствительные к действию бактериальной коллагеназы, в сливающихся фибробластах кожи человека, инкубированных в течение 24 часов с различными концентрациями этанола и HA.
Примечания: Тест ANOVA: ** P <0,01. Планки погрешностей представляют собой ± стандартное отклонение; п = 3.
Сокращения: ANOVA, дисперсионный анализ; HA, гиалуроновая кислота; ДМСО, диметилсульфоксид; dpm, распадов в минуту.
Вестерн-иммуноблот-анализ коллагена типа I в субконфлюэнтных фибробластах кожи человека (контроль), клетках, обработанных с или без HA в течение 24 часов. Интенсивность окрашивания полос определяли количественно с помощью денситометрического анализа. Тест Стьюдента t -тест, * P <0,05 и ** P <0,01.
Примечания: 1, контроль; 2, этанол 25 мМ; 3, этанол 50 мМ; 4, этанол 100 мМ; 5, НА; 6, этанол 25 мМ и НА; 7, этанол 50 мМ и НА; 8, этанол 100 мМ и НА.Образцы, используемые для электрофореза, состояли из 20 мкг белка объединенных экстрактов клеток.
Сокращения: AU, условные единицы; HA, гиалуроновая кислота.
Фермент, ответственный за рециклинг пролина для ресинтеза коллагена, — пролидаза и ММП. Добавление этанола в концентрациях 25, 50 и 100 мМ к культурам клеток способствовало снижению активности пролидазы на 29,05% (4,55% ± стандартное отклонение; n = 3), 56,15% (3,82% ± стандартное отклонение; n = 3), и 88,18% (1,16% ± стандартное отклонение; n = 3). Добавление НА оказало значительный защитный эффект на активность пролидазы в фибробластах, инкубированных с этанолом.ГК восстанавливала активность пролидазы в клетках, инкубированных с этанолом, до контрольного уровня ().
Активность пролидазы в конфлюэнтных фибробластах кожи человека, инкубированных в течение 24 часов с различными концентрациями этанола и НА.
Примечания: Тест ANOVA: * P <0,05, ** P <0,01. Планки погрешностей представляют собой ± стандартное отклонение; п = 3.
Сокращения: ANOVA, дисперсионный анализ; HA, гиалуроновая кислота.
Проведенные исследования доказывают, что этанол нарушает метаболизм коллагена в фибробластах кожи человека, что приводит к значительному снижению синтеза ДНК.Распад за минуту [ 3 H] тимидина, включенного в ДНК этих клеток, был принят за 100%. Это было эталонное значение. Мы оценили эффект этанола в присутствии или в отсутствие ГК (500 мг / мл). Воздействие на фибробласты этанола различных концентраций способствовало ингибированию синтеза ДНК на 21,06% (7,08% ± стандартное отклонение; n = 3), 44,15% (5,06% ± стандартное отклонение; n = 3), 56,27% (4,26% ± стандартное отклонение; n = 3), 50,16% (4,56% ± стандартное отклонение; n = 3) P <0,05, P <0,01, соответственно, по сравнению с контрольным значением.ГК оказывает защитное влияние на процессы, вызванные этанолом ().
Биосинтез ДНК, измеренный по включению [ 3 H] -тимидина в ДНК в фибробластах кожи человека (контроль), инкубированных в течение 24 часов с различными концентрациями этанола и НА.
Примечания: Тест ANOVA: * P <0,05, ** P <0,01. Планки погрешностей представляют собой ± стандартное отклонение; п = 3.
Сокращения: ANOVA, дисперсионный анализ; HA, гиалуроновая кислота.
Эффективность HA в снижении цитотоксичности 25, 50 и 100 мМ этанола показана на рисунке. Было показано, что этанол вызывает цитотоксичность дозозависимым образом. Наличие этанола ингибирования выживаемости клеток 20,16% (4,05% ± стандартное отклонение; n = 3), 35,18% (3,63% ± стандартное отклонение; n = 3), 56,03% (2,53% ± стандартное отклонение; n = 3) P < 0,01 соответственно по сравнению с контрольным значением. Рецептор интегрина β 1 играет ключевую роль в контроле биосинтеза коллагена и активности пролидазы. В этом исследовании мы обнаружили, что этанол снижает экспрессию рецептора интегрина β 1 дозозависимым образом.В культивируемых клетках, инкубированных с HA и этанолом, этот эффект исчез. Было обнаружено, что экспрессия рецептора интегрина в клетках, обработанных различными концентрациями этанола и HA, была такой же, как и в контрольных клетках ().
Цитотоксичность фибробластов кожи человека (контроль), инкубированных в течение 24 часов с различными концентрациями этанола и НА.
Примечания: Тест ANOVA: * P <0,05, ** P <0,01. Планки погрешностей представляют собой ± стандартное отклонение; п = 3.
Сокращения: ANOVA, дисперсионный анализ; HA, гиалуроновая кислота.
Вестерн-иммуноблот-анализ для β 1 интегрина ( A ), рецептора инсулиноподобного фактора роста I ( B ), ERK 1/2 ( C ), киназы Akt ( D ), каспаза 9 ( E ) и β-актин ( F ) в субконфлюэнтных фибробластах кожи человека (контроль), клетках, обработанных с или без HA в течение 24 часов. Интенсивность окрашивания полос определяли количественно с помощью денситометрического анализа.
Примечания: Студенческий тест t -тест: * P <0,05, ** P <0,01. 1, контроль; 2, этанол 25 мМ; 3, этанол 50 мМ; 4, этанол 100 мМ; 5, НА; 6, этанол 25 мМ и НА; 7, этанол 50 мМ и НА; 8, этанол 100 мМ и НА. Образцы, используемые для электрофореза, состояли из 20 мкг белка объединенных экстрактов клеток.
Сокращения: AU, условные единицы; ERK, киназа, регулируемая внеклеточными сигналами; HA, гиалуроновая кислота.
Известно, что перекрестное взаимодействие между рецептором интегрина β 1 и рецептором IGF-IR играет ключевую роль в активации экспрессии гена коллагена и активности пролидазы.Этанол, как и в случае рецептора интегрина, вызывал снижение экспрессии IGF-IR (дозозависимым образом). ГК также оказывает защитное действие на уровень экспрессии этого рецептора (). В этом случае экспрессия рецептора IGF-IR в клетках, инкубированных с этанолом и HA, была близка к контролю.
Сигнал, передаваемый стимулированным IGF-IR и β 1 рецептором интегрина, приводит к активации MAPK (ERK 1/2 ) и Akt.14,15. Как видно на фибробластах, обработанных этанолом, экспрессия MAPK (фосфо-ERK 1/2 ) снижалось дозозависимым образом.Добавление HA к клеткам, обработанным этанолом, оказало защитное действие на зависимое от этанола снижение экспрессии фосфо-ERK 1/2 . Этанол и этанол с HA, добавленные к культивированным фибробластам, не влияли на экспрессию фосфо-AKT киназ (). Различные концентрации этанола оказывают цитотоксическое действие на фибробласты кожи человека, что приводит к индукции апоптоза, что приводит к наблюдаемому увеличению экспрессии каспазы 9 (). Более того, применение ГК оказывает защитное действие на нарушения пролиферации клеток, вызванные этанолом.Более того, экспрессия β-актина не изменялась в клетках при обработке этанолом в присутствии или в отсутствие НА ().
Некоторые данные свидетельствуют о том, что пролидаза-зависимая регуляция биосинтеза коллагена может иметь место на уровне транскрипции, в зависимости от экспрессии NF-κB. NF-κB — это фактор транскрипции, который действует как ингибитор экспрессии альфа 1 и альфа 2 субъединиц коллагена типа I. 19,20 Мы обнаружили повышенную экспрессию NF-κB в фибробластах, обработанных этанолом ().Добавление НА к клеткам, обработанным этанолом, способствовало снижению экспрессии этого транскрипционного фактора до контрольного уровня. Более того, экспрессия β-актина не изменялась в клетках при обработке этанолом в присутствии или в отсутствие НА (). Похоже, что регуляторный механизм индуцированной этанолом аберрации коллагена имеет место в точке биосинтеза коллагена, поскольку не было обнаружено влияния этанола и ГК на процесс деградации коллагена ММП-2 и ММП-9 ().
Вестерн-иммуноблот-анализ белка p65 NF-κB ( A ) и β-актина ( B ) в субконфлюэнтных фибробластах кожи человека (контроль), клетках, обработанных с или без HA в течение 24 часов.Интенсивность окрашивания полос определяли количественно с помощью денситометрического анализа.
Примечания: Студенческий тест t -тест: ** P <0,01. 1, контроль; 2, этанол 25 мМ; 3, этанол 50 мМ; 4, этанол 100 мМ; 5, НА; 6, этанол 25 мМ и НА; 7, этанол 50 мМ и НА; 8, этанол 100 мМ и НА. Образцы, используемые для электрофореза, состояли из 20 мкг белка объединенных экстрактов клеток.
Сокращения: AU, условные единицы; HA, гиалуроновая кислота.
Зимография для MMP-9 (92 кДа) и MMP-2 (72 кДа) в субконфлюэнтных фибробластах кожи человека (контроль), клетках, обработанных с или без HA в течение 24 часов.
Примечания: Интенсивность окрашивания полос количественно определяли с помощью денситометрического анализа. 1, контроль; 2, этанол 25 мМ; 3, этанол 50 мМ; 4, этанол 100 мМ; 5, НА; 6, этанол 25 мМ и НА; 7, этанол 50 мМ и НА; 8, этанол 100 мМ и НА. Образцы, используемые для электрофореза, состояли из 20 мкг белка объединенных экстрактов клеток.
Сокращения: AU, условные единицы; HA, гиалуроновая кислота; ММП, матричная металлопротеиназа.
Обсуждение
Хотя цитотоксичность этанола хорошо известна, механизм ее воздействия на метаболизм коллагена в тканях до конца не изучен.Похоже, что аномалии метаболизма коллагена, вызванные этанолом, тканеспецифичны. В печени он может способствовать стимуляции биосинтеза коллагена с последствием фиброза тканей, в то время как в коже может происходить противоположный процесс с последствием заживления ран.
В этом исследовании мы предоставили доказательства того, что этанол подавляет метаболизм коллагена в фибробластах кожи посредством нескольких уровней регуляции этого белка. Сначала это влияет на активность пролидазы, фермента, который играет важную роль в биосинтезе коллагена.Фермент отвечает за рециркуляцию пролина для ресинтеза коллагена, тем самым определяя выработку коллагена. Пептидные связи между пролином и другими аминокислотами могут быть расщеплены также другой пептидазой, пролиназой, которой необходим пролин в N-концевом положении.21 Пролидаза — вторая иминопептидаза, которая расщепляет дипептиды С-концевым пролином для сбора свободного пролина. Фермент переваривает как эндогенные, так и диетические дипептиды Xaa-Pro.21
Другой уровень регуляции метаболизма коллагена в обработанных этанолом фибробластах был обнаружен при β 1 интегрина и IGF-IR.Ранее мы обнаружили, что перекрестные помехи между рецепторами способствуют усилению биосинтеза коллагена. 22 В настоящем исследовании мы обнаружили, что этанол способствует подавлению экспрессии обоих рецепторов. Одновременно мы обнаружили повышение транскрипционной активности NF-κB, известного ингибитора коллагена типа I, который субъединиц экспрессии гена.20 В результате проведенных исследований был сделан вывод, что этанол приводит к нарушению биосинтеза коллагена в фибробластах. культур за счет снижения активности пролидазы и экспрессии интегрина β 1 и IGF-IR.Это сопровождалось пониженной экспрессией белков сигнального пути, индуцированной интегрином β 1 и IGF-IR, то есть киназами MAPK (ERK 1/2 ). Пониженное количество синтезированного коллагена и нарушение активности пролидазы также может быть связано с активацией фактора транскрипции NF-κB, который подавляет экспрессию гена коллагена. Применение ГК в концентрации 500 мкг / мл оказывает защитное действие на нарушения, вызванные исследуемыми веществами. Совокупность процессов, на которые влияет этанол, объясняет механизм индуцированного этанолом подавления биосинтеза коллагена.Основываясь на наших предыдущих исследованиях, мы рассматривали ГК как средство, противодействующее вызванной этанолом дерегуляции метаболизма коллагена в фибробластах.11 Фактически, мы обнаружили, что ГК устраняет все изученные дефекты метаболизма коллагена, вызванные этанолом. В нашей предыдущей статье мы не наблюдали отменяющего эффекта ГК, когда кофеин подавлял синтез коллагена.23 Различные концентрации этанола оказывают цитотоксическое действие на фибробласты кожи человека, что приводит к снижению выживаемости, ингибированию биосинтеза ДНК и индукции апоптоза, что приводит к в наблюдаемом повышении экспрессии каспазы 9.Более того, применение ГК оказывает защитное действие на дефект пролиферации клеток, вызванный этанолом.
HA играет важную роль в поддержании внеклеточного матрикса и вызывает защитное действие на структуру коллагена. 24,25 HA — это искусство гликозаминогликанов, где d-глюкуроновая кислота связана с частицей N -ацетилглюкозамина через гликозидные связи26. , 27 Клетка окружена слоем гиалуронана, который отвечает за форму, адгезию и миграцию клетки.24 Кожа содержит примерно 50% всей гиалуроновой кислоты в организме. ГК улучшает процессы заживления при некоторых патологических состояниях, таких как венозные язвы или повреждения мембран. Данные литературы показывают, что ГК играет полезную роль в регенеративных процессах, связанных с дисфункцией синтеза коллагена.28 Мы можем предположить, что ГК защищает от нарушений, вызванных этанолом. Этот защитный эффект можно контролировать посредством взаимодействия гиалуронана с его рецепторами CD44 и / или RHAMM.29 По крайней мере, в эндотелиальных клетках этот механизм способствует стимуляции выработки коллагена.30 Вопрос о том, играют ли рецепторы CD44 и RHAMM важную роль в механизме НА-зависимого противодействия токсичности этанола, требует дальнейшего изучения.
Данные, представленные в этой статье, могут иметь определенное социальное значение. Они предполагают, что фибробласты особенно чувствительны к этанолу и реагируют на это соединение путем ингибирования биосинтеза коллагена. Этот процесс способствует старению кожи, что представляет особый интерес для косметологии. Принимая во внимание приведенные выше данные и тот факт, что этанол обычно используется в косметологии, можно предположить, что этанол можно заменить в косметике другим растворителем или консервантами.Также можно рассматривать включение ГК в косметические препараты, содержащие этанол.
Выражение признательности
MD является научным сотрудником в области проектных исследований, исследований, коммерциализации: программа поддержки докторантов UMB, подмера 8.2.1 Операционная программа человеческого капитала, софинансируемая Европейским союзом в рамках Европейского социального фонда. Работа частично поддержана грантами Белостокского медицинского университета (143-14749F, 143-30730F, 144-30828F).
Сноски
Раскрытие информации
Авторы сообщают об отсутствии конфликта интересов в этой работе.
Ссылки
1. Сид Б., Верракс Дж., Кальдерон ПБ. Роль активации AMPK в окислительном повреждении клеток: последствия для алкогольной болезни печени. Biochem Pharmacol. 2013. 86 (2): 200–209. [PubMed] [Google Scholar] 2. Эль-Хадж Э.С., Эль-Хадж М.К., Волошенюк Т.Г. и др. Алкогольная модуляция металлопротеиназ сердечного матрикса (ММП) и тканевых ингибиторов ММП способствует накоплению коллагена. Alcohol Clin Exp Res. 2014. 38 (2): 448–456. [Бесплатная статья PMC] [PubMed] [Google Scholar] 3. Xu GF, Li PT, Wang XY и др.Динамические изменения экспрессии матриксных металлопротеиназ и их ингибиторов, TIMP, во время фиброза печени, вызванного алкоголем у крыс. Мир Дж. Гастроэнтерол. 2004. 10 (24): 3621–3627. [Бесплатная статья PMC] [PubMed] [Google Scholar] 4. Neuman MG, Nanau RM, Oruña L, Coto G. Противовоспалительные эффекты гиалуроновой кислоты in vitro при повреждении клеток кожи, вызванном этанолом. J. Pharm. Pharm. Sci. 2011. 14 (3): 425–437. [PubMed] [Google Scholar] 5. Пржилипиак А., Рабе Т., Хафнер Дж., Пржилипиак М., Руннебаум Б.Влияние этанола на рост in vitro клеточной линии карциномы молочной железы человека MCF-7. Arch Gynecol Obstet. 1996. 258 (3): 137–140. [PubMed] [Google Scholar] 6. Джонен Ч., Хартманн Б., Штеффен И. и др. Выделение и размножение клеток кожи для трансплантации клеток ограничено у пациентов, употребляющих табак, алкоголь или страдающих сахарным диабетом. Бернс. 2006. 32 (2): 194–200. [PubMed] [Google Scholar] 7. Ранзер MJ, Чен Л., ДиПьетро Л.А. При острой интоксикации этанолом нарушается функция фибробластов и прочность на разрыв раны.Alcohol Clin Exp Res. 2011; 35 (1): 83–90. [Бесплатная статья PMC] [PubMed] [Google Scholar] 8. Бойс Дж. М.. Обновите информацию о гигиене рук. Am J Infect Control. 2013. 41 (5): 94–96. [PubMed] [Google Scholar] 9. Ким И-Ч, Пак Джей-Х, Людовице П.Дж., Праусниц MR. Синергетическое усиление проницаемости кожи N-лауроилсаркозином и этанолом. Int J Pharmaceutics. 2008. 352 (1–2): 129–138. [PubMed] [Google Scholar] 10. Pendlington RU, Whittle E, Robinson JA, Howes D. Судьба этанола, наносимого на кожу местно. Food Chem Toxicol. 2001. 39 (2): 169–174.[PubMed] [Google Scholar] 11. Surazynski A, Miltyk W, Czarnomysy R, Grabowska J, Palka J. Гиалуроновая кислота отменяет зависимую от оксида азота стимуляцию деградации коллагена в культивируемых хондроцитах человека. Pharmacol Res. 2009. 60 (1): 46–49. [PubMed] [Google Scholar] 12. Гази К., Денг-Пичон У., Варнет Дж.М., Крыса П. Фрагменты гиалуроновой кислоты улучшают заживление ран на кожной модели in vitro за счет базовой активации пуринорецептора P2X7: роль молекулярной массы. PLoS One. 2012; 7 (11): e48351. [Бесплатная статья PMC] [PubMed] [Google Scholar] 13.Nawrat P, Surazynski A, Karna E, Pałka JA. Влияние гиалуроновой кислоты на индуцированное интерлейкином-1 нарушение регуляции метаболизма коллагена в культивируемых фибробластах кожи человека. Pharmacol Res. 2005. 51 (5): 473–477. [PubMed] [Google Scholar] 14. Петеркофский Б., Дигельманн Р. Использование смеси коллагеназ, свободных от протеиназ, для специфического анализа радиоактивного коллагена в присутствии других белков. Биохимия. 1971; 10 (6): 988–994. [PubMed] [Google Scholar] 15. Myara I, Charpentier C, Lemonnier A. Оптимальные условия для анализа пролидазы колориметрическим определением пролина: применение к иминодипептидурии.Clin Chim Acta. 1982; 125 (2): 193–205. [PubMed] [Google Scholar] 16. Лоури Н., Розенбро Н., Фарр Л., Рэндалл Р. Измерение белка с реагентом фолин-фенол. J Biol Chem. 1951; 193 (1): 265–275. [PubMed] [Google Scholar] 17. Laemmli UK. Расщепление структурных белков при сборке головки бактериофага Т4. Природа. 1970. 227 (5259): 680–685. [PubMed] [Google Scholar] 18. Unemori E, Werb Z. Реорганизация полимеризованного актина: возможный спусковой механизм для индукции проколлагеназы в фибробластах, культивируемых в коллагеновых гелях и на них.J Cell Biol. 1986. 103 (3): 1021–1031. [Бесплатная статья PMC] [PubMed] [Google Scholar] 19. Коуба Д., Чунг К.-Й, Нишияма Т. и др. Ядерный фактор-κB опосредует ингибирующее действие TNF-α на транскрипцию гена коллагена α2 (I) (COL1A2) в дермальных фибробластах человека. J Immunol. 1999. 162 (7): 4226–4234. [PubMed] [Google Scholar] 20. Miltyk W, Karna E, Palka J. Независимый от пролидазы механизм камптотецина-индуцированного ингибирования биосинтеза коллагена в культивируемых фибробластах кожи человека. J Biochem. 2007. 141 (2): 287–292.[PubMed] [Google Scholar] 21. Китченер Р.Л., Грюнден А.М. Функция пролидазы в метаболизме пролина и ее медицинские и биотехнологические применения. J Appl Microbiol. 2012. 113 (2): 233–247. [PubMed] [Google Scholar] 22. Surazynski A, Miltyk W, Prokop I, Palka J. Пролидазозависимая регуляция экспрессии рецепторов TGF и TGF β в фибробластах кожи человека. Eur J Pharmacol. 2010. 649 (1–3): 115–119. [PubMed] [Google Scholar] 23. Донейко М., Пржилипиак А., Рысяк Э., Глушук К., Суразинский А. Влияние кофеина и гиалуроновой кислоты на биосинтез коллагена в фибробластах кожи человека.Drug Des Devel Ther. 2014; 8: 1923–1928. [Бесплатная статья PMC] [PubMed] [Google Scholar] 25. Karna E, Miltyk W, Surazyński A, Pałka JA. Защитный эффект гиалуроновой кислоты на индуцированную интерлейкином-1 дерегуляцию передачи сигналов рецептора бета1-интегрина и инсулиноподобного фактора роста-I и биосинтез коллагена в культивируемых хондроцитах человека. Mol Cell Biochem. 2008. 308 (1–2): 57–64. [PubMed] [Google Scholar] 26. Гириш К.С., Кемпараджу К. Волшебный клей гиалуронан и его ластик гиалуронидаза: биологический обзор.Life Sci. 2007. 80 (21): 1921–1943. [PubMed] [Google Scholar] 27. Шефер Л, Шефер РМ. Протеогликаны: от структурных соединений до сигнальных молекул. Cell Tissue Res. 2010. 339 (1): 237–246. [PubMed] [Google Scholar] 28. Суразинский А., Милтык В., Палка Дж., Панг Дж. М.. Пролидазозависимая регуляция биосинтеза коллагена. Аминокислоты. 2008. 35 (4): 731–738. [PubMed] [Google Scholar] 29. Aruffo A, Stamenkovic I, Melnick M, Underhill CB, Seed B. CD44 является основным рецептором гиалуроната на клеточной поверхности. Клетка.1990. 61 (7): 1303–1313. [PubMed] [Google Scholar] 30. Руни П., Ван М., Кумар П., Кумар С. Ангиогенные олигосахариды гиалуронана увеличивают выработку коллагенов эндотелиальными клетками. J Cell Sci. 1993. 105 (1): 213–218. [PubMed] [Google Scholar]
Гиалуроновая кислота отменяет этанол-зависимое ингибирование биосинтеза коллагена в культивируемых фибробластах человека
Drug Des Devel Ther. 2015; 9: 6225–6233.
Магдалена Донейко
1 Кафедра эстетической медицины, Медицинский университет Белостока, Белосток, Польша
Анджей Пржилипяк
1 Кафедра эстетической медицины, Медицинский университет Белостока
, Белосток, Польша
2 Кафедра медицинской химии, Медицинский университет Белостока, Белосток, Польша
Войцех Милтык
3 Кафедра фармацевтического анализа, Фармацевтический факультет, Медицинский университет Белостока, Белосток, Белосток
Кафедра эстетической медицины, Медицинский университет Белостока, Белосток, Польша
Ежи Пжилипяк
4 Медицинский офис, Белосток, Польша
Илона Заремба
2 ł Кафедра медицинской химии Беловостокского медицинского университета Польша
Аркадиуш Суразиньс ki
2 Кафедра медицинской химии Белостокского медицинского университета, Белосток, Польша
1 Кафедра эстетической медицины Белостокского медицинского университета, Белосток, Польша
2 Кафедра медицинской химии медицинского университета Белосток, Белосток, Польша
3 Кафедра фармацевтического анализа, Фармацевтический факультет, Белостокский медицинский университет, Белосток, Польша
4 Медицинский офис, Белосток, Польша
Переписка: Магдалена, Медицинский факультет, Эстонский факультет of Pharmacy, Медицинский университет Белостока, улица Академицкая 3, 15-267 Белосток, Польша, Email moc.liamg @ okjenod Авторские права © 2015 Donejko et al. Эта работа опубликована Dove Medical Press Limited и находится под лицензией Creative Commons Attribution — Non Commercial (unported, v3.0) License. Полные условия лицензии доступны по адресу http://creativecommons.org/licenses/by-nc/3.0 /. Некоммерческое использование работы разрешено без какого-либо разрешения Dove Medical Press Limited при условии правильной ссылки на эту статью. Эта статья цитируется в других статьях PMC.
Abstract
Введение
Целью исследования было оценить влияние этанола на биосинтез коллагена в культивируемых фибробластах кожи человека и роль гиалуроновой кислоты (HA) в этом процессе.Что касается механизма действия этанола на фибробласты кожи человека, мы исследовали: экспрессию интегрина β 1 и рецептора инсулиноподобного фактора роста 1 (IGF-IR), экспрессию белков сигнального пути: митоген-активированные протеинкиназы (MAPK), протеинкиназы. B (Akt), ядерный фактор, каппа B (NF-κB), фактор транскрипции, анализ цитотоксичности и апоптоза, активность металлопротеиназы, а также влияние HA на эти процессы.
Материалы и методы
Биосинтез коллагена, активность пролидазы, биосинтез ДНК и цитотоксичность были измерены в конфлюэнтных культурах фибробластов кожи человека, обработанных 25, 50 и 100 мМ этанолом, этанолом и 500 мкг / мл HA.Вестерн-блот-анализ и зимография были выполнены для оценки экспрессии коллагена типа I, рецептора интегрина β 1 , IGF-IR, белка NF-κB, белка фосфо-Akt, киназы MAPK, активности каспазы 9 и матриксных металлопротеиназ (MMP-9). и ММП-2).
Результаты
Дозозависимый этанол приводит к нарушению биосинтеза коллагена в культурах фибробластов за счет снижения активности пролидазы и экспрессии интегрина β 1 и IGF-IR. Это сопровождалось повышенной цитотоксичностью, апоптозом и снижением экспрессии белков сигнального пути, индуцированных интегрином β 1 и IGF-IR, то есть киназами MAPK (ERK 1/2 ).Пониженное количество синтезированного коллагена и нарушение активности пролидазы также может быть связано с активацией фактора транскрипции NF-κB, который подавляет экспрессию гена коллагена. Это предполагает, что снижение продукции коллагена фибробластами может быть вызвано нарушением его биосинтеза, но не деградацией. Применение ГК оказывает защитное действие на нарушения, вызванные исследуемыми веществами. По-видимому, регуляторный механизм индуцированной этанолом аберрации коллагена имеет место на уровне биосинтеза коллагена, поскольку не было обнаружено влияния этанола и ГК на процесс деградации коллагена ММП-2 и ММП-9.
Заключение
Это исследование предоставляет доказательства того, что этанол нарушает метаболизм коллагена в фибробластах кожи человека, что приводит к значительному снижению количества продуцируемого белка. Этот механизм, вероятно, связан с подавлением активности пролидазы, экспрессии интегрина β 1 и рецепторов IGF-IR, а также белков сигнального пути, индуцированных этими рецепторами.
Ключевые слова: коллаген , этанол, гиалуроновая кислота, фибробласты
Введение
Воздействие этанола (этилового спирта) может вызывать множество местных и систематических нарушений.Органы, которые особенно страдают от интоксикации этанолом, — это легкие, почки и печень.1 Было показано, что интоксикация этанолом вызывает окислительный стресс, что приводит к модуляции экспрессии металлопротеиназ и тканевых ингибиторов матриксных металлопротеиназ (ММП) в клетках сердца и печени, способствующих развитию изменения клеточного фенотипа на фибробластоподобные с дальнейшими последствиями в накоплении тканевого коллагена и фиброзе.2,3 В нескольких исследованиях задокументировано этанол-зависимое окислительное повреждение в печени.Было обнаружено, что механизм этого процесса может включать функцию митохондрий и выживаемость клеток.1 Таким образом, цитотоксичность этанола может способствовать апоптозу клеток или может вызывать провоспалительные цитокины.4 Было обнаружено, что алкоголь ингибирует рост клеток карциномы молочной железы человека MCF-7 в vitro.5
Кажется, что этанол особенно влияет на биосинтез коллагена I типа. Этот процесс происходит в основном в клетках печени, но также наблюдается и в клетках кожи. Воздействие этанола на кожу привело к появлению многих дерматологических аномалий, таких как ладонная эритема, полнокровие, инфекции и приливы.6 Биопсии, полученные с кожи доноров, злоупотребляющих алкоголем, подтвердили аномалию структуры ткани, а изолированные фибробласты вызвали длительное время пролиферации.6 Некоторые данные предполагают, что этанол может влиять на заживление ран, вмешиваясь в биосинтез коллагена I и III.7 Этанол обычно используется в косметике, фармацевтика и дезинфицирующие средства.8,9 Большое количество спиртов используется в качестве разбавителей, консервантов, ингредиентов увлажняющих веществ или ароматизаторов в косметических средствах, наносимых на кожу.9,10 Концентрация этанола в продукте для типичного применения может варьироваться от менее чем От 1% до 96.9%.
Гиалуроновая кислота (ГК) оказалась полезным средством при заживлении ран и воспалительных процессах. Это подтверждено исследованиями in vivo и in vitro.11,12 Примерно половина продуцируемого гиалуронана синтезируется фибробластами и находится во внеклеточном матриксе кожи. Связывание HA с кластером дифференцировки 44 (CD44) и рецептором для подвижности, опосредованной гиалуроновой кислотой (RHAMM) на фибробластах, может влиять на передачу сигналов, тем самым регулируя рост, дифференцировку, адгезию и синтез коллагена клеток.13 Синтез коллагена в фибробластах может запускаться разными способами, одним из которых является пролидаза-зависимый механизм. 12
Механизм защитного действия ГК в отношении нарушений метаболизма коллагена при воздействии этанола неизвестен. Поэтому мы сосредоточились на механизме индуцированного этанолом подавления биосинтеза коллагена и роли ГК в этом процессе. Чтобы изучить и охарактеризовать потенциальные негативные последствия воздействия этанола на фибробласты кожи, мы исследовали его влияние на экспрессию коллагена I типа, интегрина β 1 и рецептора инсулиноподобного фактора роста 1 (IGF-IR), фосфорилированных митоген-активируемых. протеинкиназы (MAPKs: ERK 1 / ERK 2 ), протеинкиназа B (Akt), ядерный фактор, усиливающий легкую каппа-цепь активированных B-клеток (NF-κB), каспаза 9 и активность пролидазы в культивированные фибробласты кожи человека.
Материалы и методы
Культура клеток
Первичный дермальный фибробласт: нормальный, человек, взрослый ATCC ® PCS-201-012 ™ был приобретен в ATCC (Манассас, Вирджиния, США), а натриевая соль HA H5542 была приобретена у Sigma -Олдрич (Сент-Луис, Миссури, США). Клетки поддерживали в среде Игла, модифицированной Дульбекко, с добавлением 10% фетальной бычьей сыворотки (HyClone Laboratories, Логан, Юта, США), 2 мМ глутамина, 50 Ед / мл пенициллина и 50 мкг / мл стрептомицина при 37 ° C в 5 % CO 2 инкубатор.Клетки использовали между пассажами 10 и 14 для всех экспериментов. Получено этическое разрешение Белостокского медицинского университета на использование линий клеток человека.
Синтез коллагена
Включение радиоактивного предшественника в белки измеряли после мечения конфлюэнтных фибробластов, культивируемых в питательной среде с различными концентрациями этанола и HA 500 мкг / мл в течение 24 часов в бессывороточной среде с 5 [ 3 H] пролин (5 мкКи / мл, 28 Ки / ммоль).Количество включенной метки в коллаген определяли путем переваривания белков очищенной коллагеназой Clostridium histolyticum по методу Петеркофски и Дигельмана.14
Определение активности пролидазы
Активность пролидазы измеряли с использованием метода, описанного Myara et al. Концентрацию белка измеряли методом Lowry et al.16. Клетки собирали перед центрифугированием при 200 × g в течение 15 минут. От супернатанта отказались.Затем осадок ресуспендировали в (4- (2-гидроксиэтил) -1-пиперазинэтансульфоновой кислоте (HEPES) (50 мМ, pH 7,8) и разрушали ультразвуком (3 × 10 секунд при температуре 0 ° C). После этого следовало центрифугирование при 12000 × г в течение 30 минут при 4 ° C, и белок был определен в супернатанте, и была проанализирована активность пролидазы. Затем 100 мкл пробы супернатанта клеточного экстракта были смешаны с HEPES (100 мкл, 50 мМ, pH 7,8. ), который содержал MnCl 2 (для достижения конечной концентрации 1 мМ MnCl 2 ).Образцы инкубировали при 37 ° C в течение 24 часов перед тем, как инициировать введение 100 мкл 94 мМ глицилпролина (Gly-Pro) для достижения 47 мМ конечной концентрации Gly-Pro. Затем образцы инкубировали при 7 ° C в течение 60 минут и реакцию останавливали добавлением 0,45 М трихлоруксусной кислоты (TCA) (порция 1 мл). TCA добавляли в параллельные неиспользованные пробирки в «нулевой момент». Затем следовало центрифугирование образцов в течение 15 минут при 10,000 × g . Определение пролина происходило путем добавления TCA / супернатанта (0.5 мл) к смеси (1: 1) ледяной уксусной кислоты / реактива Чинарда. Затем все инкубировали при 90 ° C в течение 10 минут. Колориметрию (поглощение при 515 нм) использовали для определения пролина по отношению к стандартам пролина. Результаты выражали в наномолях пролина, высвобождаемого в минуту на миллиграмм белка.
Биосинтез ДНК
Изучено влияние исследуемых веществ на включение фибробластов [ 3 H] -тимидина. В 24-луночные чашки для культур ткани клетки высевали из расчета 1 × 10 5 клеток / лунку, используя 1 мл ростовой среды в каждой лунке.Через 48 часов (1,6 ± 0,1 × 10 5 клеток / лунку) в лунки для культивирования добавляли различные концентрации этанола с 500 мкг / мл гиалуронана или без него на 24 часа при 37 ° C. После этого в лунки добавляли 0,5 мкКи [ 3 H] -тимидина (6,7 Ки / ммоль) и культуры инкубировали при 37 ° C в течение 4 часов. Затем клетки промывали трижды 1 мл 0,05 М трис-HCl и дважды 5% ТХК. После этого проводили лизис клеток в 1 мл 0,1 М NaOH, содержащем 1% додецилсульфат натрия (SDS).Затем добавляли 4 мл сцинтилляционной жидкости и измеряли радиоактивность на сцинтилляционном счетчике.
Анализ цитотоксичности
Жизнеспособность клеток оценивали с помощью анализа метилтиазолилтетразолия (МТТ), который основан на превращении желтого тетразолийбромида МТТ в пурпурное производное формазана митохондриальным ферментом сукцинатдегидрогеназой в жизнеспособных клетках. В конце инкубационного периода среду переносили в 96-луночные планшеты для определения цитокинов.Клетки промывали 0,2 мл фосфатно-солевого буфера и анализировали на цитотоксичность в том же лотке. Для обработанных клеток токсичность выражали в процентах.
SDS-PAGE
Метод Лэммли использовали для проведения электрофореза в пластинчатом 10% -ном додецилсульфат-полиакриламидном геле (SDS-PAGE). Анализировали образцы клеточных супернатантов (20 мкг белка). В качестве стандартов использовали: миозин (200 кДа), галактозидазу (116,2 кДа), фосфорилазу b (97,4 кДа), бычий сывороточный альбумин (66.2 кДа) и овальбумин (45 кДа) (Bio-Rad, Беркли, Калифорния, США).
Вестерн-блот-анализ
Метод Лэммли использовали для проведения электрофореза в пластинчатом SDS-PAGE. Анализировали равные порции клеточных супернатантов (20 мкг белка). Мы конденсировали десятикратную культуральную среду с использованием центриконов (отсечка 3 кДа), смешанных с буфером для образцов Лэммли (содержащим 2,5% SDS, без восстановителя). Электрофорез проводили с равными порциями (100 мкг) белка. После электрофореза клетки уравновешивали в 25 мМ Трис с 0.2 М глицин в 20% метаноле (об. / Об.) В течение 5 минут. Образцы переносили в поры нитроцеллюлозы размером 0,2 мкм при 100 мА в течение 1 часа. Для этой процедуры использовалась система электрофореза LKB 2117 Multiphor II Multiphor (GE Healthcare Bio-Sciences AB, Упсала, Швеция). Мы инкубировали нитроцеллюлозу в течение 1 часа с моноклональными антителами против коллагена I (концентрация 1: 1000), моноклональными антителами против фосфо-Akt (концентрация 1: 1000), поликлональными антителами против NF-κB (концентрация 1: 1000), моноклональное антитело против фосфо-MAPK (ERK 1/2 ) (концентрация 1: 1000), моноклональное антитело против каспазы 9 (концентрация 1: 1000).Антитела растворяли в растворе, содержащем 5% сухого молока, в трис-буферном физиологическом растворе с Tween 20 (TBS-T) (20 ммоль / л буфера Tris – HCl, pH 7,4, содержащего 150 ммоль / л NaCl и 0,05% Tween 20). . Для анализа фосфо-MAPK (ERK 1 / ERK / 2 ) и фосфо-AKT добавляли конъюгат щелочной фосфатазы против мышиного IgG (цельная молекула) в концентрации 1: 5000 в TBS-T. Для анализа NF-κB и каспазы-9, конъюгированного вторым антителом к щелочной фосфатазе, добавляли антикроличий IgG (целая молекула) в концентрации 1: 5000 в TBS-T.Для анализа коллагена типа I и конъюгированного второго антитела β-актина и щелочной фосфатазы добавляли анти-козий IgG (целая молекула) в концентрации 1: 5000 в TBS-T. Всю смесь инкубировали 30 минут при медленном встряхивании. После этого нитроцеллюлозу промывали TBS-T (5 × 5 минут) и обрабатывали реагентом жидкого субстрата 5-бром-4-хлор-3-индолилфосфат / нитросиний тетразолий. Интенсивность полос определяли количественно с помощью денситометрического анализа.
Зимография
Желатинолитическую активность измеряли с использованием метода Unemori и Werb.18 Мы конденсировали десятикратную культуральную среду с использованием центриконов (отсечка 3 кДа), смешанных с буфером для образцов (содержащим 2,5% SDS, без восстановителя). Электрофорез проводили с равными количествами белка (20 мкг) на полиакриламидных гелях (10%) в невосстанавливающих условиях. Гели пропитывали желатином (1 мг / мл). Инкубацию геля после электрофореза для удаления SDS проводили в течение 30 минут в 2% Triton X-100. После этого следовала инкубация в буфере, содержащем 50 мМ Трис – HCl, pH 8 с CaCl 2 5 мМ (субстратный буфер) в течение 18–24 часов при 37 ° C.После этого для окрашивания использовали кумасси бриллиантовый синий R250 (Thermo Fisher Scientific, Уолтем, Массачусетс, США).
Статистические методы
Средние значения по крайней мере для трех анализов ± стандартное отклонение (± SD) были рассчитаны во всех соответствующих экспериментах. Статистический анализ проводился с применением двустороннего непарного критерия Стьюдента t и дисперсионного анализа. Использовалась программа IBM SPSS 22.0 Statstics Genericom (IBM Corporation, Армонк, Нью-Йорк, США). П <0.05 и P <0,01 признан статистически значимым.
Результаты
Чтобы оценить активность этанола в синтезе коллагена в фибробластах кожи человека, клетки инкубировали в течение 24 часов в 25, 50 и 100 мМ этанола, а также в этаноле с HA в концентрации 500 мкг. / мл. Было показано, что этанол вызывает снижение синтеза коллагена дозозависимым образом (и). Воздействие на фибробласты различных концентраций этанола способствует ингибированию биосинтеза коллагена на 58.08% (2,39% ± стандартное отклонение; n = 3), 76,23% (3,52% ± стандартное отклонение; n = 3), 83,15% (4,03% ± стандартное отклонение; n = 3) P <0,05, P <0,01, соответственно по сравнению с контрольным значением. Однако в присутствии HA в концентрации 500 мкг / мл эффективность этанола по ингибированию биосинтеза коллагена была намного ниже. ГК, добавленный только к клеткам, не оказывал значительного влияния на биосинтез коллагена в контрольных клетках. Представленные результаты свидетельствуют о том, что этанол оказывает ингибирующее действие на синтез коллагена в сливающихся фибробластах кожи человека, а ГК противодействует этому процессу (и).
Биосинтез коллагена, измеренный как включение 5 [ 3 H] -пролина в белки, чувствительные к действию бактериальной коллагеназы, в сливающихся фибробластах кожи человека, инкубированных в течение 24 часов с различными концентрациями этанола и HA.
Примечания: Тест ANOVA: ** P <0,01. Планки погрешностей представляют собой ± стандартное отклонение; п = 3.
Сокращения: ANOVA, дисперсионный анализ; HA, гиалуроновая кислота; ДМСО, диметилсульфоксид; dpm, распадов в минуту.
Вестерн-иммуноблот-анализ коллагена типа I в субконфлюэнтных фибробластах кожи человека (контроль), клетках, обработанных с или без HA в течение 24 часов. Интенсивность окрашивания полос определяли количественно с помощью денситометрического анализа. Тест Стьюдента t -тест, * P <0,05 и ** P <0,01.
Примечания: 1, контроль; 2, этанол 25 мМ; 3, этанол 50 мМ; 4, этанол 100 мМ; 5, НА; 6, этанол 25 мМ и НА; 7, этанол 50 мМ и НА; 8, этанол 100 мМ и НА.Образцы, используемые для электрофореза, состояли из 20 мкг белка объединенных экстрактов клеток.
Сокращения: AU, условные единицы; HA, гиалуроновая кислота.
Фермент, ответственный за рециклинг пролина для ресинтеза коллагена, — пролидаза и ММП. Добавление этанола в концентрациях 25, 50 и 100 мМ к культурам клеток способствовало снижению активности пролидазы на 29,05% (4,55% ± стандартное отклонение; n = 3), 56,15% (3,82% ± стандартное отклонение; n = 3), и 88,18% (1,16% ± стандартное отклонение; n = 3). Добавление НА оказало значительный защитный эффект на активность пролидазы в фибробластах, инкубированных с этанолом.ГК восстанавливала активность пролидазы в клетках, инкубированных с этанолом, до контрольного уровня ().
Активность пролидазы в конфлюэнтных фибробластах кожи человека, инкубированных в течение 24 часов с различными концентрациями этанола и НА.
Примечания: Тест ANOVA: * P <0,05, ** P <0,01. Планки погрешностей представляют собой ± стандартное отклонение; п = 3.
Сокращения: ANOVA, дисперсионный анализ; HA, гиалуроновая кислота.
Проведенные исследования доказывают, что этанол нарушает метаболизм коллагена в фибробластах кожи человека, что приводит к значительному снижению синтеза ДНК.Распад за минуту [ 3 H] тимидина, включенного в ДНК этих клеток, был принят за 100%. Это было эталонное значение. Мы оценили эффект этанола в присутствии или в отсутствие ГК (500 мг / мл). Воздействие на фибробласты этанола различных концентраций способствовало ингибированию синтеза ДНК на 21,06% (7,08% ± стандартное отклонение; n = 3), 44,15% (5,06% ± стандартное отклонение; n = 3), 56,27% (4,26% ± стандартное отклонение; n = 3), 50,16% (4,56% ± стандартное отклонение; n = 3) P <0,05, P <0,01, соответственно, по сравнению с контрольным значением.ГК оказывает защитное влияние на процессы, вызванные этанолом ().
Биосинтез ДНК, измеренный по включению [ 3 H] -тимидина в ДНК в фибробластах кожи человека (контроль), инкубированных в течение 24 часов с различными концентрациями этанола и НА.
Примечания: Тест ANOVA: * P <0,05, ** P <0,01. Планки погрешностей представляют собой ± стандартное отклонение; п = 3.
Сокращения: ANOVA, дисперсионный анализ; HA, гиалуроновая кислота.
Эффективность HA в снижении цитотоксичности 25, 50 и 100 мМ этанола показана на рисунке. Было показано, что этанол вызывает цитотоксичность дозозависимым образом. Наличие этанола ингибирования выживаемости клеток 20,16% (4,05% ± стандартное отклонение; n = 3), 35,18% (3,63% ± стандартное отклонение; n = 3), 56,03% (2,53% ± стандартное отклонение; n = 3) P < 0,01 соответственно по сравнению с контрольным значением. Рецептор интегрина β 1 играет ключевую роль в контроле биосинтеза коллагена и активности пролидазы. В этом исследовании мы обнаружили, что этанол снижает экспрессию рецептора интегрина β 1 дозозависимым образом.В культивируемых клетках, инкубированных с HA и этанолом, этот эффект исчез. Было обнаружено, что экспрессия рецептора интегрина в клетках, обработанных различными концентрациями этанола и HA, была такой же, как и в контрольных клетках ().
Цитотоксичность фибробластов кожи человека (контроль), инкубированных в течение 24 часов с различными концентрациями этанола и НА.
Примечания: Тест ANOVA: * P <0,05, ** P <0,01. Планки погрешностей представляют собой ± стандартное отклонение; п = 3.
Сокращения: ANOVA, дисперсионный анализ; HA, гиалуроновая кислота.
Вестерн-иммуноблот-анализ для β 1 интегрина ( A ), рецептора инсулиноподобного фактора роста I ( B ), ERK 1/2 ( C ), киназы Akt ( D ), каспаза 9 ( E ) и β-актин ( F ) в субконфлюэнтных фибробластах кожи человека (контроль), клетках, обработанных с или без HA в течение 24 часов. Интенсивность окрашивания полос определяли количественно с помощью денситометрического анализа.
Примечания: Студенческий тест t -тест: * P <0,05, ** P <0,01. 1, контроль; 2, этанол 25 мМ; 3, этанол 50 мМ; 4, этанол 100 мМ; 5, НА; 6, этанол 25 мМ и НА; 7, этанол 50 мМ и НА; 8, этанол 100 мМ и НА. Образцы, используемые для электрофореза, состояли из 20 мкг белка объединенных экстрактов клеток.
Сокращения: AU, условные единицы; ERK, киназа, регулируемая внеклеточными сигналами; HA, гиалуроновая кислота.
Известно, что перекрестное взаимодействие между рецептором интегрина β 1 и рецептором IGF-IR играет ключевую роль в активации экспрессии гена коллагена и активности пролидазы.Этанол, как и в случае рецептора интегрина, вызывал снижение экспрессии IGF-IR (дозозависимым образом). ГК также оказывает защитное действие на уровень экспрессии этого рецептора (). В этом случае экспрессия рецептора IGF-IR в клетках, инкубированных с этанолом и HA, была близка к контролю.
Сигнал, передаваемый стимулированным IGF-IR и β 1 рецептором интегрина, приводит к активации MAPK (ERK 1/2 ) и Akt.14,15. Как видно на фибробластах, обработанных этанолом, экспрессия MAPK (фосфо-ERK 1/2 ) снижалось дозозависимым образом.Добавление HA к клеткам, обработанным этанолом, оказало защитное действие на зависимое от этанола снижение экспрессии фосфо-ERK 1/2 . Этанол и этанол с HA, добавленные к культивированным фибробластам, не влияли на экспрессию фосфо-AKT киназ (). Различные концентрации этанола оказывают цитотоксическое действие на фибробласты кожи человека, что приводит к индукции апоптоза, что приводит к наблюдаемому увеличению экспрессии каспазы 9 (). Более того, применение ГК оказывает защитное действие на нарушения пролиферации клеток, вызванные этанолом.Более того, экспрессия β-актина не изменялась в клетках при обработке этанолом в присутствии или в отсутствие НА ().
Некоторые данные свидетельствуют о том, что пролидаза-зависимая регуляция биосинтеза коллагена может иметь место на уровне транскрипции, в зависимости от экспрессии NF-κB. NF-κB — это фактор транскрипции, который действует как ингибитор экспрессии альфа 1 и альфа 2 субъединиц коллагена типа I. 19,20 Мы обнаружили повышенную экспрессию NF-κB в фибробластах, обработанных этанолом ().Добавление НА к клеткам, обработанным этанолом, способствовало снижению экспрессии этого транскрипционного фактора до контрольного уровня. Более того, экспрессия β-актина не изменялась в клетках при обработке этанолом в присутствии или в отсутствие НА (). Похоже, что регуляторный механизм индуцированной этанолом аберрации коллагена имеет место в точке биосинтеза коллагена, поскольку не было обнаружено влияния этанола и ГК на процесс деградации коллагена ММП-2 и ММП-9 ().
Вестерн-иммуноблот-анализ белка p65 NF-κB ( A ) и β-актина ( B ) в субконфлюэнтных фибробластах кожи человека (контроль), клетках, обработанных с или без HA в течение 24 часов.Интенсивность окрашивания полос определяли количественно с помощью денситометрического анализа.
Примечания: Студенческий тест t -тест: ** P <0,01. 1, контроль; 2, этанол 25 мМ; 3, этанол 50 мМ; 4, этанол 100 мМ; 5, НА; 6, этанол 25 мМ и НА; 7, этанол 50 мМ и НА; 8, этанол 100 мМ и НА. Образцы, используемые для электрофореза, состояли из 20 мкг белка объединенных экстрактов клеток.
Сокращения: AU, условные единицы; HA, гиалуроновая кислота.
Зимография для MMP-9 (92 кДа) и MMP-2 (72 кДа) в субконфлюэнтных фибробластах кожи человека (контроль), клетках, обработанных с или без HA в течение 24 часов.
Примечания: Интенсивность окрашивания полос количественно определяли с помощью денситометрического анализа. 1, контроль; 2, этанол 25 мМ; 3, этанол 50 мМ; 4, этанол 100 мМ; 5, НА; 6, этанол 25 мМ и НА; 7, этанол 50 мМ и НА; 8, этанол 100 мМ и НА. Образцы, используемые для электрофореза, состояли из 20 мкг белка объединенных экстрактов клеток.
Сокращения: AU, условные единицы; HA, гиалуроновая кислота; ММП, матричная металлопротеиназа.
Обсуждение
Хотя цитотоксичность этанола хорошо известна, механизм ее воздействия на метаболизм коллагена в тканях до конца не изучен.Похоже, что аномалии метаболизма коллагена, вызванные этанолом, тканеспецифичны. В печени он может способствовать стимуляции биосинтеза коллагена с последствием фиброза тканей, в то время как в коже может происходить противоположный процесс с последствием заживления ран.
В этом исследовании мы предоставили доказательства того, что этанол подавляет метаболизм коллагена в фибробластах кожи посредством нескольких уровней регуляции этого белка. Сначала это влияет на активность пролидазы, фермента, который играет важную роль в биосинтезе коллагена.Фермент отвечает за рециркуляцию пролина для ресинтеза коллагена, тем самым определяя выработку коллагена. Пептидные связи между пролином и другими аминокислотами могут быть расщеплены также другой пептидазой, пролиназой, которой необходим пролин в N-концевом положении.21 Пролидаза — вторая иминопептидаза, которая расщепляет дипептиды С-концевым пролином для сбора свободного пролина. Фермент переваривает как эндогенные, так и диетические дипептиды Xaa-Pro.21
Другой уровень регуляции метаболизма коллагена в обработанных этанолом фибробластах был обнаружен при β 1 интегрина и IGF-IR.Ранее мы обнаружили, что перекрестные помехи между рецепторами способствуют усилению биосинтеза коллагена. 22 В настоящем исследовании мы обнаружили, что этанол способствует подавлению экспрессии обоих рецепторов. Одновременно мы обнаружили повышение транскрипционной активности NF-κB, известного ингибитора коллагена типа I, который субъединиц экспрессии гена.20 В результате проведенных исследований был сделан вывод, что этанол приводит к нарушению биосинтеза коллагена в фибробластах. культур за счет снижения активности пролидазы и экспрессии интегрина β 1 и IGF-IR.Это сопровождалось пониженной экспрессией белков сигнального пути, индуцированной интегрином β 1 и IGF-IR, то есть киназами MAPK (ERK 1/2 ). Пониженное количество синтезированного коллагена и нарушение активности пролидазы также может быть связано с активацией фактора транскрипции NF-κB, который подавляет экспрессию гена коллагена. Применение ГК в концентрации 500 мкг / мл оказывает защитное действие на нарушения, вызванные исследуемыми веществами. Совокупность процессов, на которые влияет этанол, объясняет механизм индуцированного этанолом подавления биосинтеза коллагена.Основываясь на наших предыдущих исследованиях, мы рассматривали ГК как средство, противодействующее вызванной этанолом дерегуляции метаболизма коллагена в фибробластах.11 Фактически, мы обнаружили, что ГК устраняет все изученные дефекты метаболизма коллагена, вызванные этанолом. В нашей предыдущей статье мы не наблюдали отменяющего эффекта ГК, когда кофеин подавлял синтез коллагена.23 Различные концентрации этанола оказывают цитотоксическое действие на фибробласты кожи человека, что приводит к снижению выживаемости, ингибированию биосинтеза ДНК и индукции апоптоза, что приводит к в наблюдаемом повышении экспрессии каспазы 9.Более того, применение ГК оказывает защитное действие на дефект пролиферации клеток, вызванный этанолом.
HA играет важную роль в поддержании внеклеточного матрикса и вызывает защитное действие на структуру коллагена. 24,25 HA — это искусство гликозаминогликанов, где d-глюкуроновая кислота связана с частицей N -ацетилглюкозамина через гликозидные связи26. , 27 Клетка окружена слоем гиалуронана, который отвечает за форму, адгезию и миграцию клетки.24 Кожа содержит примерно 50% всей гиалуроновой кислоты в организме. ГК улучшает процессы заживления при некоторых патологических состояниях, таких как венозные язвы или повреждения мембран. Данные литературы показывают, что ГК играет полезную роль в регенеративных процессах, связанных с дисфункцией синтеза коллагена.28 Мы можем предположить, что ГК защищает от нарушений, вызванных этанолом. Этот защитный эффект можно контролировать посредством взаимодействия гиалуронана с его рецепторами CD44 и / или RHAMM.29 По крайней мере, в эндотелиальных клетках этот механизм способствует стимуляции выработки коллагена.30 Вопрос о том, играют ли рецепторы CD44 и RHAMM важную роль в механизме НА-зависимого противодействия токсичности этанола, требует дальнейшего изучения.
Данные, представленные в этой статье, могут иметь определенное социальное значение. Они предполагают, что фибробласты особенно чувствительны к этанолу и реагируют на это соединение путем ингибирования биосинтеза коллагена. Этот процесс способствует старению кожи, что представляет особый интерес для косметологии. Принимая во внимание приведенные выше данные и тот факт, что этанол обычно используется в косметологии, можно предположить, что этанол можно заменить в косметике другим растворителем или консервантами.Также можно рассматривать включение ГК в косметические препараты, содержащие этанол.
Выражение признательности
MD является научным сотрудником в области проектных исследований, исследований, коммерциализации: программа поддержки докторантов UMB, подмера 8.2.1 Операционная программа человеческого капитала, софинансируемая Европейским союзом в рамках Европейского социального фонда. Работа частично поддержана грантами Белостокского медицинского университета (143-14749F, 143-30730F, 144-30828F).
Сноски
Раскрытие информации
Авторы сообщают об отсутствии конфликта интересов в этой работе.
Ссылки
1. Сид Б., Верракс Дж., Кальдерон ПБ. Роль активации AMPK в окислительном повреждении клеток: последствия для алкогольной болезни печени. Biochem Pharmacol. 2013. 86 (2): 200–209. [PubMed] [Google Scholar] 2. Эль-Хадж Э.С., Эль-Хадж М.К., Волошенюк Т.Г. и др. Алкогольная модуляция металлопротеиназ сердечного матрикса (ММП) и тканевых ингибиторов ММП способствует накоплению коллагена. Alcohol Clin Exp Res. 2014. 38 (2): 448–456. [Бесплатная статья PMC] [PubMed] [Google Scholar] 3. Xu GF, Li PT, Wang XY и др.Динамические изменения экспрессии матриксных металлопротеиназ и их ингибиторов, TIMP, во время фиброза печени, вызванного алкоголем у крыс. Мир Дж. Гастроэнтерол. 2004. 10 (24): 3621–3627. [Бесплатная статья PMC] [PubMed] [Google Scholar] 4. Neuman MG, Nanau RM, Oruña L, Coto G. Противовоспалительные эффекты гиалуроновой кислоты in vitro при повреждении клеток кожи, вызванном этанолом. J. Pharm. Pharm. Sci. 2011. 14 (3): 425–437. [PubMed] [Google Scholar] 5. Пржилипиак А., Рабе Т., Хафнер Дж., Пржилипиак М., Руннебаум Б.Влияние этанола на рост in vitro клеточной линии карциномы молочной железы человека MCF-7. Arch Gynecol Obstet. 1996. 258 (3): 137–140. [PubMed] [Google Scholar] 6. Джонен Ч., Хартманн Б., Штеффен И. и др. Выделение и размножение клеток кожи для трансплантации клеток ограничено у пациентов, употребляющих табак, алкоголь или страдающих сахарным диабетом. Бернс. 2006. 32 (2): 194–200. [PubMed] [Google Scholar] 7. Ранзер MJ, Чен Л., ДиПьетро Л.А. При острой интоксикации этанолом нарушается функция фибробластов и прочность на разрыв раны.Alcohol Clin Exp Res. 2011; 35 (1): 83–90. [Бесплатная статья PMC] [PubMed] [Google Scholar] 8. Бойс Дж. М.. Обновите информацию о гигиене рук. Am J Infect Control. 2013. 41 (5): 94–96. [PubMed] [Google Scholar] 9. Ким И-Ч, Пак Джей-Х, Людовице П.Дж., Праусниц MR. Синергетическое усиление проницаемости кожи N-лауроилсаркозином и этанолом. Int J Pharmaceutics. 2008. 352 (1–2): 129–138. [PubMed] [Google Scholar] 10. Pendlington RU, Whittle E, Robinson JA, Howes D. Судьба этанола, наносимого на кожу местно. Food Chem Toxicol. 2001. 39 (2): 169–174.[PubMed] [Google Scholar] 11. Surazynski A, Miltyk W, Czarnomysy R, Grabowska J, Palka J. Гиалуроновая кислота отменяет зависимую от оксида азота стимуляцию деградации коллагена в культивируемых хондроцитах человека. Pharmacol Res. 2009. 60 (1): 46–49. [PubMed] [Google Scholar] 12. Гази К., Денг-Пичон У., Варнет Дж.М., Крыса П. Фрагменты гиалуроновой кислоты улучшают заживление ран на кожной модели in vitro за счет базовой активации пуринорецептора P2X7: роль молекулярной массы. PLoS One. 2012; 7 (11): e48351. [Бесплатная статья PMC] [PubMed] [Google Scholar] 13.Nawrat P, Surazynski A, Karna E, Pałka JA. Влияние гиалуроновой кислоты на индуцированное интерлейкином-1 нарушение регуляции метаболизма коллагена в культивируемых фибробластах кожи человека. Pharmacol Res. 2005. 51 (5): 473–477. [PubMed] [Google Scholar] 14. Петеркофский Б., Дигельманн Р. Использование смеси коллагеназ, свободных от протеиназ, для специфического анализа радиоактивного коллагена в присутствии других белков. Биохимия. 1971; 10 (6): 988–994. [PubMed] [Google Scholar] 15. Myara I, Charpentier C, Lemonnier A. Оптимальные условия для анализа пролидазы колориметрическим определением пролина: применение к иминодипептидурии.Clin Chim Acta. 1982; 125 (2): 193–205. [PubMed] [Google Scholar] 16. Лоури Н., Розенбро Н., Фарр Л., Рэндалл Р. Измерение белка с реагентом фолин-фенол. J Biol Chem. 1951; 193 (1): 265–275. [PubMed] [Google Scholar] 17. Laemmli UK. Расщепление структурных белков при сборке головки бактериофага Т4. Природа. 1970. 227 (5259): 680–685. [PubMed] [Google Scholar] 18. Unemori E, Werb Z. Реорганизация полимеризованного актина: возможный спусковой механизм для индукции проколлагеназы в фибробластах, культивируемых в коллагеновых гелях и на них.J Cell Biol. 1986. 103 (3): 1021–1031. [Бесплатная статья PMC] [PubMed] [Google Scholar] 19. Коуба Д., Чунг К.-Й, Нишияма Т. и др. Ядерный фактор-κB опосредует ингибирующее действие TNF-α на транскрипцию гена коллагена α2 (I) (COL1A2) в дермальных фибробластах человека. J Immunol. 1999. 162 (7): 4226–4234. [PubMed] [Google Scholar] 20. Miltyk W, Karna E, Palka J. Независимый от пролидазы механизм камптотецина-индуцированного ингибирования биосинтеза коллагена в культивируемых фибробластах кожи человека. J Biochem. 2007. 141 (2): 287–292.[PubMed] [Google Scholar] 21. Китченер Р.Л., Грюнден А.М. Функция пролидазы в метаболизме пролина и ее медицинские и биотехнологические применения. J Appl Microbiol. 2012. 113 (2): 233–247. [PubMed] [Google Scholar] 22. Surazynski A, Miltyk W, Prokop I, Palka J. Пролидазозависимая регуляция экспрессии рецепторов TGF и TGF β в фибробластах кожи человека. Eur J Pharmacol. 2010. 649 (1–3): 115–119. [PubMed] [Google Scholar] 23. Донейко М., Пржилипиак А., Рысяк Э., Глушук К., Суразинский А. Влияние кофеина и гиалуроновой кислоты на биосинтез коллагена в фибробластах кожи человека.Drug Des Devel Ther. 2014; 8: 1923–1928. [Бесплатная статья PMC] [PubMed] [Google Scholar] 25. Karna E, Miltyk W, Surazyński A, Pałka JA. Защитный эффект гиалуроновой кислоты на индуцированную интерлейкином-1 дерегуляцию передачи сигналов рецептора бета1-интегрина и инсулиноподобного фактора роста-I и биосинтез коллагена в культивируемых хондроцитах человека. Mol Cell Biochem. 2008. 308 (1–2): 57–64. [PubMed] [Google Scholar] 26. Гириш К.С., Кемпараджу К. Волшебный клей гиалуронан и его ластик гиалуронидаза: биологический обзор.Life Sci. 2007. 80 (21): 1921–1943. [PubMed] [Google Scholar] 27. Шефер Л, Шефер РМ. Протеогликаны: от структурных соединений до сигнальных молекул. Cell Tissue Res. 2010. 339 (1): 237–246. [PubMed] [Google Scholar] 28. Суразинский А., Милтык В., Палка Дж., Панг Дж. М.. Пролидазозависимая регуляция биосинтеза коллагена. Аминокислоты. 2008. 35 (4): 731–738. [PubMed] [Google Scholar] 29. Aruffo A, Stamenkovic I, Melnick M, Underhill CB, Seed B. CD44 является основным рецептором гиалуроната на клеточной поверхности. Клетка.1990. 61 (7): 1303–1313. [PubMed] [Google Scholar] 30. Руни П., Ван М., Кумар П., Кумар С. Ангиогенные олигосахариды гиалуронана увеличивают выработку коллагенов эндотелиальными клетками. J Cell Sci. 1993. 105 (1): 213–218. [PubMed] [Google Scholar]
Гиалуроновая кислота отменяет этанол-зависимое ингибирование биосинтеза коллагена в культивируемых фибробластах человека
Drug Des Devel Ther. 2015; 9: 6225–6233.
Магдалена Донейко
1 Кафедра эстетической медицины, Медицинский университет Белостока, Белосток, Польша
Анджей Пржилипяк
1 Кафедра эстетической медицины, Медицинский университет Белостока
, Белосток, Польша
2 Кафедра медицинской химии, Медицинский университет Белостока, Белосток, Польша
Войцех Милтык
3 Кафедра фармацевтического анализа, Фармацевтический факультет, Медицинский университет Белостока, Белосток, Белосток
Кафедра эстетической медицины, Медицинский университет Белостока, Белосток, Польша
Ежи Пжилипяк
4 Медицинский офис, Белосток, Польша
Илона Заремба
2 ł Кафедра медицинской химии Беловостокского медицинского университета Польша
Аркадиуш Суразиньс ki
2 Кафедра медицинской химии Белостокского медицинского университета, Белосток, Польша
1 Кафедра эстетической медицины Белостокского медицинского университета, Белосток, Польша
2 Кафедра медицинской химии медицинского университета Белосток, Белосток, Польша
3 Кафедра фармацевтического анализа, Фармацевтический факультет, Белостокский медицинский университет, Белосток, Польша
4 Медицинский офис, Белосток, Польша
Переписка: Магдалена, Медицинский факультет, Эстонский факультет of Pharmacy, Медицинский университет Белостока, улица Академицкая 3, 15-267 Белосток, Польша, Email moc.liamg @ okjenod Авторские права © 2015 Donejko et al. Эта работа опубликована Dove Medical Press Limited и находится под лицензией Creative Commons Attribution — Non Commercial (unported, v3.0) License. Полные условия лицензии доступны по адресу http://creativecommons.org/licenses/by-nc/3.0 /. Некоммерческое использование работы разрешено без какого-либо разрешения Dove Medical Press Limited при условии правильной ссылки на эту статью. Эта статья цитируется в других статьях PMC.
Abstract
Введение
Целью исследования было оценить влияние этанола на биосинтез коллагена в культивируемых фибробластах кожи человека и роль гиалуроновой кислоты (HA) в этом процессе.Что касается механизма действия этанола на фибробласты кожи человека, мы исследовали: экспрессию интегрина β 1 и рецептора инсулиноподобного фактора роста 1 (IGF-IR), экспрессию белков сигнального пути: митоген-активированные протеинкиназы (MAPK), протеинкиназы. B (Akt), ядерный фактор, каппа B (NF-κB), фактор транскрипции, анализ цитотоксичности и апоптоза, активность металлопротеиназы, а также влияние HA на эти процессы.
Материалы и методы
Биосинтез коллагена, активность пролидазы, биосинтез ДНК и цитотоксичность были измерены в конфлюэнтных культурах фибробластов кожи человека, обработанных 25, 50 и 100 мМ этанолом, этанолом и 500 мкг / мл HA.Вестерн-блот-анализ и зимография были выполнены для оценки экспрессии коллагена типа I, рецептора интегрина β 1 , IGF-IR, белка NF-κB, белка фосфо-Akt, киназы MAPK, активности каспазы 9 и матриксных металлопротеиназ (MMP-9). и ММП-2).
Результаты
Дозозависимый этанол приводит к нарушению биосинтеза коллагена в культурах фибробластов за счет снижения активности пролидазы и экспрессии интегрина β 1 и IGF-IR. Это сопровождалось повышенной цитотоксичностью, апоптозом и снижением экспрессии белков сигнального пути, индуцированных интегрином β 1 и IGF-IR, то есть киназами MAPK (ERK 1/2 ).Пониженное количество синтезированного коллагена и нарушение активности пролидазы также может быть связано с активацией фактора транскрипции NF-κB, который подавляет экспрессию гена коллагена. Это предполагает, что снижение продукции коллагена фибробластами может быть вызвано нарушением его биосинтеза, но не деградацией. Применение ГК оказывает защитное действие на нарушения, вызванные исследуемыми веществами. По-видимому, регуляторный механизм индуцированной этанолом аберрации коллагена имеет место на уровне биосинтеза коллагена, поскольку не было обнаружено влияния этанола и ГК на процесс деградации коллагена ММП-2 и ММП-9.
Заключение
Это исследование предоставляет доказательства того, что этанол нарушает метаболизм коллагена в фибробластах кожи человека, что приводит к значительному снижению количества продуцируемого белка. Этот механизм, вероятно, связан с подавлением активности пролидазы, экспрессии интегрина β 1 и рецепторов IGF-IR, а также белков сигнального пути, индуцированных этими рецепторами.
Ключевые слова: коллаген , этанол, гиалуроновая кислота, фибробласты
Введение
Воздействие этанола (этилового спирта) может вызывать множество местных и систематических нарушений.Органы, которые особенно страдают от интоксикации этанолом, — это легкие, почки и печень.1 Было показано, что интоксикация этанолом вызывает окислительный стресс, что приводит к модуляции экспрессии металлопротеиназ и тканевых ингибиторов матриксных металлопротеиназ (ММП) в клетках сердца и печени, способствующих развитию изменения клеточного фенотипа на фибробластоподобные с дальнейшими последствиями в накоплении тканевого коллагена и фиброзе.2,3 В нескольких исследованиях задокументировано этанол-зависимое окислительное повреждение в печени.Было обнаружено, что механизм этого процесса может включать функцию митохондрий и выживаемость клеток.1 Таким образом, цитотоксичность этанола может способствовать апоптозу клеток или может вызывать провоспалительные цитокины.4 Было обнаружено, что алкоголь ингибирует рост клеток карциномы молочной железы человека MCF-7 в vitro.5
Кажется, что этанол особенно влияет на биосинтез коллагена I типа. Этот процесс происходит в основном в клетках печени, но также наблюдается и в клетках кожи. Воздействие этанола на кожу привело к появлению многих дерматологических аномалий, таких как ладонная эритема, полнокровие, инфекции и приливы.6 Биопсии, полученные с кожи доноров, злоупотребляющих алкоголем, подтвердили аномалию структуры ткани, а изолированные фибробласты вызвали длительное время пролиферации.6 Некоторые данные предполагают, что этанол может влиять на заживление ран, вмешиваясь в биосинтез коллагена I и III.7 Этанол обычно используется в косметике, фармацевтика и дезинфицирующие средства.8,9 Большое количество спиртов используется в качестве разбавителей, консервантов, ингредиентов увлажняющих веществ или ароматизаторов в косметических средствах, наносимых на кожу.9,10 Концентрация этанола в продукте для типичного применения может варьироваться от менее чем От 1% до 96.9%.
Гиалуроновая кислота (ГК) оказалась полезным средством при заживлении ран и воспалительных процессах. Это подтверждено исследованиями in vivo и in vitro.11,12 Примерно половина продуцируемого гиалуронана синтезируется фибробластами и находится во внеклеточном матриксе кожи. Связывание HA с кластером дифференцировки 44 (CD44) и рецептором для подвижности, опосредованной гиалуроновой кислотой (RHAMM) на фибробластах, может влиять на передачу сигналов, тем самым регулируя рост, дифференцировку, адгезию и синтез коллагена клеток.13 Синтез коллагена в фибробластах может запускаться разными способами, одним из которых является пролидаза-зависимый механизм. 12
Механизм защитного действия ГК в отношении нарушений метаболизма коллагена при воздействии этанола неизвестен. Поэтому мы сосредоточились на механизме индуцированного этанолом подавления биосинтеза коллагена и роли ГК в этом процессе. Чтобы изучить и охарактеризовать потенциальные негативные последствия воздействия этанола на фибробласты кожи, мы исследовали его влияние на экспрессию коллагена I типа, интегрина β 1 и рецептора инсулиноподобного фактора роста 1 (IGF-IR), фосфорилированных митоген-активируемых. протеинкиназы (MAPKs: ERK 1 / ERK 2 ), протеинкиназа B (Akt), ядерный фактор, усиливающий легкую каппа-цепь активированных B-клеток (NF-κB), каспаза 9 и активность пролидазы в культивированные фибробласты кожи человека.
Материалы и методы
Культура клеток
Первичный дермальный фибробласт: нормальный, человек, взрослый ATCC ® PCS-201-012 ™ был приобретен в ATCC (Манассас, Вирджиния, США), а натриевая соль HA H5542 была приобретена у Sigma -Олдрич (Сент-Луис, Миссури, США). Клетки поддерживали в среде Игла, модифицированной Дульбекко, с добавлением 10% фетальной бычьей сыворотки (HyClone Laboratories, Логан, Юта, США), 2 мМ глутамина, 50 Ед / мл пенициллина и 50 мкг / мл стрептомицина при 37 ° C в 5 % CO 2 инкубатор.Клетки использовали между пассажами 10 и 14 для всех экспериментов. Получено этическое разрешение Белостокского медицинского университета на использование линий клеток человека.
Синтез коллагена
Включение радиоактивного предшественника в белки измеряли после мечения конфлюэнтных фибробластов, культивируемых в питательной среде с различными концентрациями этанола и HA 500 мкг / мл в течение 24 часов в бессывороточной среде с 5 [ 3 H] пролин (5 мкКи / мл, 28 Ки / ммоль).Количество включенной метки в коллаген определяли путем переваривания белков очищенной коллагеназой Clostridium histolyticum по методу Петеркофски и Дигельмана.14
Определение активности пролидазы
Активность пролидазы измеряли с использованием метода, описанного Myara et al. Концентрацию белка измеряли методом Lowry et al.16. Клетки собирали перед центрифугированием при 200 × g в течение 15 минут. От супернатанта отказались.Затем осадок ресуспендировали в (4- (2-гидроксиэтил) -1-пиперазинэтансульфоновой кислоте (HEPES) (50 мМ, pH 7,8) и разрушали ультразвуком (3 × 10 секунд при температуре 0 ° C). После этого следовало центрифугирование при 12000 × г в течение 30 минут при 4 ° C, и белок был определен в супернатанте, и была проанализирована активность пролидазы. Затем 100 мкл пробы супернатанта клеточного экстракта были смешаны с HEPES (100 мкл, 50 мМ, pH 7,8. ), который содержал MnCl 2 (для достижения конечной концентрации 1 мМ MnCl 2 ).Образцы инкубировали при 37 ° C в течение 24 часов перед тем, как инициировать введение 100 мкл 94 мМ глицилпролина (Gly-Pro) для достижения 47 мМ конечной концентрации Gly-Pro. Затем образцы инкубировали при 7 ° C в течение 60 минут и реакцию останавливали добавлением 0,45 М трихлоруксусной кислоты (TCA) (порция 1 мл). TCA добавляли в параллельные неиспользованные пробирки в «нулевой момент». Затем следовало центрифугирование образцов в течение 15 минут при 10,000 × g . Определение пролина происходило путем добавления TCA / супернатанта (0.5 мл) к смеси (1: 1) ледяной уксусной кислоты / реактива Чинарда. Затем все инкубировали при 90 ° C в течение 10 минут. Колориметрию (поглощение при 515 нм) использовали для определения пролина по отношению к стандартам пролина. Результаты выражали в наномолях пролина, высвобождаемого в минуту на миллиграмм белка.
Биосинтез ДНК
Изучено влияние исследуемых веществ на включение фибробластов [ 3 H] -тимидина. В 24-луночные чашки для культур ткани клетки высевали из расчета 1 × 10 5 клеток / лунку, используя 1 мл ростовой среды в каждой лунке.Через 48 часов (1,6 ± 0,1 × 10 5 клеток / лунку) в лунки для культивирования добавляли различные концентрации этанола с 500 мкг / мл гиалуронана или без него на 24 часа при 37 ° C. После этого в лунки добавляли 0,5 мкКи [ 3 H] -тимидина (6,7 Ки / ммоль) и культуры инкубировали при 37 ° C в течение 4 часов. Затем клетки промывали трижды 1 мл 0,05 М трис-HCl и дважды 5% ТХК. После этого проводили лизис клеток в 1 мл 0,1 М NaOH, содержащем 1% додецилсульфат натрия (SDS).Затем добавляли 4 мл сцинтилляционной жидкости и измеряли радиоактивность на сцинтилляционном счетчике.
Анализ цитотоксичности
Жизнеспособность клеток оценивали с помощью анализа метилтиазолилтетразолия (МТТ), который основан на превращении желтого тетразолийбромида МТТ в пурпурное производное формазана митохондриальным ферментом сукцинатдегидрогеназой в жизнеспособных клетках. В конце инкубационного периода среду переносили в 96-луночные планшеты для определения цитокинов.Клетки промывали 0,2 мл фосфатно-солевого буфера и анализировали на цитотоксичность в том же лотке. Для обработанных клеток токсичность выражали в процентах.
SDS-PAGE
Метод Лэммли использовали для проведения электрофореза в пластинчатом 10% -ном додецилсульфат-полиакриламидном геле (SDS-PAGE). Анализировали образцы клеточных супернатантов (20 мкг белка). В качестве стандартов использовали: миозин (200 кДа), галактозидазу (116,2 кДа), фосфорилазу b (97,4 кДа), бычий сывороточный альбумин (66.2 кДа) и овальбумин (45 кДа) (Bio-Rad, Беркли, Калифорния, США).
Вестерн-блот-анализ
Метод Лэммли использовали для проведения электрофореза в пластинчатом SDS-PAGE. Анализировали равные порции клеточных супернатантов (20 мкг белка). Мы конденсировали десятикратную культуральную среду с использованием центриконов (отсечка 3 кДа), смешанных с буфером для образцов Лэммли (содержащим 2,5% SDS, без восстановителя). Электрофорез проводили с равными порциями (100 мкг) белка. После электрофореза клетки уравновешивали в 25 мМ Трис с 0.2 М глицин в 20% метаноле (об. / Об.) В течение 5 минут. Образцы переносили в поры нитроцеллюлозы размером 0,2 мкм при 100 мА в течение 1 часа. Для этой процедуры использовалась система электрофореза LKB 2117 Multiphor II Multiphor (GE Healthcare Bio-Sciences AB, Упсала, Швеция). Мы инкубировали нитроцеллюлозу в течение 1 часа с моноклональными антителами против коллагена I (концентрация 1: 1000), моноклональными антителами против фосфо-Akt (концентрация 1: 1000), поликлональными антителами против NF-κB (концентрация 1: 1000), моноклональное антитело против фосфо-MAPK (ERK 1/2 ) (концентрация 1: 1000), моноклональное антитело против каспазы 9 (концентрация 1: 1000).Антитела растворяли в растворе, содержащем 5% сухого молока, в трис-буферном физиологическом растворе с Tween 20 (TBS-T) (20 ммоль / л буфера Tris – HCl, pH 7,4, содержащего 150 ммоль / л NaCl и 0,05% Tween 20). . Для анализа фосфо-MAPK (ERK 1 / ERK / 2 ) и фосфо-AKT добавляли конъюгат щелочной фосфатазы против мышиного IgG (цельная молекула) в концентрации 1: 5000 в TBS-T. Для анализа NF-κB и каспазы-9, конъюгированного вторым антителом к щелочной фосфатазе, добавляли антикроличий IgG (целая молекула) в концентрации 1: 5000 в TBS-T.Для анализа коллагена типа I и конъюгированного второго антитела β-актина и щелочной фосфатазы добавляли анти-козий IgG (целая молекула) в концентрации 1: 5000 в TBS-T. Всю смесь инкубировали 30 минут при медленном встряхивании. После этого нитроцеллюлозу промывали TBS-T (5 × 5 минут) и обрабатывали реагентом жидкого субстрата 5-бром-4-хлор-3-индолилфосфат / нитросиний тетразолий. Интенсивность полос определяли количественно с помощью денситометрического анализа.
Зимография
Желатинолитическую активность измеряли с использованием метода Unemori и Werb.18 Мы конденсировали десятикратную культуральную среду с использованием центриконов (отсечка 3 кДа), смешанных с буфером для образцов (содержащим 2,5% SDS, без восстановителя). Электрофорез проводили с равными количествами белка (20 мкг) на полиакриламидных гелях (10%) в невосстанавливающих условиях. Гели пропитывали желатином (1 мг / мл). Инкубацию геля после электрофореза для удаления SDS проводили в течение 30 минут в 2% Triton X-100. После этого следовала инкубация в буфере, содержащем 50 мМ Трис – HCl, pH 8 с CaCl 2 5 мМ (субстратный буфер) в течение 18–24 часов при 37 ° C.После этого для окрашивания использовали кумасси бриллиантовый синий R250 (Thermo Fisher Scientific, Уолтем, Массачусетс, США).
Статистические методы
Средние значения по крайней мере для трех анализов ± стандартное отклонение (± SD) были рассчитаны во всех соответствующих экспериментах. Статистический анализ проводился с применением двустороннего непарного критерия Стьюдента t и дисперсионного анализа. Использовалась программа IBM SPSS 22.0 Statstics Genericom (IBM Corporation, Армонк, Нью-Йорк, США). П <0.05 и P <0,01 признан статистически значимым.
Результаты
Чтобы оценить активность этанола в синтезе коллагена в фибробластах кожи человека, клетки инкубировали в течение 24 часов в 25, 50 и 100 мМ этанола, а также в этаноле с HA в концентрации 500 мкг. / мл. Было показано, что этанол вызывает снижение синтеза коллагена дозозависимым образом (и). Воздействие на фибробласты различных концентраций этанола способствует ингибированию биосинтеза коллагена на 58.08% (2,39% ± стандартное отклонение; n = 3), 76,23% (3,52% ± стандартное отклонение; n = 3), 83,15% (4,03% ± стандартное отклонение; n = 3) P <0,05, P <0,01, соответственно по сравнению с контрольным значением. Однако в присутствии HA в концентрации 500 мкг / мл эффективность этанола по ингибированию биосинтеза коллагена была намного ниже. ГК, добавленный только к клеткам, не оказывал значительного влияния на биосинтез коллагена в контрольных клетках. Представленные результаты свидетельствуют о том, что этанол оказывает ингибирующее действие на синтез коллагена в сливающихся фибробластах кожи человека, а ГК противодействует этому процессу (и).
Биосинтез коллагена, измеренный как включение 5 [ 3 H] -пролина в белки, чувствительные к действию бактериальной коллагеназы, в сливающихся фибробластах кожи человека, инкубированных в течение 24 часов с различными концентрациями этанола и HA.
Примечания: Тест ANOVA: ** P <0,01. Планки погрешностей представляют собой ± стандартное отклонение; п = 3.
Сокращения: ANOVA, дисперсионный анализ; HA, гиалуроновая кислота; ДМСО, диметилсульфоксид; dpm, распадов в минуту.
Вестерн-иммуноблот-анализ коллагена типа I в субконфлюэнтных фибробластах кожи человека (контроль), клетках, обработанных с или без HA в течение 24 часов. Интенсивность окрашивания полос определяли количественно с помощью денситометрического анализа. Тест Стьюдента t -тест, * P <0,05 и ** P <0,01.
Примечания: 1, контроль; 2, этанол 25 мМ; 3, этанол 50 мМ; 4, этанол 100 мМ; 5, НА; 6, этанол 25 мМ и НА; 7, этанол 50 мМ и НА; 8, этанол 100 мМ и НА.Образцы, используемые для электрофореза, состояли из 20 мкг белка объединенных экстрактов клеток.
Сокращения: AU, условные единицы; HA, гиалуроновая кислота.
Фермент, ответственный за рециклинг пролина для ресинтеза коллагена, — пролидаза и ММП. Добавление этанола в концентрациях 25, 50 и 100 мМ к культурам клеток способствовало снижению активности пролидазы на 29,05% (4,55% ± стандартное отклонение; n = 3), 56,15% (3,82% ± стандартное отклонение; n = 3), и 88,18% (1,16% ± стандартное отклонение; n = 3). Добавление НА оказало значительный защитный эффект на активность пролидазы в фибробластах, инкубированных с этанолом.ГК восстанавливала активность пролидазы в клетках, инкубированных с этанолом, до контрольного уровня ().
Активность пролидазы в конфлюэнтных фибробластах кожи человека, инкубированных в течение 24 часов с различными концентрациями этанола и НА.
Примечания: Тест ANOVA: * P <0,05, ** P <0,01. Планки погрешностей представляют собой ± стандартное отклонение; п = 3.
Сокращения: ANOVA, дисперсионный анализ; HA, гиалуроновая кислота.
Проведенные исследования доказывают, что этанол нарушает метаболизм коллагена в фибробластах кожи человека, что приводит к значительному снижению синтеза ДНК.Распад за минуту [ 3 H] тимидина, включенного в ДНК этих клеток, был принят за 100%. Это было эталонное значение. Мы оценили эффект этанола в присутствии или в отсутствие ГК (500 мг / мл). Воздействие на фибробласты этанола различных концентраций способствовало ингибированию синтеза ДНК на 21,06% (7,08% ± стандартное отклонение; n = 3), 44,15% (5,06% ± стандартное отклонение; n = 3), 56,27% (4,26% ± стандартное отклонение; n = 3), 50,16% (4,56% ± стандартное отклонение; n = 3) P <0,05, P <0,01, соответственно, по сравнению с контрольным значением.ГК оказывает защитное влияние на процессы, вызванные этанолом ().
Биосинтез ДНК, измеренный по включению [ 3 H] -тимидина в ДНК в фибробластах кожи человека (контроль), инкубированных в течение 24 часов с различными концентрациями этанола и НА.
Примечания: Тест ANOVA: * P <0,05, ** P <0,01. Планки погрешностей представляют собой ± стандартное отклонение; п = 3.
Сокращения: ANOVA, дисперсионный анализ; HA, гиалуроновая кислота.
Эффективность HA в снижении цитотоксичности 25, 50 и 100 мМ этанола показана на рисунке. Было показано, что этанол вызывает цитотоксичность дозозависимым образом. Наличие этанола ингибирования выживаемости клеток 20,16% (4,05% ± стандартное отклонение; n = 3), 35,18% (3,63% ± стандартное отклонение; n = 3), 56,03% (2,53% ± стандартное отклонение; n = 3) P < 0,01 соответственно по сравнению с контрольным значением. Рецептор интегрина β 1 играет ключевую роль в контроле биосинтеза коллагена и активности пролидазы. В этом исследовании мы обнаружили, что этанол снижает экспрессию рецептора интегрина β 1 дозозависимым образом.В культивируемых клетках, инкубированных с HA и этанолом, этот эффект исчез. Было обнаружено, что экспрессия рецептора интегрина в клетках, обработанных различными концентрациями этанола и HA, была такой же, как и в контрольных клетках ().
Цитотоксичность фибробластов кожи человека (контроль), инкубированных в течение 24 часов с различными концентрациями этанола и НА.
Примечания: Тест ANOVA: * P <0,05, ** P <0,01. Планки погрешностей представляют собой ± стандартное отклонение; п = 3.
Сокращения: ANOVA, дисперсионный анализ; HA, гиалуроновая кислота.
Вестерн-иммуноблот-анализ для β 1 интегрина ( A ), рецептора инсулиноподобного фактора роста I ( B ), ERK 1/2 ( C ), киназы Akt ( D ), каспаза 9 ( E ) и β-актин ( F ) в субконфлюэнтных фибробластах кожи человека (контроль), клетках, обработанных с или без HA в течение 24 часов. Интенсивность окрашивания полос определяли количественно с помощью денситометрического анализа.
Примечания: Студенческий тест t -тест: * P <0,05, ** P <0,01. 1, контроль; 2, этанол 25 мМ; 3, этанол 50 мМ; 4, этанол 100 мМ; 5, НА; 6, этанол 25 мМ и НА; 7, этанол 50 мМ и НА; 8, этанол 100 мМ и НА. Образцы, используемые для электрофореза, состояли из 20 мкг белка объединенных экстрактов клеток.
Сокращения: AU, условные единицы; ERK, киназа, регулируемая внеклеточными сигналами; HA, гиалуроновая кислота.
Известно, что перекрестное взаимодействие между рецептором интегрина β 1 и рецептором IGF-IR играет ключевую роль в активации экспрессии гена коллагена и активности пролидазы.Этанол, как и в случае рецептора интегрина, вызывал снижение экспрессии IGF-IR (дозозависимым образом). ГК также оказывает защитное действие на уровень экспрессии этого рецептора (). В этом случае экспрессия рецептора IGF-IR в клетках, инкубированных с этанолом и HA, была близка к контролю.
Сигнал, передаваемый стимулированным IGF-IR и β 1 рецептором интегрина, приводит к активации MAPK (ERK 1/2 ) и Akt.14,15. Как видно на фибробластах, обработанных этанолом, экспрессия MAPK (фосфо-ERK 1/2 ) снижалось дозозависимым образом.Добавление HA к клеткам, обработанным этанолом, оказало защитное действие на зависимое от этанола снижение экспрессии фосфо-ERK 1/2 . Этанол и этанол с HA, добавленные к культивированным фибробластам, не влияли на экспрессию фосфо-AKT киназ (). Различные концентрации этанола оказывают цитотоксическое действие на фибробласты кожи человека, что приводит к индукции апоптоза, что приводит к наблюдаемому увеличению экспрессии каспазы 9 (). Более того, применение ГК оказывает защитное действие на нарушения пролиферации клеток, вызванные этанолом.Более того, экспрессия β-актина не изменялась в клетках при обработке этанолом в присутствии или в отсутствие НА ().
Некоторые данные свидетельствуют о том, что пролидаза-зависимая регуляция биосинтеза коллагена может иметь место на уровне транскрипции, в зависимости от экспрессии NF-κB. NF-κB — это фактор транскрипции, который действует как ингибитор экспрессии альфа 1 и альфа 2 субъединиц коллагена типа I. 19,20 Мы обнаружили повышенную экспрессию NF-κB в фибробластах, обработанных этанолом ().Добавление НА к клеткам, обработанным этанолом, способствовало снижению экспрессии этого транскрипционного фактора до контрольного уровня. Более того, экспрессия β-актина не изменялась в клетках при обработке этанолом в присутствии или в отсутствие НА (). Похоже, что регуляторный механизм индуцированной этанолом аберрации коллагена имеет место в точке биосинтеза коллагена, поскольку не было обнаружено влияния этанола и ГК на процесс деградации коллагена ММП-2 и ММП-9 ().
Вестерн-иммуноблот-анализ белка p65 NF-κB ( A ) и β-актина ( B ) в субконфлюэнтных фибробластах кожи человека (контроль), клетках, обработанных с или без HA в течение 24 часов.Интенсивность окрашивания полос определяли количественно с помощью денситометрического анализа.
Примечания: Студенческий тест t -тест: ** P <0,01. 1, контроль; 2, этанол 25 мМ; 3, этанол 50 мМ; 4, этанол 100 мМ; 5, НА; 6, этанол 25 мМ и НА; 7, этанол 50 мМ и НА; 8, этанол 100 мМ и НА. Образцы, используемые для электрофореза, состояли из 20 мкг белка объединенных экстрактов клеток.
Сокращения: AU, условные единицы; HA, гиалуроновая кислота.
Зимография для MMP-9 (92 кДа) и MMP-2 (72 кДа) в субконфлюэнтных фибробластах кожи человека (контроль), клетках, обработанных с или без HA в течение 24 часов.
Примечания: Интенсивность окрашивания полос количественно определяли с помощью денситометрического анализа. 1, контроль; 2, этанол 25 мМ; 3, этанол 50 мМ; 4, этанол 100 мМ; 5, НА; 6, этанол 25 мМ и НА; 7, этанол 50 мМ и НА; 8, этанол 100 мМ и НА. Образцы, используемые для электрофореза, состояли из 20 мкг белка объединенных экстрактов клеток.
Сокращения: AU, условные единицы; HA, гиалуроновая кислота; ММП, матричная металлопротеиназа.
Обсуждение
Хотя цитотоксичность этанола хорошо известна, механизм ее воздействия на метаболизм коллагена в тканях до конца не изучен.Похоже, что аномалии метаболизма коллагена, вызванные этанолом, тканеспецифичны. В печени он может способствовать стимуляции биосинтеза коллагена с последствием фиброза тканей, в то время как в коже может происходить противоположный процесс с последствием заживления ран.
В этом исследовании мы предоставили доказательства того, что этанол подавляет метаболизм коллагена в фибробластах кожи посредством нескольких уровней регуляции этого белка. Сначала это влияет на активность пролидазы, фермента, который играет важную роль в биосинтезе коллагена.Фермент отвечает за рециркуляцию пролина для ресинтеза коллагена, тем самым определяя выработку коллагена. Пептидные связи между пролином и другими аминокислотами могут быть расщеплены также другой пептидазой, пролиназой, которой необходим пролин в N-концевом положении.21 Пролидаза — вторая иминопептидаза, которая расщепляет дипептиды С-концевым пролином для сбора свободного пролина. Фермент переваривает как эндогенные, так и диетические дипептиды Xaa-Pro.21
Другой уровень регуляции метаболизма коллагена в обработанных этанолом фибробластах был обнаружен при β 1 интегрина и IGF-IR.Ранее мы обнаружили, что перекрестные помехи между рецепторами способствуют усилению биосинтеза коллагена. 22 В настоящем исследовании мы обнаружили, что этанол способствует подавлению экспрессии обоих рецепторов. Одновременно мы обнаружили повышение транскрипционной активности NF-κB, известного ингибитора коллагена типа I, который субъединиц экспрессии гена.20 В результате проведенных исследований был сделан вывод, что этанол приводит к нарушению биосинтеза коллагена в фибробластах. культур за счет снижения активности пролидазы и экспрессии интегрина β 1 и IGF-IR.Это сопровождалось пониженной экспрессией белков сигнального пути, индуцированной интегрином β 1 и IGF-IR, то есть киназами MAPK (ERK 1/2 ). Пониженное количество синтезированного коллагена и нарушение активности пролидазы также может быть связано с активацией фактора транскрипции NF-κB, который подавляет экспрессию гена коллагена. Применение ГК в концентрации 500 мкг / мл оказывает защитное действие на нарушения, вызванные исследуемыми веществами. Совокупность процессов, на которые влияет этанол, объясняет механизм индуцированного этанолом подавления биосинтеза коллагена.Основываясь на наших предыдущих исследованиях, мы рассматривали ГК как средство, противодействующее вызванной этанолом дерегуляции метаболизма коллагена в фибробластах.11 Фактически, мы обнаружили, что ГК устраняет все изученные дефекты метаболизма коллагена, вызванные этанолом. В нашей предыдущей статье мы не наблюдали отменяющего эффекта ГК, когда кофеин подавлял синтез коллагена.23 Различные концентрации этанола оказывают цитотоксическое действие на фибробласты кожи человека, что приводит к снижению выживаемости, ингибированию биосинтеза ДНК и индукции апоптоза, что приводит к в наблюдаемом повышении экспрессии каспазы 9.Более того, применение ГК оказывает защитное действие на дефект пролиферации клеток, вызванный этанолом.
HA играет важную роль в поддержании внеклеточного матрикса и вызывает защитное действие на структуру коллагена. 24,25 HA — это искусство гликозаминогликанов, где d-глюкуроновая кислота связана с частицей N -ацетилглюкозамина через гликозидные связи26. , 27 Клетка окружена слоем гиалуронана, который отвечает за форму, адгезию и миграцию клетки.24 Кожа содержит примерно 50% всей гиалуроновой кислоты в организме. ГК улучшает процессы заживления при некоторых патологических состояниях, таких как венозные язвы или повреждения мембран. Данные литературы показывают, что ГК играет полезную роль в регенеративных процессах, связанных с дисфункцией синтеза коллагена.28 Мы можем предположить, что ГК защищает от нарушений, вызванных этанолом. Этот защитный эффект можно контролировать посредством взаимодействия гиалуронана с его рецепторами CD44 и / или RHAMM.29 По крайней мере, в эндотелиальных клетках этот механизм способствует стимуляции выработки коллагена.30 Вопрос о том, играют ли рецепторы CD44 и RHAMM важную роль в механизме НА-зависимого противодействия токсичности этанола, требует дальнейшего изучения.
Данные, представленные в этой статье, могут иметь определенное социальное значение. Они предполагают, что фибробласты особенно чувствительны к этанолу и реагируют на это соединение путем ингибирования биосинтеза коллагена. Этот процесс способствует старению кожи, что представляет особый интерес для косметологии. Принимая во внимание приведенные выше данные и тот факт, что этанол обычно используется в косметологии, можно предположить, что этанол можно заменить в косметике другим растворителем или консервантами.Также можно рассматривать включение ГК в косметические препараты, содержащие этанол.
Выражение признательности
MD является научным сотрудником в области проектных исследований, исследований, коммерциализации: программа поддержки докторантов UMB, подмера 8.2.1 Операционная программа человеческого капитала, софинансируемая Европейским союзом в рамках Европейского социального фонда. Работа частично поддержана грантами Белостокского медицинского университета (143-14749F, 143-30730F, 144-30828F).
Сноски
Раскрытие информации
Авторы сообщают об отсутствии конфликта интересов в этой работе.
Ссылки
1. Сид Б., Верракс Дж., Кальдерон ПБ. Роль активации AMPK в окислительном повреждении клеток: последствия для алкогольной болезни печени. Biochem Pharmacol. 2013. 86 (2): 200–209. [PubMed] [Google Scholar] 2. Эль-Хадж Э.С., Эль-Хадж М.К., Волошенюк Т.Г. и др. Алкогольная модуляция металлопротеиназ сердечного матрикса (ММП) и тканевых ингибиторов ММП способствует накоплению коллагена. Alcohol Clin Exp Res. 2014. 38 (2): 448–456. [Бесплатная статья PMC] [PubMed] [Google Scholar] 3. Xu GF, Li PT, Wang XY и др.Динамические изменения экспрессии матриксных металлопротеиназ и их ингибиторов, TIMP, во время фиброза печени, вызванного алкоголем у крыс. Мир Дж. Гастроэнтерол. 2004. 10 (24): 3621–3627. [Бесплатная статья PMC] [PubMed] [Google Scholar] 4. Neuman MG, Nanau RM, Oruña L, Coto G. Противовоспалительные эффекты гиалуроновой кислоты in vitro при повреждении клеток кожи, вызванном этанолом. J. Pharm. Pharm. Sci. 2011. 14 (3): 425–437. [PubMed] [Google Scholar] 5. Пржилипиак А., Рабе Т., Хафнер Дж., Пржилипиак М., Руннебаум Б.Влияние этанола на рост in vitro клеточной линии карциномы молочной железы человека MCF-7. Arch Gynecol Obstet. 1996. 258 (3): 137–140. [PubMed] [Google Scholar] 6. Джонен Ч., Хартманн Б., Штеффен И. и др. Выделение и размножение клеток кожи для трансплантации клеток ограничено у пациентов, употребляющих табак, алкоголь или страдающих сахарным диабетом. Бернс. 2006. 32 (2): 194–200. [PubMed] [Google Scholar] 7. Ранзер MJ, Чен Л., ДиПьетро Л.А. При острой интоксикации этанолом нарушается функция фибробластов и прочность на разрыв раны.Alcohol Clin Exp Res. 2011; 35 (1): 83–90. [Бесплатная статья PMC] [PubMed] [Google Scholar] 8. Бойс Дж. М.. Обновите информацию о гигиене рук. Am J Infect Control. 2013. 41 (5): 94–96. [PubMed] [Google Scholar] 9. Ким И-Ч, Пак Джей-Х, Людовице П.Дж., Праусниц MR. Синергетическое усиление проницаемости кожи N-лауроилсаркозином и этанолом. Int J Pharmaceutics. 2008. 352 (1–2): 129–138. [PubMed] [Google Scholar] 10. Pendlington RU, Whittle E, Robinson JA, Howes D. Судьба этанола, наносимого на кожу местно. Food Chem Toxicol. 2001. 39 (2): 169–174.[PubMed] [Google Scholar] 11. Surazynski A, Miltyk W, Czarnomysy R, Grabowska J, Palka J. Гиалуроновая кислота отменяет зависимую от оксида азота стимуляцию деградации коллагена в культивируемых хондроцитах человека. Pharmacol Res. 2009. 60 (1): 46–49. [PubMed] [Google Scholar] 12. Гази К., Денг-Пичон У., Варнет Дж.М., Крыса П. Фрагменты гиалуроновой кислоты улучшают заживление ран на кожной модели in vitro за счет базовой активации пуринорецептора P2X7: роль молекулярной массы. PLoS One. 2012; 7 (11): e48351. [Бесплатная статья PMC] [PubMed] [Google Scholar] 13.Nawrat P, Surazynski A, Karna E, Pałka JA. Влияние гиалуроновой кислоты на индуцированное интерлейкином-1 нарушение регуляции метаболизма коллагена в культивируемых фибробластах кожи человека. Pharmacol Res. 2005. 51 (5): 473–477. [PubMed] [Google Scholar] 14. Петеркофский Б., Дигельманн Р. Использование смеси коллагеназ, свободных от протеиназ, для специфического анализа радиоактивного коллагена в присутствии других белков. Биохимия. 1971; 10 (6): 988–994. [PubMed] [Google Scholar] 15. Myara I, Charpentier C, Lemonnier A. Оптимальные условия для анализа пролидазы колориметрическим определением пролина: применение к иминодипептидурии.Clin Chim Acta. 1982; 125 (2): 193–205. [PubMed] [Google Scholar] 16. Лоури Н., Розенбро Н., Фарр Л., Рэндалл Р. Измерение белка с реагентом фолин-фенол. J Biol Chem. 1951; 193 (1): 265–275. [PubMed] [Google Scholar] 17. Laemmli UK. Расщепление структурных белков при сборке головки бактериофага Т4. Природа. 1970. 227 (5259): 680–685. [PubMed] [Google Scholar] 18. Unemori E, Werb Z. Реорганизация полимеризованного актина: возможный спусковой механизм для индукции проколлагеназы в фибробластах, культивируемых в коллагеновых гелях и на них.J Cell Biol. 1986. 103 (3): 1021–1031. [Бесплатная статья PMC] [PubMed] [Google Scholar] 19. Коуба Д., Чунг К.-Й, Нишияма Т. и др. Ядерный фактор-κB опосредует ингибирующее действие TNF-α на транскрипцию гена коллагена α2 (I) (COL1A2) в дермальных фибробластах человека. J Immunol. 1999. 162 (7): 4226–4234. [PubMed] [Google Scholar] 20. Miltyk W, Karna E, Palka J. Независимый от пролидазы механизм камптотецина-индуцированного ингибирования биосинтеза коллагена в культивируемых фибробластах кожи человека. J Biochem. 2007. 141 (2): 287–292.[PubMed] [Google Scholar] 21. Китченер Р.Л., Грюнден А.М. Функция пролидазы в метаболизме пролина и ее медицинские и биотехнологические применения. J Appl Microbiol. 2012. 113 (2): 233–247. [PubMed] [Google Scholar] 22. Surazynski A, Miltyk W, Prokop I, Palka J. Пролидазозависимая регуляция экспрессии рецепторов TGF и TGF β в фибробластах кожи человека. Eur J Pharmacol. 2010. 649 (1–3): 115–119. [PubMed] [Google Scholar] 23. Донейко М., Пржилипиак А., Рысяк Э., Глушук К., Суразинский А. Влияние кофеина и гиалуроновой кислоты на биосинтез коллагена в фибробластах кожи человека.Drug Des Devel Ther. 2014; 8: 1923–1928. [Бесплатная статья PMC] [PubMed] [Google Scholar] 25. Karna E, Miltyk W, Surazyński A, Pałka JA. Защитный эффект гиалуроновой кислоты на индуцированную интерлейкином-1 дерегуляцию передачи сигналов рецептора бета1-интегрина и инсулиноподобного фактора роста-I и биосинтез коллагена в культивируемых хондроцитах человека. Mol Cell Biochem. 2008. 308 (1–2): 57–64. [PubMed] [Google Scholar] 26. Гириш К.С., Кемпараджу К. Волшебный клей гиалуронан и его ластик гиалуронидаза: биологический обзор.Life Sci. 2007. 80 (21): 1921–1943. [PubMed] [Google Scholar] 27. Шефер Л, Шефер РМ. Протеогликаны: от структурных соединений до сигнальных молекул. Cell Tissue Res. 2010. 339 (1): 237–246. [PubMed] [Google Scholar] 28. Суразинский А., Милтык В., Палка Дж., Панг Дж. М.. Пролидазозависимая регуляция биосинтеза коллагена. Аминокислоты. 2008. 35 (4): 731–738. [PubMed] [Google Scholar] 29. Aruffo A, Stamenkovic I, Melnick M, Underhill CB, Seed B. CD44 является основным рецептором гиалуроната на клеточной поверхности. Клетка.1990. 61 (7): 1303–1313. [PubMed] [Google Scholar] 30. Руни П., Ван М., Кумар П., Кумар С. Ангиогенные олигосахариды гиалуронана увеличивают выработку коллагенов эндотелиальными клетками. J Cell Sci. 1993. 105 (1): 213–218. [PubMed] [Google Scholar]
Как вы стареете изнутри и снаружи — Coastal Detox
Когда вы думаете о влиянии алкоголя на ваше здоровье и благополучие, большинство людей думают только о том, как он влияет на их внутренние органы. Но действительно ли вы понимаете его разрушительное воздействие на самый большой орган вашего тела?
Каждый восьмой взрослый в США борется с алкоголизмом.Если вы обнаружите, что регулярное употребление алкоголя мешает вам выполнять определенное обязательство или его чрезмерное употребление вызывает повторяющиеся межличностные проблемы, возможно, вам стоит подумать о том, чтобы вообще отказаться от него.
А пока в этой статье исследуется негативное воздействие алкоголя на кожные ткани, о котором вы, вероятно, не знали. Читать дальше.
Безудержное обезвоживание
Если вы никогда не замечали, существует прямая зависимость между количеством потребляемого вами алкоголя и частотой ваших походов в туалет.Это больше, чем простое совпадение.
Чрезмерное употребление алкоголя снижает выработку антидиуретического гормона (АДГ). Организм использует его в первую очередь для реабсорбции воды тканями тела. Поскольку алкоголь подавляет его производство, ваше тело теряет много воды из-за частого мочеиспускания.
Так что же он делает с вашей кожей? Во-первых, алкоголь и морщины идут рука об руку. Вы начнете замечать появление на коже тонких морщинок. Он начинает терять яркость и жизненную силу.
Ваша кожа содержит молекулы, известные как гиалуроновая кислота, которые предназначены для захвата и удержания воды глубоко под поверхностью кожи. Когда эти молекулы обезвоживаются, вы начнете замечать морщинки вокруг глаз, затем на лице, шее и руках — как правило, на тех участках тела, где ваша кожа наиболее тонкая.
Затем организм пытается бороться с этим, выделяя больше кожного сала в клетки кожи, что, в свою очередь, вызывает жирность кожи. Вы увидите это проявление в виде черных точек, белых точек, папул и блеска.
Чем больше алкоголя вы потребляете в течение длительного периода времени, тем меньше гиалуроновой кислоты вырабатывает ваше тело. Это приводит к появлению глубоких морщин.
Еще один эффект обезвоживания — задержка воды. Это, пожалуй, наиболее заметное воздействие алкоголя на кожные ткани.
Из-за того, как быстро ваше тело теряет воду, когда вы принимаете алкоголь, ваши клетки изо всех сил стараются удержать имеющееся небольшое количество воды. Это приводит к тому, что ваша кожа выглядит опухшей, особенно на лице.
Хроническое воспаление кожи
После ночи, проведенной в большом количестве алкоголя, кожа становится красной. Для этого есть причина, связанная с алкоголем.
Когда вы пьете, ваше тело классифицирует алкоголь как токсичное вещество, которое ему необходимо расщепить и вывести из организма. Здесь на помощь приходит печень. Она превращает алкоголь в побочный продукт, известный как ацетальдегид.
Это химическое вещество токсично для тканей организма и оставляет их обезвоженными. Повреждение кожи алкоголем возникает из-за того, что ткани не только обезвожены, но и воспалены.Это заставляет ткани организма выделять гистамин, который расширяет кровеносные сосуды кожи.
Чем больше крови проходит через капилляры кожи, тем больше кожа приобретает красноватый оттенок. Когда это усугубляется чрезмерным увлечением в течение нескольких лет, кровеносные капилляры остаются расширенными, что делает покраснение на коже необратимым. Так что вы всегда будете выглядеть как «загар», но при этом не испытаете никаких солнечных ожогов!
На этом негативные последствия воспаления кожи не заканчиваются.Алкоголь также расширяет поры кожи. Затем поры забиваются бактериями, кожным салом и мертвыми клетками кожи, которые вызывают появление черных точек и белых точек.
Если это будет продолжаться, они могут превратиться в полноценные кистозные прыщи и шишки, похожие на поражения, возникающие в результате воспаленных кожных папул. В конечном итоге они вызывают постоянные рубцы на коже. Последствия воспаления наиболее заметны на лице, но оно также влияет на шею, грудь, спину, плечи, плечи и туловище.
Плохой сон вызывает плохое состояние кожи
Вопреки тому, что вы думаете, алкоголь и хороший ночной сон подобны маслу и воде — они просто не смешиваются.Это может позволить вам заснуть быстрее, чем обычно, но на самом деле это гораздо более разрушительно для сна.
Видите ли, сон состоит из разных стадий. Есть фаза без быстрого сна и фаза быстрого сна. REM означает быстрое движение глаз.
Медленная фаза сна — легкая. Вас легко разбудить. Когда ваш пульс замедляется, а температура тела падает, ваше тело начинает переходить в глубокую стадию медленного сна.
Это когда процессы ремонта и обслуживания вашего тела происходят.Они включают восстановление и восстановление тканей, а также регенерацию костных и мышечных клеток. Это также когда организм работает над укреплением своей иммунной системы.
Итак, если вы задаетесь вопросом: «Как же, черт возьми, выпивка вызывает морщины?» Продолжай читать. Алкоголь ухудшает качество вашего сна. Это буквально мешает вам заснуть прекрасным сном.
Он не позволяет вам добраться до более глубоких стадий цикла сна, когда происходит восстановление и восстановление клеток кожи.При этом ваша кожа не может сбалансировать себя должным образом.
Это означает, что вы заметите, что он либо слишком сухой, либо слишком жирный, либо теряет свою эластичность из-за нарушения выработки коллагена. Вы также можете заметить появление темных кругов вокруг глаз и появление морщин.
Чрезмерное длительное употребление алкоголя помешает вам хорошо выспаться даже в те ночи, когда вы не пьете. Таким образом, ваше тело никогда не сможет получить глубокий сон, необходимый для генерации новых клеток кожи.
Негативное влияние сладких алкогольных напитков на здоровье кожи
Если вы думаете, что именно крепкие напитки разрушают вашу кожу, вы, к сожалению, ошибаетесь. Хотя иногда коктейль может не сильно повлиять на вашу кожу, употребление сладких алкогольных напитков часто также приводит к потере эластичности кожи и развитию преждевременных морщин.
Вот небольшой урок химии об алкоголе и стареющей коже. Когда вы употребляете сладкие напитки, организм быстро превращает этот сахар в глюкозу.Это, в свою очередь, приводит к резкому скачку уровня инсулина, поскольку он помогает быстро избавиться от выброса глюкозы из кровотока.
Скачок уровня инсулина вызывает вспышку воспаления по всему телу, включая кожу. В процессе вырабатываются ферменты, расщепляющие коллаген. Коллаген — это самый распространенный белок в организме, который содержится во всех соединительных тканях в сухожилиях, мышцах связок, а также, как вы уже догадались, в коже.
Это то, что придает вашей коже ее структуру.Это также замедляет процесс старения вашей кожи, уменьшая появление морщин и появление сухости. Таким образом, посредством процесса, называемого гликированием, молекулы глюкозы навсегда прикрепляются к коллагену в тканях вашей кожи. Эта реакция способствует развитию прыщей, темных пятен и складок на коже по всему телу.
Отсюда и термин «реакция приливания спиртом». Это постоянный красноватый цвет лица, который люди, которые пьют в течение многих лет, получают даже после того, как в конце концов бросают пить.
Худшие виды спирта для кожи
Помните, что весь алкоголь содержит ацетальдегиды, разрушительные молекулы, разрушающие ваше тело. Они вызывают обширное воспаление и повреждение клеток как внутренних органов, так и кожи. Объедините их с этими сладкими охотниками, и вы получите рецепт катастрофы.
Тем не менее, есть некоторые виды алкоголя, которые особенно вредны для вашей кожи. Вот некоторые из них, отсортированные от наименее вредного до наиболее вредного для здоровья вашей кожи:
Текила
Текила содержит наименьшее количество сахара по сравнению с большинством других алкогольных напитков.Его высокая чистота делает его самым благоприятным для кожи.
Но будьте осторожны — он безопасен для кожи только при периодическом употреблении в небольших количествах. Чрезмерное употребление текилы в течение длительного времени все равно в конечном итоге повредит вашу кожу.
Пиво
Пиво может и не очень вредно для кожи, но это не самое худшее из всех возможных. Скорее всего, это потому, что он не содержит высоких концентраций алкоголя, как другие.
Однако в нем есть много других добавок, таких как сахар и соль, которые усложняют метаболизм печени.В частности, темное пиво содержит намного больше добавок, чем прозрачное. Так что лучше их вообще избегать.
Водка / Джин-тоник
И водка, и джин содержат значительно меньше сахара, чем другие напитки, что делает их более «добрыми» для кожи. Чего нельзя сказать о вреде, который они наносят вашим внутренним органам.
Белое вино
Если у вас когда-нибудь было винное похмелье, то вы знаете, насколько ужасными они могут быть. Высокое содержание сахара тоже не пойдет на пользу вашей коже.
Мохито
Вы бы хотели избавиться от морщин? Вот насколько вреден мохито для вашей кожи. Каждый стакан содержит необычно высокий уровень сахара, и вы знаете, что это значит для вашего коллагена, не так ли?
Маргарита
Это еще один виновник коктейлей. Он содержит много соли в дополнение к высокому уровню сахара, который он содержит. Неудивительно, что после ночи, проведенной за маргаритой, вы просыпаетесь с видом, будто грузовик наехал вам на лицо — из-за всей отечности и воспаления.
Красное вино
Не обманывайтесь, думая, что красное вино полезно для здоровья. Можно возразить, что у него нет никаких искупаемых качеств.
Это может быть антиоксидант, но на самом деле, если вы взвесите его за и против, вы также можете найти альтернативный источник антиоксидантов. Хорошим началом было бы поесть сырого винограда.
Красное вино — это печально известный выброс гистамина. Поэтому, если вы склонны к появлению прыщей или покраснений, держитесь от них подальше.
Влияние алкоголя на ткани кожи: еще не поздно спасти кожу
Рискуя заявить, что у вас здоровая кожа, вам необходимо резко сократить количество потребляемого алкоголя.Если вы обнаружите, что не можете придерживаться рекомендованных пороговых значений потребления алкоголя, это может быть признаком более серьезной проблемы. С этой целью наилучшей альтернативой является полный отказ от алкоголя.
Кроме того, невозможно переоценить важность сбалансированного питания и достаточного потребления воды. Хотя употребление достаточного количества воды омолаживает вашу кожу, слишком большое ее количество может привести к потере жизненно важных минералов.
Вы также можете попытаться изменить свой образ жизни, включив регулярный режим тренировок.Помимо пользы для сердечно-сосудистой системы, упражнения являются одним из ключей к здоровой и яркой коже.
Увеличивает приток крови к тканям кожи, принося с собой важные питательные вещества, жизненно важные для питания клеток кожи. Повышенный кровоток также помогает уносить отходы, такие как свободные радикалы, от рабочих клеток. Поэтому вместо того, чтобы проводить ночь в городе, выпейте с друзьями, займитесь спортом, чтобы предотвратить преждевременное старение кожи.
Имейте в виду, что длительное воспаление кожи может привести к воспалению прыщей, которое может распространиться и, в конечном итоге, вызвать рубцевание.Если вы начнете замечать это, есть множество безрецептурных препаратов, которые вы можете использовать для лечения этого состояния.
Вы можете попробовать использовать перекись бензоила, которая нейтрализует бактерии акне, которые могут забивать поры вашей кожи. Салициловая кислота также хорошо удаляет омертвевшие клетки кожи из глубины пор.
Наконец, вы можете начать принимать добавки с коллагеном, чтобы уменьшить воспаление, улучшить эластичность кожи и уменьшить морщины. Более того, исследования показывают, что регулярный прием этих добавок при сокращении (или полном исключении) алкоголя из своего рациона стимулирует организм самостоятельно вырабатывать коллаген.
Итог
Негативное воздействие алкоголя на кожные ткани и другие внутренние органы тела невозможно переоценить. Вы будете удивлены всеми преимуществами, которые получите, если откажетесь от этого. Это не только улучшит ваше социальное благополучие, но и сделает вашу жизнь намного более здоровой и продуктивной.
Вы ищете удобное и безмятежное место, которое поможет вам на пути к детоксикации? Поговорите с нами сегодня. Мы будем рады протянуть руку помощи.
Артикулы:
DIY дезинфицирующее средство для рук с гиалуроновой кислотой и медицинским изопропиловым спиртом
Этот пост содержит партнерские ссылки. Щелкните здесь, чтобы ознакомиться с моей политикой партнерства.
Мытье рук всегда должно быть вашим выбором №1, но важно держать бутылку хорошего дезинфицирующего средства в любом общественном месте.
Но что такое хорошее дезинфицирующее средство для рук? Центры по контролю и профилактике заболеваний рекомендуют дезинфицирующее средство, содержащее не менее 60% спирта, когда мытье рук недоступно. Вот почему важно быть разборчивым с тем, какое дезинфицирующее средство вы выберете или сделаете, так как не все рецепты содержат достаточно алкоголя, чтобы быть эффективными.
Прокрутите вниз, чтобы узнать мой домашний рецепт дезинфицирующего средства для рук, содержащего 73% спирта.
Преимущества выбранных ингредиентов:
Спирт использовался в качестве дезинфицирующего средства на протяжении веков, начиная с Древнего Египта и вплоть до современного мира медицины. Изопропиловый спирт , также известный как медицинский спирт, обладает быстрым противомикробным действием против бактерий, грибков и вирусов, особенно в растворах с содержанием спирта 60–90% и 10–40% очищенной воды. Гиалуроновая кислота — это увлажнитель, что означает, что он поглощает влагу и удерживает ее, чтобы кожа могла ее впитать. Один грамм ГК может вместить до шести литров воды! ГК обладает антивозрастными свойствами, укрепляет защитный барьер кожи и способствует заживлению. Он также обеспечивает антиоксидантную защиту от УФ-излучения.
Масло чайного дерева содержит несколько соединений, включая терпинен-4-ол, которые обладают свойствами борьбы с микробами. Это мощный антисептик, стимулятор иммунной системы, который полезен для уничтожения бактерий, вирусов и грибков.
Ингредиенты
30 мл (1 унция) Минеральная вода
0,42 г Порошок гиалуроновой кислоты (найти здесь: США / Великобритания / Канада )
- Медицинский 99,9% изопропиловый спирт ( здесь )
2 мл (40 капель) Tea Tree EO (найти здесь: US / UK / Canada ).
Посуда
Этот рецепт требует точности, так как необходимо соблюдать соотношение, чтобы продукт оставался эффективным против микробов.Вот что вы можете использовать для изготовления этого дезинфицирующего средства для рук своими руками:
Градуированный цилиндр на 100 мл (3,3 унции) (его можно найти здесь: US / UK / Canada )
Небольшой смеситель из нержавеющей стали чаша
Мини-венчик из нержавеющей стали (находится здесь: US / UK / Канада )
100 мл (3,3 унции) многоразовый пустой контейнер для геля / лосьона (найти его здесь: US / UK / Canada )
Высокоточные весы (находятся здесь: US / UK / Canada )
A термометр для приготовления пищи
: Я заказал гиалуроновую кислоту и изопропиловый спирт медицинского класса на Amazon, потому что доставка на Amazon Prime такая недорогая.Вы можете попробовать 30-дневную бесплатную пробную версию и получить БЕСПЛАТНУЮ двухдневную доставку для всех ваших заказов.
Моя коллекция эфирных масел в основном из Plant Therapy . У них есть органические эфирные масла высочайшего качества и специальный выбор масел, безопасных для детей. Посетите их веб-сайт, чтобы узнать о последних предложениях!
Инструкции
Нагрейте минеральную воду до 75 ° C (167 ° F).
Налейте воду в миксерную чашу и добавьте гиалуроновую кислоту.Хорошо перемешайте мини-венчиком. Накройте крышкой и оставьте на 20 минут, затем снова перемешайте. Если консистенция недостаточно гладкая, вы можете повторить этот шаг (накрыть крышкой, подождать 20 минут и перемешать, чтобы раствориться).
Nota Bene: При добавлении в воду гиалуроновая кислота образует гель. Но если воды недостаточно, гель становится комковатым и жестким. Все дело в поддержании правильного баланса;)Шаг за шагом (5 мл за раз) добавьте изопропиловый спирт в гель и перемешайте.
Добавьте эфирное масло чайного дерева и хорошо перемешайте.
Перелейте гель из емкости в емкость многоразового использования. Если вам не удалось получить идеально гладкий гель при смешивании минеральной воды с гиалуроновой кислотой (шаг 2), оставьте готовый продукт на 12 часов. ГК полностью растворится за это время.
Пытаетесь ли вы убить бактерии или оболочечные вирусы, включая коронавирус, многие исследования показали, что для эффективности необходима концентрация алкоголя 60 процентов или выше.Если вы соблюдаете пропорции этого рецепта, вы получите самодельное дезинфицирующее средство для рук с концентрацией спирта 73%.
Альтернатива: Если вы ищете хорошее дезинфицирующее средство для рук ручной работы, сделанное в США и доступное даже в периоды высокого спроса, я рекомендую это от Z Skin . Он очень эффективен против микробов и бактерий благодаря концентрации спирта 70%, алоэ вера и эфирным маслам.


 А самого косметолога тоже нужно выбирать очень тщательно, ведь ему доверяешь свою внешность.
А самого косметолога тоже нужно выбирать очень тщательно, ведь ему доверяешь свою внешность. Отек «задержится», при этом он может распространиться на все тело.
Отек «задержится», при этом он может распространиться на все тело. При этом сами обезболивающие свойства алкоголя сильно переоценены – ни в какое сравнение со стандартным кремом-анестетиком они не идут;
При этом сами обезболивающие свойства алкоголя сильно переоценены – ни в какое сравнение со стандартным кремом-анестетиком они не идут; Такой эффект заметно усилит ту отечность, которая в норме возникает после введения гиалуроновой кислотыиз-за повреждения тканей иглой – и лицо в течение 1-2 дней может выглядеть крайне непрезентабельно.
Такой эффект заметно усилит ту отечность, которая в норме возникает после введения гиалуроновой кислотыиз-за повреждения тканей иглой – и лицо в течение 1-2 дней может выглядеть крайне непрезентабельно. Оценивать действие каждого из них по отдельности большого смысла нет, потому связывать подозрительно недолгий эффект инъекционного препарата только лишь с употреблением спиртного не стоит. Кратковременное повышение кровотока в тканях, вызываемое опьянением, тоже не имеет существенного влияния на скорость обменных процессов: расширение сосудов лица происходит по многу раз в течение дня, не только после спиртного, но и как реакция на эмоции, физическую нагрузку, изменение температуры и влажности воздуха и т.п.
Оценивать действие каждого из них по отдельности большого смысла нет, потому связывать подозрительно недолгий эффект инъекционного препарата только лишь с употреблением спиртного не стоит. Кратковременное повышение кровотока в тканях, вызываемое опьянением, тоже не имеет существенного влияния на скорость обменных процессов: расширение сосудов лица происходит по многу раз в течение дня, не только после спиртного, но и как реакция на эмоции, физическую нагрузку, изменение температуры и влажности воздуха и т.п. Это происходит благодаря стимуляции деления клеток с увеличением числа фибробластов и активного синтеза коллагена и эластина. В умеренном количестве это дает омолаживающий лифтинговый эффект, в избыточном – приводит к рубцеванию, появлению под кожей плотных шишек. Спровоцировать чересчур активное развитие соединительной ткани могут инфекция, нарушение процессов заживления в результате недостатка кислорода (гипоксия), внешние воздействия. Спиртное в связи с кратковременным нахождением этилового спирта в организме оказать подобного влияния не в состоянии. Чуть более опасная в этом плане привычка – курение, так как помимо хронической интоксикации, никотин нарушает процесс насыщения тканей кислородом.
Это происходит благодаря стимуляции деления клеток с увеличением числа фибробластов и активного синтеза коллагена и эластина. В умеренном количестве это дает омолаживающий лифтинговый эффект, в избыточном – приводит к рубцеванию, появлению под кожей плотных шишек. Спровоцировать чересчур активное развитие соединительной ткани могут инфекция, нарушение процессов заживления в результате недостатка кислорода (гипоксия), внешние воздействия. Спиртное в связи с кратковременным нахождением этилового спирта в организме оказать подобного влияния не в состоянии. Чуть более опасная в этом плане привычка – курение, так как помимо хронической интоксикации, никотин нарушает процесс насыщения тканей кислородом.