Действие гиалуроновой кислоты: Что такое гиалуроновая кислота: как и зачем применять, отзывы врача :: Здоровье :: РБК Стиль
Что такое гиалуроновая кислота: как и зачем применять, отзывы врача :: Здоровье :: РБК Стиль
Гиалуроновая кислота, пожалуй, один из самых известных ингредиентов красоты. О ней слышали даже люди, далекие от бьюти-индустрии. Тем не менее часто познания о гиалуроновой кислоте ограничиваются тем, что она уменьшает морщины. На самом деле все не так просто.
Маргарита Гехт,
ведущий врач-дерматолог благотворительного фонда «Дети-бабочки», преподаватель онлайн-академии проблем кожи Skill for Skin
- Что такое гиалуроновая кислота
- Как понять, что коже необходима гиалуроновая кислота
- Добавки с гиалуроновой кислотой
- Почему препараты с гиалуроновой кислотой не работают
- Для какого типа кожи подходят средства с гиалуроновой кислотой
- Какие названия на упаковках может иметь гиалуроновая кислота
- Какие продукты ухода за кожей содержат гиалуроновую кислоту
- Каковы побочные эффекты при использовании гиалуроновой кислоты
- Какой должна быть гиалуроновая кислота
- С какими компонентами удачно сочетается гиалуроновая кислота
- Другие медицинские преимущества гиалуроновой кислоты
- Инъекции гиалуроновой кислоты
Что такое гиалуроновая кислота
Гиалуроновая кислота — самая универсальная «молекула красоты». Она была открыта в 1934 году Карлом Мейером и его ассистентом Джоном Палмером.
Она была открыта в 1934 году Карлом Мейером и его ассистентом Джоном Палмером.
Гиалуроновая кислота содержится в костях, соединительной ткани, хрящах, волосяных фолликулах и коже. При этом в коже присутствует почти половина гиалуроновой кислоты, где она, действуя как магнит, связывается с водой, замедляя скорость ее испарения и помогая клеткам удерживать влагу. Всего 1 г гиалуроновой кислоты обладает впечатляющей способностью удерживать до 6 л воды. Добавьте к этому способность регулировать уровень влаги внутри клеток, и вы получите феноменальный клеточный компонент. Он позволяет коже сохранять высокий уровень увлажненности, оставаться упругой и здоровой.
Таким образом гиалуроновая кислота оказывает три основных эффекта:
- антивозрастной;
- увлажняющий;
- ранозаживляющий.
Гиалуроновая кислота может быть разрушена свободными радикалами под действием ультрафиолета, табачного дыма и загрязненной окружающей среды.
Как понять, что коже необходима гиалуроновая кислота
После 25 лет клетки кожи вырабатывают меньше гиалуроновой кислоты. Это происходит из-за замедления способности клеток делиться и удерживать влагу. Обезвоженная кожа имеет неоднородную структуру, усеяна мелкими морщинами и выглядит тусклой.
Это происходит из-за замедления способности клеток делиться и удерживать влагу. Обезвоженная кожа имеет неоднородную структуру, усеяна мелкими морщинами и выглядит тусклой.
Для того чтобы кожа оставалась мягкой, упругой и сияла, начиная с 25 лет можно включать в ежедневный уход кремы и препараты с гиалуроновой кислотой, а после 30 лет еще и гиалуроновую сыворотку.
Добавки с гиалуроновой кислотой
При недостатке гиалуроновой кислоты показан прием соответствующих добавок. Исследованиями доказано, что прием 120–240 мг гиалуроновой кислоты в день в течение по крайней мере одного месяца значительно повышает увлажненность кожи и уменьшают ее сухость. БАДы с гиалуроновой кислотой можно принимать начиная с 20 лет.
Почему препараты с гиалуроновой кислотой не работают
Если кожа достаточно увлажнена, препараты с гиалуроновой кислотой при нанесении могут скатываться — это означает, что необходимости в использовании данного компонента в настоящий момент нет.
Если после использования крема или сыворотки с гиалуроновой кислотой возникает ощущение пленки на коже, значит, кожа не нуждается в гиалуроновой кислоте.
Для какого типа кожи подходят средства с гиалуроновой кислотой
Существует три главных типа кожи:
- нормальный;
- сухой;
- жирный.
Кожа любого типа может испытывать состояния обезвоженности и чувствительности. То есть и жирная, и нормальная кожа могут быть обезвоженными. При этом важно не путать состояние обезвоженности и сухой тип кожи. Причина сухой кожи в недостатке липидов, а не воды.
Какие названия на упаковках может иметь гиалуроновая кислота
Гиалуроновая кислота имеет следующие названия:
- гидролизованная гиалуроновая кислота;
- ацетилированный гиалуронат;
- натрия гиалуронат;
- натриевая соль гиалуроновой кислоты.
Какие продукты ухода за кожей содержат гиалуроновую кислоту
Сыворотки
Они имеют легкую текстуру, минимальный состав и отличаются наибольшей концентрацией гиалуроновой кислоты. Кроме того, в текстуре сыворотки гиалуроновая кислота быстрее проникает в кожу. Лучше всего использовать комбинацию больших и малых молекул для мгновенного увлажнения верхнего слоя кожи и более длительного воздействия на нижний эпидермис.
Кроме того, в текстуре сыворотки гиалуроновая кислота быстрее проникает в кожу. Лучше всего использовать комбинацию больших и малых молекул для мгновенного увлажнения верхнего слоя кожи и более длительного воздействия на нижний эпидермис.
Как правильно использовать сыворотку с гиалуроновой кислотой
Сыворотку с гиалуроновой кислотой очень важно наносить правильно. Дело в том, что если во влажной комнате на сухую кожу нанести сыворотку с гиалуроновой кислотой без последующего нанесения крема, сыворотка вытянет влагу из воздуха и создаст ощущение стянутости, не высушив при этом лицо. Если кожа увлажнена, а помещение сухое, гиалуроновая кислота, находящаяся на поверхности лица, вытянет воду из кожи и испарит ее в воздух, создав ощущение сухости.
Поэтому важно наносить сыворотку с гиалуроновой кислотой на слегка влажную кожу — можно сбрызнуть лицо термальной водой или не до конца высушить полотенцем, а после сыворотки сразу же нанести увлажняющий крем, чтобы «запечатать» гиалуроновую кислоту в коже.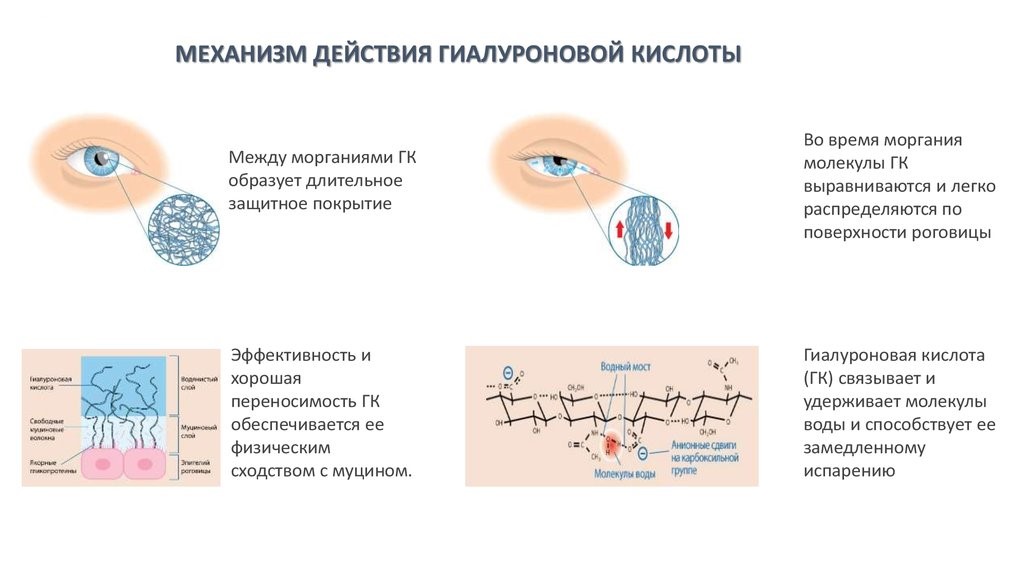 Так эффект увлажнения будет максимальным. Такая схема подходит для любого типа кожи.
Так эффект увлажнения будет максимальным. Такая схема подходит для любого типа кожи.
Средства для очищения
Синденты с гиалуронатом натрия помогут удалить макияж, грязь и излишки кожного сала. Средство наносится на влажную кожу, затем смывается.
Лосьон с гиалуронатом натрия
Может использоваться как для лица, так и для тела.
Гель с гиалуронатом натрия
Гель нужно наносить на кожу до полного впитывания.
Крем для лица
Гиалуроновая кислота — «командный игрок», который лучше всего работает в сочетании с кремом.
Каковы побочные эффекты при использовании гиалуроновой кислоты
Гиалуроновая кислота, пожалуй, самый безобидный для кожи в плане побочных эффектов ингредиент. Поскольку гиалуроновая кислота это нормальная составляющая кожи, аллергическая реакция на нее очень редка.
Использование данной кислоты, в отличие от гликолевой, салициловой и других, направлено не на обновление эпидермиса, а на увлажнение и поддержания гидролипидной мантии кожи. Поэтому она не «обнажает» кожу и не провоцирует покраснение. Ее использование при местном применении не стимулирует процессы отшелушивания кожи.
Поэтому она не «обнажает» кожу и не провоцирует покраснение. Ее использование при местном применении не стимулирует процессы отшелушивания кожи.
Если после использования препарата с содержанием гиалуроновой кислоты возникли побочные эффекты, следует обратить внимание на состав средства — аллергия может возникнуть на другие ингредиенты. Такая реакция может стать результатом использования слишком высокой концентрации гиалуроновой кислоты. Поэтому, чтобы избежать раздражения или сухости, рекомендуется избегать концентрации гиалуроновой кислоты выше 2%.
Также целесообразно проводить предварительное «патч-тестирование» — нанести небольшое количество любого нового продукта на тыльную сторону запястья и оценить на побочные эффекты в течение 24 часов. При возникновении каких-либо побочных эффектов после использования гиалуроновой кислоты следует обратиться за консультацией к дерматологу.
При беременности или кормлении грудью использование наружных препаратов с содержанием гиалуроновой кислоты безопасно.
Какой должна быть гиалуроновая кислота
Польза гиалуроновой кислоты напрямую зависит от ее молекулярной массы и концентрации. Диаметр гиалуроновой кислоты также важен, поскольку он определяет способность ингредиента проникать в кожу.
Молекулярный вес измеряется в так называемых единицах атомной массы — дальтонах, или кДа. Гиалуроновая кислота весом от 50 до 1000 кДа наиболее полезна для кожи; оптимальным считается вес около 130 кДа. Превышение этого показателя не имеет качественного значения.
Почему именно вес 130 кДа оказывает максимальный эффект?
В одном исследовании ученые оценили влияние на кожу гиалуроновой кислоты с различными молекулярными массами, включая 50, 130, 300, 800 и 2000 кДа. Через месяц после начала применения наружных препаратов с разным весом кислоты специалисты обнаружили, что использование 130 кДа было наиболее эффективным — эластичность кожи повысилась на 20%. Как в группе 50 кДА, так и в группе 130 кДа через 60 дней наблюдалось значительное уменьшение глубины морщин и шероховатости кожи. Все остальные молекулярные массы также увеличивали эластичность и увлажненность кожи, но в меньшей степени.
Как в группе 50 кДА, так и в группе 130 кДа через 60 дней наблюдалось значительное уменьшение глубины морщин и шероховатости кожи. Все остальные молекулярные массы также увеличивали эластичность и увлажненность кожи, но в меньшей степени.
С какими компонентами удачно сочетается гиалуроновая кислота
Если вы ищете пару ингредиентов для оптимального ухода за кожей, выберите гиалуроновую кислоту и витамин С. Они дополняют друг друга и способствуют максимальному увлажнению, защите и восстановлению кожи.
Есть еще одна причина, по которой эти ингредиенты отлично сочетаются, — слишком высокая концентрация витамина С может вызвать раздражение, сухость кожи и даже появление прыщей, а гиалуроновая кислота не только успокаивает и восстанавливает кожу, помогая создать барьер влаги, но выступает прекрасным курьером, доставляющим витамин С к клеткам.
Другие медицинские преимущества гиалуроновой кислоты
Помимо отличного косметического эффекта в уходе за кожей, гиалуронат натрия имеет и другие медицинские показания для использования.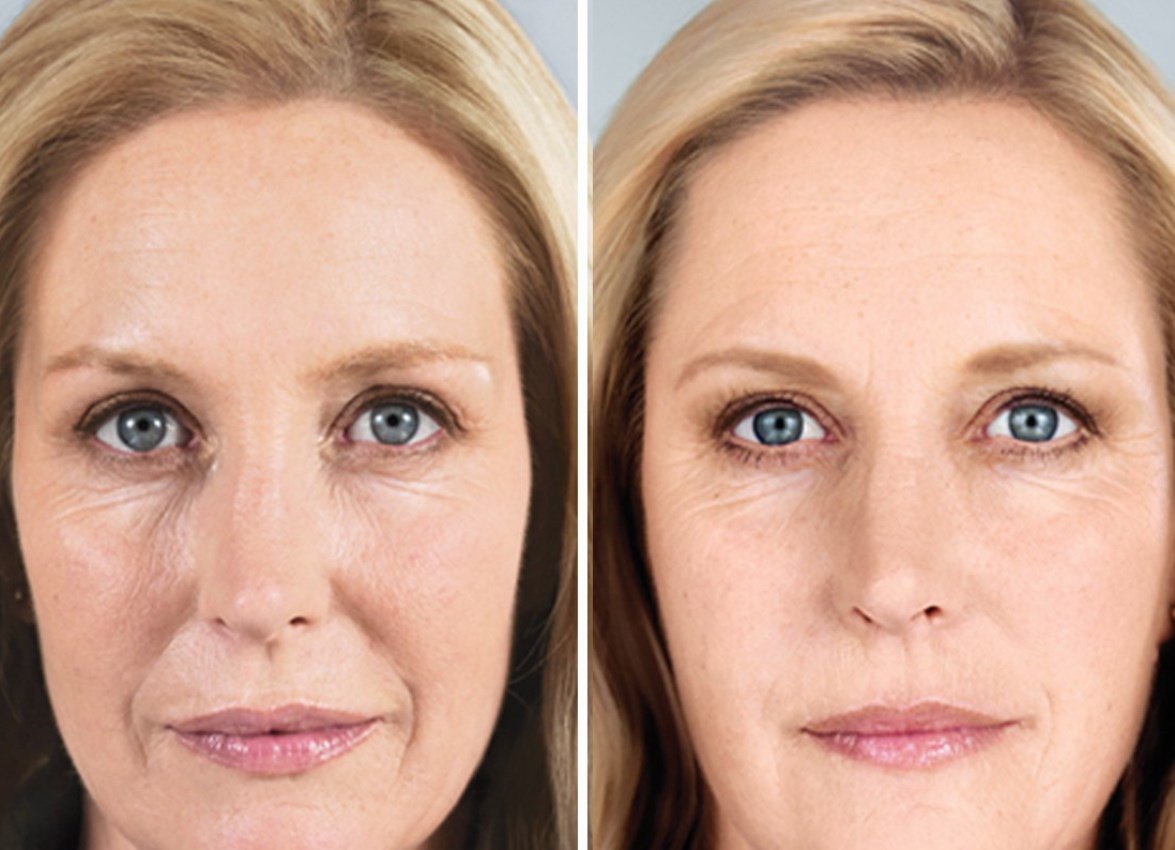
Остеоартрит коленного сустава
Гиалуроновая кислота содержится в суставной жидкости и хрящах. Однако при остеоартрите уровень гиалуроната натрия в суставах становится низким. Инъекция гиалуроната натрия может помочь при остеоартрите в колене. Лекарство вводится непосредственно в колено и способствует уменьшению боли в этой области.
Хирургия глаза
Капли с гиалуронатом натрия полезны в таких процедурах, как:
- хирургия трансплантации роговицы;
- коррекция глаукомы;
- вторичная имплантация интраокулярной линзы;
- хирургия катаракты.
Благодаря своему противовоспалительному и увлажняющему эффекту гиалуронат натрия уменьшает сухость глаз, которая может возникнуть после операции.
Назальный спрей с гиалуронатом натрия
Такое средство эффективно для увлажнения и регенерации слизистой полости носовых пазух.
Инъекции гиалуроновой кислоты
Инъекционные наполнители для морщин могут придать подтянутый вид коже более щадящим способом, чем традиционная подтяжка лица. Большинство наполнителей или филлеров заполняют впадины, линии и морщины менее чем за 30 минут и дают результат, который может длиться от 4 месяцев до года.
Большинство наполнителей или филлеров заполняют впадины, линии и морщины менее чем за 30 минут и дают результат, который может длиться от 4 месяцев до года.
Какой эффект оказывают инъекции
Область применения геля гиалуроновой кислоты широка:
- разглаживание морщин
- увеличение губ
- моделирование контуров лица
- интенсивное увлажнение кожи
Самой популярной категорией наполнителей для морщин является гиалуроновая кислота. Каждый тип препарата работает по-разному и дает различные результаты.
Наполнители морщин гиалуроновой кислотой включают в себя:
- Баланс Белотеро
- Juvederm Voluma XC
- Juvederm XC
- Juvederm Ultra XC
- Juvederm Volbella XC
- Juvederm Ultra
- Juvederm Ultra Plus
- Juvederm Vollure XC
- Превелльский шелк
- Рестилан
- Рестилайн-Л
- Рестилайн-Лайфт
- РестилайнШелк
- Рестилайн Рефайн
- Рестилан Дефайн
Побочные эффекты
Побочные эффекты таких инъекций редки, но могут включать:
- покраснение;
- отек;
- кровоподтеки в месте инъекции.

Наполнитель также может проявляться под кожей в виде крошечных бугорков, однако в течение дня это проходит.
При приеме препаратов, разжижающих кровь, например, аспирина, место инъекции будет кровоточить дольше, на нем также могут образоваться небольшие синяки.
Что стоит знать перед инъекцией с гиалуроновой кислотой
- Не стоит руководствоваться исключительно ценой процедуры.
- Если вам предлагают коррекцию морщин по значительно более низкой цене, вполне возможно, что мастерство или качество продукта оставляют желать лучшего.
- Процедура должна выполняться исключительно в медицинском центре.
- Процедуры должны проводиться исключительно в медицинских условиях вне зависимости от того, кто их проводит.
- Всегда спрашивайте название препарата.
- Перед инъекцией специалист должен озвучить название препарата и показать, как он вскрывает новую упаковку. Если специалист не предоставит эту информацию, от процедуры лучше отказаться.

Используйте солнцезащитный крем ежедневно. Это поможет продлить действие наполнителя и защитить от поствоспалительных изменений пигмента, которые могут возникнуть в месте инъекции.
Особые меры предосторожности при проведении инъекций гиалуроновой кислоты
Беременность
Данных, подтверждающих безопасность инъекций гиалуроновой кислоты во время беременности, нет.
Грудное вскармливание
Данных о безопасности инъекций с гиалуроновой кислотой, проводимых в период грудного вскармливания, и их влияния на ребенка, также пока нет.
Сопутствующие видимые заболевания кожи
Нанесение гиалуроновой кислоты может усугубить кожный процесс у людей со склеродермией. При этой патологии местное применение средств с гиалуроновой кислотой нецелесообразно.
Как проводится инъекция гиалуроновой кислотой
Гиалуроновая кислота вводится под кожу тонкой иглой в малых объемах. В зависимости от чувствительности к боли и места инъекции возможно предварительное нанесение обезболивающего крема или применение местной анестезии в виде обкалывания кожи анестетиком. При использовании наружного обезболивающего препарата анестезирующий эффект наступает через 2-3 минуты.
При использовании наружного обезболивающего препарата анестезирующий эффект наступает через 2-3 минуты.
В каких зонах лица используют инъекции с гиалуроновой кислотой
- глабеллярные линии в сочетании с ботулотоксином;
- носогубные линии и «линии марионетки»;
- мелкие морщинки вокруг рта и губ.
Нужно помнить, что поверхностные или очень глубокие морщины трудно поддаются лечению. В этих случаях врач может посоветовать комбинацию геля гиалуроновой кислоты с другим препаратом и последующим подбором ухода за кожей.
Сколько длится процедура введения гиалуроновой кислоты
Процедура занимает 15–60 минут. Но поскольку область губ намного меньше по сравнению с другими зонами инъекций, продолжительность работы с ней тоже меньше.
Как долго длится эффект лечения гиалуроновой кислотой
Продолжительность действия отличается от пациента к пациенту и зависит от многих факторов, в том числе от образа жизни, типа кожи, возраста и техники инъекций.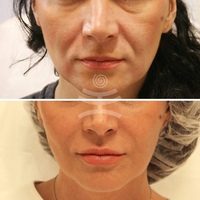 Например, после увеличения губ до следующего введения препарата должно пройти не менее шести месяцев.
Например, после увеличения губ до следующего введения препарата должно пройти не менее шести месяцев.
С какими процедурами по уходу за кожей можно сочетать гиалуроновую кислоту
Гиалуроновая кислота сочетается с большинством других ингредиентов, в том числе с пилингами, ретинолами, витаминами и другими кислотами. Единственное исключение — кислоты с низким уровнем рН, такие как гликолевая кислота, потому что она может угнетать действие гиалуроновой кислоты и значительно снизить ее эффективность.
Что делать после введения филлеров в домашних условиях
- Избегайте массирования или растирания обработанных участков в течение первых 48 часов после лечения.
- В течение первых восьми часов после процедуры не следует без необходимости прикасаться к обработанным участкам лица. Позже можно вымыть лицо с мылом и нанести легкий макияж.
- До тех пор пока первоначальное покраснение и отек кожи не уменьшатся, следует избегать экстремального нагревания кожи (солярий и солнечные ванны) и переохлаждения.

Можно ли удалить гиалуроновую кислоту после лечения
Нет. Если вы не довольны результатом, можно постепенно проводить лечение, пока нужный эффект не будет достигнут.
Что такое биоревитализация
Биоревитализация — это форма мезотерапии с использованием гиалуроновой кислоты с более высокой концентрацией. Ее не следует путать с наполнителем, который действует как пломбировочный материал для морщин и не обеспечивает кожу питательными веществами.
Биоревитализацию можно применять на шее, декольте, руках, кистях и участках вокруг колен.
Основная задача терапии — наполнение кожи гиалуроновой кислотой, которая стимулирует естественную выработку коллагена, гиалуроновой кислоты и осуществляет активный обмен веществ под кожей, что способствует ее омоложению.
Для этого в кожу вводят очищенную гиалуроновую кислоту неживотного происхождения. Это значит, что она синтезируется из бактериологических штаммов стрептококка, полностью органична для организма человека и не вызывает побочных реакций. Этот метод омоложения кожи считается более легким, чем другие косметические процедуры, но при этом не менее эффективным.
Этот метод омоложения кожи считается более легким, чем другие косметические процедуры, но при этом не менее эффективным.
Биоревитализация рекомендуется после 25–30 лет, когда количество нативной гиалуроновой кислоты начинает значительно снижаться, а кожа интенсивно теряет влагу. Это приводит к потере тонуса и эластичности, повышенной сухости и склонности к воспалениям. Результат виден уже после первой процедуры, но для идеального эффекта нужно пройти курс лечения.
Что такое мезотерапия
Мезотерапия — омоложение уставших тканей. Основная цель методики — обогатить кожу полезными веществами и питательными веществами. Благодаря инъекциям этот процесс проходит глубже и интенсивнее, чем в случае применения кремов и масок. В зависимости от задач коррекции врач подбирает готовое решение или составляет его индивидуально с учетом особенностей организма пациента.
Компонентами мезотерапии могут быть:
- гиалуроновая кислота;
- витаминно-минеральные комплексы;
- аминокислоты, антиоксиданты;
- пептиды;
- фитоэкстракты.

Процедура выполняется очень тонкими иглами. Мезотерапия обладает длительным эффектом после первого сеанса инъекции и позволяет решить целый комплекс проблем. Она направлена на улучшение общего состояния кожи, нормализацию микроциркуляции в клетках и межклеточном пространстве, повышение эластичности тканей и устранение различных эстетических дефектов. Молодость и свежесть кожи сохраняются до десяти месяцев и могут поддерживаться повторными инъекциями.
Что выбрать — мезотерапию или биоревитализацию
Однозначного ответа нет. Инъекции для биоревитализации содержат только гиалуроновую кислоту, которая необходима, прежде всего, для увлажнения и восстановления поврежденных тканей.
Мезотерапевтические коктейли — это целый комплекс биологически активных компонентов, которые оказывают комплексное воздействие на ткани и способны решать сразу несколько эстетических задач.
Мезотерапия также поможет там, где есть специфические проблемы, такие как:
- темные круги и мешки под глазами;
- целлюлит;
- выпадение волос;
- рубцы.

Мезотерапия включает в себя как поверхностное введение препаратов на глубину до 2 мм, так и глубокие проколы.
Таким образом, для пациентов 30 лет и старше оптимальна мезотерапия, которая особенно актуальна при решении косметических проблем, связанных с акне и рубцами, а биоревитализация станет лучшим вариантом для пациентов старше 25 лет.
Гиалуроновая кислота. Что это? Эффективность для кожи лица
…
Доверять или нет? Эффективно ли? Не опасно?
Гиалуроновая кислота — что это за вещество? Попробуем разобраться.
Что такое гиалуроновая кислота?
Мы попытаемся рассказать об этом популярном веществе простым языком.
Потому что в медицинской терминологии определение гиалуроновой кислоты мало кому даст понимание того, что же это за чудо-вещество: гиалуроновая кислота — это несульфированный гликозаминогликан, компонент межклеточного матрикса и органический полисахарид.
Ну а теперь простыми, не медицинскими терминами.
Гиалуронат, гиалуроновая кислота или же по-простому — гиалуронка (именно так чаще всего ее называют потребители), является органическим веществом, которое вырабатывается в большем или меньшем количестве практически во всех клетках жидкостей и тканей нашего организма. Большое количество гиалуроновой кислоты вырабатывается в молекулах тканей суставных хрящей, глазного яблока, головного мозга, сердечных клапанов, слюны и, конечно, кожи. Именно на кожу приходится больше половины всего гиалуроната, находящегося в теле человека.
Гиалуроновая кислота обеспечивает упругость и нормальное функционирование тканей за счет удерживания молекул воды и их связывания в межклеточном пространстве. В этом и состоит ее основная задача – поддержка водного баланса всех тканей организма. Это увлажнение клеток, сохранение их молодости и функциональности. Также гиалуронат способствует разрастанию клеток и их восстановлению.
Самая главная и удивительная особенность гиалуроновой кислоты заключается в способности одной молекулы вещества удержать влагу в тысячу раз больше собственной массы. Благодаря такому свойству клетки соединительных тканей защищены от обезвоживания.
Так, один грамм гиалуроната может притянуть до 6 литров воды, при этом удерживается только нужное количество воды, перенасыщение клетки невозможно – такова уникальная способность гиалуроната.
Именно поэтому гиалуроновая кислота стала столь востребована в бьюти-сфере.
Но если наш организм способен самостоятельно вырабатывать гиалуроновую кислоту, почему же она так популярна в использовании извне? Тому есть несколько причин.
· На один килограмм всего организма приходится около 0,2 грамма гиалуроната. При среднем весе 65 кг в теле человека содержится лишь 14 грамм гиалуроната (примерно одна чайная ложка вещества на весь организм), при этом третья часть (около 5 грамм) ежедневно расщепляется и синтезируется.
· Процесс расщепления гиалуроновой кислоты ускоряется под воздействием ультрафиолетовых лучей, в клетках кожи прекращается ее синтез, поэтому после длительного пребывания на солнце кожа становится сухой и обезвоженной, процессы старения ускоряются.
· После различных травм и операций в составе кожных покровов гиалуроновой кислоты становится значительно меньше, т.к. увеличивается ее расход на восстановление органов и пораженных тканей.
· На выработку гиалуроновой кислоты также влияет ряд различных внешних факторов. Количество выработанного вещества снижается по следующим причинам: вредные привычки, неправильное питание, стрессы, неблагоприятная экология, некачественная вода и другие отрицательные внешние факторы.
· Самая весомая, потому что самая неизбежная причина – это возраст. В достаточном количестве гиалуроновая кислота вырабатывается в возрасте до 25 лет. После 25 лет синтез гиалуроната замедляется, после 40 лет из-за его нехватки организм не может в достаточном количестве синтезировать коллаген, процесс старения становится необратимым. Соответственно, если гиалуроната в организме недостаточно, появляются первые признаки старения – сухость кожи, морщинки, тусклый цвет лица. Пополняя недостаток гиалуроновой кислоты, мы тем самым замедляем процессы старения.
После 25 лет синтез гиалуроната замедляется, после 40 лет из-за его нехватки организм не может в достаточном количестве синтезировать коллаген, процесс старения становится необратимым. Соответственно, если гиалуроната в организме недостаточно, появляются первые признаки старения – сухость кожи, морщинки, тусклый цвет лица. Пополняя недостаток гиалуроновой кислоты, мы тем самым замедляем процессы старения.
В этом и заключается секрет популярности гиалуроновой кислоты.
Способы восполнения недостатка гиалуроновой кислоты в организме.
С годами выработка гиалуроната в организме сокращается, начинается естественный процесс старения.
Что мы можем предпринять для восполнения количества гиалуроновой кислоты, тем самым замедляя процесс увядания кожи?
· Ведение здорового образа жизни (исключение вредных привычек, таких как курение и употребление алкоголя)
· Соблюдение питьевого режима (здоровому человеку рекомендовано употреблять в сутки 35 мл воды на 1 килограмм массы тела, то есть около 2 литров воды для женщин и 3 литров для мужчин)
· Правильное питание и добавление в рацион продуктов, содержащих гиалуроновую кислоту (мясные хрящи и бульоны, бананы, бобовые, соевые, крупы, а также картофель, свекла и другие крахмалосодержащие овощи)
· Уход за кожей (увлажнение косметическими средствами и защита от ультрафиолетовых лучей)
· Косметические процедуры (инъекционные методики)
Как получают гиалуроновую кислоту?
Гиалуроновую кислоту получают двумя способами: животное сырье и искусственный метод.
Первый способ добывания гиалуроната из рыбы, хрящей крупного рогатого скота и петушиных гребней остался в прошлом.
Более широко и повсеместно используется второй, искусственный метод — синтез гиалуроновой кислоты в лабораториях, с помощью которого получается препарат, абсолютно идентичный натуральному, но с высокой степенью очистки и без посторонних компонентов, вызывающих аллергические реакции.
Гиалуроновую кислоту применяют в медицине, косметологии, дерматологии:
— офтальмотология и глазная хирургия, производство контактных линз
— ортопедия: лечение суставов и костных заболеваний
— эстетическая медицина
— хирургия: лечение ран, трофических язв, ожогов
— пищевые добавки
— уход за кожей лица
— изменение и коррекция форм, заполнение, моделирование овала лица.
Гиалуроновая кислота востребована в косметологии благодаря потрясающему и видимому эффекту, который она оказывает на кожу лица.
Воздействие на кожу лица
Гиалуроновая кислота отличается потрясающим увлажняющим эффектом, который превосходит по эффективности любые другие увлажняющие косметические средства:
— притягивает молекулы воды и удерживает их
— препятствует испарению влаги путем образования защитной пленки
— защищает от неблагоприятных внешних факторов
— синтезирует эластан и коллаген
Можно сказать, что гиалуроновая кислота обладает омолаживающим и освежающим эффектом. Увлажненная кожа – здоровая кожа.
Воздействие на кожу лица:
— интенсивное увлажнение кожи
— улучшение цвета, сияние
— повышение упругости
— уменьшение шероховатости
— разглаживание мелких морщин
— замедление процессов старения
Достаточный уровень увлажненности позволяет процессу восстановления тканей работать в полном объеме.
Для кожи лица гиалуронат используется в двух целях: увлажнение и контурная пластика. Увлажняющий эффект достигается с помощью косметических средств, содержащих гиалуроновую кислоту. Контурная пластика – разглаживание морщин, коррекция и изменение объемов различных зон лица – подразумевает инъекции методики.
Применение гиалуроновой кислоты в косметике
С каждым годом популярность гиалуроновой кислоты растет, ее используют в составах всевозможных косметических средств — кремов, лосьонов, масок, сывороток, губных помад и других средств для ухода за кожей.
Существует заблуждение, что такой способ использования гиалуронки неэффективен, т.к. диаметр ее молекулы в разы больше расстояния между молекул кожи. Однако, исследования говорят об обратном. Гиалуроновая кислота, длительное время находящаяся на поверхности кожи, попадает и в верхние ее слои, и в дерму, отдавая необходимую влагу клеткам, тем самым увлажняя их и препятствуя преждевременному старению. К слову, для увлажнения верхних слоев кожи достаточно нахождения вещества на поверхности.
Для более глубокого проникновения в слои кожи в косметических средствах используется раздробленная молекула гиалуроната.
Но не стоит забывать при использовании средств, содержащих гиалуроновую кислоту, что в составе косметики гиалуронат отвечает только за увлажняющий эффект. Ощущение свежести на коже, отдохнувший вид лица, румянец, защита от внешних неблагоприятных факторов окружающей среды – такой результат подарит средство при ежедневном использовании. Добавьте сюда правильное питание, полноценный сон, прогулки на свежем воздухе – и результат не заставит себя ждать.
Для более глубокого увлажнения, для разглаживания морщин или изменения форм скул, губ и других частей лица применяются инъекции и различные аппаратные методики с использованием гиалуроновой кислоты.
Применение гиалуроновой кислоты в косметологии и дерматологии
Огромную популярность гиалуроновая кислота приобрела в косметологии, потому что ни одно косметическое средство не решит задачу насыщения кожи так, как это сделают косметические процедуры.
Для более эффективного и видимого результата в сравнении с использованием косметических средств применяются инъекции с гиалуронатом.
Поговорим более подробно о методе – инъекции гиалуроновой кислоты.
Инъекции гиалуроновой кислоты на сегодняшний день являются одним из самых безопасных и самых эффективных методов омоложения кожи. С их помощью стало возможным изменить и исправить, казалось бы, необратимые возрастные процессы, такие как глубокие и неглубокие морщины и складки, вялость кожи; стало возможным общее омоложение, моделирование и добавление недостающего объема отдельным частям лица, которые с возрастом меняются. Эффект от процедур заметен сразу – кожа приобретает ровный тон, становится эластичной и подтянутой, морщины разглаживаются.
Подобные инъекционные процедуры стали прекрасной альтернативой хирургическому вмешательству. Процедура занимает относительно немного времени, практически безболезненна и не требует времени на восстановление и реабилитацию. Уколы вводятся непосредственно в проблемное место, заполняя пустоты и исправляя недостатки кожи. Использование инъекций гиалуроновой кислоты возможно как для кожи лица, так и для других частей тела.
Помните, что для применения данных процедур необходима консультация с врачом-косметологом или дерматологом. Также не стоит забывать, что косметические процедуры с использованием гиалуроновой кислоты имеют длительный, но не пожизненный эффект! Действие гиалуроновой кислоты может сохраняться от 8 до 12 месяцев. Далее часть вещества выводится из организма, другая часть усваивается как естественный компонент.
Показания к применению гиалуроновой кислоты
Показания для назначения процедур с использованием гиалуроновой кислоты:
— глубокие и неглубокие морщины
— складки
— рубцы и растяжки
— пигментные пятна
— дряблость и сухость кожи
— несимметричный овал лица
— добавление объема, коррекция форм отдельных частей лица
— укрепление волосяных луковиц
Препараты с гиалуроновой кислотой назначают для увлажнения, лифтинга, общего улучшения состояния кожи, разглаживания морщин, коррекции форм и изменения объема отдельных частей лица (губы, скулы, щеки и др.). Также препараты применяются для заживления пораженных участков кожи.
Существует несколько видов инъекционных процедур с использованием разных типов гиалуроновой кислоты.
Виды гиалуроновой кислоты
Гиалуроновая кислота – это вещество, молекулы которого могут иметь разное строение. Именно от строения молекулы зависит то, какими свойствами обладает тот или иной вид гиалуроновой кислоты и как он влияет на клетки нашего организма.
· Гиалуроновая низкомолекулярная кислота
Низкомолекулярная гиалуроновая кислота обладает отличным противовоспалительным свойством и используется для лечения различных видов сыпи, угрей, некоторых кожных заболеваний, таких как псориаз. Также низкомолекулярную гиалуроновую кислоту используют в составах косметических кремов, т.к. она способна более глубоко проникать в слои эпидермиса (наружный слой кожи).
· Гиалуроновая среднемолекулярная кислота
Среднемолекулярная кислота стимулирует процесс деления клеток и запускает синтез собственной гиалуроновой кислоты. Чаще используется в медицине с целью лечения глазных болезней и артрита.
· Гиалуроновая высокомолекулярная кислота
Данная гиалуроновая кислота востребована в косметологии благодаря медленному расщеплению в тканях. Функция высокомолекулярной кислоты – удержание молекул воды. Такая кислота удерживает и поглощает воды больше других видов гиалуроновой кислоты. Используется в медицине, в косметологии и не используется в косметических средствах.
Врач-косметолог назначает ту или иную процедуру в зависимости от возраста, состояния кожи и потребностей пациента. Рассмотрим более подробно виды инъекционных процедур с использованием гиалуроновой кислоты, применяемых в косметологии.
Виды инъекционных процедур с использованием гиалуроновой кислоты
В современной косметологии существует множество процедур с использованием гиалуроновой кислоты, мы рассмотрим самые распространенные способы борьбы с нежелательными возрастными изменениями.
· Биоревитализация
Данная процедура подразумевает введение препарата с помощью серии уколов. За счет введения гиалуроновой кислоты в средние и глубокие слои эпидермиса и дермы, стимулируется работу фибропластов клеток кожи, которые отвечают за выработку коллагена и эластина, результат – глубокое увлажнение кожи и ее омоложение. Гиалуроновая кислота активизирует обновление клеток, все обменные процессы ускоряются.
Данная процедура, как правило, проводится на открытых участках кожи, подверженных ультрафиолетовому излучению – лицо, шея, зона декольте, руки. Хотя теоретически данная процедура подходит для любой части кожного покрова.
Биоревитализация проводится как для лечебных целей (работа с возрастными изменениями и пигментацией кожи), так и для профилактики (раннее старение, сухость кожи).
· Мезотерапия
С помощью мезотерапии препарат, в состав которого входит гиалуроновая кислота, совместно с аминокислотами, витаминами группы А, С, Е, Р вводится в более глубокие слои дермы (слой кожи, находящийся глубже верхнего слоя — эпидермиса). Процедура является высокоэффективной за счет более глубокого введения препарата в слои кожи, процесс омоложения запускается внутри. После введения препарат начинает взаимодействовать с молекулами воды, образуется гелеобразное вещество, которое заполняет морщинки и иные неровности кожи.
Процедуру мезотерапии назначают при наличии неглубоких шрамов и рубцов, растяжек, морщин, наличии сухости кожи и угревой сыпи. А также применяется для коррекции объемов тела.
Данный процедура используется как на открытых участках кожи (отдельные части лица, руки, шея, зона декольте), так и в области живота, бедер и ягодиц.
· Инъекционная контурная пластика
Один из самых популярных методов омоложения в косметологии, прекрасная альтернатива пластическим операциям. Один час процедуры, никаких разрезов, скальпелей и перевязок, результат – коррекция возрастных изменений, устранение недостатков кожи и восполнение утраченных объемов.
Возможности контурной пластики:
— разглаживание межбровных и носогубных складок
— улучшение овала лица
— коррекция мелких морщин, гусиные лапки (кисетных морщин)
— сглаживание носослезной борозды
— коррекция формы губ, носа и подбородка
— восполнение утраченных объемов губ
Это далеко не все возможности контурной пластики. Так, например, можно даже скрыть выступающие вены на руках и других частях тела.
В контурной пластике в качестве наполнителя используются филлеры. Не нужно путать дермальные филлеры и уколы ботокса. Это два разных препарата с разным механизмом воздействия.
Рассмотрим, что такое филлеры на основе гиалуроновой кислоты.
Что такое филлеры?
Филлеры – это инъекционные препараты – кожные наполнители, которые используются в контурной пластике и являются альтернативой пластической хирургии. Применяются для разглаживания морщин и увеличения объема различных частей лица. Филлеры с гиалуроновой кислотой представляют собой гель, который после введения длительное время не рассасывается, тем самым выполняет функцию наполнителя. Результат – эффект лифтинга, моделирование и увеличение объема.
Результат виден сразу после процедуры. Не стоит забывать, что действие любых филлеров не пожизненное. Так, эффект филлеров на основе гиалуроновой кислоты сохраняется от 6 до 18 месяцев.
Филлеры обладают такими свойствами, как эластичность и пластичность – они восстанавливают форму, при этом не растекаются и не смещаются при подвижности мышц и под воздействием внешних факторов.
В зависимости от задач, которые нужно решить, подбираются филлеры разной степени вязкости.
Для заполнения мелких морщин используются филлеры с низкой степенью вязкости – мягкий гель. Для глубоких складок и для добавления объема формам (губы, скулы и пр.) используют филлеры с высокой степенью вязкости.
Чаще всего филлеры с гиалуроновой кислотой применяют в следующих целях:
— коррекция овала лица
— коррекция линии скул
— разглаживание носогубных складок
— увеличение объема губ
— разглаживание морщин
— разглаживание складок
Одно из преимуществ филлеров на основе гиалуроновой кислоты – это возможность все вернуть обратно с помощью фермента, который способен расщеплять введенный гиалуронат.
После проведения процедур с инъекциями гиалуроновой кислоты следует выполнять следующие рекомендации:
— не использовать декоративные косметические средства 2-3 дня (пудра, тональный крем, румяна и пр.)
— использовать средства, назначенные лечащим врачом
— воздержаться от посещения бани и сауны в течение 7-10 дней
— воздержаться от спортивных нагрузок
— избегать пребывания на солнце в течение 14 дней
Противопоказания
Не смотря на всю безопасность и эффективность препарата, не стоит забывать о противопоказаниях к применению гиалуроновой кислоты. Так, не рекомендуется вводить инъекции гиалуроната в следующих случаях:
— беременность и грудное вскармливание
— аутоимунные заболевания
— онкологические заболевания
— сахарный диабет
— инфекционные заболевания
— острая форма герпеса
— плохая свертываемость крови
— гиперчувствительность кожи
— индивидуальная непереносимость препарата
Также не рекомендуется процедура после лазерных и химических пилингов и при наличии воспалений на коже в той области, где необходимо введение инъекции.
Помните, что перед проведением инъекционных процедур требуется консультация специалиста.
Может ли гиалуроновая кислота нанести вред?
Любые вмешательства извне, любые манипуляции, особенно в отношении нашего лица, вызывают у многих опасения и сомнения. Давайте разберемся, может ли гиалуроновая кислота нанести вред коже и организму в целом.
При безинъекционном методе возможно проявление аллергической реакции.
Если используется косметическое средство, обязательно нужно ознакомиться с составом.
Что касается инъекционного метода, то основной риск заключается в том, что при столь широкой популярности гиалуроновой кислоты стало появляться немало подделок. Поэтому будьте предельно внимательны – проверяйте наличие сертификата продукта, а также настаивайте на том, чтобы препарат вскрывался при вас. Стоит ли говорить о том, что лучше за подобными процедурами обращаться к профессионалам и избегать посещений непроверенных сомнительных специалистов?
Возможные незначительные осложнения после инъекционных процедур:
· Болезненные ощущения в месте инъекций
В данном случае используются обезболивающие препараты (гели, мази и др.).
· Покраснения и припухлости
Проходят в течение быстрого времени – от нескольких часов до двух-трех дней.
· Синяки
Перед назначением любых инъекционных процедур опытный косметолог обязательно проведет предварительный осмотр и выявит предрасположенность к появлению отеков и синяков, если таковая имеется. В данном случае назначается прием препаратов, укрепляющих сосуды.
Незначительные видимые следы на коже от проведённой процедуры проходят быстро и практически безболезненно. Посещайте проверенных специалистов, надежные клиники, выполняйте рекомендации и назначения врача после процедуры, и результат не заставит себя ждать!
Статья проверена: заместителем генерального директора клиники «Наноэстетик», кандидатом медицинских наук, врачом косметологом, трихологом, Махневой Еленой Андреевной.
Косметологи клиники «Наноэстетик» имеют 10 летний опыт увлажнения и омоложения кожи при помощи инъекций гиалуроновой кислоты. Примеры наших работ здесь.
Записаться на прием к специалисту вы можете на сайте или по телефону (3452) 65-94-32.
Инъекции гиалуроновой кислоты
Биоревитализация. «Уколы красоты»
Интенсивное увлажнение и эффективное омоложение кожи лица, рук, шеи и области декольте инъекциями гиалуроновой кислоты. Создание в коже мощного регенерационного слоя, активно восполняющего водно-солевой баланс и устраняющего мелкие морщинки. Подробнее
Контурная пластика лица
Нехирургический метод борьбы со следами старения на коже, имеющий минимум противопоказаний и максимум эффективности. В основе методики — гиалуроновая кислота для лица и тела — естественный компонент кожи человека. Подробнее
Процедура имеет противопоказания. Косметолог клиники проконсультирует Вас!
Клиника эстетической косметологии Versailles имеет честь представить:
инъекции гиалуроновой кислоты
«Уколы красоты» (именно такое название получили инъекции гиалуроновой кислоты) — ультрасовременная методика, решающая проблемы с кожей комплексно. Это и легкая подтяжка контуров лица, и устранение возрастных и мимических морщин (в т.ч. носослезной борозды и носогубных впадин), и увеличение объема губ, и коррекция формы носа, и мощное увлажнение кожи, и даже подтяжка ягодиц. При всей универсальности и результативности уколы гиалуроновой кислоты исключают необходимость хирургического вмешательства, и оказывают исключительно положительный эффект.
Оцените возможности!
- Лифтинг-эффект достигается уже после одной процедуры, которой зачастую оказывается достаточно, и сохраняется до 1,5 лет.
- Восполнение недостатка влаги естественным компонентом, содержащимся в коже человека и не вызывающем аллергических или отторгающих реакций у него.
- Уколы красоты гиалуроновой кислотой активизируют процессы регенерации кожного покрова, значительно замедляя процесс старения.
- Омоложение без реабилитации!
- Полное заживление мест проколов уже через неделю после процедуры.
- Экономия и безопасность по сравнению с пластической хирургией.
- Эффект от уколов гиалуроновой кислоты виден сразу после процедуры.
- «Уколы красоты» не только устраняют имеющиеся морщины, но и эффективно предотвращают появление новых.
Уколы красоты гиалуроновой кислотой
Почему наша кожа с возрастом теряет былую упругость и бархатистый вид? Причина ее «увядания» кроется в недостатке влаги, уровень которой в подкожном слое контролирует гиалуроновая кислота. Инъекции гиалуроновой кислоты восстанавливают необходимый РН кожи, устраняя при этом возрастные и мимические морщины, возвращая коже упругость и здоровый румянец.
Гиалуроновая кислота в косметологии
По своему назначению гиалуроновая кислота напоминает губку — в кратчайшие сроки она притягивает и «впитывает» в себя молекулы воды, заполняющие имеющиеся пустоты в подкожном слое (именно из-за них появляются морщины), и активизирует выработку коллагена и эластана — основных компонентов подкожного каркаса.
Действие гиалуроновой кислоты начинается непосредственно после процедуры уколов и продолжается до 1,5 лет. Затем кислота полностью растворяется в организме, распадаясь на безвредные для него вещества. Для достижения нового эффекта стоит повторить инъекции гиалуроновой кислотой.
Важные рекомендации:
- В течение 10 дней после процедуры инъекций гиалуроновой кислоты стоит отказаться от посещения солярия, пляжей, саун и бань.
- Вероятность возникновения гематом в местах проколов у курящих людей гораздо выше, чем у некурящих, поэтому следует заранее предупредить косметолога о своих пристрастиях.
- В косметологии гиалуроновая кислота применяется и для клиентов моложе 25 лет, т.к. имеет свойство останавливать процесс старения кожи даже на самых ранних стадиях.
- Перед процедурой откажитесь от приема любых препаратов, влияющих на свертываемость крови.
Противопоказания:
- беременность и лактация;
- аутоиммунные заболевания;
- склонность к появлению келоидных рубцов;
- любые тяжелые заболевания;
- нарушение кожных покровов;
- болезни крови, связанные с нарушением свертываемости.
Инъекции гиалуроновой кислоты. Цены
Цены на биоревитализацию
| Биоревитализация: Эвгулон | 9 900 ₽ |
| Биоревитализация: Белотеро Софт 1 мл | 12 500 ₽ |
| Биоревитализация: Teosyal Redensity 1,0 мл. | 15 000 ₽ |
| Биоревитализация: Teosyal Redensity II 1,0 мл. | 17 900 ₽ |
| Биоревитализация: IAL-System 1.1 мл. | 9 000 ₽ |
| Биоревитализация: IAL-System ACP 1,1 мл. | 11 600 ₽ |
| Биоревитализация: Juvederm hydrate 1,0 мл. | 13 300 ₽ |
| Биоревитализация: Jalupro 3,0 мл. | 8 900 ₽ |
| Биоревитализация: Jalupro 6,0 мл. | 18 890 ₽ |
| Биоревитализация: MesoEye C71 1 мл. | 17 000 ₽ |
| Биоревитализация: MesoSculpt C71 1 мл. | 18 000 ₽ |
| Биоревитализация: Meso-Xanthin F199 1,5 мл. | 18 500 ₽ |
| Биоревитализация: Meso-Whartonp199 1,5 мл. | 18 500 ₽ |
| Биоревитализация: TeosyalMeso-Expert 3,0 мл. | 19 000 ₽ |
| Биоревитализация: Filorga NCTF 135 HA+ 3,0 мл. | 8 890 ₽ |
| Биоревитализация: Filorga М-НА 18 1,0 мл. | 11 800 ₽ |
| Биоревитализация: Yvoire Gydro 1,0 мл. | 11 900 ₽ |
| Биоревитализация: Restylane Vital 1,0 мл. | 17 900 ₽ |
| Инъекция препаратом 2% гиалуроновой кислоты 2,5 мл (Германия) | 12 000 ₽ |
Цены на контурную пластику
| Деградация филлера гиалуронидазой | 3000 ₽ |
| Контурная пластика — работа канюлей | 2700 ₽ |
| Контурная пластика интимных зон | 4500 ₽ |
| Инъекции препаратом Yvoire Volume 1,0 мл | 18900 ₽ |
| Инъекции препаратом Yvoire Classic 1,0 мл | 17000 ₽ |
| Инъекции препаратом Juvederm ultra Смайл 0,55 мл | 14000 ₽ |
| Инъекции препаратом Juvederm ultra 3-1,0 мл | 18500 ₽ |
| Инъекции препаратом Juvederm Voibella 1,0 мл | 19700 ₽ |
| Инъекции препаратом Juvederm Volift 1,0 мл | 19700 ₽ |
| Juvederm voluma 1,0 мл. | 21000 ₽ |
Что такое гиалуроновая кислота и почему все ею одержимы — Wonderzine
Существует несколько видов филлеров: коллагеновые, гидроксиапатитовые, жировые и гиалуроновые. В последнее время всё чаще используются именно гиалуроновые. Считается, что они наиболее приближены к «идеальному» филлеру, который, по мнению учёных, должен сочетать в себе лёгкое введение, иметь стабильный продолжительный эффект, быть безболезненным, не провоцировать аллергию и кожные заболевания, не двигаться с места введения и быть доступен как специалистам, так и пациентам. Так как гиалуроновая кислота — это родственный коже компонент, то он является и наиболее безопасным по сравнению с другими видами филлеров, причём как при нахождении в коже, так и после того, как распадается.
Ещё одно преимущество гиалуроновых филлеров заключается в том, что для них существует антидот — гиалуронидаза. Это фермент, который расщепляет полисахариды. В случае если результат от процедуры не такой, как планировалось, и было введено слишком много препарата, гиалуронидаза вернёт всё на место, но эффект от инъекции пропадёт полностью, и придётся начинать всё сначала. Аллергические реакции на гиалуроновые филлеры случаются независимо от компетентности врача и могут проявиться как сразу, так и в течение нескольких недель. Также на месте ввода препарата могут появиться синяки, отёки и покраснения, которые со временем проходят. Главный недостаток инъекций гиалуроновой кислоты заключается в том, что эффект от них держится недолго — в среднем около полугода, после чего процедуру нужно повторять. При высокой стоимости препаратов и процедур этот вид контурной пластики могут позволить себе далеко не все.
В любом случае под рукой всегда остаются куда более бюджетные и доступные средства для домашнего ухода с гиалуроновой кислотой. Однако если эффективность гиалуронки в увлажнении кожи любого типа доказана, то её антивозрастные и лечебные свойства учёным ещё предстоит изучить. Использовать косметику с гиалуроновой кислотой или нет — вопрос личного выбора. Как и любой другой компонент, она подходит не всем. Понять, какой эффект произведёт гиалуроновая кислота на конкретного человека, можно только опытным путём, и лучше всего под присмотром проверенного косметолога. Но уже понятно, что это ингредиент, на который стоит обратить внимание.
Фотографии: Arsha— stock.adobe.com, Olexandr — stock.adobe.com, rimglow — stock.adobe.com, fotos-v— stock.adobe.com
Гиалуроновая кислота: действие, мифы, крем
Гиалуроновая кислота, пожалуй, главный косметический ингредиент. Чудо-компонент увлажняет и разглаживает мелкие морщинки, благодаря чему его можно найти практически в любой косметике — начиная от патчей для глаз и заканчивая кремом для рук. Рассказываем, что нужно знать о гиалуроновой кислоте, какие мифы о ней существуют и — самое интересное — в каких средствах искать главную косметическую помощницу.
Что такое гиалуроновая кислота
Гиалуроновая кислота изначально есть в каждом: если быть точнее, то в вашем теле ее примерно 10–15 граммов. Кислота — основной компонент биологической смазки, она входит в состав суставного хряща, а в коже участвует в процессе регенерации тканей.
Откуда берется гиалуроновая кислота
Сразу задаетесь вопросом, откуда тогда ее добывают? Изначально, когда этот компонент только обнаружили в 1934 году, его синтезировали из стекловидного тела глаза крупного рогатого скота. Позже в ход пошли петушиные гребешки. Теперь же чаще используются более гуманные способы — ее добывают из пшеницы с помощью микробной ферментации.
Как работает гиалуроновая кислота
Если говорить просто, то главное свойство гиалуроновой кислоты — эффективно удерживать воду. Как мы уже сказали, кислота и так изначально есть в организме, но с возрастом ее выработка уменьшается — это влияет на здоровье глаз, суставов и кожи.
Как еще используется гиалуроновая кислота
Встречается гиалуроновая кислота далеко не только в косметических составах. В первую очередь ее применяли даже не в целях улучшить состояние кожи. Она используется в медицине для лечения суставов и глаз, а также без нее не обходятся пластические хирурги и косметологи.
Как гиалуроновая кислота отличается от других кислот
В отличие от других, гиалуроновая не обладает привычными функциями кислот. Это значит, что она не отшелушивает кожу и не имеет растворяющих свойств.
Какие мифы есть о гиалуроновой кислоте
Возможно, вы слышали, что косметика с гиалуроном не работает — якобы ее молекулы слишком большие, чтобы проникать глубоко в кожу. Но фишка в том, что гиалуроновой кислоте и не нужно туда попадать — ее главная работа состоит в удержании влаги, и эту задачу компонент выполняет на поверхности.
Косметика с гиалуроновой кислотой: что использовать
Косметика с гиалуроновой кислотой есть в любом ценовом сегменте, так что найти ее не составит труда. В составе ищите следующие наименования: hyaluronic acid, sodium hyaluronate, potassium hyaluronate, L-sodium hyaluronate, disodium acetyl glucosamine phosphate, sodium hyaluronic acid, sodium acetyl hyaluronate, hydrolyzed hyaluronic acid, hyaluronan. В основном они отличаются по размеру молекул. Особый шик, когда в составе есть несколько вариантов. Ниже — список средств, которые стоит попробовать.
На сайте могут фигурировать ссылки на внешние ресурсы, которые мы не администрируем и не контролируем. Политика конфиденциальности, практикуемая другими сайтами, не находится в сфере нашего влияния. Как только вы осуществляете переход на другие ресурсы, вы должны найти информацию об их политике конфиденциальности, прежде чем вводить на них свои данные.
что такое, польза и вред для кожи, применение в косметологии
Подробный гид, посвященный главному бьюти-ингредиенту современности
Чем хороша гиалуроновая кислота, как она работает и в каких случаях наиболее эффективна в уходе за лицом? Отвечаем на самые популярные вопросы.
Что такое гиалуроновая кислота?
Гиалуроновая кислота — это полисахарид, который синтезируется в организме человека. Она представляет собой прозрачное липкое вещество и содержится преимущественно в соединительной ткани. Слово «кислота» в названии немного пугает, но гиалуронка действует совсем не так, как кислоты, которые первыми приходят на ум. По сути, она выступает в роли магнита: быстро притягивает влагу и, что еще важнее, отлично удерживает ее в клетках.
© Getty Images
Впечатляющий факт: один грамм гиалуроновой кислоты способен удержать до шести (!) литров воды.
На этикетке гиалуроновая кислота может скрываться под одним из следующих названий:
Вернуться к оглавлению
Польза гиалуроновой кислоты для кожи лица
Эффект от воздействия гиалуроновой кислоты на кожу лица всесторонний — и достаточно явный:
-
увлажняет кожу, устраняет сухость и шелушение,
-
повышает эластичность кожи,
-
разглаживает мимические морщины, носогубные складки,
-
смягчает,
-
нивелирует возрастные изменения кожи.
Кроме того, она эффективно заживляет раны, способствуя регенерации кожи.
© Getty Images
Количество гиалуроновой кислоты в организме уменьшается с возрастом (это же происходит, например, с коллагеном и эластином). Факторы, которые ускоряют этот неприятный процесс, — воздействие солнечных лучей, табачного дыма, загрязненного воздуха. Но даже если максимально оградить свой организм от негативного влияния окружающей среды, процесс естественной выработки все равно однажды начнет замедляться. В результате водный баланс в тканях нарушается, кожа и волосы выглядят тусклыми и обезвоженными, организм быстрее стареет.
«Пополнять» запасы извне можно разными способами. Кто-то отдает предпочтение инъекциям (их еще называют «уколами красоты») и пищевым добавкам, другие ограничиваются косметикой с гиалуроновой кислотой в составе.
© Getty Images
Вернуться к оглавлению
Виды гиалуроновой кислоты
Она может иметь разный молекулярный вес — и, как следствие, по-разному воздействовать на кожу.
Высокомолекулярная
Молекулы гиалуроновой кислоты большего размера притягивают больший объем воды и дольше ее удерживают. Габариты не позволяют этим молекулам «просачиваться» в кожу, значительная часть остается на поверхности, образуя особого рода пленку. Она препятствует испарению влаги, что сохраняет уровень увлажненности кожи на высоте. Высокомолекулярную гиалуронку также используют при проведении инъекционных процедур.
Низкомолекулярная
Низкомолекулярная гиалуроновая кислота не остается на поверхности, она может проникать в эпидермис и там работать, стимулируя синтез гиалуроновой кислоты в организме, а также коллагена и эластина. Такой подход хорош и для моментального эффекта, и для долгосрочной перспективы.
© Getty Images
Как понять, какой вид гиалуроновой кислоты был использован при создании конкретного бьюти-средства? По составу это определить невозможно, поэтому придется довериться описанию. Обратите внимание, что именно обещает производитель в рекламе: моментальное увлажнение или накопительный эффект anti-age?
Вернуться к оглавлению
Гиалуроновая кислота в составе средств ухода за кожей
Ее используют и в базовом уходе, и в средствах, предназначенных для решения более специфических проблем.
Крем с гиалуроновой кислотой
-
Крем для лица
Гиалуроновая кислота встречается сегодня в составе чуть ли не каждого второго крема для лица. Так что при выборе обращайте внимание не столько на этот компонент, сколько на другие особенности крема: для какого типа кожи и времени суток предназначен, какой эффект обещает. Например, у L’Oréal Paris есть целая линейка «Гиалурон Эксперт», включающая дневной и ночной кремы, а также средство для области вокруг глаз, — ударная доза увлажнения обеспечена.
© L’Oréal Paris
-
Крем для кожи вокруг глаз
Кожа вокруг глаз более тонкая и нежная, а значит, нуждается в специфическом уходе. Присмотритесь к Hydraphase Intense Yeux от La Roche-Posay: легкая кремово-гелевая текстура — самое то для области глаз. Низкомолекулярная гиалуроновая кислота в паре с глицерином отвечает за интенсивное увлажнение, а кофеин помогает справиться с отечностью.
© La Roche-Posay
-
Крем для рук
Крем для рук или тела с гиалуроном — относительно редкое явление. Но если встретите, покупайте не раздумывая: гиалуроновая кислота хороша в любом виде.
Сыворотка для лица
Использование сыворотки с гиалуронкой повышает эффективность крема, но ее вполне можно применять и соло. Например, Vital Skin-Strengthening Super Serum от Kiehl’s справляется с задачей укрепления защитных свойств кожи самостоятельно. Сыворотка содержит фрагментированную гиалуроновую кислоту, которая проникает в самые глубокие слои эпидермиса. Упругость и эластичность кожи повышаются уже через 4 недели, что подтвердил клинический тест.
© Kiehl’s
Патчи с гиалуроновой кислотой
Спасут после тяжелого перелета и помогут коже восстановиться после бурной вечеринки. Советуем присмотреться к тканевым патчам для глаз «Увлажнение + сияние молодости» от Garnier на основе формулы с зеленым чаем и гиалуроновой кислотой. Они интенсивно увлажняют, придают сияние, разглаживают мелкие морщинки — и все это за каких-то 15 минут.
© Garnier
Маски
Если лицо нужно взбодрить в экспресс-режиме, маска с гиалуроновой кислотой — один из лучших видов SOS-средств. Обратите внимание на LiftActiv Hyalu Mask от Vichy: она содержит сразу два вида — низкомолекулярную и высокомолекулярную, а значит, решает задачи на разных уровнях. Формула дополнена экстрактом дрожжей агавы, который активизирует выработку собственной гиалуроновой кислоты.
© Vichy
Поклонникам тканевых масок тоже есть из чего выбрать: например, Garnier выпустили для лица целую линейку масок с гиалуроновой кислотой. Ночные и универсальные, против черных точек и антистресс — каждый найдет оптимальное решение для своей кожи.
© Garnier
Гели
В очищающих средствах для лица гиалуроновая кислота тоже показывает себя с лучшей стороны. Однако значение имеет и хорошее соседство: так, «Гиалуроновый Алоэ гель-пенка» от Garnier содержит 96% натуральных ингредиентов и подходит даже веганам.
© Garnier
Вернуться к оглавлению
Гиалуроновая кислота в составе декоративной косметики
Встретить гиалуроновую кислоту в списке ингредиентов увлажняющего крема или сыворотки для лица совсем не удивительно. Но если внимательно присмотреться к составу тонального крема, помады или блеска для губ, знакомое название можно увидеть и там.
Тональный крем
Легендарная линейка тональных средств Alliance Perfect «Совершенное слияние» в прошлом году пережила реновацию — теперь в составе формул есть гиалуроновая кислота. А это обещает ряд дополнительных преимуществ: более легкое распределение, идеальное слияние с кожей и увлажнение на срок до 24 часов.
© L’Oréal Paris
Праймер
Гелевый праймер Honey Dew Me Up от NYX Professional Makeup может при необходимости заменить даже средство ухода за кожей, ведь в его составе есть целая россыпь ценных компонентов. Гиалуроновая кислота, натуральный мед, пантенол, коллаген — рекомендуем!
© NYX Professional Makeup
Помада
Благодаря гиалурону в составе помады-бальзама NYX Professional Makeup Filler Instinct кожа губ остается увлажненной до 8 часов. А дополняющий его экстракт имбиря обеспечивает вау-эффект: губы визуально становятся более пухлыми.
© NYX Professional Makeup
Блеск для губ
Линейка блесков для губ Infaillible от L’Oréal Paris известна в первую очередь благодаря разнообразию текстур и оттенков. Но мало кто знает, что состав средства также достоин пристального внимания: он обогащен гиалуроновой кислотой, витаминами и антиоксидантами.
© L’Oréal Paris
Сыворотка для ресниц
Гиалуроновая кислота хороша не только для кожи, но также для волос и ресниц. Прекрасно, если она есть в составе туши или средства по уходу за ресницами. Например, сыворотка Lash Builder от Shu Uemura может похвастаться наличием гиалуронки в составе, а также других ценных компонентов: лимонной кислоты, аргинина, масла ши и пантенола. Комплекс отлично ухаживает за ресницами и укрепляет их — лучшее решение для тех, кто пользуется тушью каждый день.
© Shu Uemura
Вернуться к оглавлению
Как правильно пользоваться косметикой для лица с гиалуроновой кислотой?
Гиалуронка хороша тем, что не требует особого внимания. Разумеется, делать инъекции гиалуроновой кислоты в домашних условиях нельзя, а вот средства ухода очень просто использовать самостоятельно: просто нанесите крем или сыворотку на слегка увлажненную кожу и дождитесь полного впитывания. Важно, что гиалуроновая кислота сочетается с большинством других ингредиентов, в том числе с кислотами, витаминами и маслами, а это значит, что косметика с этим ингредиентом не будет вступать в конфликт с другими средствами.
Вернуться к оглавлению
Самые распространенные вопросы о гиалуроновой кислоте
Отвечаем на пять самых популярных вопросов.
Безопасно ли использование гиалуроновой кислоты для лица?
Гиалуроновая кислота безопасна в использовании. Поскольку организм вырабатывает ее естественным образом, аллергические реакции возникают очень редко. После инъекции на коже могут появиться покраснения или небольшие синяки, но чаще всего это реакция на уколы, а не на компонент.
Существуют ли противопоказания?
Базовое противопоказание — повышенная чувствительность к гиалуроновой кислоте или любому из компонентов препарата, в составе которого есть гиалуронка. Если речь идет об инъекции, у этой процедуры есть отдельный перечень противопоказаний — нужно обязательно проконсультироваться с врачом.
© Getty Images
Как получают гиалуроновую кислоту?
В организме она синтезируется фибробластами; искусственно — добывают из растительного сырья, например пшеницы.
Чем заменить гиалуроновую кислоту в домашних условиях?
Существует целый ряд других влагоудерживающих средств, в том числе, например, глицерин и мочевина.
С какого возраста можно применять средства для лица с гиалуроновой кислотой?
Средства для лица с гиалуроновой кислотой можно использовать в любом возрасте, по показаниям. А вот с инъекциями лучше подождать хотя бы до 25 лет.
Вернуться к оглавлению
Расскажите о ваших любимых средствах с гиалуроновой кислотой в комментариях!
Гиалуроновая кислота — свойства, формы и польза
Не самое простое название ингредиента – «гиалуроновая кислота» – сейчас известно практически любому человеку, хоть немного интересующемуся темой косметологии. Гиалуроновую кислоту (ГК) пьют, вводят с помощью инъекций, наносят на кожу, надеясь навечно сохранить молодость.
Гиалуроновая кислота, если говорить о ней с позиций химии, представляет собой полисахарид гликозаминогликан, который можно называть также гиалуронаном или гиалуронатом (но никак не гиалуронкой!). Это полимер, состоящий из молекул D-глюкуроновой кислоты и D-N-ацетилглюкозамина, соединенных между собой.
Размер молекулы гиалуроновой кислоты – величина непостоянная. В разных тканях человеческого организма цепочки полисахарида могут быть неодинаковой длины, включать в себя до 25 000 фрагментов названных выше соединений и иметь размер от 5000 до 20 млн ДА.
Гиалуроновую кислоту обнаруживают в тканях нервной системы, соединительной и эпителиальной ткани. Но она же играет большую роль в миграции злокачественных опухолей и распространении стрептококковой инфекции. Таким образом, недостаток или избыток гиалуронана может быть как полезен, так и вреден.
Популярность препаратов на основе гиалуроновой кислоты в косметологии привела к тому, что многие специалисты ошибочно полагают, что ГК – фактическая основа дермы, и довольно наивно думают, будто любое введение гиалуроновой кислоты даст эффект «восстановления» дермы. Эти заблуждения привели к появлению разнообразных коммерческих терминов, не имеющих научного обоснования, типа «ревитализация» или «редермализация». На самом же деле гиалуроновой кислоты в организме не так много: в теле женщины, весящей около 70 кг, содержится приблизительно 15 г чистой гиалуроновой кислоты, треть которой ежедневно разрушается и обновляется. Фактически полное обновление всего объема гиалуроновой кислоты у здорового человека среднего возраста занимает около трех-четырех суток.
Синтез гиалуроновой кислоты может ускоряться и замедляться, количество его может уменьшаться и возрастать, что далеко не всегда связано с возрастными процессами. Мы привыкли считать, будто количество гиалуроновой кислоты – маркер старения кожи, именно из этого принято исходить при назначении препаратов гиалуроновой кислоты с косметической целью. На самом же деле все обстоит немного иначе. Самый важный фактор, ускоряющий синтез гиалуроновой кислоты в тканях, – воспаление, в том числе воспаление как результат повреждения или травмы.
Интересно, что гиалуроновая кислота может как усиливать и продлевать воспалительную реакцию, так и ускорять процесс заживления. В коже гиалуронат активно участвует в процессах, связанных с ранозаживлением: он задействован в гемостазе, реакциях воспаления, а также в реэпителизации и ремоделировании дермы. Очень важной особенностью ГК является ее способность защищать клетки от свободно-радикального повреждения.
В коже гиалуронан в высокой концентрации обнаруживается не только в дерме, но в первую очередь в эпидермисе, где он играет ключевую роль в обновлении кожи. При уменьшении количества гиалуроновой кислоты в эпидермисе наблюдается активация локальных воспалительных реакций, ухудшение защитных свойств кожи, нарушение процессов заживления, уменьшение способности к удержанию влаги кожей и снижение эластичности. Внешне это выглядит как резкое повышение чувствительности кожи, появление сухости, очагов шелушения и раздражения, а в дальнейшем и присоединение мелких морщинок и заметное ухудшение тонуса кожи.
Что же приводит к уменьшению количества гиалуроновой кислоты в коже?
Вопреки существующему мнению, отнюдь не возрастные изменения являются основной причиной. Важнейший фактор – повреждение в первую очередь ультрафиолетовыми лучами типа B. Ультрафиолетовое облучение приводит к снижению синтеза гиалуроновой кислоты и одновременно активизирует ее разрушение. Фрагменты ГК сами по себе вызывают воспаление и формирование гранулем. Такого рода физиологические реакции развиваются и после введения филлеров на основе гиалуроновой кислоты, что трактуется как осложнение инъекции. Предсказать подобные реакции очень трудно, и следовательно, почти невозможно их предупредить. Единственное, что можно сделать, чтобы избежать гранулем в данном случае, – отказаться от использования филлеров, как в старом анекдоте об идеальном методе контрацепции: «чай не до и не после, а вместо».
Итак, на что же мы можем рассчитывать, когда наносим ГК на кожу?
Прежде всего важен эффект поверхностного увлажнения рогового слоя. Эта кислота относится к классу хумектантов – увлажняющих ингредиентов, которые притягивают и удерживают большое количество молекул воды, в сотни раз превышающее собственный молекулярный вес ГК. В составе косметических средств ГК легко сочетается с другими хумектантами, например, с глицерином или полисахаридами морского происхождения.
Главный момент, который необходимо учитывать при нанесении препаратов на основе гиалуроновой кислоты – влажность воздуха. В том случае, когда влажность воздуха низкая, гиалуроновая кислота дает противоположный эффект, высушивая верхние слои кожи и стягивая их, что быстро создает ощущение стянутости и скованности лица. Избежать этого можно, если после нанесения препарата на основе ГК сразу нанести питательный или увлажняющий крем в форме эмульсии, что предупредит «вытягивание» влаги из кожи.
Низкомолекулярные формы гиалуроновой кислоты в последние годы активно используются в топических формах противовозрастных препаратов. Небольшой размер молекулы (от 5000 до 20 000 Да) позволяет ГК проникать в глубокие слои эпидермиса и воздействовать на дерму.
Относительно крупные молекулы ГК, имеющие размер порядка 500 000 Да, не проникают в глубокие слои кожи, но при этом дают противовоспалительный и успокаивающий эффект. Особенно ярко это проявляется при использовании крупномолекулярных препаратов с ГК после лазерных шлифовок, химических пилингов или других повреждений кожи. Также можно рекомендовать использовать подобные препараты во время курса терапии ретинолом и его производными – для уменьшения выраженности воспалительного эффекта.
Препараты, которые содержат несколько форм гиалуроновой кислоты одновременно, оказывают универсальное действие. Их можно применять с целью коррекции морщин, повышения тонуса кожи, увлажнения и успокоения, а также для реабилитации после травматичных воздействий.
Гиалуроновая кислота
INCI: Hyaluronic Acid.
Другие названия: Acide hyaluronique, Hyaluronsäure, Acidum Hyaluronicum, Hyaloronic Acid, Hydrolyzed Hyaluronic Acid.
Производится путем бактериальной ферментации.
Используется в средствах для ухода за сухой кожей, чувствительной кожей, стареющей кожей.
Рекомендуемая концентрация: 0,01–2 %.
Механизм действия гиалуроновой кислоты при остеоартрите коленного сустава: систематический обзор
BMC Musculoskelet Disord. 2015; 16: 321.
, , , , и
RD Altman
Отдел ревматологии и иммунологии Медицинской школы Дэвида Геффена Калифорнийского университета в Лос-Анджелесе, 1000 ветеранов Ave,
Los Angeles, CA USA
A. Manjoo
Отделение ортопедии, Университет Макмастера, Гамильтон, Канада
A.Fierlinger
Ferring Pharmaceuticals Inc., Парсиппани, Нью-Джерси, США
F. Niazi
Ferring Pharmaceuticals Inc., Parsippany, NJ USA
M. Nicholls
Kentucky Orthopaedic Surge Surge Ortho Kentucky, Lexington, KY USA
Отделение ревматологии и иммунологии, Медицинская школа Дэвида Геффена, Калифорнийский университет в Лос-Анджелесе, 1000 Veterans Ave,
Los Angeles, CA USA
Отделение ортопедии, Университет Макмастера , Гамильтон, Онтарио, Канада
Ferring Pharmaceuticals Inc., Парсиппани, штат Нью-Джерси, США
Кентукки Ортопедические хирурги и хирурги кистей рук, отделение Ortho Kentucky, Лексингтон, штат Кентукки, США
Автор, отвечающий за переписку.
Поступило 12 августа 2015 г .; Принято 15 октября 2015 г.
Открытый доступ Эта статья распространяется в соответствии с условиями Международной лицензии Creative Commons Attribution 4.0 (http://creativecommons.org/licenses/by/4.0/), которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии вы должным образом указываете первоначального автора (авторов) и источник, предоставляете ссылку на лицензию Creative Commons и указываете, были ли внесены изменения.Отказ Creative Commons Public Domain Dedication (http://creativecommons.org/publicdomain/zero/1.0/) распространяется на данные, представленные в этой статье, если не указано иное. Эта статья цитируется в других статьях PMC.
Abstract
Предпосылки
Остеоартроз коленного сустава (ОА) является одной из основных причин инвалидности среди взрослого населения. Текущие варианты лечения ОА коленного сустава включают внутрисуставную (IA) гиалуроновую кислоту (HA), молекулу, которая находится внутри коленного сустава, которая обеспечивает вязкоупругие свойства синовиальной жидкости.В современной базовой литературе описаны различные механизмы, с помощью которых ГК борется с остеоартритом коленного сустава.
Методы
Мы провели всесторонний поиск литературы, чтобы определить доступные в настоящее время первичные доклинические фундаментальные научные статьи, посвященные механизму действия лечения IA-HA. Включенные статьи были оценены и распределены по категориям на основе описанного в них механизма действия. Основные результаты и выводы из каждой включенной статьи были получены и проанализированы в совокупности с исследованиями того же категориального задания.
Результаты
Хондрозащита была наиболее частым механизмом, о котором сообщалось во включенных статьях, за ней следуют синтез протеогликанов и гликозаминогликанов, противовоспалительное, механическое, субхондральное и обезболивающее действие. Связывание рецептора HA-кластера дифференцировки 44 (CD44) было наиболее часто упоминаемой биологической причиной представленных механизмов. Было обнаружено, что ГК с высоким молекулярным весом превосходит продукты ГК с более низким молекулярным весом. ГК, полученная в процессе биологической ферментации, также описывается как имеющая более благоприятные результаты безопасности по сравнению с продуктами ГК птичьего происхождения.
Выводы
Доклиническая фундаментальная научная литература предоставляет доказательства многочисленных механизмов, с помощью которых ГК действует на структуры и функции суставов. Эти действия подтверждают предполагаемую клиническую пользу IA-HA при остеоартрите коленного сустава. Дальнейшие исследования должны быть сосредоточены не только на обезболивании, обеспечиваемом лечением IA-HA, но и на свойствах модификации заболевания, которыми обладает этот метод лечения.
Ключевые слова: Остеоартрит, Гиалуроновая кислота, Терапия, Внутрисуставная терапия, Систематический обзор, Механизм действия
Предпосылки
Хотя остеоартрит (ОА) коленного сустава чаще всего является медленно прогрессирующим заболеванием суставов, он является одним из ведущие причины инвалидности взрослого населения [1].ОА коленного сустава, заболевание всего сустава, характеризуется болью в суставах, дегенерацией хряща и увеличением инвалидности [2]. Прогрессирующий характер ОА приводит к снижению функции коленного сустава, влияя на способность человека выполнять повседневную деятельность [3]. ОА коленного сустава также негативно влияет на социально-экономические факторы, поскольку связанная с этим инвалидность часто приводит к снижению производительности труда и раннему выходу на пенсию [4].
Поскольку не существует установленного агента, модифицирующего заболевание при ОА, существует множество вариантов лечения ОА коленного сустава.Среди фармакологических методов лечения чаще всего назначают нестероидные противовоспалительные препараты (НПВП) и внутрисуставные (IA) инъекции кортикостероидов [5]. Этим вариантам присущи ограничения, так как НПВП имеют потенциально серьезные побочные эффекты, связанные с их использованием [6], а инъекции кортикостероидов IA часто обеспечивают относительно короткий период эффективного облегчения [7]. Хотя инъекция кортикостероидов обычно имеет положительный профиль безопасности, было показано, что она вызывает временное повышение уровня глюкозы в крови, что может вызывать беспокойство у пациентов с диабетом [8].IA инъекция гиалуроновой кислоты (HA) — еще один вариант лечения боли при остеоартрите коленного сустава. ГК почти повсеместно присутствует в организме и представляет собой молекулу, которая находится внутри коленного сустава, где она придает вязкоупругие свойства синовиальной жидкости [9]. По мере прогрессирования ОА естественная концентрация ГК и распределение ГК в суставе смещается в сторону более низких диапазонов молекулярной массы ГК, что приводит к деградации механических / вязкоупругих свойств эндогенной синовиальной жидкости [2, 10, 11]. Также было показано, что более низкие диапазоны молекулярно-массового распределения сильно коррелируют с болью [11].Назначение IA-HA было направлено на восстановление этого снижения концентрации HA и среднего молекулярно-массового распределения внутри OA колена [9].
IA-HA, как предполагалось, обладает множеством терапевтических механизмов действия в коленном суставе с остеоартритом, включая поглощение ударов, смазку суставов, противовоспалительные эффекты, хондрозащиту, синтез протеогликанов и изменения хрящевого матрикса [2]. Корреляция между этими различными эффектами позволила лучше понять, как лечение IA-HA может оказывать терапевтический эффект для пациентов с остеоартритом коленного сустава [12].Имеются также данные, свидетельствующие о различиях в механизмах действия продуктов НА разной молекулярной массы. То есть ГК с более высокой молекулярной массой (HMW), как сообщается, обеспечивает более сильные противовоспалительные эффекты и эффекты синтеза протеогликанов, а также смазывание суставов и поддержание вязкоупругости [9, 13]. Также, по-видимому, существуют доказательства различных профилей безопасности между ГК, полученным в процессе биологической ферментации (Bio-HA), и ГК птичьего происхождения (AD-HA), поскольку AD-HA имеет потенциал для местных реакций IA [14, 15] .
Мы стремимся обобщить механизмы действия IA-HA лечения ОА коленного сустава, описанные в современной литературе, чтобы определить обоснованность вышеупомянутых механизмов действия. Мы будем систематически оценивать и обрисовывать определенные механизмы, с помощью которых ГК может оказывать терапевтическое действие, одновременно анализируя сообщаемые различия между эффектами лечения ИА-ГК, зависящими от характеристик продукта.
Методы
Поиск литературы
Мы провели всесторонний поиск литературы с использованием баз данных MEDLINE, EMBASE и PubMed (таблица).Поиск был проведен 4 мая -го , 2014. Критерии включения, соблюдаемые на протяжении всего процесса отбора, были следующими: 1) Статьи, описывающие механизм лечения ГК при ОА, 2) Статьи, посвященные ОА коленного сустава, и 3) Основные доклинические фундаментальные научные статьи, посвященные «добавлению вязкости» / лечению ГК. Статьи, которые были опубликованы до 1990 года или не были опубликованы на английском языке, были исключены из исследования. Если одним и тем же автором было опубликовано несколько исследований, содержащих похожие результаты, для включения принималось только самое последнее исследование.
Таблица 1
| MEDLINE и EMBASE — 1470 статей | PubMed — 1395 статей |
|---|---|
| 1. Гиалуроновая кислота [название] | 1. Гиалуроновая кислота [название] |
| 2. Hylan [title] | |
| 3. Гиалуронан [title] | 3. Гиалуронан [title] |
| 4. Добавки для вязкости [title] | 4. Добавки для вязкости [title] | 5.1 или 2 или 3 или 4 | 5. 1 или 2 или 3 или 4 |
| 6. Остеоартрит * .mp | 6. Остеоартрит * |
| 7. Артрит * .mp | 7. Артрит * |
| 8. Боль в суставах.mp | 8. Боль в суставах |
| 9. 6 или 7 или 8 | 9. 6 или 7 или 8 |
| 10. Эффект * .mp | 10. Эффект * |
| 11. Механизм * .mp | 11. Механизм * |
| 12.10 или 11 | 12. 10 или 11 |
| 13. 5 и 9 и 12 | 13. 5 и 9 и 12 |
Абстракция данных
Включенные статьи были оценены и классифицированы на основе механизма действие, описанное в них. Отдельные статьи включались в несколько категорий, если они анализировали более одного механизма действия НА в рамках своего дизайна исследования. Категории механизмов, использованные в процессе извлечения данных, включали: хондрозащиту, изменения синтеза протеогликана и / или гликозаминогликана (ГАГ), противовоспалительные эффекты, механические модификации, изменения в субхондральной кости и анальгетические эффекты.
Анализ данных
Ключевые выводы и заключения по каждой включенной статье были получены и проанализированы в совокупности с исследованиями той же присвоенной категории. Представленные результаты были получены путем интерпретации общего и последовательного механизма действия в рамках каждой вышеупомянутой категории.
Результаты
Стратегия поиска
Поиск литературы выявил 2782 потенциальных статьи, из которых 91 статья соответствовала критериям включения (рис.). Тринадцать дополнительных статей были извлечены специалистом по содержанию путем ручного поиска литературы. В результате было включено 104 статьи. Выводы и основные выводы каждой статьи были определены в рамках вышеупомянутых категорий механизмов (таблица).
Процесс проверки статей
Таблица 2
Ключевые механизмы действия, указанные во включенных статьях
| Механизм действия | Количество статей | % включенных статей | Ссылки | |
|---|---|---|---|---|
| Chondrotective | 67 | 64.42% | [9, 12, 16–80] | |
| Синтез протеогликанов / гликозаминогликанов | 22 | 21,15% | [27, 42, 44, 48, 62, 69, 83–98] | |
| Противовоспалительное | 21 | 20,19% | [13, 20, 21, 25, 27, 52, 54, 55, 68, 72, 96, 97, 99–107] | |
| Механический | 10 | 9,61% | [41, 49, 86, 108–114] | |
| Субхондральная кость | 8 | 7.69% | [23, 31, 32, 45, 115–118] | |
| Анальгетик | 6 | 5,76% | [76, 80, 119–122] |
Хондрозащита
Шестьдесят семь из включенных статей описывают хондрозащитные эффекты лечения IA-HA [9, 12, 16–80]. Было показано, что IA-HA снижает апоптоз хондроцитов, одновременно увеличивая пролиферацию хондроцитов [19, 20]. Существует множество наблюдаемых эффектов лечения IA-HA, которые вызывают хондрозащиту, многие из которых являются результатом связывания HA с рецепторами кластера дифференцировки 44 (CD44).Связывание HA с CD44 ингибирует экспрессию интерлейкина (IL) -1β, что приводит к снижению продукции матриксной металлопротеиназы (MMP) -1, 2, 3, 9 и 13 [32, 34]. Было показано, что это связывание с CD44 имеет больший эффект для продуктов HA с более высокой молекулярной массой [21]. HA также связывается с рецептором опосредованной гиалуронаном подвижности (RHAMM), который, как полагают, способствует хондропротекции в дополнение к связыванию с CD44 [34]. Ингибирование экспрессии IL-1β посредством связывания CD44 осуществляется посредством индукции митоген-активируемой протеинкиназы фосфатазы (MKP) -1: негативного регулятора IL-1β [43].Это ингибирование различных MMP препятствует активности катаболических ферментов в суставном хряще [59]. Было показано, что HMW HA имеет больший эффект в ингибирующем действии на продукцию MMP [21], хотя эти результаты неясны, поскольку другое исследование продемонстрировало благоприятный ингибирующий эффект MMP продуктов с более низкой молекулярной массой (LMW) [72].
События апоптоза хондроцитов дополнительно уменьшаются за счет связывания HA-CD44 за счет снижения экспрессии дезинтегрина и металлопротеиназы с тромбоспондиновыми мотивами (ADAMTS) [38].Эти пептидазы участвуют в расщеплении важных синовиальных компонентов, включая аггрекан, версикан и бревикан [81, 82]. Было показано, что различная экспрессия ADAMTS снижается в результате связывания HA-CD44, обеспечивая дополнительный режим хондропротекции для лечения IA-HA [36, 38, 43]. Производство активных форм кислорода (АФК), таких как оксид азота (NO), приводит к дегенерации хряща за счет увеличения апоптоза хондроцитов [33]. Лечение IA-HA продемонстрировало снижение индуцированного IL-1β окислительного стресса за счет ингибирования продукции NO в синовиальной оболочке [48, 57].Дополнительные результаты связывания CD44-HA, приводящие к хондропротекторным эффектам, упомянутые в современной литературе, включают снижение синтеза простагландина E2 (PGE2) [42, 46, 61] и повышенную сверхэкспрессию белка теплового шока 70 (Hsp70) [25, 70]. Эти эффекты аналогичным образом обеспечивают терапевтический эффект за счет уменьшения апоптоза хондроцитов. Важно отметить, что HMW продукты HA продемонстрировали большее подавление экспрессии PGE2, чем LMW компараторы в сравнительном исследовании, что привело к более сильному хондрозащитному эффекту [61].
Синтез протеогликанов и гликозаминогликанов
В 22 из идентифицированных исследований сообщалось об усилении синтеза протеогликанов и гликозаминогликанов, связанном с лечением IA-HA [27, 42, 44, 48, 62, 69, 83–98]. По мере прогрессирования ОА внутренние концентрации протеогликана и ГАГ в хряще снижаются. Результаты показали, что обработка IA-HA стимулировала синтез протеогликана, задерживая прогрессирование OA [69, 88]. Аггрекан является первичным протеогликаном в суставном хряще, и показано, что лечение IA-HA как подавляет деградацию аггрекана, так и способствует внутреннему развитию аггрекана [62, 93].Показано, что обработка IA-HA мобилизует вновь синтезированный протеогликан во внешний матрикс хондроцитов, потенциально обеспечивая защиту от деградации. Внешний HA способствует перемещению вновь синтезированного протеогликана из ассоциированного с клетками матрикса в далее удаленный матрикс в модели альгинатного геля, что предполагает, что IA-HA может обеспечивать терапевтическое облегчение OA за счет укрепления межтерриториального хрящевого матрикса [92]. Маркер синтеза протеогликана, сульфат ( 35 SO 4 ), как видно, все больше включается в хондроциты после введения HA [87].Биологический путь, в котором HA изменяет уровни аггрекана, проявляется через эффекты связывания CD44 и молекулы межклеточной адгезии (ICAM) -1 [62]. В одном исследовании было показано, что HMW HA обеспечивает больший эффект синтеза протеогликанов, чем LMW HA, за счет стимуляции пути инсулиноподобного фактора роста (IGF) -1 [89]. Также показано, что лечение IA-HA увеличивает выработку эндогенного ГАГ. Обработка IA-HA не только дополняла синовиальную оболочку HA, но и способствовала внутренней продукции HA [27].
Противовоспалительное
В 21 из идентифицированных исследований сообщалось о противовоспалительных эффектах лечения IA-HA [13, 20, 21, 25, 27, 52, 54, 55, 68, 72, 96, 97 , 99–107].Известно, что IL-1β демонстрирует провоспалительные эффекты, и вышеупомянутое подавление экспрессии IL-1β с помощью HA обеспечивает противовоспалительные эффекты [52]. IL-1β является ключевым медиатором противовоспалительного действия HA и регулируется посредством связывания HA-CD44 [59, 104]. Подавление IL-1β приводит к подавлению MMPs, как упоминалось ранее, что также способствует противовоспалительному эффекту HA [52]. Дальнейшее подавление провоспалительных медиаторов IL-8, IL-6, PGE 2 и фактора некроза опухоли (TNFα) обеспечивает противовоспалительные эффекты лечения IA-HA [13, 21].Связь между Toll-подобными рецепторами (TLR) и воспалительным ответом демонстрируется, поскольку продукты деградации HA индуцируют воспалительный ответ через взаимодействие CD44 и TLR. Этот провоспалительный ответ от связывания продукта деградации HA с рецепторами TLR и CD44 приводит к увеличению продукции Nf-kB, IL-1β, TNFα, IL-6 и IL-33 [105]. Было продемонстрировано, что HMW HA подавляет множество медиаторов воспаления посредством связывания TLR 2 и 4, включая TNF-α, IL-1-β, IL-17, MMP-13 и индуцибельную синтазу оксида азота (iNOS) [106].Прямая корреляция между молекулярной массой и противовоспалительным действием продемонстрировала более сильные эффекты ингибирования PGE 2 и IL-6 при лечении HMW HA [13]. IL-6 представляет собой провоспалительный цитокин, регулируемый ядерным фактором, энхансером легкой каппа-цепи активированных В-клеток (Nf-кB). Связывание HA с ICAM-1 подавляет Nf-kB, что, в свою очередь, снижает продукцию IL-6 [21, 104]. HMW HA, подавляющая регуляцию TNFα, IL-1B и IL-8, является дополнительным фактором, способствующим противовоспалительным эффектам, обеспечиваемым HMW HA [72, 97].
Механический
Десять из включенных исследований описывали механические эффекты ГК при лечении ОА коленного сустава [41, 49, 86, 108–114]. Показано, что вязкая природа лечения ГК смазывает суставную капсулу, предотвращая дегенерацию за счет снижения трения [86]. ГК дополнительно защищает капсулу сустава за счет благотворного эффекта поглощения ударов. HA обеспечивает амортизацию для поглощения давления и вибрации в суставе, которые в противном случае могут привести к деградации хондроцитов [41]. Сообщается, что колени с остеоартритом имеют более высокое трение в суставной щели, чем здоровые колени, чему противодействует способность суставной смазки, которой обладает HA [110].Было продемонстрировано, что HMW HA обеспечивает больший эффект снижения трения благодаря своим вязким свойствам. Уменьшение трения в суставе может обеспечить терапевтический эффект, поскольку хрящ защищен от механической деградации [111].
Субхондральная кость
Восемь из включенных исследований описали эффекты, которые IA-HA оказывает на субхондральную кость [23, 31, 32, 45, 115–118]. Ранее было показано, что взаимодействие между остеобластами субхондральной кости и хондроцитами суставного хряща в суставах с остеоартритом изменяет экспрессию ADAMTS-4/5 и MMP-1, MMP-2, MMP-3, MMP-8, MMP-9 и MMP-13. и регуляция, опосредованная митоген-активируемой протеинкиназой (MAPK) и сигнальными путями, регулируемыми внеклеточными сигналами киназ 1 и 2 (ERK 1/2) [118].IA-HA также влияет на субхондральную кость путем подавления MMP-13 и IL-6 через связывание CD44, что потенциально предотвращает аномальный метаболизм костной ткани [116]. Было высказано предположение, что подавление экспрессии MMP-13 с помощью IA-HA является критическим фактором воздействия на субхондральную кость при ОА [117]. Эффект, который IA-HA оказывает на MMPs, особенно MMP-13, посредством связывания CD44, как предполагалось, ингибирует эффекты OA в субхондральной кости в многочисленных доклинических фундаментальных научных исследованиях [32, 45, 116–118].ГК эффективно изменяет плотность и толщину субхондральной кости за счет изменений трабекулярной структуры, что приводит к большей податливости субхондральной кости. В конечном итоге показано, что это снижает нагрузку на хрящ во время ударной нагрузки [23]. Признаком стимуляции IA-HA обмена коллагена типа II на границе раздела хрящ и костей является повышение уровней сшивок коллагена на карбокси-конце (CTX) -II в моче, наблюдаемое после лечения IA-HA, которое продемонстрировало улучшение остеоартрита колена [31].В конечном итоге ГК, по-видимому, ограничивает изменения субхондральной кости, характерные для раннего ОА [115].
Анальгетик
Шесть из включенных статей описывают обезболивающие эффекты лечения IA-HA [76, 80, 119–122]. Одна инъекция ГК продемонстрировала значительное снижение связанного с болью поведения на мышиной модели [119]. Одно исследование показало, что HA не связывается напрямую с рецепторами брадикинина, но оказывает обезболивающее за счет взаимодействия с рецепторами HA и / или свободными нервными окончаниями в суставной ткани [121].Было показано, что обезболивающие эффекты HA проявляются в механочувствительных ионных каналах, активируемых растяжением, где активность канала значительно снижается при связывании HA [122]. Было показано, что HMW HA снижает механическую чувствительность ионных каналов, активируемых растяжением, которые эффективно блокируют болевой ответ. Было обнаружено, что LMW HA менее эффективен в блокировании этого ответа [122]. ГК снижает действие ноцицепторов суставов, что обеспечивает уменьшение боли в суставе. На сенсибилизированные ноцицептивные окончания в суставной ткани влияет концентрация HA, снижая болевую реакцию, проявляемую этими терминалами [120].
Обсуждение
Наш обзор существующей литературы дает общее мнение о том, что IA-HA при ОА коленного сустава имеет положительные эффекты через несколько механизмов действия; однако преобладающий механизм терапевтического эффекта не совсем ясен [2]. В перспективе неясно, какие из этих механизмов являются клинически значимыми, поскольку понятно, что полезные механизмы действия не обязательно переносятся на пользу в клинических условиях.В настоящее время предполагается, что клиническая польза IA-HA при ОА коленного сустава обусловлена несколькими параллельными механизмами действия, а не каким-либо одним конкретным механизмом действия.
Большая часть экзогенной ГК остается в суставе в течение нескольких дней; однако клинические терапевтические эффекты лечения ГК могут наблюдаться в течение 6 месяцев или более. Это может указывать на то, что IA-HA обладает свойствами, модифицирующими болезнь, и действует не только за счет восстановления вязкоупругих свойств синовиальной жидкости [123].Инъекции ГК могут стимулировать эндогенную продукцию дополнительной ГК синовиоцитами человека, способствуя нормализации распределения ГК в синовиальной жидкости [124]. В доклинических фундаментальных научных исследованиях во многих сообщениях описывается связывание CD44 как основной способ, при котором НА обеспечивает действие против ОА коленного сустава. Показано, что CD44-опосредованные эффекты IA-HA вносят вклад в потенциальную хондрозащиту, синтез протеогликанов / гликозаминогликанов, противовоспалительные и субхондральные механизмы. Показано, что это связывание оказывает разнообразные эффекты на многочисленные сигнальные пути, каждый из которых демонстрирует своего рода вмешательство в прогрессирование ОА [13, 21, 32, 36, 38, 42, 43, 46, 59, 61, 104 , 116].Было высказано предположение, что подавление IL-1β и IL-6 и последующие эффекты этого подавления являются ключевым фактором в терапевтическом механизме, обеспечиваемом связыванием HA-CD44 [123]. Очевидно, что связывание HA-CD44 является основным компонентом механизма, в котором HA обеспечивает терапевтический эффект; однако существуют дополнительные механизмы, которые обеспечивают альтернативные пути эффективности лечения ГК при ОА коленях, включая связывание ICAM, механические улучшения, связанные с поглощением удара и смазкой, увеличение обмена коллагена типа II на границе раздела хрящ / кость, а также анальгетические эффекты. через взаимодействие с нервными окончаниями и ноцицепторами суставов [31, 41, 86, 97, 121, 122].Связывание HA с рецептором RHAMM способствует заживлению ран, активирует функции промиграции и инвазии, регулирует клеточные ответы на факторы роста и играет роль в миграции и подвижности фибробластов [125–127]. Эти результаты связывания HA-RHAMM являются потенциальными факторами, участвующими в эффектах модификации заболевания при лечении HA при ОА.
Имеются данные, которые демонстрируют, что определенные внутренние свойства определенных продуктов IA-HA могут давать положительные результаты по сравнению с другими продуктами IA-HA.Наиболее известным из этих внутренних свойств является молекулярная масса. В отличие от предыдущего фундаментального научного обзора, проведенного Ghosh et al., Который предположил потенциальное преимущество LMW HA в обеспечении восстановления реологических свойств по сравнению с HMW HA [128], данные текущего обзора продемонстрировали благоприятные результаты для лечения HMW HA. Текущий обзор поддерживает точку зрения, что HMW HA обеспечивает превосходные хондропротекторные, протеогликановые и гликозаминогликановые механизмы синтеза, противовоспалительные, механические и обезболивающие механизмы действия [61, 89, 97, 111, 122].Исследование Huang et al. продемонстрировали превосходные противовоспалительные эффекты HMW HA, но лучшие хондрозащитные эффекты LMW HA; однако эти результаты относительно хондрозащиты неясны из-за отсутствия дополнительных доказательств в фундаментальной научной литературе по ОА коленного сустава [72]. Было показано, что повышенная продукция воспалительных цитокинов и хемокинов, привлечение медиаторов воспаления и образование кровеносных сосудов являются ответом на LMW HA ниже 500 кДа. Хотя средний молекулярный вес доступных продуктов ГК на рынке сильно различается, следует отметить, что, насколько нам известно, все доступные в настоящее время продукты во всем мире имеют молекулярную массу> 500 кДа [129, 130].Анализ взаимодействия HA-CD44 показал, что размер HA имеет прямое влияние на сродство, при котором HA связывается с рецептором CD44 [131]. Эти результаты демонстрируют способность HMW HA лечить прогрессирование ОА коленного сустава посредством связывания HA с CD44. Эти фундаментальные научные данные согласуются с систематическими обзорами клинических испытаний и сравнительных исследований, которые продемонстрировали, что HMW HA обеспечивает большую терапевтическую пользу, чем LMW HA при лечении ОА коленного сустава [6, 132], хотя текущая литература не обеспечивает консенсуса в отношении различие в клинической эффективности ГК с низким и высоким молекулярным весом [133].
Традиционно продукты ГК получали из птичьих источников; однако некоторые доступные продукты производятся путем биологической ферментации. Этот процесс позволяет избежать присутствия молекул птичьего происхождения, которые, как предполагается, могут быть потенциальной причиной неблагоприятных местных реакций [134]. Отсутствуют подробные отчеты о потенциале Bio-HA по сравнению с AD-HA. Одно исследование показало, что места инъекции AD-HA могут быть причиной синовита в их группе пациентов, но точный патологический агент неизвестен [135].Результаты второго исследования также указывают на способность гилана AD-HA вызывать гранулематозную реакцию типа гигантских клеток на инородное тело [136]. Исследования показали, что обострения, связанные с инъекцией гилана, могут быть связаны с накоплением гилана или продуктов его распада, поскольку обострения в месте инъекции обычно не возникают при первой инъекции [14]. Было показано, что белки птичьего происхождения являются причиной обострения в месте инъекции, поскольку антитела к белку куриной сыворотки присутствовали у пациентов, у которых наблюдалась неблагоприятная реакция в месте инъекции после лечения AD-HA [15].Имеются некоторые высококачественные клинические доказательства того, что Bio-HA имеет значительно меньшую частоту нежелательных явлений в месте инъекции, чем AD-HA [134]; однако в современной литературе это не исследовано досконально. Необходимо более всестороннее исследование разницы в частоте нежелательных явлений в месте инъекции между Bio-HA и AD-HA как с фундаментальной науки, так и с клинической точки зрения.
Этот обзор имеет методологическую силу благодаря систематическому и тщательному поиску доступных фундаментальных научных данных в нескольких базах данных.Текущий отчет также демонстрирует строгость в его представлении множественных механизмов, в которых действует HA, предоставляя доказательства обо всех механизмах, независимо от того, подробно или нечасто описаны в текущей литературе. Ограничения данного исследования возникают из-за субъективной классификации включенной статьи механизм действия основных выводов. Включенные статьи могут кратко упоминать альтернативные механизмы действия, но не были отнесены к соответствующей категории, потому что упомянутый альтернативный механизм не был ключевым результатом или заключением исследования.В будущих исследованиях следует проанализировать взаимосвязь между различными механизмами, представленными в этом отчете, и прояснить, как эти механизмы перекрываются и могут работать вместе для облегчения симптомов ОА коленного сустава. Дальнейшие исследования также должны быть направлены на выявление различий между механизмами, проявляемыми продуктами с высокой и низкой молекулярной массой, а также на анализ различий в профилях безопасности между Bio-HA и AD-HA.
Выводы
Доклиническая фундаментальная научная литература предоставляет доказательства многочисленных механизмов, с помощью которых IA-HA может обеспечить клиническую пользу при ОА коленного сустава.Хондропротекция является наиболее часто описываемым механизмом, причем связывание HA-CD44 является наиболее частым источником этих эффектов. Сообщается также, что IA-HA обеспечивает синтез протеогликанов и гликозаминогликанов, оказывает противовоспалительное, механическое, субхондральное и обезболивающее действие. Имеются данные о благоприятных результатах лечения HMW HA по сравнению с лечением LMW HA. Также показано, что Bio HA обеспечивает более выгодный профиль безопасности по сравнению с AD-HA, поскольку отчеты демонстрируют связь между обострениями в месте инъекции и белками птичьего происхождения.Существует множество описанных механизмов, в которых показано, что ИА-ГК лечит ОА коленного сустава, а также многочисленные характеристики продукта, которые влияют на результаты лечения ИА-ГК. Чтобы признать применимость и целесообразность лечения IA-HA для колено О.А. Дальнейшие исследования должны быть сосредоточены не только на обезболивании, обеспечиваемом лечением IA-HA, но и на свойствах модификации заболевания, которыми может обладать этот метод лечения.
Благодарности
Этот обзор финансируется Ferring Pharmaceuticals Inc. Авторы хотели бы поблагодарить Марка Филлипса и Global Research Solutions Inc. за их помощь в подготовке рукописи.
Аббревиатуры
| ADAMTS | Дезинтегрин и металлопротеиназа с тромбоспондиновыми мотивами | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| AD-HA | Гиалуроновая кислота птичьего происхождения | Биологическая кислота | Биологическая кислота | CD | Кластер дифференцировки | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CTX | Сшивки карбоксиконцевого коллагена | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ERK 1/2 | Киназа 1 и 2, регулируемая внеклеточным сигналом | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| GAG12122 90og3511 | Гиалуроновая кислота | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| HMW | Более высокая молекулярная масса | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hsp70 | Белок теплового шока 70 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| IA | Внутрисуставной | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| IL | Интерлейкин | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| iNOS | Индуцируемый оксид азота LMW, низкомолекулярный вес | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| MAPK | MAPK | Митоген-активированная протеинкиназа | 90sp MMP | Металлопротеиназа | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nf-кB | Ядерный фактор, усилитель легкой цепи каппа активированных В-клеток | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NO | Оксид азота | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 12 НПВП | OA | Остеоартрит | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PGE2 | Простагландин E2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| RHAMM | Рецептор для подвижности, опосредованной гиалуронаном |
Фут примечания
Конкурирующие интересы
Рой Д.Альтман: Консультант: Cytori, DuPuy (Bioventus Global), Ferring, Flexion, Iroko, McNeil, Novartis, Oletec, Pfizer, QMed, Rotta, Strategic Science and Technologies, Teva.
Спикер: Ферринг, Ироко.
Аджай Манджу: Нет конфликта интересов
Анке Фирлингер: оплачиваемый сотрудник Ferring Pharmaceuticals Inc.
Файзан Ниази: оплачиваемый сотрудник Ferring Pharmaceuticals Inc.
Мэтью Николлс: работает в консультативных советах Ferring.
Вклад авторов
AF и FN участвовали в разработке и разработке исследования. RDA обеспечило интерпретацию данных и внесение значительного письменного вклада в рукопись. Все авторы представили рукопись критическую рецензию и исправления. Все авторы прочитали и одобрили окончательную рукопись.
Ссылки
1. Cheng OT, Souzdalnitski D, Vrooman B, Cheng J. Доказательные инъекции в колено для лечения артрита. Pain Med.2012. 13 (6): 740–753. DOI: 10.1111 / j.1526-4637.2012.01394.x. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 2. Морленд Л.В. Внутрисуставной гиалуронан (гиалуроновая кислота) и гиланы для лечения остеоартрита: механизмы действия. Лечение артрита Res. 2003; 5 (2): 54. DOI: 10.1186 / ar623. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 3. Беллами Н., Кэмпбелл Дж., Робинсон В., Джи Т., Борн Р., Уэллс Г. Вискозиметрические добавки для лечения остеоартрита колена. Кокрановская база данных Syst Rev.2006; 2 [PubMed] [Google Scholar] 4. Тригкилидас Д., Ананд А. Эффективность внутрисуставных инъекций гиалуроновой кислоты при лечении боли в коленях при остеоартрите. Ann R Coll Surg Engl. 2013. 95 (8): 545–551. DOI: 10.1308 / rcsann.2013.95.8.545. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 5. Colen S, van den Bekerom MP, Mulier M, Haverkamp D. Гиалуроновая кислота в лечении остеоартрита коленного сустава: систематический обзор и метаанализ с упором на эффективность различных продуктов. BioDrugs.2012. 26 (4): 257–268. DOI: 10.1007 / BF03261884. [PubMed] [CrossRef] [Google Scholar] 6. Rutjes A, Juni P, da Costa B, Trelle S, Nuesch E, Reichenbach S. Viscosupplementation для остеоартрита коленного сустава: систематический обзор и метаанализ. Ann Intern Med. 2012; 157: 180–191. DOI: 10.7326 / 0003-4819-157-3-201208070-00473. [PubMed] [CrossRef] [Google Scholar] 7. Баннуру Р.Р., Натов Н.С., Обадан И.Е., Прайс Л.Л., Шмид С.Х., Макалиндон Т.Е. Терапевтическая траектория гиалуроновой кислоты по сравнению с кортикостероидами в лечении остеоартрита коленного сустава: систематический обзор и метаанализ.Ревматоидный артрит. 2009. 61 (12): 1704–1711. DOI: 10.1002 / art.24925. [PubMed] [CrossRef] [Google Scholar] 8. Хабиб Г.С. Системные эффекты внутрисуставных кортикостероидов. Clin Rheumatol. 2009. 28 (7): 749–756. DOI: 10.1007 / s10067-009-1135-х. [PubMed] [CrossRef] [Google Scholar] 9. Элморси С., Фунакоши Т., Сасазава Ф., Тодох М., Тадано С., Ивасаки Н. Хондропротекторные эффекты высокомолекулярной поперечно-сшитой гиалуроновой кислоты на модели остеоартрита коленного сустава кролика. Хрящевой артроз. 2014; 22 (1): 121–127.DOI: 10.1016 / j.joca.2013.10.005. [PubMed] [CrossRef] [Google Scholar] 10. Kosinska MK, Ludwig TE, Liebisch G, Zhang R, Siebert HC, Wilhelm J, et al. Смазки для суставов при остеоартрите и ревматоидном артрите имеют измененные уровни и молекулярные формы. PLoS One. 2015; 10 (5) DOI: 10.1371 / journal.pone.0125192. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 11. Band PA, Heeter J, Wisniewski HG, Liublinska V, Pattanayak CW, Karia RJ, et al. Распределение молекулярной массы гиалуроновой кислоты связано с риском прогрессирования остеоартрита коленного сустава.Хрящевой артроз. 2015; 23 (1): 70–76. DOI: 10.1016 / j.joca.2014.09.017. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 12. Диас-Гальего Л., Прието Дж. Г., Коронель П., Гамазо Л. Е., Гимено М., Альварес А. И.. Апоптоз и оксид азота в экспериментальной модели остеоартрита у кролика после лечения гиалуроновой кислотой. J Orthop Res. 2005. 23 (6): 1370–1376. DOI: 10.1016 / j.orthres.2005.05.003.1100230619. [PubMed] [CrossRef] [Google Scholar] 13. Lajeunesse D, Delalandre A, Martel-Pelletier J, Pelletier J-P.Гиалуроновая кислота устраняет аномальную синтетическую активность остеоартрита субхондральных костных остеобластов человека. Кость. 2003. 33 (4): 703–710. DOI: 10.1016 / S8756-3282 (03) 00206-0. [PubMed] [CrossRef] [Google Scholar] 14. Pullman-Mooar S, Mooar P, Sieck M, Clayburne G, Schumacher HR. Есть ли характерные воспалительные обострения после внутрисуставных инъекций hylan g-f 20? J Rheumatol, декабрь 2002 г., 29 (12): 2611–2614. [PubMed] [Google Scholar] 15. Гольдберг В.М., Куттс Р.Д. Псевдосептические реакции на добавку hylan viscos: диагностика и лечение.Clin Orthop Relat Res, февраль 2004 г .; 419: 130–137. DOI: 10.1097 / 00003086-200402000-00021. [PubMed] [CrossRef] [Google Scholar] 16. Ando A, Hagiwara Y, Chimoto E, Hatori K, Onoda Y, Itoi E. Внутрисуставная инъекция гиалуронана снижает потерю хондроцитов в модели с иммобилизованным коленом крысы. Tohoku J Exp Med. 2008. 215 (4): 321–331. DOI: 10.1620 / tjem.215.321. [PubMed] [CrossRef] [Google Scholar] 17. Ariyoshi W, Okinaga T, Knudson CB, Knudson W., Nishihara T. Высокомолекулярная гиалуроновая кислота регулирует образование остеокластов путем ингибирования активатора рецептора лиганда NF-kappaB через Rho-киназу.Хрящевой артроз. 2014. 22 (1): 111–120. DOI: 10.1016 / j.joca.2013.10.013. [PubMed] [CrossRef] [Google Scholar] 18. Asari A, Miyauchi S, Matsuzaka S, Itoh T, Uchiyama Y. Гиалуронат на белке теплового шока и синовиальных клетках в модели остеоартрита у собак. Хрящевой артроз. 1996. 4 (3): 213–215. DOI: 10.1016 / S1063-4584 (96) 80018-5. [PubMed] [CrossRef] [Google Scholar] 19. Брун П., Панфило С., Дага Гордини Д., Кортиво Р., Абатанджело Г. Влияние гиалуронана на CD44-опосредованное выживание нормальных и поврежденных гидроксильными радикалами хондроцитов.Хрящевой артроз. 2003. 11 (3): 208–216. DOI: 10.1016 / S1063-4584 (02) 00352-7. [PubMed] [CrossRef] [Google Scholar] 20. Брун П., Заван Б., Виндини В., Скьявинато А., Поццуоли А., Якобеллис С. и др. In vitro ответ остеоартрозных хондроцитов и фибробластоподобных синовиоцитов на производное гиалуронанамида 500-730 кДа. J Biomed Mater Res B Appl Biomater. 2012. 100 (8): 2073–2081. DOI: 10.1002 / jbm.b.32771. [PubMed] [CrossRef] [Google Scholar] 21. Chang CC, Hsieh MS, Liao ST, Chen YH, Cheng CW, Huang PT и др.Гиалуронан регулирует PPARgamma и воспалительные реакции в клетках хондросаркомы человека, стимулированных IL-1beta, которые являются моделью остеоартрита. Carbohydr Polym. 2012; 90 (2): 1168–1175. DOI: 10.1016 / j.carbpol.2012.06.071. [PubMed] [CrossRef] [Google Scholar] 22. Creamer P, Sharif M, George E, Meadows K, Cushnaghan J, Shinmei M и др. Внутрисуставная гиалуроновая кислота при остеоартрозе коленного сустава: исследование механизмов действия. Хрящевой артроз. 1994. 2 (2): 133–140. DOI: 10.1016 / S1063-4584 (05) 80063-9.[PubMed] [CrossRef] [Google Scholar] 23. Динг М., Кристиан Даниэльсен С., Хвид И. Влияние гиалуронана на трехмерную микроархитектуру субхондральных костных тканей при первичном остеоартрозе морских свинок. Кость. 2005. 36 (3): 489–501. DOI: 10.1016 / j.bone.2004.12.010. [PubMed] [CrossRef] [Google Scholar] 24. Элерс Э.М., Беренс П., Вунш Л., Кунель В., Русслис М. Влияние гиалуроновой кислоты на морфологию и пролиферацию хондроцитов человека в первичной культуре клеток. Анн Анат. 2001. 183 (1): 13–17. DOI: 10.1016 / S0940-9602 (01) 80007-8. [PubMed] [CrossRef] [Google Scholar] 25. Галуа Л., Этьен С., Хенрионне С., Скала-Бертола Дж., Гроссин Л., Майнард Д. и др. Амбивалентные свойства гиалуроната и гилана при посттравматическом ОА коленного сустава крысы. Biomed Mater Eng. 2012. 22 (4): 235–242. [PubMed] [Google Scholar] 26. Gonzalez-Fuentes AM, Green DM, Rossen RD, Ng B. Внутрисуставная гиалуроновая кислота увеличивает биомаркер разрушения хряща у пациентов с остеоартрозом коленного сустава. Clin Rheumatol. 2010. 29 (6): 619–624. DOI: 10.1007 / s10067-010-1376-8. [PubMed] [CrossRef] [Google Scholar] 27. Гринберг Д.Д., Стокер А., Кейн С., Кокрелл М., Кук Дж. Биохимические эффекты двух различных продуктов гиалуроновой кислоты в модели совместного культивирования остеоартрита. Хрящевой артроз. 2006. 14 (8): 814–822. DOI: 10.1016 / j.joca.2006.02.006. [PubMed] [CrossRef] [Google Scholar] 28. Гришко В., Сюй М., Хо Р., Мейтс А., Уотсон С., Ким Дж. Т. и др. Влияние гиалуроновой кислоты на функцию митохондрий и митохондриальный апоптоз после окислительного стресса в хондроцитах человека.J Biol Chem. 2009. 284 (14): 9132–9139. DOI: 10.1074 / jbc.M804178200. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 29. Хашизуме М., Михара М. Желаемый эффект комбинированной терапии с высоким молекулярным гиалуронатом и НПВП на продукцию ММП. Хрящевой артроз. 2009. 17 (11): 1513–1518. DOI: 10.1016 / j.joca.2009.04.018. [PubMed] [CrossRef] [Google Scholar] 30. Homandberg GA, Hui F, Wen C, Kuettner KE, Williams JM. Гиалуроновая кислота подавляет хондролиз хряща, опосредованный фрагментом фибронектина: I. In vitro . Хрящевой артроз. 1997. 5 (5): 309–319. DOI: 10.1016 / S1063-4584 (97) 80035-0. [PubMed] [CrossRef] [Google Scholar] 31. Исидзима М., Накамура Т., Симидзу К., Хаяси К., Кикучи Х., Соен С. и др. Различные изменения биомаркера CTX-II после внутрисуставной инъекции высокомолекулярной гиалуроновой кислоты и пероральных нестероидных противовоспалительных препаратов для пациентов с остеоартрозом коленного сустава: многоцентровое рандомизированное контролируемое исследование. Osteoarthr Cartil. 2013; 21: S292. DOI: 10.1016 / j.joca.2013.02.612. [CrossRef] [Google Scholar] 32. Джулови С.М., Ясуда Т., Шимицу М., Хирамицу Т., Накамура Т. Ингибирование индуцированного интерлейкином-1бета продукции матриксных металлопротеиназ гиалуронаном через CD44 в суставном хряще человека. Ревматоидный артрит. 2004. 50 (2): 516–525. DOI: 10.1002 / art.20004. [PubMed] [CrossRef] [Google Scholar] 33. Kalaci A, Yilmaz HR, Aslan B, Sogut S, Yanat AN, Uz E. Влияние гиалуронана на уровни оксида азота и активность супероксиддисмутазы в синовиальной жидкости при остеоартрите коленного сустава.Clin Rheumatol. 2007. 26 (8): 1306–1311. DOI: 10.1007 / s10067-006-0504-у. [PubMed] [CrossRef] [Google Scholar] 34. Карна Э., Милтык В, Суразинский А, Палка Я. Защитный эффект гиалуроновой кислоты на индуцированную интерлейкином-1 дерегуляцию передачи сигналов рецептора бета1-интегрина и инсулиноподобного фактора роста-I и биосинтез коллагена в культивируемых хондроцитах человека. Mol Cell Biochem. 2008. 308 (1-2): 57–64. DOI: 10.1007 / s11010-007-9612-5. [PubMed] [CrossRef] [Google Scholar] 35. Кобаяши К., Амиэль М., Харвуд Флорида, Хили Р.М., Сонода М., Мория Х. и др.Долгосрочные эффекты гиалуронана во время развития остеоартрита после частичной менискэктомии на модели кролика. Хрящевой артроз. 2000. 8 (5): 359–365. DOI: 10.1053 / joca.1999.0310. [PubMed] [CrossRef] [Google Scholar] 36. Кога Х. Действие гиалуроновой кислоты на суставной хрящ, пораженный артритом. Connect Tissue Res. 2012; 53 (1): 48–93. DOI: 10.3109 / 03008207.2011.637147. [CrossRef] [Google Scholar] 37. Лазаро Дж., Гранадо П., дель Соль Дж., Медина А., Гальего Л., Сандовал Д., Фернандес Дж. Роль различных гиалуроновых кислот в суставном хряще кролика.Открытая Ортопедия J. 2010; 4: 44–47. DOI: 10,2174 / 1874325001004010044. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 38. Ли Дж., Горски Д. Д., Анемает В., Веласко Дж., Такеучи Дж., Сэнди Дж. Д. и др. Инъекция гиалуронана при остеоартрите мышей предотвращает индуцированную TGFbeta 1 синовиальную неоваскуляризацию и фиброз и поддерживает целостность суставного хряща посредством CD44-зависимого механизма. Arthritis Res Ther. 2012; 14 (3): R151. DOI: 10.1186 / ar3887. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 39.Ли П., Райчева Д., Хавс М., Моран Н., Ю Икс, Ван Ф. и др. Hylan G-F 20 поддерживает целостность хряща и снижает образование остеофитов при остеоартрите за счет как анаболических, так и антикатаболических механизмов. Хрящевой артроз. 2012. 20 (11): 1336–1346. DOI: 10.1016 / j.joca.2012.07.004. [PubMed] [CrossRef] [Google Scholar] 40. Лисиньоли Г., Грасси Ф., Зини Н., Тонегуцци С., Пьячентини А., Гуидолин Д. и др. Анти-Fas-индуцированный апоптоз в хондроцитах, сниженный гиалуронаном: свидетельство инвазии CD44 и CD54 (молекула межклеточной адгезии 1).Ревматоидный артрит. 2001. 44 (8): 1800–1807. DOI: 10.1002 / 1529-0131 (200108) 44: 8 <1800 :: AID-ART317> 3.0.CO; 2-1. [PubMed] [CrossRef] [Google Scholar] 41. Lu HT, Sheu MT, Lin YF, Lan J, Chin YP, Hsieh MS и др. Инъекционная терапия гидрогелем доксициклина гиалуроновой кислоты при экспериментальном остеоартрите кроликов. BMC Vet Res. 2013; 9: 68. DOI: 10.1186 / 1746-6148-9-68. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 42. Манейро Э., де Андрес М.С., Фернандес-Суэйро Ю.Л., Гальдо Ф., Бланко Ф.Дж. Биологическое действие гиалуронана на суставные хондроциты остеоартрита человека: важность молекулярной массы.Clin Exp Rheumatol. 2004. 22 (3): 307–312. [PubMed] [Google Scholar] 43. Михара М., Хашизуме М. Влияние высокомолекулярной гиалуроновой кислоты на индукцию ферментов деградации матрикса IL-6, IL-1β и TNF-α Osteoarthr Cartil. 2012; 20: S134 – S135. DOI: 10.1016 / j.joca.2012.02.181. [CrossRef] [Google Scholar] 44. Мики Ю., Терамура Т., Томияма Т., Онодера Ю., Мацуока Т., Фукуда К. и др. Гиалуронан обратил синтез протеогликанов, подавленный механическим стрессом: возможное участие антиоксидантного эффекта.Inflamm Res. 2010. 59 (6): 471–477. DOI: 10.1007 / s00011-009-0147-у. [PubMed] [CrossRef] [Google Scholar] 45. Младенович З., Заурел А.С., Беренбаум Ф., Жак С. Потенциальная роль гиалуроновой кислоты в костях при остеоартрите: матриксные металлопротеиназы, агреканазы и экспрессия RANKL частично предотвращаются гиалуроновой кислотой в остеобластах, стимулированных интерлейкином-1. J Rheumatol. 2014. 41 (5): 945–954. DOI: 10.3899 / jrheum.130378. [PubMed] [CrossRef] [Google Scholar] 46. Mongkhon JM, Thach M, Shi Q, Fernandes JC, Fahmi H, Benderdour M.Гиалуроновая кислота, модифицированная сорбитом, снижает окислительный стресс, апоптоз и медиаторов воспаления и катаболизма в хондроцитах человека, страдающих остеоартритом. Inflamm Res. 2014; 63 (8): 691–701. DOI: 10.1007 / s00011-014-0742-4. [PubMed] [CrossRef] [Google Scholar] 47. Оно S, Im HJ, Knudson CB, Knudson W. Индуцированная гиалуронановым олигосахаридом активация факторов транскрипции в суставных хондроцитах крупного рогатого скота. Ревматоидный артрит. 2005. 52 (3): 800–809. DOI: 10.1002 / art.20937. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 48.Peng H, Zhou JL, Liu SQ, Hu QJ, Ming JH, Qiu B. Гиалуроновая кислота ингибирует апоптоз, вызванный оксидом азота, и дедифференцировку суставных хондроцитов in vitro . Inflamm Res. 2010. 59 (7): 519–530. DOI: 10.1007 / s00011-010-0156-х. [PubMed] [CrossRef] [Google Scholar] 49. Плаас А., Ли Дж., Риеско Дж., Дас Р., Сэнди Дж. Д., Харрисон А. Внутрисуставная инъекция гиалуронана предотвращает эрозию хряща, периартикулярный фиброз и механическую аллодинию и нормализует время пребывания в стойке при остеоартрите коленного сустава у мышей.Arthritis Res Ther. 2011; 13 (2): R46. DOI: 10.1186 / ar3286. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 50. Цю Б., Лю С. К., Пэн Х. Влияние гиалуроната натрия на экспрессию iNOS в синовиальной оболочке и содержание NO в синовиальной жидкости кроликов с травматическим остеоартритом. Chin J Traumatol. 2008. 11 (5): 293–296. DOI: 10.1016 / S1008-1275 (08) 60059-0. [PubMed] [CrossRef] [Google Scholar] 51. Сакакибара Ю., Миура Т., Ивата Х, Кикучи Т., Ямагути Т., Йошими Т. и др. Влияние высокомолекулярного гиалуроната натрия на иммобилизованное колено кролика.Clin Orthop Relat Res. 1994; 299: 282–292. [PubMed] [Google Scholar] 52. Сасаки А., Сасаки К., Конттинен Ю.Т., Сантавирта С., Такахара М., Такей Х. и др. Гиалуронат подавляет индуцированную интерлейкином-1бета экспрессию матриксной металлопротеиназы (MMP) -1 и MMP-3 в синовиальных клетках человека. Tohoku J Exp Med. 2004. 204 (2): 99–107. DOI: 10.1620 / tjem.204.99. [PubMed] [CrossRef] [Google Scholar] 53. Симидзу С., Йошиока М., Коуттс Р.Д., Харвуд Флорида, Кубо Т., Хирасава И. и др. Долгосрочные эффекты гиалуронана при экспериментальном остеоартрозе коленного сустава кролика.Хрящевой артроз. 1998. 6 (1): 1–9. DOI: 10.1053 / joca.1997.0086. [PubMed] [CrossRef] [Google Scholar] 54. Смит М.М., Торт М.А., Гош П., Скьявинато А., Рид Р.А., Литтл СВ. Значительная синовиальная патология в модели менискэктомии остеоартрита: модификация внутрисуставной гиалуроновой терапией. Ревматология (Оксфорд) 2008; 47 (8): 1172–1178. DOI: 10.1093 / ревматология / ken219. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 55. Смит М.М., Рассел А.К., Скьявинато А., Литтл CB. Гексадециламидное производное гиалуронана (HYMOVIS®) оказывает более благоприятное воздействие на хондроциты и синовиоциты человека, страдающие остеоартритом, чем немодифицированный гиалуронан.Журнал Инфламм (Лондон) 2013; 10:26. DOI: 10.1186 / 1476-9255-10-26. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 56. Такахаши К., Гумер Р.С., Харвуд Ф., Кубо Т., Хирасава Й., Амиэль Д. Эффекты гиалуронана на матриксную металлопротеиназу-3 (ММР-3), интерлейкин-1бета (ИЛ-1бета) и тканевой ингибитор металлопротеиназы-1 ( Экспрессия гена ТИМП-1) при развитии остеоартрита. Хрящевой артроз. 1999. 7 (2): 182–190. DOI: 10.1053 / joca.1998.0207. [PubMed] [CrossRef] [Google Scholar] 57.Такахаши К., Хашимото С., Кубо Т., Хирасава Ю., Лотц М., Амиэль Д. Гиалуронан подавлял выработку оксида азота в мениске и синовиальной оболочке модели остеоартрита кролика. J Orthop Res. 2001. 19 (3): 500–503. DOI: 10.1016 / S0736-0266 (00)
-X. [PubMed] [CrossRef] [Google Scholar] 58. Танака М., Масуко-Хонго К., Като Т., Нисиока К., Накамура Х. Подавляющее действие гиалуронана на продукцию MMP-1 и RANTES хондроцитами. Rheumatol Int. 2006. 26 (3): 185–190. DOI: 10.1007 / s00296-004-0547-9. [PubMed] [CrossRef] [Google Scholar] 59.Уодделл Д.Д., Коломыткин О.В., Данн С, Марино А.А. Гиалуронан подавляет активность металлопротеиназы, индуцированную IL-1beta, в синовиальной ткани. Clin Orthop Relat Res. 2007; 465: 241–248. [PubMed] [Google Scholar] 60. Ясуда Т. Активация ядерного фактора-kappaB пептидом коллагена II типа в суставных хондроцитах: его ингибирование гиалуронаном через рецепторы. Мод Ревматол. 2013. 23 (6): 1116–1123. DOI: 10.3109 / s10165-012-0804-9. [PubMed] [CrossRef] [Google Scholar] 61. Ясуи Т., Акацука М., Тобетто К., Хаяиси М., Андо Т.Влияние гиалуронана на индуцированную интерлейкином-1 альфа продукцию простагландина E2 в синовиальных клетках остеоартрита человека. Действия агентов. 1992. 37 (1-2): 155–156. DOI: 10.1007 / BF01987905. [PubMed] [CrossRef] [Google Scholar] 62. Ятабэ Т., Мочизуки С., Такидзава М., Чидзива М., Окада А., Кимура Т. и др. Гиалуронан подавляет экспрессию ADAMTS4 (аггреканазы-1) в хондроцитах человека, страдающих остеоартритом. Ann Rheum Dis. 2009. 68 (6): 1051–1058. DOI: 10.1136 / ard.2007.086884. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 63.Йошими Т., Кикучи Т., Обара Т., Ямагути Т., Сакакибара Ю., Ито Х. и др. Влияние высокомолекулярного гиалуроната натрия на экспериментальный остеоартроз, вызванный резекцией передней крестообразной связки кролика. Clin Orthop Relat Res. 1994; 298: 296–304. [PubMed] [Google Scholar] 64. Йошиока М., Симидзу С., Харвуд Флорида, Куттс Р.Д., Амиэль Д. Эффекты гиалуронана во время развития остеоартрита. Хрящевой артроз. 1997. 5 (4): 251–260. DOI: 10.1016 / S1063-4584 (97) 80021-0. [PubMed] [CrossRef] [Google Scholar] 65.Yu CJ, Ko CJ, Hsieh CH, Chien CT, Huang LH, Lee CW и др. Протеомный анализ хондроцитов, страдающих остеоартритом, выявляет регулируемые гиалуроновой кислотой белки, участвующие в хондропротекторном эффекте при окислительном стрессе. J Proteomics. 2014; 99: 40–53. DOI: 10.1016 / j.jprot.2014.01.016. [PubMed] [CrossRef] [Google Scholar] 66. Zhang FJ, Gao SG, Cheng L, Tian J, Xu WS, Luo W. и др. Влияние гиалуроновой кислоты на остеопонтин и мРНК CD44 фибробластоподобных синовиоцитов у пациентов с остеоартрозом коленного сустава.Rheumatol Int. 2013. 33 (1): 79–83. DOI: 10.1007 / s00296-011-2339-3. [PubMed] [CrossRef] [Google Scholar] 67. Zhou JL, Liu SQ, Qiu B, Hu QJ, Ming JH, Peng H. Защитный эффект гиалуроната натрия на хрящ от остеоартрита кроликов путем ингибирования экспрессии рецепторной гамма-матричной РНК, активируемой пролифератором пероксисом. Йонсей Мед Дж. 2009; 50 (6): 832–837. DOI: 10.3349 / ymj.2009.50.6.832. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 68. Чжоу PH, Лю С.К., Пэн Х. Эффект гиалуроновой кислоты на индуцированный IL-1beta апоптоз хондроцитов в модели остеоартрита на крысах.J Orthop Res. 2008. 26 (12): 1643–1648. DOI: 10.1002 / jor.20683. [PubMed] [CrossRef] [Google Scholar] 69. Уильямс Дж. Эффекты гиалуроновой кислоты на хондролиз хряща, опосредованный фибронектиновым фрагментом, у скелетно зрелых кроликов. Osteoarthr Cartil. 2003. 11 (1): 44–49. DOI: 10.1053 / joca.2002.0864. [PubMed] [CrossRef] [Google Scholar] 70. Сюй Х., Ито Т., Тавада А., Маеда Х., Яманокучи Х., Исахара К. и др. Влияние олигосахаридов гиалуронана на экспрессию белка теплового шока 72. J Biol Chem. 2002. 277 (19): 17308–17314.DOI: 10.1074 / jbc.M112371200. [PubMed] [CrossRef] [Google Scholar] 71. Чжоу J-L, Лю С.-Q, Цю Б., Ху Q-J, Мин J-H, Пэн Х. Влияние гиалуронана на фактор роста эндотелия сосудов и экспрессию рецептора-2 на модели остеоартрита кроликов. J Orthop Sci. 2009. 14 (3): 313–319. DOI: 10.1007 / s00776-009-1329-8. [PubMed] [CrossRef] [Google Scholar] 72. Хуанг Т.Л., Сюй ХК, Ян К.С., Яо СН, Линь Ф.Х. Влияние гиалуронанов разной молекулярной массы на продукцию белка, связанного с остеоартритом, в фибробластоподобных синовиоцитах пациентов с переломом плато большеберцовой кости.J Trauma. 2010. 68 (1): 146–152. DOI: 10.1097 / TA.0b013e3181a92cf8. [PubMed] [CrossRef] [Google Scholar] 73. Амиэль Д., Тойогучи Т., Кобаяши К., Боуден К., Амиэль М.Э., Хили Р.М. Долгосрочный эффект гиалуроната натрия (Hyalgan) на прогрессирование остеоартрита на модели кролика. Остеоартроз и хрящи / OARS, Osteoarthritis Res Soc. 2003. 11 (9): 636–643. DOI: 10.1016 / S1063-4584 (03) 00119-5. [PubMed] [CrossRef] [Google Scholar] 74. Ким NH, Хан CD, Ли ХМ, Ян И.Х. Влияние гиалуроната натрия на профилактику остеоартрита.Йонсей Мед Дж. 1991; 32 (2): 139–146. DOI: 10.3349 / ymj.1991.32.2.139. [PubMed] [CrossRef] [Google Scholar] 75. Лю Дж., Сун В., Юань Т., Сюй З., Цзя В., Чжан С. Сравнение плазмы, обогащенной тромбоцитами (PRP), и гиалуроновой кислоты при заживлении дефектов хряща. PLoS One. 2014; 9 (5) DOI: 10.1371 / journal.pone.0097293. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 76. Михара М., Хиго С., Учияма Ю., Танабе К., Сайто К. Различные эффекты высокомолекулярного гиалуроната натрия и НПВП на прогрессирование дегенерации хряща в модели ОА кролика.Osteoarthritis Cartilage / OARS, Osteoarthritis Res Soc. 2007. 15 (5): 543–549. DOI: 10.1016 / j.joca.2006.11.001. [PubMed] [CrossRef] [Google Scholar] 77. Цю Б., Лю С.К., Пэн Х., Ван HB. Влияние гиалуроната натрия на экспрессию мРНК матриксной металлопротеиназы-1, -3 и тканевого ингибитора металлопротеиназы-1 в хряще и синовиальной оболочке модели травматического остеоартрита. Chin J Traumatol. 2005; 8 (1): 8–12. [PubMed] [Google Scholar] 78. Озкан Ф.У., Озкан К., Рамадан С., Гувен З. Хондропротекторный эффект N-ацетилглюкозамина и гиалуроната на ранних стадиях остеоартрита — экспериментальное исследование на кроликах.Bull NYU Hosp Jt Dis. 2009. 67 (4): 352–357. [PubMed] [Google Scholar] 79. Ян Л, Чжан Дж, Ван Г. Эффект гиалуроната натрия при лечении остеоартрита коленного сустава на интерлейкин-1бета синовиальной жидкости и механизм клинического лечения. Pak J Pharm Sci. 2015; 28 (1 приложение): 407–410. [PubMed] [Google Scholar] 80. Йошиока К., Ясуда И., Кисукеда Т., Нодера Р., Танака Ю., Миямото К. Фармакологические эффекты нового поперечно-сшитого гиалуроната, геля-200, в экспериментальных моделях остеоартрита на животных и клеточных линиях человека.Хрящевой артроз. 2014. 22 (6): 879–887. DOI: 10.1016 / j.joca.2014.04.019. [PubMed] [CrossRef] [Google Scholar] 81. Хуэй А.Ю., Маккарти В.Дж., Масуда К., Файрштейн Г.С., Сах Р.Л. Системно-биологический подход к смазке синовиальных суставов при здоровье, травмах и болезнях. Wiley Interdiscip Rev Syst Biol Med. 2012. 4 (1): 15–37. DOI: 10.1002 / wsbm.157. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 83. Асари А., Мияути С., Мацудзака С., Ито Т., Коминами Е., Учияма Ю. Эффекты гиалуроната, зависимые от молекулярного веса, на синовиальную оболочку артрита.Arch Histol Cytol. 1998. 61 (2): 125–135. DOI: 10.1679 / aohc.61.125. [PubMed] [CrossRef] [Google Scholar] 84. Багга Х, Буркхардт Д., Сэмбрук П., Марч Л. Долгосрочные эффекты внутрисуставного гиалуронана на синовиальную жидкость при остеоартрите коленного сустава. J Rheumatol. 2006; 33 (5): 946–950. [PubMed] [Google Scholar] 85. Бауэр Ч., Баумгартнер Р., Хорноф М., Хальбвирт Ф., Никулеску-Морца Э., Цвикл Х. и др. Каркасы из поперечно-сшитой гиалуроновой кислоты: потенциальное использование для регенерации хряща? Osteoarthr Cartil. 2013; 21: S312.DOI: 10.1016 / j.joca.2013.02.646. [CrossRef] [Google Scholar] 86. Форси Р., Фишер Дж., Томпсон Дж., Стоун М., Белл С., Ингхэм Э. Влияние смазок на основе гиалуроновой кислоты и фосфолипидов на трение в модели повреждения хряща человека. Биоматериалы. 2006. 27 (26): 4581–4590. DOI: 10.1016 / j.biomaterials.2006.04.018. [PubMed] [CrossRef] [Google Scholar] 87. Frean S, Abraham L, Lees P. In vitro стимуляция синтеза протеогликанов суставного хряща лошади гиалуронаном и карпрофеном.Res Vet Sci. 1999. 67: 181–188. DOI: 10.1053 / rvsc.1999.0328. [PubMed] [CrossRef] [Google Scholar] 88. Хан Ф, Исигуро Н., Ито Т., Сакаи Т., Ивата Х. Влияние гиалуроната натрия на экспериментальный остеоартрит в коленных суставах кролика. Med Sci. 1999; 62. [PubMed] 89. Хомандберг Г.А., Уммади В., Канг Х. Роль инсулиноподобного фактора роста-I в опосредованном гиалуронаном восстановлении культивируемых эксплантатов хряща. Inflamm Res. 2004; 53: 8. [PubMed] [Google Scholar] 90. Hulmes D. Внутрисуставной гиалуронат при экспериментальном остеоартрите кроликов может предотвратить изменения в содержании протеогликанов хряща.Osteoarthr Cartil. 2004. 12 (3): 232–238. DOI: 10.1016 / j.joca.2003.11.007. [PubMed] [CrossRef] [Google Scholar] 91. Канг Й., Эгер В., Кепп Х., Уильямс Дж. М., Кюттнер К. Э., Хомандберг Г. А.. Гиалуронан подавляет опосредованное фрагментом фибронектина повреждение культур эксплантата хряща человека за счет усиления синтеза протеогликана. J Orthop Res. 1999. 17 (6): 858–869. DOI: 10.1002 / jor.1100170611. [PubMed] [CrossRef] [Google Scholar] 92. Кикучи Т., Ямада Х., Фудзикава К. Влияние высокомолекулярного гиалуронана на распределение и движение протеогликана вокруг хондроцитов, культивируемых в альгинатных шариках.Osteoarthr Cartil. 2001. 9 (4): 351–356. DOI: 10.1053 / joca.2000.0395. [PubMed] [CrossRef] [Google Scholar] 93. Kobayashi K, Matsuzaka S, Yoshida Y, Miyauchi S, Wada Y, Moriya H. Влияние внутрисуставного введения гиалуроната натрия на уровни интактного аггрекана и оксида азота в суставной жидкости пациентов с остеоартрозом коленного сустава. Osteoarthr Cartil. 2004. 12 (7): 536–542. DOI: 10.1016 / j.joca.2004.03.005. [PubMed] [CrossRef] [Google Scholar] 94. Nishida Y, Knudson CB, Knudson W. Восстановление внеклеточного матрикса суставными хондроцитами человека после лечения гиалуронановыми гексасахаридами или гиалуронидазой Streptomyces.Мод Ревматол. 2003. 13 (1): 62–68. DOI: 10.3109 / s101650300009. [PubMed] [CrossRef] [Google Scholar] 95. Смит Г. Н., младший, Миклер Е. А., Майерс С. Л., Брандт К. Д.. Влияние внутрисуставной инъекции гиалуронана на гиалуронан в синовиальную жидкость на ранней стадии посттравматического остеоартрита у собак. J Rheumatol. 2001. 28 (6): 1341–1346. [PubMed] [Google Scholar] 96. Stove J, Gerlach C, Huch K, Gunther KP, Puhl W, Scharf HP. Влияние гиалуронана на содержание протеогликанов в хондроцитах при остеоартрите in vitro. J Orthop Res.2002. 20 (3): 551–555. DOI: 10.1016 / S0736-0266 (01) 00141-3. [PubMed] [CrossRef] [Google Scholar] 97. Wang C, Lin Y, Chiang B, Hou S. Высокомолекулярная гиалуроновая кислота подавляет экспрессию генов цитокинов и ферментов, связанных с остеоартритом, в фибробластоподобных синовиоцитах пациентов с ранним остеоартритом. Osteoarthr Cartil. 2006. 14 (12): 1237–1247. DOI: 10.1016 / j.joca.2006.05.009. [PubMed] [CrossRef] [Google Scholar] 98. Abatangelo G, Botti P, Del Bue M, Gei G, Samson JC, Cortivo R и др.Внутрисуставные инъекции гиалуроната натрия в экспериментальной модели остеоартрита Понд-Нуки у собак. I. Биохимические результаты. Clin Orthop Relat Res. 1989. 241: 278–285. [PubMed] [Google Scholar] 99. Асари А., Мизуно С., Танака И., Суносе А., Курияма С., Миядзаки К. и др. Подавление продукции гиалуронана и простагландина E2 в синовиальных клетках травматического артрита гиалуронатом натрия. Соединительная ткань. 1997; 29: 1–5. [Google Scholar] 100. Лисиньоли Г., Грасси Ф., Пьячентини А., Коккини Б., Ремидди Г., Бевилаква С. и др.Гиалуронан не влияет на экспрессию цитокинов и хемокинов в хондроцитах и синовиоцитах, пораженных остеоартритом. Хрящевой артроз. 2001. 9 (2): 161–168. DOI: 10.1053 / joca.2000.0372. [PubMed] [CrossRef] [Google Scholar] 101. Оливьеро Ф., Сканю А., Рамонда Р., Фраллонардо П., Сфризо П., Дайер Дж. И др. Механизмы, участвующие в подавлении воспаления в клетках THP-1 гексадециламидным производным гиалуроновой кислоты. Osteoarthr Cartil. 2014; 22: S292 – S293. DOI: 10.1016 / j.joca.2014.02.544. [CrossRef] [Google Scholar] 102.Сезгин М., Демирел А.Г., Караджа С., Ортанджил О, Юлкар Г.Б., Каник А. и др. Влияет ли гиалуронан на воспалительные цитокины при остеоартрите коленного сустава? Rheumatol Int. 2004. 25 (4): 264–269. DOI: 10.1007 / s00296-003-0428-7. [PubMed] [CrossRef] [Google Scholar] 103. Шихан К.М., Делотт Л.Б., Дэй С.М., Дехир Д.Х. Hyalgan® оказывает дифференцированное дозозависимое действие на пролиферацию макрофагов и гибель клеток. J Orthop Res. 2003. 21 (4): 744–751. DOI: 10.1016 / S0736-0266 (03) 00007-X. [PubMed] [CrossRef] [Google Scholar] 104. Ясуда Т.Гиалуронан ингибирует Akt, что приводит к подавлению регуляции ядерного фактора-каппаB в макрофагах U937, стимулированных липополисахаридами. J Pharmacol Sci. 2011. 115 (4): 509–515. DOI: 10.1254 / jphs.10244FP. [PubMed] [CrossRef] [Google Scholar] 105. Campo GM, Avenoso A, D’Ascola A, Prestipino V, Scuruchi M, Nastasi G и др. Ингибирование синтеза гиалуронана снижает воспалительную реакцию в синовиальных фибробластах мышей, подвергшихся индуцированному коллагеном артриту. Arch Biochem Biophys. 2012; 518 (1): 42–52. DOI: 10.1016 / j.abb.2011.12.005. [PubMed] [CrossRef] [Google Scholar] 106. Campo GM, Avenoso A, Nastasi G, Micali A, Prestipino V, Vaccaro M и др. Гиалуронан уменьшает воспаление при экспериментальном артрите, модулируя экспрессию в хряще TLR-2 и TLR-4. Biochim Biophys Acta. 2011; 1812 (9): 1170–1181. DOI: 10.1016 / j.bbadis.2011.06.006. [PubMed] [CrossRef] [Google Scholar] 107. Schumacher HR, Paul C, Hitchon CA, El-Gabalawy H, Zonay L., Clayburne G, et al. Воздействие гиалуроната на синовиальную оболочку и синовиальную жидкость. Проспективное слепое исследование пациентов с остеоартрозом коленного сустава.Хрящевой артроз. 2006. 14 (5): 501–503. DOI: 10.1016 / j.joca.2005.11.013. [PubMed] [CrossRef] [Google Scholar] 108. Белл CJ, Ingham E, Fisher J. Влияние гиалуроновой кислоты на зависящую от времени фрикционную реакцию суставного хряща в различных условиях. Proc Inst Mech Eng H. 2006; 220 (1): 23–31. DOI: 10.1243 / 095441105X69060. [PubMed] [CrossRef] [Google Scholar] 109. Гош П., Рид Р., Нумата Ю., Смит С., Армстронг С., Уилсон Д. Эффекты внутрисуставного введения гиалуронана на модели раннего остеоартрита у овец.II. Состав хряща и метаболизм протеогликанов. Semin Arthritis Rheum. 1993; 22 (6 Suppl 1): 31–42. DOI: 10.1016 / S0049-0172 (10) 80017-4. [PubMed] [CrossRef] [Google Scholar] 110. Обара Т., Мабучи К., Исо Т., Ямагути Т. Повышенное трение суставов животных путем экспериментальной дегенерации и восстановления путем добавления гиалуроновой кислоты. Clin Biomech (Бристоль, Эйвон) 1997; 12 (4): 246–252. DOI: 10.1016 / S0268-0033 (97) 00004-1. [PubMed] [CrossRef] [Google Scholar] 111. Уоллер К.А., Чжан Л.X., Флеминг Б.К., Джей Г.Д. Предотвращение апоптоза хондроцитов, вызванного трением: сравнение синовиальной жидкости человека и Hylan G-F 20.J Rheumatol. 2012. 39 (7): 1473–1480. DOI: 10.3899 / jrheum.111427. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 112. Yu L-P, Yang H, Voschin E, Skrabut E. Вязкоупругие свойства и молекулярная масса гилана G-F 20 по сравнению с другими коммерческими добавками для вязкости на основе гиалуронана. Osteoarthr Cartil. 2011; 19 (S1): S235. DOI: 10.1016 / S1063-4584 (11) 60535-9. [CrossRef] [Google Scholar] 114. Тан С.Ф., Чен С.П., Чен М.Дж., Пей Ю.К., Лау Ю.К., Леонг С.П. Изменения сил сагиттальной реакции опоры после внутрисуставных инъекций гиалуроната при остеоартрозе коленного сустава.Arch Phys Med Rehabil. 2004. 85 (6): 951–955. DOI: 10.1016 / j.apmr.2003.08.095. [PubMed] [CrossRef] [Google Scholar] 115. Армстронг С., Рид Р., Гош П. Эффекты внутрисуставного гиалуронана на изменения хряща и субхондральной кости в модели раннего остеоартрита у овец. J Rheumatol. 1994. 21 (4): 680–688. [PubMed] [Google Scholar] 116. Hiraoka N, Takahashi Y, Arai K, Honjo S, Nakawaga S, Tsuchida S и др. Гиалуронан и периодическое гидростатическое давление синергетически подавляли экспрессию MMP-13 и Il-6 в остеобластах субхондральной кости при остеоартрите.Osteoarthr Cartil. 2009; 17 (1): S97. DOI: 10.1016 / S1063-4584 (09) 60186-2. [CrossRef] [Google Scholar] 117. Hiraoka N, Takahashi KA, Arai Y, Sakao K, Mazda O, Kishida T и др. Внутрисуставная инъекция гиалуронана восстанавливает аберрантную экспрессию матриксной металлопротеиназы-13 в субхондральной кости, пораженной остеоартритом. J Orthop Res. 2011. 29 (3): 354–360. DOI: 10.1002 / jor.21240. [PubMed] [CrossRef] [Google Scholar] 118. Prasadam I, Crawford R, Xiao Y. Обострение ADAMTS и продукции матриксной металлопротеиназы и роль пути ERK1 / 2 во взаимодействии остеоартрита субхондральных костных остеобластов и хондроцитов суставного хряща — возможная патогенная роль при остеоартрите.J Rheumatol. 2012. 39 (3): 621–634. DOI: 10.3899 / jrheum.110777. [PubMed] [CrossRef] [Google Scholar] 119. Boettger MK, Kummel D, Harrison A, Schaible HG. Оценка долгосрочных антиноцицептивных свойств препарата стабилизированной гиалуроновой кислоты (NASHA) на животной модели повторяющейся боли в суставах. Arthritis Res Ther. 2011; 13 (4): R110. DOI: 10.1186 / ar3394. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 120. Гомис А., Мираллес А., Шмидт Р.Ф., Бельмонте С. Внутрисуставные инъекции растворов гиалуронана разной эластовязкости снижают активность ноцицептивного нерва на модели остеоартрита коленного сустава морской свинки.Osteoarthr Cartil. 2009. 17 (6): 798–804. DOI: 10.1016 / j.joca.2008.11.013. [PubMed] [CrossRef] [Google Scholar] 121. Гото С., Оная Дж., Абэ М., Миядзаки К., Хамай А., Хори К. и др. Влияние молекулярной массы гиалуроновой кислоты и механизмов ее действия на экспериментальную боль в суставах у крыс. Ann Rheum Dis. 1993. 52 (11): 817–822. DOI: 10.1136 / ard.52.11.817. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 122. Pena Ede L, Sala S, Rovira JC, Schmidt RF, Belmonte C. Эластовязкие вещества с обезболивающим действием при боли в суставах снижают активность ионных каналов, активируемых растяжением, in vitro.Боль. 2002. 99 (3): 501–508. DOI: 10.1016 / S0304-3959 (02) 00260-9. [PubMed] [CrossRef] [Google Scholar] 123. Дугадос М. Терапия гиалуронатом натрия при остеоартрите: аргументы в пользу потенциального положительного структурного эффекта. Semin Arthritis Rheum. 2000; 30 (2 Suppl 1): 19–25. DOI: 10.1053 / sarh.2000.0246. [PubMed] [CrossRef] [Google Scholar] 124. Балаш Э.А., Денлингер Ж.Л. Вязкие добавки: новая концепция лечения остеоартрита. J Rheumatol Suppl. 1993; 39: 3–9. [PubMed] [Google Scholar] 125. Карбовник М.С., Новак Ю.З.Гиалуронан: к новым противораковым препаратам. Pharmacol Rep., 2013; 65 (5): 1056–1074. DOI: 10.1016 / S1734-1140 (13) 71465-8. [PubMed] [CrossRef] [Google Scholar] 126. Фахари А., Беркланд С. Применение и новые тенденции применения гиалуроновой кислоты в тканевой инженерии, в качестве кожного наполнителя и при лечении остеоартрита. Acta Biomater. 2013; 9 (7): 7081–7092. DOI: 10.1016 / j.actbio.2013.03.005. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
127. Harris E, Weigel PH. Функциональные аспекты рецепторов гиалуроновой кислоты и хондроитина сульфата.В: Raton B, ed: CRC Press; 2009: 171–192.
128. Гош П., Гуидолин Д. Возможный механизм действия внутрисуставной гиалуроновой терапии при остеоартрите: зависят ли эффекты от молекулярной массы? Semin Arthritis Rheum. 2002. 32 (1): 10–37. DOI: 10.1053 / sarh.2002.33720. [PubMed] [CrossRef] [Google Scholar] 130. Камениш Т.Д., Макдональд Дж. А. Гиалуронан: больше лучше? Am J Respir Cell Mol Biol. 2000. 23 (4): 431–433. DOI: 10.1165 / ajrcmb.23.4.f201. [PubMed] [CrossRef] [Google Scholar] 131. Мизрахи С., Раз С.Р., Хасгаард М., Лю Х., Соффер-Цур Н., Коэн К. и др.Наночастицы, покрытые гиалуроновой оболочкой: влияние молекулярной массы на взаимодействия CD44-гиалуронана и на иммунный ответ. J Control Release. 2011. 156 (2): 231–238. DOI: 10.1016 / j.jconrel.2011.06.031. [PubMed] [CrossRef] [Google Scholar] 132. Jevsevar DS, Jones DL, Matzkin EG, Manner PA, Mooar P, Schousboe JT, et al. Американская академия хирургов-ортопедов. Лечение остеоартроза коленного сустава: руководство, основанное на доказательствах, 2-е издание. JBJS. 2013. 95 (20): 1885–1886. [PubMed] [Google Scholar] 133.Ли ПБ, Ким Ю.С., Лим Й.Дж., Ли СиДжей, Сим У.С., Ха Ч.В. и др. Сравнение гиалуронатов с высокой и низкой молекулярной массой у пациентов с остеоартритом коленного сустава: открытое рандомизированное многоцентровое клиническое исследование. J Int Med Res. 2006. 34 (1): 77–87. DOI: 10.1177 / 147323000603400110. [PubMed] [CrossRef] [Google Scholar] 134. Киршнер М., Маршалл Д. Двойное слепое рандомизированное контролируемое исследование по сравнению альтернативных форм высокомолекулярного гиалуронана для лечения остеоартрита коленного сустава. Osteoarthr Cartil.2006. 14 (2): 154–162. DOI: 10.1016 / j.joca.2005.09.003. [PubMed] [CrossRef] [Google Scholar] 135. Чен А.Л., Десаи П., Адлер Э.М., Ди Чезаре ЧП. Гранулематозное воспаление после вискозиметрии колена Hylan G-F 20: отчет о шести случаях. J Bone Joint Surg Am. 2002; 84-А (7): 1142–1147. [PubMed] [Google Scholar] 136. Зардави И.М., Чан И. Синвисковидный перисиновит. Патология. 2001. 33 (4): 519–520. DOI: 10.1080 / 00313020120083296. [PubMed] [CrossRef] [Google Scholar]
Механизм действия гиалуроновой кислоты при остеоартрите коленного сустава: систематический обзор
BMC Musculoskelet Disord.2015; 16: 321.
, , , , и
RD Altman
Отдел ревматологии и иммунологии Медицинской школы Дэвида Геффена Калифорнийского университета в Лос-Анджелесе, 1000 ветеранов Ave,
Лос-Анджелес, Калифорния, США
A. Manjoo
Отделение ортопедии, Университет Макмастера, Гамильтон, Канада
A. Fierlinger
Ferring Pharmaceuticals Inc., Парсиппани, штат Нью-Джерси, США
F. Niazi
Ferring Pharmaceuticals Inc., Парсиппани, штат Нью-Джерси, США
М. Николлс
Кентукки Ортопедические хирурги и хирурги кистей рук, Подразделение Ortho Kentucky, Лексингтон,
США
Отделение ревматологии и иммунологии, Медицинская школа Дэвида Геффена, Калифорнийский университет в Лос-Анджелесе, 1000 Veterans Ave,
Лос-Анджелес, Калифорния, США
Отделение ортопедии, Университет Макмастера, Гамильтон, Канада
Ferring Pharmaceuticals Inc., Парсиппани, штат Нью-Джерси, США
Кентукки Ортопедические хирурги и хирурги кистей рук, отделение Ortho Kentucky, Лексингтон, штат Кентукки, США
Автор, отвечающий за переписку.
Поступило 12 августа 2015 г .; Принято 15 октября 2015 г.
Открытый доступ Эта статья распространяется в соответствии с условиями Международной лицензии Creative Commons Attribution 4.0 (http://creativecommons.org/licenses/by/4.0/), которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии вы должным образом указываете первоначального автора (авторов) и источник, предоставляете ссылку на лицензию Creative Commons и указываете, были ли внесены изменения.Отказ Creative Commons Public Domain Dedication (http://creativecommons.org/publicdomain/zero/1.0/) распространяется на данные, представленные в этой статье, если не указано иное. Эта статья цитируется в других статьях PMC.
Abstract
Предпосылки
Остеоартроз коленного сустава (ОА) является одной из основных причин инвалидности среди взрослого населения. Текущие варианты лечения ОА коленного сустава включают внутрисуставную (IA) гиалуроновую кислоту (HA), молекулу, которая находится внутри коленного сустава, которая обеспечивает вязкоупругие свойства синовиальной жидкости.В современной базовой литературе описаны различные механизмы, с помощью которых ГК борется с остеоартритом коленного сустава.
Методы
Мы провели всесторонний поиск литературы, чтобы определить доступные в настоящее время первичные доклинические фундаментальные научные статьи, посвященные механизму действия лечения IA-HA. Включенные статьи были оценены и распределены по категориям на основе описанного в них механизма действия. Основные результаты и выводы из каждой включенной статьи были получены и проанализированы в совокупности с исследованиями того же категориального задания.
Результаты
Хондрозащита была наиболее частым механизмом, о котором сообщалось во включенных статьях, за ней следуют синтез протеогликанов и гликозаминогликанов, противовоспалительное, механическое, субхондральное и обезболивающее действие. Связывание рецептора HA-кластера дифференцировки 44 (CD44) было наиболее часто упоминаемой биологической причиной представленных механизмов. Было обнаружено, что ГК с высоким молекулярным весом превосходит продукты ГК с более низким молекулярным весом. ГК, полученная в процессе биологической ферментации, также описывается как имеющая более благоприятные результаты безопасности по сравнению с продуктами ГК птичьего происхождения.
Выводы
Доклиническая фундаментальная научная литература предоставляет доказательства многочисленных механизмов, с помощью которых ГК действует на структуры и функции суставов. Эти действия подтверждают предполагаемую клиническую пользу IA-HA при остеоартрите коленного сустава. Дальнейшие исследования должны быть сосредоточены не только на обезболивании, обеспечиваемом лечением IA-HA, но и на свойствах модификации заболевания, которыми обладает этот метод лечения.
Ключевые слова: Остеоартрит, Гиалуроновая кислота, Терапия, Внутрисуставная терапия, Систематический обзор, Механизм действия
Предпосылки
Хотя остеоартрит (ОА) коленного сустава чаще всего является медленно прогрессирующим заболеванием суставов, он является одним из ведущие причины инвалидности взрослого населения [1].ОА коленного сустава, заболевание всего сустава, характеризуется болью в суставах, дегенерацией хряща и увеличением инвалидности [2]. Прогрессирующий характер ОА приводит к снижению функции коленного сустава, влияя на способность человека выполнять повседневную деятельность [3]. ОА коленного сустава также негативно влияет на социально-экономические факторы, поскольку связанная с этим инвалидность часто приводит к снижению производительности труда и раннему выходу на пенсию [4].
Поскольку не существует установленного агента, модифицирующего заболевание при ОА, существует множество вариантов лечения ОА коленного сустава.Среди фармакологических методов лечения чаще всего назначают нестероидные противовоспалительные препараты (НПВП) и внутрисуставные (IA) инъекции кортикостероидов [5]. Этим вариантам присущи ограничения, так как НПВП имеют потенциально серьезные побочные эффекты, связанные с их использованием [6], а инъекции кортикостероидов IA часто обеспечивают относительно короткий период эффективного облегчения [7]. Хотя инъекция кортикостероидов обычно имеет положительный профиль безопасности, было показано, что она вызывает временное повышение уровня глюкозы в крови, что может вызывать беспокойство у пациентов с диабетом [8].IA инъекция гиалуроновой кислоты (HA) — еще один вариант лечения боли при остеоартрите коленного сустава. ГК почти повсеместно присутствует в организме и представляет собой молекулу, которая находится внутри коленного сустава, где она придает вязкоупругие свойства синовиальной жидкости [9]. По мере прогрессирования ОА естественная концентрация ГК и распределение ГК в суставе смещается в сторону более низких диапазонов молекулярной массы ГК, что приводит к деградации механических / вязкоупругих свойств эндогенной синовиальной жидкости [2, 10, 11]. Также было показано, что более низкие диапазоны молекулярно-массового распределения сильно коррелируют с болью [11].Назначение IA-HA было направлено на восстановление этого снижения концентрации HA и среднего молекулярно-массового распределения внутри OA колена [9].
IA-HA, как предполагалось, обладает множеством терапевтических механизмов действия в коленном суставе с остеоартритом, включая поглощение ударов, смазку суставов, противовоспалительные эффекты, хондрозащиту, синтез протеогликанов и изменения хрящевого матрикса [2]. Корреляция между этими различными эффектами позволила лучше понять, как лечение IA-HA может оказывать терапевтический эффект для пациентов с остеоартритом коленного сустава [12].Имеются также данные, свидетельствующие о различиях в механизмах действия продуктов НА разной молекулярной массы. То есть ГК с более высокой молекулярной массой (HMW), как сообщается, обеспечивает более сильные противовоспалительные эффекты и эффекты синтеза протеогликанов, а также смазывание суставов и поддержание вязкоупругости [9, 13]. Также, по-видимому, существуют доказательства различных профилей безопасности между ГК, полученным в процессе биологической ферментации (Bio-HA), и ГК птичьего происхождения (AD-HA), поскольку AD-HA имеет потенциал для местных реакций IA [14, 15] .
Мы стремимся обобщить механизмы действия IA-HA лечения ОА коленного сустава, описанные в современной литературе, чтобы определить обоснованность вышеупомянутых механизмов действия. Мы будем систематически оценивать и обрисовывать определенные механизмы, с помощью которых ГК может оказывать терапевтическое действие, одновременно анализируя сообщаемые различия между эффектами лечения ИА-ГК, зависящими от характеристик продукта.
Методы
Поиск литературы
Мы провели всесторонний поиск литературы с использованием баз данных MEDLINE, EMBASE и PubMed (таблица).Поиск был проведен 4 мая -го , 2014. Критерии включения, соблюдаемые на протяжении всего процесса отбора, были следующими: 1) Статьи, описывающие механизм лечения ГК при ОА, 2) Статьи, посвященные ОА коленного сустава, и 3) Основные доклинические фундаментальные научные статьи, посвященные «добавлению вязкости» / лечению ГК. Статьи, которые были опубликованы до 1990 года или не были опубликованы на английском языке, были исключены из исследования. Если одним и тем же автором было опубликовано несколько исследований, содержащих похожие результаты, для включения принималось только самое последнее исследование.
Таблица 1
| MEDLINE и EMBASE — 1470 статей | PubMed — 1395 статей |
|---|---|
| 1. Гиалуроновая кислота [название] | 1. Гиалуроновая кислота [название] |
| 2. Hylan [title] | |
| 3. Гиалуронан [title] | 3. Гиалуронан [title] |
| 4. Добавки для вязкости [title] | 4. Добавки для вязкости [title] | 5.1 или 2 или 3 или 4 | 5. 1 или 2 или 3 или 4 |
| 6. Остеоартрит * .mp | 6. Остеоартрит * |
| 7. Артрит * .mp | 7. Артрит * |
| 8. Боль в суставах.mp | 8. Боль в суставах |
| 9. 6 или 7 или 8 | 9. 6 или 7 или 8 |
| 10. Эффект * .mp | 10. Эффект * |
| 11. Механизм * .mp | 11. Механизм * |
| 12.10 или 11 | 12. 10 или 11 |
| 13. 5 и 9 и 12 | 13. 5 и 9 и 12 |
Абстракция данных
Включенные статьи были оценены и классифицированы на основе механизма действие, описанное в них. Отдельные статьи включались в несколько категорий, если они анализировали более одного механизма действия НА в рамках своего дизайна исследования. Категории механизмов, использованные в процессе извлечения данных, включали: хондрозащиту, изменения синтеза протеогликана и / или гликозаминогликана (ГАГ), противовоспалительные эффекты, механические модификации, изменения в субхондральной кости и анальгетические эффекты.
Анализ данных
Ключевые выводы и заключения по каждой включенной статье были получены и проанализированы в совокупности с исследованиями той же присвоенной категории. Представленные результаты были получены путем интерпретации общего и последовательного механизма действия в рамках каждой вышеупомянутой категории.
Результаты
Стратегия поиска
Поиск литературы выявил 2782 потенциальных статьи, из которых 91 статья соответствовала критериям включения (рис.). Тринадцать дополнительных статей были извлечены специалистом по содержанию путем ручного поиска литературы. В результате было включено 104 статьи. Выводы и основные выводы каждой статьи были определены в рамках вышеупомянутых категорий механизмов (таблица).
Процесс проверки статей
Таблица 2
Ключевые механизмы действия, указанные во включенных статьях
| Механизм действия | Количество статей | % включенных статей | Ссылки | |
|---|---|---|---|---|
| Chondrotective | 67 | 64.42% | [9, 12, 16–80] | |
| Синтез протеогликанов / гликозаминогликанов | 22 | 21,15% | [27, 42, 44, 48, 62, 69, 83–98] | |
| Противовоспалительное | 21 | 20,19% | [13, 20, 21, 25, 27, 52, 54, 55, 68, 72, 96, 97, 99–107] | |
| Механический | 10 | 9,61% | [41, 49, 86, 108–114] | |
| Субхондральная кость | 8 | 7.69% | [23, 31, 32, 45, 115–118] | |
| Анальгетик | 6 | 5,76% | [76, 80, 119–122] |
Хондрозащита
Шестьдесят семь из включенных статей описывают хондрозащитные эффекты лечения IA-HA [9, 12, 16–80]. Было показано, что IA-HA снижает апоптоз хондроцитов, одновременно увеличивая пролиферацию хондроцитов [19, 20]. Существует множество наблюдаемых эффектов лечения IA-HA, которые вызывают хондрозащиту, многие из которых являются результатом связывания HA с рецепторами кластера дифференцировки 44 (CD44).Связывание HA с CD44 ингибирует экспрессию интерлейкина (IL) -1β, что приводит к снижению продукции матриксной металлопротеиназы (MMP) -1, 2, 3, 9 и 13 [32, 34]. Было показано, что это связывание с CD44 имеет больший эффект для продуктов HA с более высокой молекулярной массой [21]. HA также связывается с рецептором опосредованной гиалуронаном подвижности (RHAMM), который, как полагают, способствует хондропротекции в дополнение к связыванию с CD44 [34]. Ингибирование экспрессии IL-1β посредством связывания CD44 осуществляется посредством индукции митоген-активируемой протеинкиназы фосфатазы (MKP) -1: негативного регулятора IL-1β [43].Это ингибирование различных MMP препятствует активности катаболических ферментов в суставном хряще [59]. Было показано, что HMW HA имеет больший эффект в ингибирующем действии на продукцию MMP [21], хотя эти результаты неясны, поскольку другое исследование продемонстрировало благоприятный ингибирующий эффект MMP продуктов с более низкой молекулярной массой (LMW) [72].
События апоптоза хондроцитов дополнительно уменьшаются за счет связывания HA-CD44 за счет снижения экспрессии дезинтегрина и металлопротеиназы с тромбоспондиновыми мотивами (ADAMTS) [38].Эти пептидазы участвуют в расщеплении важных синовиальных компонентов, включая аггрекан, версикан и бревикан [81, 82]. Было показано, что различная экспрессия ADAMTS снижается в результате связывания HA-CD44, обеспечивая дополнительный режим хондропротекции для лечения IA-HA [36, 38, 43]. Производство активных форм кислорода (АФК), таких как оксид азота (NO), приводит к дегенерации хряща за счет увеличения апоптоза хондроцитов [33]. Лечение IA-HA продемонстрировало снижение индуцированного IL-1β окислительного стресса за счет ингибирования продукции NO в синовиальной оболочке [48, 57].Дополнительные результаты связывания CD44-HA, приводящие к хондропротекторным эффектам, упомянутые в современной литературе, включают снижение синтеза простагландина E2 (PGE2) [42, 46, 61] и повышенную сверхэкспрессию белка теплового шока 70 (Hsp70) [25, 70]. Эти эффекты аналогичным образом обеспечивают терапевтический эффект за счет уменьшения апоптоза хондроцитов. Важно отметить, что HMW продукты HA продемонстрировали большее подавление экспрессии PGE2, чем LMW компараторы в сравнительном исследовании, что привело к более сильному хондрозащитному эффекту [61].
Синтез протеогликанов и гликозаминогликанов
В 22 из идентифицированных исследований сообщалось об усилении синтеза протеогликанов и гликозаминогликанов, связанном с лечением IA-HA [27, 42, 44, 48, 62, 69, 83–98]. По мере прогрессирования ОА внутренние концентрации протеогликана и ГАГ в хряще снижаются. Результаты показали, что обработка IA-HA стимулировала синтез протеогликана, задерживая прогрессирование OA [69, 88]. Аггрекан является первичным протеогликаном в суставном хряще, и показано, что лечение IA-HA как подавляет деградацию аггрекана, так и способствует внутреннему развитию аггрекана [62, 93].Показано, что обработка IA-HA мобилизует вновь синтезированный протеогликан во внешний матрикс хондроцитов, потенциально обеспечивая защиту от деградации. Внешний HA способствует перемещению вновь синтезированного протеогликана из ассоциированного с клетками матрикса в далее удаленный матрикс в модели альгинатного геля, что предполагает, что IA-HA может обеспечивать терапевтическое облегчение OA за счет укрепления межтерриториального хрящевого матрикса [92]. Маркер синтеза протеогликана, сульфат ( 35 SO 4 ), как видно, все больше включается в хондроциты после введения HA [87].Биологический путь, в котором HA изменяет уровни аггрекана, проявляется через эффекты связывания CD44 и молекулы межклеточной адгезии (ICAM) -1 [62]. В одном исследовании было показано, что HMW HA обеспечивает больший эффект синтеза протеогликанов, чем LMW HA, за счет стимуляции пути инсулиноподобного фактора роста (IGF) -1 [89]. Также показано, что лечение IA-HA увеличивает выработку эндогенного ГАГ. Обработка IA-HA не только дополняла синовиальную оболочку HA, но и способствовала внутренней продукции HA [27].
Противовоспалительное
В 21 из идентифицированных исследований сообщалось о противовоспалительных эффектах лечения IA-HA [13, 20, 21, 25, 27, 52, 54, 55, 68, 72, 96, 97 , 99–107].Известно, что IL-1β демонстрирует провоспалительные эффекты, и вышеупомянутое подавление экспрессии IL-1β с помощью HA обеспечивает противовоспалительные эффекты [52]. IL-1β является ключевым медиатором противовоспалительного действия HA и регулируется посредством связывания HA-CD44 [59, 104]. Подавление IL-1β приводит к подавлению MMPs, как упоминалось ранее, что также способствует противовоспалительному эффекту HA [52]. Дальнейшее подавление провоспалительных медиаторов IL-8, IL-6, PGE 2 и фактора некроза опухоли (TNFα) обеспечивает противовоспалительные эффекты лечения IA-HA [13, 21].Связь между Toll-подобными рецепторами (TLR) и воспалительным ответом демонстрируется, поскольку продукты деградации HA индуцируют воспалительный ответ через взаимодействие CD44 и TLR. Этот провоспалительный ответ от связывания продукта деградации HA с рецепторами TLR и CD44 приводит к увеличению продукции Nf-kB, IL-1β, TNFα, IL-6 и IL-33 [105]. Было продемонстрировано, что HMW HA подавляет множество медиаторов воспаления посредством связывания TLR 2 и 4, включая TNF-α, IL-1-β, IL-17, MMP-13 и индуцибельную синтазу оксида азота (iNOS) [106].Прямая корреляция между молекулярной массой и противовоспалительным действием продемонстрировала более сильные эффекты ингибирования PGE 2 и IL-6 при лечении HMW HA [13]. IL-6 представляет собой провоспалительный цитокин, регулируемый ядерным фактором, энхансером легкой каппа-цепи активированных В-клеток (Nf-кB). Связывание HA с ICAM-1 подавляет Nf-kB, что, в свою очередь, снижает продукцию IL-6 [21, 104]. HMW HA, подавляющая регуляцию TNFα, IL-1B и IL-8, является дополнительным фактором, способствующим противовоспалительным эффектам, обеспечиваемым HMW HA [72, 97].
Механический
Десять из включенных исследований описывали механические эффекты ГК при лечении ОА коленного сустава [41, 49, 86, 108–114]. Показано, что вязкая природа лечения ГК смазывает суставную капсулу, предотвращая дегенерацию за счет снижения трения [86]. ГК дополнительно защищает капсулу сустава за счет благотворного эффекта поглощения ударов. HA обеспечивает амортизацию для поглощения давления и вибрации в суставе, которые в противном случае могут привести к деградации хондроцитов [41]. Сообщается, что колени с остеоартритом имеют более высокое трение в суставной щели, чем здоровые колени, чему противодействует способность суставной смазки, которой обладает HA [110].Было продемонстрировано, что HMW HA обеспечивает больший эффект снижения трения благодаря своим вязким свойствам. Уменьшение трения в суставе может обеспечить терапевтический эффект, поскольку хрящ защищен от механической деградации [111].
Субхондральная кость
Восемь из включенных исследований описали эффекты, которые IA-HA оказывает на субхондральную кость [23, 31, 32, 45, 115–118]. Ранее было показано, что взаимодействие между остеобластами субхондральной кости и хондроцитами суставного хряща в суставах с остеоартритом изменяет экспрессию ADAMTS-4/5 и MMP-1, MMP-2, MMP-3, MMP-8, MMP-9 и MMP-13. и регуляция, опосредованная митоген-активируемой протеинкиназой (MAPK) и сигнальными путями, регулируемыми внеклеточными сигналами киназ 1 и 2 (ERK 1/2) [118].IA-HA также влияет на субхондральную кость путем подавления MMP-13 и IL-6 через связывание CD44, что потенциально предотвращает аномальный метаболизм костной ткани [116]. Было высказано предположение, что подавление экспрессии MMP-13 с помощью IA-HA является критическим фактором воздействия на субхондральную кость при ОА [117]. Эффект, который IA-HA оказывает на MMPs, особенно MMP-13, посредством связывания CD44, как предполагалось, ингибирует эффекты OA в субхондральной кости в многочисленных доклинических фундаментальных научных исследованиях [32, 45, 116–118].ГК эффективно изменяет плотность и толщину субхондральной кости за счет изменений трабекулярной структуры, что приводит к большей податливости субхондральной кости. В конечном итоге показано, что это снижает нагрузку на хрящ во время ударной нагрузки [23]. Признаком стимуляции IA-HA обмена коллагена типа II на границе раздела хрящ и костей является повышение уровней сшивок коллагена на карбокси-конце (CTX) -II в моче, наблюдаемое после лечения IA-HA, которое продемонстрировало улучшение остеоартрита колена [31].В конечном итоге ГК, по-видимому, ограничивает изменения субхондральной кости, характерные для раннего ОА [115].
Анальгетик
Шесть из включенных статей описывают обезболивающие эффекты лечения IA-HA [76, 80, 119–122]. Одна инъекция ГК продемонстрировала значительное снижение связанного с болью поведения на мышиной модели [119]. Одно исследование показало, что HA не связывается напрямую с рецепторами брадикинина, но оказывает обезболивающее за счет взаимодействия с рецепторами HA и / или свободными нервными окончаниями в суставной ткани [121].Было показано, что обезболивающие эффекты HA проявляются в механочувствительных ионных каналах, активируемых растяжением, где активность канала значительно снижается при связывании HA [122]. Было показано, что HMW HA снижает механическую чувствительность ионных каналов, активируемых растяжением, которые эффективно блокируют болевой ответ. Было обнаружено, что LMW HA менее эффективен в блокировании этого ответа [122]. ГК снижает действие ноцицепторов суставов, что обеспечивает уменьшение боли в суставе. На сенсибилизированные ноцицептивные окончания в суставной ткани влияет концентрация HA, снижая болевую реакцию, проявляемую этими терминалами [120].
Обсуждение
Наш обзор существующей литературы дает общее мнение о том, что IA-HA при ОА коленного сустава имеет положительные эффекты через несколько механизмов действия; однако преобладающий механизм терапевтического эффекта не совсем ясен [2]. В перспективе неясно, какие из этих механизмов являются клинически значимыми, поскольку понятно, что полезные механизмы действия не обязательно переносятся на пользу в клинических условиях.В настоящее время предполагается, что клиническая польза IA-HA при ОА коленного сустава обусловлена несколькими параллельными механизмами действия, а не каким-либо одним конкретным механизмом действия.
Большая часть экзогенной ГК остается в суставе в течение нескольких дней; однако клинические терапевтические эффекты лечения ГК могут наблюдаться в течение 6 месяцев или более. Это может указывать на то, что IA-HA обладает свойствами, модифицирующими болезнь, и действует не только за счет восстановления вязкоупругих свойств синовиальной жидкости [123].Инъекции ГК могут стимулировать эндогенную продукцию дополнительной ГК синовиоцитами человека, способствуя нормализации распределения ГК в синовиальной жидкости [124]. В доклинических фундаментальных научных исследованиях во многих сообщениях описывается связывание CD44 как основной способ, при котором НА обеспечивает действие против ОА коленного сустава. Показано, что CD44-опосредованные эффекты IA-HA вносят вклад в потенциальную хондрозащиту, синтез протеогликанов / гликозаминогликанов, противовоспалительные и субхондральные механизмы. Показано, что это связывание оказывает разнообразные эффекты на многочисленные сигнальные пути, каждый из которых демонстрирует своего рода вмешательство в прогрессирование ОА [13, 21, 32, 36, 38, 42, 43, 46, 59, 61, 104 , 116].Было высказано предположение, что подавление IL-1β и IL-6 и последующие эффекты этого подавления являются ключевым фактором в терапевтическом механизме, обеспечиваемом связыванием HA-CD44 [123]. Очевидно, что связывание HA-CD44 является основным компонентом механизма, в котором HA обеспечивает терапевтический эффект; однако существуют дополнительные механизмы, которые обеспечивают альтернативные пути эффективности лечения ГК при ОА коленях, включая связывание ICAM, механические улучшения, связанные с поглощением удара и смазкой, увеличение обмена коллагена типа II на границе раздела хрящ / кость, а также анальгетические эффекты. через взаимодействие с нервными окончаниями и ноцицепторами суставов [31, 41, 86, 97, 121, 122].Связывание HA с рецептором RHAMM способствует заживлению ран, активирует функции промиграции и инвазии, регулирует клеточные ответы на факторы роста и играет роль в миграции и подвижности фибробластов [125–127]. Эти результаты связывания HA-RHAMM являются потенциальными факторами, участвующими в эффектах модификации заболевания при лечении HA при ОА.
Имеются данные, которые демонстрируют, что определенные внутренние свойства определенных продуктов IA-HA могут давать положительные результаты по сравнению с другими продуктами IA-HA.Наиболее известным из этих внутренних свойств является молекулярная масса. В отличие от предыдущего фундаментального научного обзора, проведенного Ghosh et al., Который предположил потенциальное преимущество LMW HA в обеспечении восстановления реологических свойств по сравнению с HMW HA [128], данные текущего обзора продемонстрировали благоприятные результаты для лечения HMW HA. Текущий обзор поддерживает точку зрения, что HMW HA обеспечивает превосходные хондропротекторные, протеогликановые и гликозаминогликановые механизмы синтеза, противовоспалительные, механические и обезболивающие механизмы действия [61, 89, 97, 111, 122].Исследование Huang et al. продемонстрировали превосходные противовоспалительные эффекты HMW HA, но лучшие хондрозащитные эффекты LMW HA; однако эти результаты относительно хондрозащиты неясны из-за отсутствия дополнительных доказательств в фундаментальной научной литературе по ОА коленного сустава [72]. Было показано, что повышенная продукция воспалительных цитокинов и хемокинов, привлечение медиаторов воспаления и образование кровеносных сосудов являются ответом на LMW HA ниже 500 кДа. Хотя средний молекулярный вес доступных продуктов ГК на рынке сильно различается, следует отметить, что, насколько нам известно, все доступные в настоящее время продукты во всем мире имеют молекулярную массу> 500 кДа [129, 130].Анализ взаимодействия HA-CD44 показал, что размер HA имеет прямое влияние на сродство, при котором HA связывается с рецептором CD44 [131]. Эти результаты демонстрируют способность HMW HA лечить прогрессирование ОА коленного сустава посредством связывания HA с CD44. Эти фундаментальные научные данные согласуются с систематическими обзорами клинических испытаний и сравнительных исследований, которые продемонстрировали, что HMW HA обеспечивает большую терапевтическую пользу, чем LMW HA при лечении ОА коленного сустава [6, 132], хотя текущая литература не обеспечивает консенсуса в отношении различие в клинической эффективности ГК с низким и высоким молекулярным весом [133].
Традиционно продукты ГК получали из птичьих источников; однако некоторые доступные продукты производятся путем биологической ферментации. Этот процесс позволяет избежать присутствия молекул птичьего происхождения, которые, как предполагается, могут быть потенциальной причиной неблагоприятных местных реакций [134]. Отсутствуют подробные отчеты о потенциале Bio-HA по сравнению с AD-HA. Одно исследование показало, что места инъекции AD-HA могут быть причиной синовита в их группе пациентов, но точный патологический агент неизвестен [135].Результаты второго исследования также указывают на способность гилана AD-HA вызывать гранулематозную реакцию типа гигантских клеток на инородное тело [136]. Исследования показали, что обострения, связанные с инъекцией гилана, могут быть связаны с накоплением гилана или продуктов его распада, поскольку обострения в месте инъекции обычно не возникают при первой инъекции [14]. Было показано, что белки птичьего происхождения являются причиной обострения в месте инъекции, поскольку антитела к белку куриной сыворотки присутствовали у пациентов, у которых наблюдалась неблагоприятная реакция в месте инъекции после лечения AD-HA [15].Имеются некоторые высококачественные клинические доказательства того, что Bio-HA имеет значительно меньшую частоту нежелательных явлений в месте инъекции, чем AD-HA [134]; однако в современной литературе это не исследовано досконально. Необходимо более всестороннее исследование разницы в частоте нежелательных явлений в месте инъекции между Bio-HA и AD-HA как с фундаментальной науки, так и с клинической точки зрения.
Этот обзор имеет методологическую силу благодаря систематическому и тщательному поиску доступных фундаментальных научных данных в нескольких базах данных.Текущий отчет также демонстрирует строгость в его представлении множественных механизмов, в которых действует HA, предоставляя доказательства обо всех механизмах, независимо от того, подробно или нечасто описаны в текущей литературе. Ограничения данного исследования возникают из-за субъективной классификации включенной статьи механизм действия основных выводов. Включенные статьи могут кратко упоминать альтернативные механизмы действия, но не были отнесены к соответствующей категории, потому что упомянутый альтернативный механизм не был ключевым результатом или заключением исследования.В будущих исследованиях следует проанализировать взаимосвязь между различными механизмами, представленными в этом отчете, и прояснить, как эти механизмы перекрываются и могут работать вместе для облегчения симптомов ОА коленного сустава. Дальнейшие исследования также должны быть направлены на выявление различий между механизмами, проявляемыми продуктами с высокой и низкой молекулярной массой, а также на анализ различий в профилях безопасности между Bio-HA и AD-HA.
Выводы
Доклиническая фундаментальная научная литература предоставляет доказательства многочисленных механизмов, с помощью которых IA-HA может обеспечить клиническую пользу при ОА коленного сустава.Хондропротекция является наиболее часто описываемым механизмом, причем связывание HA-CD44 является наиболее частым источником этих эффектов. Сообщается также, что IA-HA обеспечивает синтез протеогликанов и гликозаминогликанов, оказывает противовоспалительное, механическое, субхондральное и обезболивающее действие. Имеются данные о благоприятных результатах лечения HMW HA по сравнению с лечением LMW HA. Также показано, что Bio HA обеспечивает более выгодный профиль безопасности по сравнению с AD-HA, поскольку отчеты демонстрируют связь между обострениями в месте инъекции и белками птичьего происхождения.Существует множество описанных механизмов, в которых показано, что ИА-ГК лечит ОА коленного сустава, а также многочисленные характеристики продукта, которые влияют на результаты лечения ИА-ГК. Чтобы признать применимость и целесообразность лечения IA-HA для колено О.А. Дальнейшие исследования должны быть сосредоточены не только на обезболивании, обеспечиваемом лечением IA-HA, но и на свойствах модификации заболевания, которыми может обладать этот метод лечения.
Благодарности
Этот обзор финансируется Ferring Pharmaceuticals Inc. Авторы хотели бы поблагодарить Марка Филлипса и Global Research Solutions Inc. за их помощь в подготовке рукописи.
Аббревиатуры
| ADAMTS | Дезинтегрин и металлопротеиназа с тромбоспондиновыми мотивами | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| AD-HA | Гиалуроновая кислота птичьего происхождения | Биологическая кислота | Биологическая кислота | CD | Кластер дифференцировки | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CTX | Сшивки карбоксиконцевого коллагена | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ERK 1/2 | Киназа 1 и 2, регулируемая внеклеточным сигналом | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| GAG12122 90og3511 | Гиалуроновая кислота | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| HMW | Более высокая молекулярная масса | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hsp70 | Белок теплового шока 70 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| IA | Внутрисуставной | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| IL | Интерлейкин | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| iNOS | Индуцируемый оксид азота LMW, низкомолекулярный вес | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| MAPK | MAPK | Митоген-активированная протеинкиназа | 90sp MMP | Металлопротеиназа | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nf-кB | Ядерный фактор, усилитель легкой цепи каппа активированных В-клеток | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NO | Оксид азота | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 12 НПВП | OA | Остеоартрит | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PGE2 | Простагландин E2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| RHAMM | Рецептор для подвижности, опосредованной гиалуронаном |
Фут примечания
Конкурирующие интересы
Рой Д.Альтман: Консультант: Cytori, DuPuy (Bioventus Global), Ferring, Flexion, Iroko, McNeil, Novartis, Oletec, Pfizer, QMed, Rotta, Strategic Science and Technologies, Teva.
Спикер: Ферринг, Ироко.
Аджай Манджу: Нет конфликта интересов
Анке Фирлингер: оплачиваемый сотрудник Ferring Pharmaceuticals Inc.
Файзан Ниази: оплачиваемый сотрудник Ferring Pharmaceuticals Inc.
Мэтью Николлс: работает в консультативных советах Ferring.
Вклад авторов
AF и FN участвовали в разработке и разработке исследования. RDA обеспечило интерпретацию данных и внесение значительного письменного вклада в рукопись. Все авторы представили рукопись критическую рецензию и исправления. Все авторы прочитали и одобрили окончательную рукопись.
Ссылки
1. Cheng OT, Souzdalnitski D, Vrooman B, Cheng J. Доказательные инъекции в колено для лечения артрита. Pain Med.2012. 13 (6): 740–753. DOI: 10.1111 / j.1526-4637.2012.01394.x. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 2. Морленд Л.В. Внутрисуставной гиалуронан (гиалуроновая кислота) и гиланы для лечения остеоартрита: механизмы действия. Лечение артрита Res. 2003; 5 (2): 54. DOI: 10.1186 / ar623. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 3. Беллами Н., Кэмпбелл Дж., Робинсон В., Джи Т., Борн Р., Уэллс Г. Вискозиметрические добавки для лечения остеоартрита колена. Кокрановская база данных Syst Rev.2006; 2 [PubMed] [Google Scholar] 4. Тригкилидас Д., Ананд А. Эффективность внутрисуставных инъекций гиалуроновой кислоты при лечении боли в коленях при остеоартрите. Ann R Coll Surg Engl. 2013. 95 (8): 545–551. DOI: 10.1308 / rcsann.2013.95.8.545. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 5. Colen S, van den Bekerom MP, Mulier M, Haverkamp D. Гиалуроновая кислота в лечении остеоартрита коленного сустава: систематический обзор и метаанализ с упором на эффективность различных продуктов. BioDrugs.2012. 26 (4): 257–268. DOI: 10.1007 / BF03261884. [PubMed] [CrossRef] [Google Scholar] 6. Rutjes A, Juni P, da Costa B, Trelle S, Nuesch E, Reichenbach S. Viscosupplementation для остеоартрита коленного сустава: систематический обзор и метаанализ. Ann Intern Med. 2012; 157: 180–191. DOI: 10.7326 / 0003-4819-157-3-201208070-00473. [PubMed] [CrossRef] [Google Scholar] 7. Баннуру Р.Р., Натов Н.С., Обадан И.Е., Прайс Л.Л., Шмид С.Х., Макалиндон Т.Е. Терапевтическая траектория гиалуроновой кислоты по сравнению с кортикостероидами в лечении остеоартрита коленного сустава: систематический обзор и метаанализ.Ревматоидный артрит. 2009. 61 (12): 1704–1711. DOI: 10.1002 / art.24925. [PubMed] [CrossRef] [Google Scholar] 8. Хабиб Г.С. Системные эффекты внутрисуставных кортикостероидов. Clin Rheumatol. 2009. 28 (7): 749–756. DOI: 10.1007 / s10067-009-1135-х. [PubMed] [CrossRef] [Google Scholar] 9. Элморси С., Фунакоши Т., Сасазава Ф., Тодох М., Тадано С., Ивасаки Н. Хондропротекторные эффекты высокомолекулярной поперечно-сшитой гиалуроновой кислоты на модели остеоартрита коленного сустава кролика. Хрящевой артроз. 2014; 22 (1): 121–127.DOI: 10.1016 / j.joca.2013.10.005. [PubMed] [CrossRef] [Google Scholar] 10. Kosinska MK, Ludwig TE, Liebisch G, Zhang R, Siebert HC, Wilhelm J, et al. Смазки для суставов при остеоартрите и ревматоидном артрите имеют измененные уровни и молекулярные формы. PLoS One. 2015; 10 (5) DOI: 10.1371 / journal.pone.0125192. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 11. Band PA, Heeter J, Wisniewski HG, Liublinska V, Pattanayak CW, Karia RJ, et al. Распределение молекулярной массы гиалуроновой кислоты связано с риском прогрессирования остеоартрита коленного сустава.Хрящевой артроз. 2015; 23 (1): 70–76. DOI: 10.1016 / j.joca.2014.09.017. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 12. Диас-Гальего Л., Прието Дж. Г., Коронель П., Гамазо Л. Е., Гимено М., Альварес А. И.. Апоптоз и оксид азота в экспериментальной модели остеоартрита у кролика после лечения гиалуроновой кислотой. J Orthop Res. 2005. 23 (6): 1370–1376. DOI: 10.1016 / j.orthres.2005.05.003.1100230619. [PubMed] [CrossRef] [Google Scholar] 13. Lajeunesse D, Delalandre A, Martel-Pelletier J, Pelletier J-P.Гиалуроновая кислота устраняет аномальную синтетическую активность остеоартрита субхондральных костных остеобластов человека. Кость. 2003. 33 (4): 703–710. DOI: 10.1016 / S8756-3282 (03) 00206-0. [PubMed] [CrossRef] [Google Scholar] 14. Pullman-Mooar S, Mooar P, Sieck M, Clayburne G, Schumacher HR. Есть ли характерные воспалительные обострения после внутрисуставных инъекций hylan g-f 20? J Rheumatol, декабрь 2002 г., 29 (12): 2611–2614. [PubMed] [Google Scholar] 15. Гольдберг В.М., Куттс Р.Д. Псевдосептические реакции на добавку hylan viscos: диагностика и лечение.Clin Orthop Relat Res, февраль 2004 г .; 419: 130–137. DOI: 10.1097 / 00003086-200402000-00021. [PubMed] [CrossRef] [Google Scholar] 16. Ando A, Hagiwara Y, Chimoto E, Hatori K, Onoda Y, Itoi E. Внутрисуставная инъекция гиалуронана снижает потерю хондроцитов в модели с иммобилизованным коленом крысы. Tohoku J Exp Med. 2008. 215 (4): 321–331. DOI: 10.1620 / tjem.215.321. [PubMed] [CrossRef] [Google Scholar] 17. Ariyoshi W, Okinaga T, Knudson CB, Knudson W., Nishihara T. Высокомолекулярная гиалуроновая кислота регулирует образование остеокластов путем ингибирования активатора рецептора лиганда NF-kappaB через Rho-киназу.Хрящевой артроз. 2014. 22 (1): 111–120. DOI: 10.1016 / j.joca.2013.10.013. [PubMed] [CrossRef] [Google Scholar] 18. Asari A, Miyauchi S, Matsuzaka S, Itoh T, Uchiyama Y. Гиалуронат на белке теплового шока и синовиальных клетках в модели остеоартрита у собак. Хрящевой артроз. 1996. 4 (3): 213–215. DOI: 10.1016 / S1063-4584 (96) 80018-5. [PubMed] [CrossRef] [Google Scholar] 19. Брун П., Панфило С., Дага Гордини Д., Кортиво Р., Абатанджело Г. Влияние гиалуронана на CD44-опосредованное выживание нормальных и поврежденных гидроксильными радикалами хондроцитов.Хрящевой артроз. 2003. 11 (3): 208–216. DOI: 10.1016 / S1063-4584 (02) 00352-7. [PubMed] [CrossRef] [Google Scholar] 20. Брун П., Заван Б., Виндини В., Скьявинато А., Поццуоли А., Якобеллис С. и др. In vitro ответ остеоартрозных хондроцитов и фибробластоподобных синовиоцитов на производное гиалуронанамида 500-730 кДа. J Biomed Mater Res B Appl Biomater. 2012. 100 (8): 2073–2081. DOI: 10.1002 / jbm.b.32771. [PubMed] [CrossRef] [Google Scholar] 21. Chang CC, Hsieh MS, Liao ST, Chen YH, Cheng CW, Huang PT и др.Гиалуронан регулирует PPARgamma и воспалительные реакции в клетках хондросаркомы человека, стимулированных IL-1beta, которые являются моделью остеоартрита. Carbohydr Polym. 2012; 90 (2): 1168–1175. DOI: 10.1016 / j.carbpol.2012.06.071. [PubMed] [CrossRef] [Google Scholar] 22. Creamer P, Sharif M, George E, Meadows K, Cushnaghan J, Shinmei M и др. Внутрисуставная гиалуроновая кислота при остеоартрозе коленного сустава: исследование механизмов действия. Хрящевой артроз. 1994. 2 (2): 133–140. DOI: 10.1016 / S1063-4584 (05) 80063-9.[PubMed] [CrossRef] [Google Scholar] 23. Динг М., Кристиан Даниэльсен С., Хвид И. Влияние гиалуронана на трехмерную микроархитектуру субхондральных костных тканей при первичном остеоартрозе морских свинок. Кость. 2005. 36 (3): 489–501. DOI: 10.1016 / j.bone.2004.12.010. [PubMed] [CrossRef] [Google Scholar] 24. Элерс Э.М., Беренс П., Вунш Л., Кунель В., Русслис М. Влияние гиалуроновой кислоты на морфологию и пролиферацию хондроцитов человека в первичной культуре клеток. Анн Анат. 2001. 183 (1): 13–17. DOI: 10.1016 / S0940-9602 (01) 80007-8. [PubMed] [CrossRef] [Google Scholar] 25. Галуа Л., Этьен С., Хенрионне С., Скала-Бертола Дж., Гроссин Л., Майнард Д. и др. Амбивалентные свойства гиалуроната и гилана при посттравматическом ОА коленного сустава крысы. Biomed Mater Eng. 2012. 22 (4): 235–242. [PubMed] [Google Scholar] 26. Gonzalez-Fuentes AM, Green DM, Rossen RD, Ng B. Внутрисуставная гиалуроновая кислота увеличивает биомаркер разрушения хряща у пациентов с остеоартрозом коленного сустава. Clin Rheumatol. 2010. 29 (6): 619–624. DOI: 10.1007 / s10067-010-1376-8. [PubMed] [CrossRef] [Google Scholar] 27. Гринберг Д.Д., Стокер А., Кейн С., Кокрелл М., Кук Дж. Биохимические эффекты двух различных продуктов гиалуроновой кислоты в модели совместного культивирования остеоартрита. Хрящевой артроз. 2006. 14 (8): 814–822. DOI: 10.1016 / j.joca.2006.02.006. [PubMed] [CrossRef] [Google Scholar] 28. Гришко В., Сюй М., Хо Р., Мейтс А., Уотсон С., Ким Дж. Т. и др. Влияние гиалуроновой кислоты на функцию митохондрий и митохондриальный апоптоз после окислительного стресса в хондроцитах человека.J Biol Chem. 2009. 284 (14): 9132–9139. DOI: 10.1074 / jbc.M804178200. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 29. Хашизуме М., Михара М. Желаемый эффект комбинированной терапии с высоким молекулярным гиалуронатом и НПВП на продукцию ММП. Хрящевой артроз. 2009. 17 (11): 1513–1518. DOI: 10.1016 / j.joca.2009.04.018. [PubMed] [CrossRef] [Google Scholar] 30. Homandberg GA, Hui F, Wen C, Kuettner KE, Williams JM. Гиалуроновая кислота подавляет хондролиз хряща, опосредованный фрагментом фибронектина: I. In vitro . Хрящевой артроз. 1997. 5 (5): 309–319. DOI: 10.1016 / S1063-4584 (97) 80035-0. [PubMed] [CrossRef] [Google Scholar] 31. Исидзима М., Накамура Т., Симидзу К., Хаяси К., Кикучи Х., Соен С. и др. Различные изменения биомаркера CTX-II после внутрисуставной инъекции высокомолекулярной гиалуроновой кислоты и пероральных нестероидных противовоспалительных препаратов для пациентов с остеоартрозом коленного сустава: многоцентровое рандомизированное контролируемое исследование. Osteoarthr Cartil. 2013; 21: S292. DOI: 10.1016 / j.joca.2013.02.612. [CrossRef] [Google Scholar] 32. Джулови С.М., Ясуда Т., Шимицу М., Хирамицу Т., Накамура Т. Ингибирование индуцированного интерлейкином-1бета продукции матриксных металлопротеиназ гиалуронаном через CD44 в суставном хряще человека. Ревматоидный артрит. 2004. 50 (2): 516–525. DOI: 10.1002 / art.20004. [PubMed] [CrossRef] [Google Scholar] 33. Kalaci A, Yilmaz HR, Aslan B, Sogut S, Yanat AN, Uz E. Влияние гиалуронана на уровни оксида азота и активность супероксиддисмутазы в синовиальной жидкости при остеоартрите коленного сустава.Clin Rheumatol. 2007. 26 (8): 1306–1311. DOI: 10.1007 / s10067-006-0504-у. [PubMed] [CrossRef] [Google Scholar] 34. Карна Э., Милтык В, Суразинский А, Палка Я. Защитный эффект гиалуроновой кислоты на индуцированную интерлейкином-1 дерегуляцию передачи сигналов рецептора бета1-интегрина и инсулиноподобного фактора роста-I и биосинтез коллагена в культивируемых хондроцитах человека. Mol Cell Biochem. 2008. 308 (1-2): 57–64. DOI: 10.1007 / s11010-007-9612-5. [PubMed] [CrossRef] [Google Scholar] 35. Кобаяши К., Амиэль М., Харвуд Флорида, Хили Р.М., Сонода М., Мория Х. и др.Долгосрочные эффекты гиалуронана во время развития остеоартрита после частичной менискэктомии на модели кролика. Хрящевой артроз. 2000. 8 (5): 359–365. DOI: 10.1053 / joca.1999.0310. [PubMed] [CrossRef] [Google Scholar] 36. Кога Х. Действие гиалуроновой кислоты на суставной хрящ, пораженный артритом. Connect Tissue Res. 2012; 53 (1): 48–93. DOI: 10.3109 / 03008207.2011.637147. [CrossRef] [Google Scholar] 37. Лазаро Дж., Гранадо П., дель Соль Дж., Медина А., Гальего Л., Сандовал Д., Фернандес Дж. Роль различных гиалуроновых кислот в суставном хряще кролика.Открытая Ортопедия J. 2010; 4: 44–47. DOI: 10,2174 / 1874325001004010044. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 38. Ли Дж., Горски Д. Д., Анемает В., Веласко Дж., Такеучи Дж., Сэнди Дж. Д. и др. Инъекция гиалуронана при остеоартрите мышей предотвращает индуцированную TGFbeta 1 синовиальную неоваскуляризацию и фиброз и поддерживает целостность суставного хряща посредством CD44-зависимого механизма. Arthritis Res Ther. 2012; 14 (3): R151. DOI: 10.1186 / ar3887. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 39.Ли П., Райчева Д., Хавс М., Моран Н., Ю Икс, Ван Ф. и др. Hylan G-F 20 поддерживает целостность хряща и снижает образование остеофитов при остеоартрите за счет как анаболических, так и антикатаболических механизмов. Хрящевой артроз. 2012. 20 (11): 1336–1346. DOI: 10.1016 / j.joca.2012.07.004. [PubMed] [CrossRef] [Google Scholar] 40. Лисиньоли Г., Грасси Ф., Зини Н., Тонегуцци С., Пьячентини А., Гуидолин Д. и др. Анти-Fas-индуцированный апоптоз в хондроцитах, сниженный гиалуронаном: свидетельство инвазии CD44 и CD54 (молекула межклеточной адгезии 1).Ревматоидный артрит. 2001. 44 (8): 1800–1807. DOI: 10.1002 / 1529-0131 (200108) 44: 8 <1800 :: AID-ART317> 3.0.CO; 2-1. [PubMed] [CrossRef] [Google Scholar] 41. Lu HT, Sheu MT, Lin YF, Lan J, Chin YP, Hsieh MS и др. Инъекционная терапия гидрогелем доксициклина гиалуроновой кислоты при экспериментальном остеоартрите кроликов. BMC Vet Res. 2013; 9: 68. DOI: 10.1186 / 1746-6148-9-68. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 42. Манейро Э., де Андрес М.С., Фернандес-Суэйро Ю.Л., Гальдо Ф., Бланко Ф.Дж. Биологическое действие гиалуронана на суставные хондроциты остеоартрита человека: важность молекулярной массы.Clin Exp Rheumatol. 2004. 22 (3): 307–312. [PubMed] [Google Scholar] 43. Михара М., Хашизуме М. Влияние высокомолекулярной гиалуроновой кислоты на индукцию ферментов деградации матрикса IL-6, IL-1β и TNF-α Osteoarthr Cartil. 2012; 20: S134 – S135. DOI: 10.1016 / j.joca.2012.02.181. [CrossRef] [Google Scholar] 44. Мики Ю., Терамура Т., Томияма Т., Онодера Ю., Мацуока Т., Фукуда К. и др. Гиалуронан обратил синтез протеогликанов, подавленный механическим стрессом: возможное участие антиоксидантного эффекта.Inflamm Res. 2010. 59 (6): 471–477. DOI: 10.1007 / s00011-009-0147-у. [PubMed] [CrossRef] [Google Scholar] 45. Младенович З., Заурел А.С., Беренбаум Ф., Жак С. Потенциальная роль гиалуроновой кислоты в костях при остеоартрите: матриксные металлопротеиназы, агреканазы и экспрессия RANKL частично предотвращаются гиалуроновой кислотой в остеобластах, стимулированных интерлейкином-1. J Rheumatol. 2014. 41 (5): 945–954. DOI: 10.3899 / jrheum.130378. [PubMed] [CrossRef] [Google Scholar] 46. Mongkhon JM, Thach M, Shi Q, Fernandes JC, Fahmi H, Benderdour M.Гиалуроновая кислота, модифицированная сорбитом, снижает окислительный стресс, апоптоз и медиаторов воспаления и катаболизма в хондроцитах человека, страдающих остеоартритом. Inflamm Res. 2014; 63 (8): 691–701. DOI: 10.1007 / s00011-014-0742-4. [PubMed] [CrossRef] [Google Scholar] 47. Оно S, Im HJ, Knudson CB, Knudson W. Индуцированная гиалуронановым олигосахаридом активация факторов транскрипции в суставных хондроцитах крупного рогатого скота. Ревматоидный артрит. 2005. 52 (3): 800–809. DOI: 10.1002 / art.20937. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 48.Peng H, Zhou JL, Liu SQ, Hu QJ, Ming JH, Qiu B. Гиалуроновая кислота ингибирует апоптоз, вызванный оксидом азота, и дедифференцировку суставных хондроцитов in vitro . Inflamm Res. 2010. 59 (7): 519–530. DOI: 10.1007 / s00011-010-0156-х. [PubMed] [CrossRef] [Google Scholar] 49. Плаас А., Ли Дж., Риеско Дж., Дас Р., Сэнди Дж. Д., Харрисон А. Внутрисуставная инъекция гиалуронана предотвращает эрозию хряща, периартикулярный фиброз и механическую аллодинию и нормализует время пребывания в стойке при остеоартрите коленного сустава у мышей.Arthritis Res Ther. 2011; 13 (2): R46. DOI: 10.1186 / ar3286. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 50. Цю Б., Лю С. К., Пэн Х. Влияние гиалуроната натрия на экспрессию iNOS в синовиальной оболочке и содержание NO в синовиальной жидкости кроликов с травматическим остеоартритом. Chin J Traumatol. 2008. 11 (5): 293–296. DOI: 10.1016 / S1008-1275 (08) 60059-0. [PubMed] [CrossRef] [Google Scholar] 51. Сакакибара Ю., Миура Т., Ивата Х, Кикучи Т., Ямагути Т., Йошими Т. и др. Влияние высокомолекулярного гиалуроната натрия на иммобилизованное колено кролика.Clin Orthop Relat Res. 1994; 299: 282–292. [PubMed] [Google Scholar] 52. Сасаки А., Сасаки К., Конттинен Ю.Т., Сантавирта С., Такахара М., Такей Х. и др. Гиалуронат подавляет индуцированную интерлейкином-1бета экспрессию матриксной металлопротеиназы (MMP) -1 и MMP-3 в синовиальных клетках человека. Tohoku J Exp Med. 2004. 204 (2): 99–107. DOI: 10.1620 / tjem.204.99. [PubMed] [CrossRef] [Google Scholar] 53. Симидзу С., Йошиока М., Коуттс Р.Д., Харвуд Флорида, Кубо Т., Хирасава И. и др. Долгосрочные эффекты гиалуронана при экспериментальном остеоартрозе коленного сустава кролика.Хрящевой артроз. 1998. 6 (1): 1–9. DOI: 10.1053 / joca.1997.0086. [PubMed] [CrossRef] [Google Scholar] 54. Смит М.М., Торт М.А., Гош П., Скьявинато А., Рид Р.А., Литтл СВ. Значительная синовиальная патология в модели менискэктомии остеоартрита: модификация внутрисуставной гиалуроновой терапией. Ревматология (Оксфорд) 2008; 47 (8): 1172–1178. DOI: 10.1093 / ревматология / ken219. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 55. Смит М.М., Рассел А.К., Скьявинато А., Литтл CB. Гексадециламидное производное гиалуронана (HYMOVIS®) оказывает более благоприятное воздействие на хондроциты и синовиоциты человека, страдающие остеоартритом, чем немодифицированный гиалуронан.Журнал Инфламм (Лондон) 2013; 10:26. DOI: 10.1186 / 1476-9255-10-26. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 56. Такахаши К., Гумер Р.С., Харвуд Ф., Кубо Т., Хирасава Й., Амиэль Д. Эффекты гиалуронана на матриксную металлопротеиназу-3 (ММР-3), интерлейкин-1бета (ИЛ-1бета) и тканевой ингибитор металлопротеиназы-1 ( Экспрессия гена ТИМП-1) при развитии остеоартрита. Хрящевой артроз. 1999. 7 (2): 182–190. DOI: 10.1053 / joca.1998.0207. [PubMed] [CrossRef] [Google Scholar] 57.Такахаши К., Хашимото С., Кубо Т., Хирасава Ю., Лотц М., Амиэль Д. Гиалуронан подавлял выработку оксида азота в мениске и синовиальной оболочке модели остеоартрита кролика. J Orthop Res. 2001. 19 (3): 500–503. DOI: 10.1016 / S0736-0266 (00)
-X. [PubMed] [CrossRef] [Google Scholar] 58. Танака М., Масуко-Хонго К., Като Т., Нисиока К., Накамура Х. Подавляющее действие гиалуронана на продукцию MMP-1 и RANTES хондроцитами. Rheumatol Int. 2006. 26 (3): 185–190. DOI: 10.1007 / s00296-004-0547-9. [PubMed] [CrossRef] [Google Scholar] 59.Уодделл Д.Д., Коломыткин О.В., Данн С, Марино А.А. Гиалуронан подавляет активность металлопротеиназы, индуцированную IL-1beta, в синовиальной ткани. Clin Orthop Relat Res. 2007; 465: 241–248. [PubMed] [Google Scholar] 60. Ясуда Т. Активация ядерного фактора-kappaB пептидом коллагена II типа в суставных хондроцитах: его ингибирование гиалуронаном через рецепторы. Мод Ревматол. 2013. 23 (6): 1116–1123. DOI: 10.3109 / s10165-012-0804-9. [PubMed] [CrossRef] [Google Scholar] 61. Ясуи Т., Акацука М., Тобетто К., Хаяиси М., Андо Т.Влияние гиалуронана на индуцированную интерлейкином-1 альфа продукцию простагландина E2 в синовиальных клетках остеоартрита человека. Действия агентов. 1992. 37 (1-2): 155–156. DOI: 10.1007 / BF01987905. [PubMed] [CrossRef] [Google Scholar] 62. Ятабэ Т., Мочизуки С., Такидзава М., Чидзива М., Окада А., Кимура Т. и др. Гиалуронан подавляет экспрессию ADAMTS4 (аггреканазы-1) в хондроцитах человека, страдающих остеоартритом. Ann Rheum Dis. 2009. 68 (6): 1051–1058. DOI: 10.1136 / ard.2007.086884. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 63.Йошими Т., Кикучи Т., Обара Т., Ямагути Т., Сакакибара Ю., Ито Х. и др. Влияние высокомолекулярного гиалуроната натрия на экспериментальный остеоартроз, вызванный резекцией передней крестообразной связки кролика. Clin Orthop Relat Res. 1994; 298: 296–304. [PubMed] [Google Scholar] 64. Йошиока М., Симидзу С., Харвуд Флорида, Куттс Р.Д., Амиэль Д. Эффекты гиалуронана во время развития остеоартрита. Хрящевой артроз. 1997. 5 (4): 251–260. DOI: 10.1016 / S1063-4584 (97) 80021-0. [PubMed] [CrossRef] [Google Scholar] 65.Yu CJ, Ko CJ, Hsieh CH, Chien CT, Huang LH, Lee CW и др. Протеомный анализ хондроцитов, страдающих остеоартритом, выявляет регулируемые гиалуроновой кислотой белки, участвующие в хондропротекторном эффекте при окислительном стрессе. J Proteomics. 2014; 99: 40–53. DOI: 10.1016 / j.jprot.2014.01.016. [PubMed] [CrossRef] [Google Scholar] 66. Zhang FJ, Gao SG, Cheng L, Tian J, Xu WS, Luo W. и др. Влияние гиалуроновой кислоты на остеопонтин и мРНК CD44 фибробластоподобных синовиоцитов у пациентов с остеоартрозом коленного сустава.Rheumatol Int. 2013. 33 (1): 79–83. DOI: 10.1007 / s00296-011-2339-3. [PubMed] [CrossRef] [Google Scholar] 67. Zhou JL, Liu SQ, Qiu B, Hu QJ, Ming JH, Peng H. Защитный эффект гиалуроната натрия на хрящ от остеоартрита кроликов путем ингибирования экспрессии рецепторной гамма-матричной РНК, активируемой пролифератором пероксисом. Йонсей Мед Дж. 2009; 50 (6): 832–837. DOI: 10.3349 / ymj.2009.50.6.832. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 68. Чжоу PH, Лю С.К., Пэн Х. Эффект гиалуроновой кислоты на индуцированный IL-1beta апоптоз хондроцитов в модели остеоартрита на крысах.J Orthop Res. 2008. 26 (12): 1643–1648. DOI: 10.1002 / jor.20683. [PubMed] [CrossRef] [Google Scholar] 69. Уильямс Дж. Эффекты гиалуроновой кислоты на хондролиз хряща, опосредованный фибронектиновым фрагментом, у скелетно зрелых кроликов. Osteoarthr Cartil. 2003. 11 (1): 44–49. DOI: 10.1053 / joca.2002.0864. [PubMed] [CrossRef] [Google Scholar] 70. Сюй Х., Ито Т., Тавада А., Маеда Х., Яманокучи Х., Исахара К. и др. Влияние олигосахаридов гиалуронана на экспрессию белка теплового шока 72. J Biol Chem. 2002. 277 (19): 17308–17314.DOI: 10.1074 / jbc.M112371200. [PubMed] [CrossRef] [Google Scholar] 71. Чжоу J-L, Лю С.-Q, Цю Б., Ху Q-J, Мин J-H, Пэн Х. Влияние гиалуронана на фактор роста эндотелия сосудов и экспрессию рецептора-2 на модели остеоартрита кроликов. J Orthop Sci. 2009. 14 (3): 313–319. DOI: 10.1007 / s00776-009-1329-8. [PubMed] [CrossRef] [Google Scholar] 72. Хуанг Т.Л., Сюй ХК, Ян К.С., Яо СН, Линь Ф.Х. Влияние гиалуронанов разной молекулярной массы на продукцию белка, связанного с остеоартритом, в фибробластоподобных синовиоцитах пациентов с переломом плато большеберцовой кости.J Trauma. 2010. 68 (1): 146–152. DOI: 10.1097 / TA.0b013e3181a92cf8. [PubMed] [CrossRef] [Google Scholar] 73. Амиэль Д., Тойогучи Т., Кобаяши К., Боуден К., Амиэль М.Э., Хили Р.М. Долгосрочный эффект гиалуроната натрия (Hyalgan) на прогрессирование остеоартрита на модели кролика. Остеоартроз и хрящи / OARS, Osteoarthritis Res Soc. 2003. 11 (9): 636–643. DOI: 10.1016 / S1063-4584 (03) 00119-5. [PubMed] [CrossRef] [Google Scholar] 74. Ким NH, Хан CD, Ли ХМ, Ян И.Х. Влияние гиалуроната натрия на профилактику остеоартрита.Йонсей Мед Дж. 1991; 32 (2): 139–146. DOI: 10.3349 / ymj.1991.32.2.139. [PubMed] [CrossRef] [Google Scholar] 75. Лю Дж., Сун В., Юань Т., Сюй З., Цзя В., Чжан С. Сравнение плазмы, обогащенной тромбоцитами (PRP), и гиалуроновой кислоты при заживлении дефектов хряща. PLoS One. 2014; 9 (5) DOI: 10.1371 / journal.pone.0097293. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 76. Михара М., Хиго С., Учияма Ю., Танабе К., Сайто К. Различные эффекты высокомолекулярного гиалуроната натрия и НПВП на прогрессирование дегенерации хряща в модели ОА кролика.Osteoarthritis Cartilage / OARS, Osteoarthritis Res Soc. 2007. 15 (5): 543–549. DOI: 10.1016 / j.joca.2006.11.001. [PubMed] [CrossRef] [Google Scholar] 77. Цю Б., Лю С.К., Пэн Х., Ван HB. Влияние гиалуроната натрия на экспрессию мРНК матриксной металлопротеиназы-1, -3 и тканевого ингибитора металлопротеиназы-1 в хряще и синовиальной оболочке модели травматического остеоартрита. Chin J Traumatol. 2005; 8 (1): 8–12. [PubMed] [Google Scholar] 78. Озкан Ф.У., Озкан К., Рамадан С., Гувен З. Хондропротекторный эффект N-ацетилглюкозамина и гиалуроната на ранних стадиях остеоартрита — экспериментальное исследование на кроликах.Bull NYU Hosp Jt Dis. 2009. 67 (4): 352–357. [PubMed] [Google Scholar] 79. Ян Л, Чжан Дж, Ван Г. Эффект гиалуроната натрия при лечении остеоартрита коленного сустава на интерлейкин-1бета синовиальной жидкости и механизм клинического лечения. Pak J Pharm Sci. 2015; 28 (1 приложение): 407–410. [PubMed] [Google Scholar] 80. Йошиока К., Ясуда И., Кисукеда Т., Нодера Р., Танака Ю., Миямото К. Фармакологические эффекты нового поперечно-сшитого гиалуроната, геля-200, в экспериментальных моделях остеоартрита на животных и клеточных линиях человека.Хрящевой артроз. 2014. 22 (6): 879–887. DOI: 10.1016 / j.joca.2014.04.019. [PubMed] [CrossRef] [Google Scholar] 81. Хуэй А.Ю., Маккарти В.Дж., Масуда К., Файрштейн Г.С., Сах Р.Л. Системно-биологический подход к смазке синовиальных суставов при здоровье, травмах и болезнях. Wiley Interdiscip Rev Syst Biol Med. 2012. 4 (1): 15–37. DOI: 10.1002 / wsbm.157. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 83. Асари А., Мияути С., Мацудзака С., Ито Т., Коминами Е., Учияма Ю. Эффекты гиалуроната, зависимые от молекулярного веса, на синовиальную оболочку артрита.Arch Histol Cytol. 1998. 61 (2): 125–135. DOI: 10.1679 / aohc.61.125. [PubMed] [CrossRef] [Google Scholar] 84. Багга Х, Буркхардт Д., Сэмбрук П., Марч Л. Долгосрочные эффекты внутрисуставного гиалуронана на синовиальную жидкость при остеоартрите коленного сустава. J Rheumatol. 2006; 33 (5): 946–950. [PubMed] [Google Scholar] 85. Бауэр Ч., Баумгартнер Р., Хорноф М., Хальбвирт Ф., Никулеску-Морца Э., Цвикл Х. и др. Каркасы из поперечно-сшитой гиалуроновой кислоты: потенциальное использование для регенерации хряща? Osteoarthr Cartil. 2013; 21: S312.DOI: 10.1016 / j.joca.2013.02.646. [CrossRef] [Google Scholar] 86. Форси Р., Фишер Дж., Томпсон Дж., Стоун М., Белл С., Ингхэм Э. Влияние смазок на основе гиалуроновой кислоты и фосфолипидов на трение в модели повреждения хряща человека. Биоматериалы. 2006. 27 (26): 4581–4590. DOI: 10.1016 / j.biomaterials.2006.04.018. [PubMed] [CrossRef] [Google Scholar] 87. Frean S, Abraham L, Lees P. In vitro стимуляция синтеза протеогликанов суставного хряща лошади гиалуронаном и карпрофеном.Res Vet Sci. 1999. 67: 181–188. DOI: 10.1053 / rvsc.1999.0328. [PubMed] [CrossRef] [Google Scholar] 88. Хан Ф, Исигуро Н., Ито Т., Сакаи Т., Ивата Х. Влияние гиалуроната натрия на экспериментальный остеоартрит в коленных суставах кролика. Med Sci. 1999; 62. [PubMed] 89. Хомандберг Г.А., Уммади В., Канг Х. Роль инсулиноподобного фактора роста-I в опосредованном гиалуронаном восстановлении культивируемых эксплантатов хряща. Inflamm Res. 2004; 53: 8. [PubMed] [Google Scholar] 90. Hulmes D. Внутрисуставной гиалуронат при экспериментальном остеоартрите кроликов может предотвратить изменения в содержании протеогликанов хряща.Osteoarthr Cartil. 2004. 12 (3): 232–238. DOI: 10.1016 / j.joca.2003.11.007. [PubMed] [CrossRef] [Google Scholar] 91. Канг Й., Эгер В., Кепп Х., Уильямс Дж. М., Кюттнер К. Э., Хомандберг Г. А.. Гиалуронан подавляет опосредованное фрагментом фибронектина повреждение культур эксплантата хряща человека за счет усиления синтеза протеогликана. J Orthop Res. 1999. 17 (6): 858–869. DOI: 10.1002 / jor.1100170611. [PubMed] [CrossRef] [Google Scholar] 92. Кикучи Т., Ямада Х., Фудзикава К. Влияние высокомолекулярного гиалуронана на распределение и движение протеогликана вокруг хондроцитов, культивируемых в альгинатных шариках.Osteoarthr Cartil. 2001. 9 (4): 351–356. DOI: 10.1053 / joca.2000.0395. [PubMed] [CrossRef] [Google Scholar] 93. Kobayashi K, Matsuzaka S, Yoshida Y, Miyauchi S, Wada Y, Moriya H. Влияние внутрисуставного введения гиалуроната натрия на уровни интактного аггрекана и оксида азота в суставной жидкости пациентов с остеоартрозом коленного сустава. Osteoarthr Cartil. 2004. 12 (7): 536–542. DOI: 10.1016 / j.joca.2004.03.005. [PubMed] [CrossRef] [Google Scholar] 94. Nishida Y, Knudson CB, Knudson W. Восстановление внеклеточного матрикса суставными хондроцитами человека после лечения гиалуронановыми гексасахаридами или гиалуронидазой Streptomyces.Мод Ревматол. 2003. 13 (1): 62–68. DOI: 10.3109 / s101650300009. [PubMed] [CrossRef] [Google Scholar] 95. Смит Г. Н., младший, Миклер Е. А., Майерс С. Л., Брандт К. Д.. Влияние внутрисуставной инъекции гиалуронана на гиалуронан в синовиальную жидкость на ранней стадии посттравматического остеоартрита у собак. J Rheumatol. 2001. 28 (6): 1341–1346. [PubMed] [Google Scholar] 96. Stove J, Gerlach C, Huch K, Gunther KP, Puhl W, Scharf HP. Влияние гиалуронана на содержание протеогликанов в хондроцитах при остеоартрите in vitro. J Orthop Res.2002. 20 (3): 551–555. DOI: 10.1016 / S0736-0266 (01) 00141-3. [PubMed] [CrossRef] [Google Scholar] 97. Wang C, Lin Y, Chiang B, Hou S. Высокомолекулярная гиалуроновая кислота подавляет экспрессию генов цитокинов и ферментов, связанных с остеоартритом, в фибробластоподобных синовиоцитах пациентов с ранним остеоартритом. Osteoarthr Cartil. 2006. 14 (12): 1237–1247. DOI: 10.1016 / j.joca.2006.05.009. [PubMed] [CrossRef] [Google Scholar] 98. Abatangelo G, Botti P, Del Bue M, Gei G, Samson JC, Cortivo R и др.Внутрисуставные инъекции гиалуроната натрия в экспериментальной модели остеоартрита Понд-Нуки у собак. I. Биохимические результаты. Clin Orthop Relat Res. 1989. 241: 278–285. [PubMed] [Google Scholar] 99. Асари А., Мизуно С., Танака И., Суносе А., Курияма С., Миядзаки К. и др. Подавление продукции гиалуронана и простагландина E2 в синовиальных клетках травматического артрита гиалуронатом натрия. Соединительная ткань. 1997; 29: 1–5. [Google Scholar] 100. Лисиньоли Г., Грасси Ф., Пьячентини А., Коккини Б., Ремидди Г., Бевилаква С. и др.Гиалуронан не влияет на экспрессию цитокинов и хемокинов в хондроцитах и синовиоцитах, пораженных остеоартритом. Хрящевой артроз. 2001. 9 (2): 161–168. DOI: 10.1053 / joca.2000.0372. [PubMed] [CrossRef] [Google Scholar] 101. Оливьеро Ф., Сканю А., Рамонда Р., Фраллонардо П., Сфризо П., Дайер Дж. И др. Механизмы, участвующие в подавлении воспаления в клетках THP-1 гексадециламидным производным гиалуроновой кислоты. Osteoarthr Cartil. 2014; 22: S292 – S293. DOI: 10.1016 / j.joca.2014.02.544. [CrossRef] [Google Scholar] 102.Сезгин М., Демирел А.Г., Караджа С., Ортанджил О, Юлкар Г.Б., Каник А. и др. Влияет ли гиалуронан на воспалительные цитокины при остеоартрите коленного сустава? Rheumatol Int. 2004. 25 (4): 264–269. DOI: 10.1007 / s00296-003-0428-7. [PubMed] [CrossRef] [Google Scholar] 103. Шихан К.М., Делотт Л.Б., Дэй С.М., Дехир Д.Х. Hyalgan® оказывает дифференцированное дозозависимое действие на пролиферацию макрофагов и гибель клеток. J Orthop Res. 2003. 21 (4): 744–751. DOI: 10.1016 / S0736-0266 (03) 00007-X. [PubMed] [CrossRef] [Google Scholar] 104. Ясуда Т.Гиалуронан ингибирует Akt, что приводит к подавлению регуляции ядерного фактора-каппаB в макрофагах U937, стимулированных липополисахаридами. J Pharmacol Sci. 2011. 115 (4): 509–515. DOI: 10.1254 / jphs.10244FP. [PubMed] [CrossRef] [Google Scholar] 105. Campo GM, Avenoso A, D’Ascola A, Prestipino V, Scuruchi M, Nastasi G и др. Ингибирование синтеза гиалуронана снижает воспалительную реакцию в синовиальных фибробластах мышей, подвергшихся индуцированному коллагеном артриту. Arch Biochem Biophys. 2012; 518 (1): 42–52. DOI: 10.1016 / j.abb.2011.12.005. [PubMed] [CrossRef] [Google Scholar] 106. Campo GM, Avenoso A, Nastasi G, Micali A, Prestipino V, Vaccaro M и др. Гиалуронан уменьшает воспаление при экспериментальном артрите, модулируя экспрессию в хряще TLR-2 и TLR-4. Biochim Biophys Acta. 2011; 1812 (9): 1170–1181. DOI: 10.1016 / j.bbadis.2011.06.006. [PubMed] [CrossRef] [Google Scholar] 107. Schumacher HR, Paul C, Hitchon CA, El-Gabalawy H, Zonay L., Clayburne G, et al. Воздействие гиалуроната на синовиальную оболочку и синовиальную жидкость. Проспективное слепое исследование пациентов с остеоартрозом коленного сустава.Хрящевой артроз. 2006. 14 (5): 501–503. DOI: 10.1016 / j.joca.2005.11.013. [PubMed] [CrossRef] [Google Scholar] 108. Белл CJ, Ingham E, Fisher J. Влияние гиалуроновой кислоты на зависящую от времени фрикционную реакцию суставного хряща в различных условиях. Proc Inst Mech Eng H. 2006; 220 (1): 23–31. DOI: 10.1243 / 095441105X69060. [PubMed] [CrossRef] [Google Scholar] 109. Гош П., Рид Р., Нумата Ю., Смит С., Армстронг С., Уилсон Д. Эффекты внутрисуставного введения гиалуронана на модели раннего остеоартрита у овец.II. Состав хряща и метаболизм протеогликанов. Semin Arthritis Rheum. 1993; 22 (6 Suppl 1): 31–42. DOI: 10.1016 / S0049-0172 (10) 80017-4. [PubMed] [CrossRef] [Google Scholar] 110. Обара Т., Мабучи К., Исо Т., Ямагути Т. Повышенное трение суставов животных путем экспериментальной дегенерации и восстановления путем добавления гиалуроновой кислоты. Clin Biomech (Бристоль, Эйвон) 1997; 12 (4): 246–252. DOI: 10.1016 / S0268-0033 (97) 00004-1. [PubMed] [CrossRef] [Google Scholar] 111. Уоллер К.А., Чжан Л.X., Флеминг Б.К., Джей Г.Д. Предотвращение апоптоза хондроцитов, вызванного трением: сравнение синовиальной жидкости человека и Hylan G-F 20.J Rheumatol. 2012. 39 (7): 1473–1480. DOI: 10.3899 / jrheum.111427. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 112. Yu L-P, Yang H, Voschin E, Skrabut E. Вязкоупругие свойства и молекулярная масса гилана G-F 20 по сравнению с другими коммерческими добавками для вязкости на основе гиалуронана. Osteoarthr Cartil. 2011; 19 (S1): S235. DOI: 10.1016 / S1063-4584 (11) 60535-9. [CrossRef] [Google Scholar] 114. Тан С.Ф., Чен С.П., Чен М.Дж., Пей Ю.К., Лау Ю.К., Леонг С.П. Изменения сил сагиттальной реакции опоры после внутрисуставных инъекций гиалуроната при остеоартрозе коленного сустава.Arch Phys Med Rehabil. 2004. 85 (6): 951–955. DOI: 10.1016 / j.apmr.2003.08.095. [PubMed] [CrossRef] [Google Scholar] 115. Армстронг С., Рид Р., Гош П. Эффекты внутрисуставного гиалуронана на изменения хряща и субхондральной кости в модели раннего остеоартрита у овец. J Rheumatol. 1994. 21 (4): 680–688. [PubMed] [Google Scholar] 116. Hiraoka N, Takahashi Y, Arai K, Honjo S, Nakawaga S, Tsuchida S и др. Гиалуронан и периодическое гидростатическое давление синергетически подавляли экспрессию MMP-13 и Il-6 в остеобластах субхондральной кости при остеоартрите.Osteoarthr Cartil. 2009; 17 (1): S97. DOI: 10.1016 / S1063-4584 (09) 60186-2. [CrossRef] [Google Scholar] 117. Hiraoka N, Takahashi KA, Arai Y, Sakao K, Mazda O, Kishida T и др. Внутрисуставная инъекция гиалуронана восстанавливает аберрантную экспрессию матриксной металлопротеиназы-13 в субхондральной кости, пораженной остеоартритом. J Orthop Res. 2011. 29 (3): 354–360. DOI: 10.1002 / jor.21240. [PubMed] [CrossRef] [Google Scholar] 118. Prasadam I, Crawford R, Xiao Y. Обострение ADAMTS и продукции матриксной металлопротеиназы и роль пути ERK1 / 2 во взаимодействии остеоартрита субхондральных костных остеобластов и хондроцитов суставного хряща — возможная патогенная роль при остеоартрите.J Rheumatol. 2012. 39 (3): 621–634. DOI: 10.3899 / jrheum.110777. [PubMed] [CrossRef] [Google Scholar] 119. Boettger MK, Kummel D, Harrison A, Schaible HG. Оценка долгосрочных антиноцицептивных свойств препарата стабилизированной гиалуроновой кислоты (NASHA) на животной модели повторяющейся боли в суставах. Arthritis Res Ther. 2011; 13 (4): R110. DOI: 10.1186 / ar3394. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 120. Гомис А., Мираллес А., Шмидт Р.Ф., Бельмонте С. Внутрисуставные инъекции растворов гиалуронана разной эластовязкости снижают активность ноцицептивного нерва на модели остеоартрита коленного сустава морской свинки.Osteoarthr Cartil. 2009. 17 (6): 798–804. DOI: 10.1016 / j.joca.2008.11.013. [PubMed] [CrossRef] [Google Scholar] 121. Гото С., Оная Дж., Абэ М., Миядзаки К., Хамай А., Хори К. и др. Влияние молекулярной массы гиалуроновой кислоты и механизмов ее действия на экспериментальную боль в суставах у крыс. Ann Rheum Dis. 1993. 52 (11): 817–822. DOI: 10.1136 / ard.52.11.817. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 122. Pena Ede L, Sala S, Rovira JC, Schmidt RF, Belmonte C. Эластовязкие вещества с обезболивающим действием при боли в суставах снижают активность ионных каналов, активируемых растяжением, in vitro.Боль. 2002. 99 (3): 501–508. DOI: 10.1016 / S0304-3959 (02) 00260-9. [PubMed] [CrossRef] [Google Scholar] 123. Дугадос М. Терапия гиалуронатом натрия при остеоартрите: аргументы в пользу потенциального положительного структурного эффекта. Semin Arthritis Rheum. 2000; 30 (2 Suppl 1): 19–25. DOI: 10.1053 / sarh.2000.0246. [PubMed] [CrossRef] [Google Scholar] 124. Балаш Э.А., Денлингер Ж.Л. Вязкие добавки: новая концепция лечения остеоартрита. J Rheumatol Suppl. 1993; 39: 3–9. [PubMed] [Google Scholar] 125. Карбовник М.С., Новак Ю.З.Гиалуронан: к новым противораковым препаратам. Pharmacol Rep., 2013; 65 (5): 1056–1074. DOI: 10.1016 / S1734-1140 (13) 71465-8. [PubMed] [CrossRef] [Google Scholar] 126. Фахари А., Беркланд С. Применение и новые тенденции применения гиалуроновой кислоты в тканевой инженерии, в качестве кожного наполнителя и при лечении остеоартрита. Acta Biomater. 2013; 9 (7): 7081–7092. DOI: 10.1016 / j.actbio.2013.03.005. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
127. Harris E, Weigel PH. Функциональные аспекты рецепторов гиалуроновой кислоты и хондроитина сульфата.В: Raton B, ed: CRC Press; 2009: 171–192.
128. Гош П., Гуидолин Д. Возможный механизм действия внутрисуставной гиалуроновой терапии при остеоартрите: зависят ли эффекты от молекулярной массы? Semin Arthritis Rheum. 2002. 32 (1): 10–37. DOI: 10.1053 / sarh.2002.33720. [PubMed] [CrossRef] [Google Scholar] 130. Камениш Т.Д., Макдональд Дж. А. Гиалуронан: больше лучше? Am J Respir Cell Mol Biol. 2000. 23 (4): 431–433. DOI: 10.1165 / ajrcmb.23.4.f201. [PubMed] [CrossRef] [Google Scholar] 131. Мизрахи С., Раз С.Р., Хасгаард М., Лю Х., Соффер-Цур Н., Коэн К. и др.Наночастицы, покрытые гиалуроновой оболочкой: влияние молекулярной массы на взаимодействия CD44-гиалуронана и на иммунный ответ. J Control Release. 2011. 156 (2): 231–238. DOI: 10.1016 / j.jconrel.2011.06.031. [PubMed] [CrossRef] [Google Scholar] 132. Jevsevar DS, Jones DL, Matzkin EG, Manner PA, Mooar P, Schousboe JT, et al. Американская академия хирургов-ортопедов. Лечение остеоартроза коленного сустава: руководство, основанное на доказательствах, 2-е издание. JBJS. 2013. 95 (20): 1885–1886. [PubMed] [Google Scholar] 133.Ли ПБ, Ким Ю.С., Лим Й.Дж., Ли СиДжей, Сим У.С., Ха Ч.В. и др. Сравнение гиалуронатов с высокой и низкой молекулярной массой у пациентов с остеоартритом коленного сустава: открытое рандомизированное многоцентровое клиническое исследование. J Int Med Res. 2006. 34 (1): 77–87. DOI: 10.1177 / 147323000603400110. [PubMed] [CrossRef] [Google Scholar] 134. Киршнер М., Маршалл Д. Двойное слепое рандомизированное контролируемое исследование по сравнению альтернативных форм высокомолекулярного гиалуронана для лечения остеоартрита коленного сустава. Osteoarthr Cartil.2006. 14 (2): 154–162. DOI: 10.1016 / j.joca.2005.09.003. [PubMed] [CrossRef] [Google Scholar] 135. Чен А.Л., Десаи П., Адлер Э.М., Ди Чезаре ЧП. Гранулематозное воспаление после вискозиметрии колена Hylan G-F 20: отчет о шести случаях. J Bone Joint Surg Am. 2002; 84-А (7): 1142–1147. [PubMed] [Google Scholar] 136. Зардави И.М., Чан И. Синвисковидный перисиновит. Патология. 2001. 33 (4): 519–520. DOI: 10.1080 / 00313020120083296. [PubMed] [CrossRef] [Google Scholar]
Механизм действия гиалуроновой кислоты при остеоартрите коленного сустава: систематический обзор
BMC Musculoskelet Disord.2015; 16: 321.
, , , , и
RD Altman
Отдел ревматологии и иммунологии Медицинской школы Дэвида Геффена Калифорнийского университета в Лос-Анджелесе, 1000 ветеранов Ave,
Лос-Анджелес, Калифорния, США
A. Manjoo
Отделение ортопедии, Университет Макмастера, Гамильтон, Канада
A. Fierlinger
Ferring Pharmaceuticals Inc., Парсиппани, штат Нью-Джерси, США
F. Niazi
Ferring Pharmaceuticals Inc., Парсиппани, штат Нью-Джерси, США
М. Николлс
Кентукки Ортопедические хирурги и хирурги кистей рук, Подразделение Ortho Kentucky, Лексингтон,
США
Отделение ревматологии и иммунологии, Медицинская школа Дэвида Геффена, Калифорнийский университет в Лос-Анджелесе, 1000 Veterans Ave,
Лос-Анджелес, Калифорния, США
Отделение ортопедии, Университет Макмастера, Гамильтон, Канада
Ferring Pharmaceuticals Inc., Парсиппани, штат Нью-Джерси, США
Кентукки Ортопедические хирурги и хирурги кистей рук, отделение Ortho Kentucky, Лексингтон, штат Кентукки, США
Автор, отвечающий за переписку.
Поступило 12 августа 2015 г .; Принято 15 октября 2015 г.
Открытый доступ Эта статья распространяется в соответствии с условиями Международной лицензии Creative Commons Attribution 4.0 (http://creativecommons.org/licenses/by/4.0/), которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии вы должным образом указываете первоначального автора (авторов) и источник, предоставляете ссылку на лицензию Creative Commons и указываете, были ли внесены изменения.Отказ Creative Commons Public Domain Dedication (http://creativecommons.org/publicdomain/zero/1.0/) распространяется на данные, представленные в этой статье, если не указано иное. Эта статья цитируется в других статьях PMC.
Abstract
Предпосылки
Остеоартроз коленного сустава (ОА) является одной из основных причин инвалидности среди взрослого населения. Текущие варианты лечения ОА коленного сустава включают внутрисуставную (IA) гиалуроновую кислоту (HA), молекулу, которая находится внутри коленного сустава, которая обеспечивает вязкоупругие свойства синовиальной жидкости.В современной базовой литературе описаны различные механизмы, с помощью которых ГК борется с остеоартритом коленного сустава.
Методы
Мы провели всесторонний поиск литературы, чтобы определить доступные в настоящее время первичные доклинические фундаментальные научные статьи, посвященные механизму действия лечения IA-HA. Включенные статьи были оценены и распределены по категориям на основе описанного в них механизма действия. Основные результаты и выводы из каждой включенной статьи были получены и проанализированы в совокупности с исследованиями того же категориального задания.
Результаты
Хондрозащита была наиболее частым механизмом, о котором сообщалось во включенных статьях, за ней следуют синтез протеогликанов и гликозаминогликанов, противовоспалительное, механическое, субхондральное и обезболивающее действие. Связывание рецептора HA-кластера дифференцировки 44 (CD44) было наиболее часто упоминаемой биологической причиной представленных механизмов. Было обнаружено, что ГК с высоким молекулярным весом превосходит продукты ГК с более низким молекулярным весом. ГК, полученная в процессе биологической ферментации, также описывается как имеющая более благоприятные результаты безопасности по сравнению с продуктами ГК птичьего происхождения.
Выводы
Доклиническая фундаментальная научная литература предоставляет доказательства многочисленных механизмов, с помощью которых ГК действует на структуры и функции суставов. Эти действия подтверждают предполагаемую клиническую пользу IA-HA при остеоартрите коленного сустава. Дальнейшие исследования должны быть сосредоточены не только на обезболивании, обеспечиваемом лечением IA-HA, но и на свойствах модификации заболевания, которыми обладает этот метод лечения.
Ключевые слова: Остеоартрит, Гиалуроновая кислота, Терапия, Внутрисуставная терапия, Систематический обзор, Механизм действия
Предпосылки
Хотя остеоартрит (ОА) коленного сустава чаще всего является медленно прогрессирующим заболеванием суставов, он является одним из ведущие причины инвалидности взрослого населения [1].ОА коленного сустава, заболевание всего сустава, характеризуется болью в суставах, дегенерацией хряща и увеличением инвалидности [2]. Прогрессирующий характер ОА приводит к снижению функции коленного сустава, влияя на способность человека выполнять повседневную деятельность [3]. ОА коленного сустава также негативно влияет на социально-экономические факторы, поскольку связанная с этим инвалидность часто приводит к снижению производительности труда и раннему выходу на пенсию [4].
Поскольку не существует установленного агента, модифицирующего заболевание при ОА, существует множество вариантов лечения ОА коленного сустава.Среди фармакологических методов лечения чаще всего назначают нестероидные противовоспалительные препараты (НПВП) и внутрисуставные (IA) инъекции кортикостероидов [5]. Этим вариантам присущи ограничения, так как НПВП имеют потенциально серьезные побочные эффекты, связанные с их использованием [6], а инъекции кортикостероидов IA часто обеспечивают относительно короткий период эффективного облегчения [7]. Хотя инъекция кортикостероидов обычно имеет положительный профиль безопасности, было показано, что она вызывает временное повышение уровня глюкозы в крови, что может вызывать беспокойство у пациентов с диабетом [8].IA инъекция гиалуроновой кислоты (HA) — еще один вариант лечения боли при остеоартрите коленного сустава. ГК почти повсеместно присутствует в организме и представляет собой молекулу, которая находится внутри коленного сустава, где она придает вязкоупругие свойства синовиальной жидкости [9]. По мере прогрессирования ОА естественная концентрация ГК и распределение ГК в суставе смещается в сторону более низких диапазонов молекулярной массы ГК, что приводит к деградации механических / вязкоупругих свойств эндогенной синовиальной жидкости [2, 10, 11]. Также было показано, что более низкие диапазоны молекулярно-массового распределения сильно коррелируют с болью [11].Назначение IA-HA было направлено на восстановление этого снижения концентрации HA и среднего молекулярно-массового распределения внутри OA колена [9].
IA-HA, как предполагалось, обладает множеством терапевтических механизмов действия в коленном суставе с остеоартритом, включая поглощение ударов, смазку суставов, противовоспалительные эффекты, хондрозащиту, синтез протеогликанов и изменения хрящевого матрикса [2]. Корреляция между этими различными эффектами позволила лучше понять, как лечение IA-HA может оказывать терапевтический эффект для пациентов с остеоартритом коленного сустава [12].Имеются также данные, свидетельствующие о различиях в механизмах действия продуктов НА разной молекулярной массы. То есть ГК с более высокой молекулярной массой (HMW), как сообщается, обеспечивает более сильные противовоспалительные эффекты и эффекты синтеза протеогликанов, а также смазывание суставов и поддержание вязкоупругости [9, 13]. Также, по-видимому, существуют доказательства различных профилей безопасности между ГК, полученным в процессе биологической ферментации (Bio-HA), и ГК птичьего происхождения (AD-HA), поскольку AD-HA имеет потенциал для местных реакций IA [14, 15] .
Мы стремимся обобщить механизмы действия IA-HA лечения ОА коленного сустава, описанные в современной литературе, чтобы определить обоснованность вышеупомянутых механизмов действия. Мы будем систематически оценивать и обрисовывать определенные механизмы, с помощью которых ГК может оказывать терапевтическое действие, одновременно анализируя сообщаемые различия между эффектами лечения ИА-ГК, зависящими от характеристик продукта.
Методы
Поиск литературы
Мы провели всесторонний поиск литературы с использованием баз данных MEDLINE, EMBASE и PubMed (таблица).Поиск был проведен 4 мая -го , 2014. Критерии включения, соблюдаемые на протяжении всего процесса отбора, были следующими: 1) Статьи, описывающие механизм лечения ГК при ОА, 2) Статьи, посвященные ОА коленного сустава, и 3) Основные доклинические фундаментальные научные статьи, посвященные «добавлению вязкости» / лечению ГК. Статьи, которые были опубликованы до 1990 года или не были опубликованы на английском языке, были исключены из исследования. Если одним и тем же автором было опубликовано несколько исследований, содержащих похожие результаты, для включения принималось только самое последнее исследование.
Таблица 1
| MEDLINE и EMBASE — 1470 статей | PubMed — 1395 статей |
|---|---|
| 1. Гиалуроновая кислота [название] | 1. Гиалуроновая кислота [название] |
| 2. Hylan [title] | |
| 3. Гиалуронан [title] | 3. Гиалуронан [title] |
| 4. Добавки для вязкости [title] | 4. Добавки для вязкости [title] | 5.1 или 2 или 3 или 4 | 5. 1 или 2 или 3 или 4 |
| 6. Остеоартрит * .mp | 6. Остеоартрит * |
| 7. Артрит * .mp | 7. Артрит * |
| 8. Боль в суставах.mp | 8. Боль в суставах |
| 9. 6 или 7 или 8 | 9. 6 или 7 или 8 |
| 10. Эффект * .mp | 10. Эффект * |
| 11. Механизм * .mp | 11. Механизм * |
| 12.10 или 11 | 12. 10 или 11 |
| 13. 5 и 9 и 12 | 13. 5 и 9 и 12 |
Абстракция данных
Включенные статьи были оценены и классифицированы на основе механизма действие, описанное в них. Отдельные статьи включались в несколько категорий, если они анализировали более одного механизма действия НА в рамках своего дизайна исследования. Категории механизмов, использованные в процессе извлечения данных, включали: хондрозащиту, изменения синтеза протеогликана и / или гликозаминогликана (ГАГ), противовоспалительные эффекты, механические модификации, изменения в субхондральной кости и анальгетические эффекты.
Анализ данных
Ключевые выводы и заключения по каждой включенной статье были получены и проанализированы в совокупности с исследованиями той же присвоенной категории. Представленные результаты были получены путем интерпретации общего и последовательного механизма действия в рамках каждой вышеупомянутой категории.
Результаты
Стратегия поиска
Поиск литературы выявил 2782 потенциальных статьи, из которых 91 статья соответствовала критериям включения (рис.). Тринадцать дополнительных статей были извлечены специалистом по содержанию путем ручного поиска литературы. В результате было включено 104 статьи. Выводы и основные выводы каждой статьи были определены в рамках вышеупомянутых категорий механизмов (таблица).
Процесс проверки статей
Таблица 2
Ключевые механизмы действия, указанные во включенных статьях
| Механизм действия | Количество статей | % включенных статей | Ссылки | |
|---|---|---|---|---|
| Chondrotective | 67 | 64.42% | [9, 12, 16–80] | |
| Синтез протеогликанов / гликозаминогликанов | 22 | 21,15% | [27, 42, 44, 48, 62, 69, 83–98] | |
| Противовоспалительное | 21 | 20,19% | [13, 20, 21, 25, 27, 52, 54, 55, 68, 72, 96, 97, 99–107] | |
| Механический | 10 | 9,61% | [41, 49, 86, 108–114] | |
| Субхондральная кость | 8 | 7.69% | [23, 31, 32, 45, 115–118] | |
| Анальгетик | 6 | 5,76% | [76, 80, 119–122] |
Хондрозащита
Шестьдесят семь из включенных статей описывают хондрозащитные эффекты лечения IA-HA [9, 12, 16–80]. Было показано, что IA-HA снижает апоптоз хондроцитов, одновременно увеличивая пролиферацию хондроцитов [19, 20]. Существует множество наблюдаемых эффектов лечения IA-HA, которые вызывают хондрозащиту, многие из которых являются результатом связывания HA с рецепторами кластера дифференцировки 44 (CD44).Связывание HA с CD44 ингибирует экспрессию интерлейкина (IL) -1β, что приводит к снижению продукции матриксной металлопротеиназы (MMP) -1, 2, 3, 9 и 13 [32, 34]. Было показано, что это связывание с CD44 имеет больший эффект для продуктов HA с более высокой молекулярной массой [21]. HA также связывается с рецептором опосредованной гиалуронаном подвижности (RHAMM), который, как полагают, способствует хондропротекции в дополнение к связыванию с CD44 [34]. Ингибирование экспрессии IL-1β посредством связывания CD44 осуществляется посредством индукции митоген-активируемой протеинкиназы фосфатазы (MKP) -1: негативного регулятора IL-1β [43].Это ингибирование различных MMP препятствует активности катаболических ферментов в суставном хряще [59]. Было показано, что HMW HA имеет больший эффект в ингибирующем действии на продукцию MMP [21], хотя эти результаты неясны, поскольку другое исследование продемонстрировало благоприятный ингибирующий эффект MMP продуктов с более низкой молекулярной массой (LMW) [72].
События апоптоза хондроцитов дополнительно уменьшаются за счет связывания HA-CD44 за счет снижения экспрессии дезинтегрина и металлопротеиназы с тромбоспондиновыми мотивами (ADAMTS) [38].Эти пептидазы участвуют в расщеплении важных синовиальных компонентов, включая аггрекан, версикан и бревикан [81, 82]. Было показано, что различная экспрессия ADAMTS снижается в результате связывания HA-CD44, обеспечивая дополнительный режим хондропротекции для лечения IA-HA [36, 38, 43]. Производство активных форм кислорода (АФК), таких как оксид азота (NO), приводит к дегенерации хряща за счет увеличения апоптоза хондроцитов [33]. Лечение IA-HA продемонстрировало снижение индуцированного IL-1β окислительного стресса за счет ингибирования продукции NO в синовиальной оболочке [48, 57].Дополнительные результаты связывания CD44-HA, приводящие к хондропротекторным эффектам, упомянутые в современной литературе, включают снижение синтеза простагландина E2 (PGE2) [42, 46, 61] и повышенную сверхэкспрессию белка теплового шока 70 (Hsp70) [25, 70]. Эти эффекты аналогичным образом обеспечивают терапевтический эффект за счет уменьшения апоптоза хондроцитов. Важно отметить, что HMW продукты HA продемонстрировали большее подавление экспрессии PGE2, чем LMW компараторы в сравнительном исследовании, что привело к более сильному хондрозащитному эффекту [61].
Синтез протеогликанов и гликозаминогликанов
В 22 из идентифицированных исследований сообщалось об усилении синтеза протеогликанов и гликозаминогликанов, связанном с лечением IA-HA [27, 42, 44, 48, 62, 69, 83–98]. По мере прогрессирования ОА внутренние концентрации протеогликана и ГАГ в хряще снижаются. Результаты показали, что обработка IA-HA стимулировала синтез протеогликана, задерживая прогрессирование OA [69, 88]. Аггрекан является первичным протеогликаном в суставном хряще, и показано, что лечение IA-HA как подавляет деградацию аггрекана, так и способствует внутреннему развитию аггрекана [62, 93].Показано, что обработка IA-HA мобилизует вновь синтезированный протеогликан во внешний матрикс хондроцитов, потенциально обеспечивая защиту от деградации. Внешний HA способствует перемещению вновь синтезированного протеогликана из ассоциированного с клетками матрикса в далее удаленный матрикс в модели альгинатного геля, что предполагает, что IA-HA может обеспечивать терапевтическое облегчение OA за счет укрепления межтерриториального хрящевого матрикса [92]. Маркер синтеза протеогликана, сульфат ( 35 SO 4 ), как видно, все больше включается в хондроциты после введения HA [87].Биологический путь, в котором HA изменяет уровни аггрекана, проявляется через эффекты связывания CD44 и молекулы межклеточной адгезии (ICAM) -1 [62]. В одном исследовании было показано, что HMW HA обеспечивает больший эффект синтеза протеогликанов, чем LMW HA, за счет стимуляции пути инсулиноподобного фактора роста (IGF) -1 [89]. Также показано, что лечение IA-HA увеличивает выработку эндогенного ГАГ. Обработка IA-HA не только дополняла синовиальную оболочку HA, но и способствовала внутренней продукции HA [27].
Противовоспалительное
В 21 из идентифицированных исследований сообщалось о противовоспалительных эффектах лечения IA-HA [13, 20, 21, 25, 27, 52, 54, 55, 68, 72, 96, 97 , 99–107].Известно, что IL-1β демонстрирует провоспалительные эффекты, и вышеупомянутое подавление экспрессии IL-1β с помощью HA обеспечивает противовоспалительные эффекты [52]. IL-1β является ключевым медиатором противовоспалительного действия HA и регулируется посредством связывания HA-CD44 [59, 104]. Подавление IL-1β приводит к подавлению MMPs, как упоминалось ранее, что также способствует противовоспалительному эффекту HA [52]. Дальнейшее подавление провоспалительных медиаторов IL-8, IL-6, PGE 2 и фактора некроза опухоли (TNFα) обеспечивает противовоспалительные эффекты лечения IA-HA [13, 21].Связь между Toll-подобными рецепторами (TLR) и воспалительным ответом демонстрируется, поскольку продукты деградации HA индуцируют воспалительный ответ через взаимодействие CD44 и TLR. Этот провоспалительный ответ от связывания продукта деградации HA с рецепторами TLR и CD44 приводит к увеличению продукции Nf-kB, IL-1β, TNFα, IL-6 и IL-33 [105]. Было продемонстрировано, что HMW HA подавляет множество медиаторов воспаления посредством связывания TLR 2 и 4, включая TNF-α, IL-1-β, IL-17, MMP-13 и индуцибельную синтазу оксида азота (iNOS) [106].Прямая корреляция между молекулярной массой и противовоспалительным действием продемонстрировала более сильные эффекты ингибирования PGE 2 и IL-6 при лечении HMW HA [13]. IL-6 представляет собой провоспалительный цитокин, регулируемый ядерным фактором, энхансером легкой каппа-цепи активированных В-клеток (Nf-кB). Связывание HA с ICAM-1 подавляет Nf-kB, что, в свою очередь, снижает продукцию IL-6 [21, 104]. HMW HA, подавляющая регуляцию TNFα, IL-1B и IL-8, является дополнительным фактором, способствующим противовоспалительным эффектам, обеспечиваемым HMW HA [72, 97].
Механический
Десять из включенных исследований описывали механические эффекты ГК при лечении ОА коленного сустава [41, 49, 86, 108–114]. Показано, что вязкая природа лечения ГК смазывает суставную капсулу, предотвращая дегенерацию за счет снижения трения [86]. ГК дополнительно защищает капсулу сустава за счет благотворного эффекта поглощения ударов. HA обеспечивает амортизацию для поглощения давления и вибрации в суставе, которые в противном случае могут привести к деградации хондроцитов [41]. Сообщается, что колени с остеоартритом имеют более высокое трение в суставной щели, чем здоровые колени, чему противодействует способность суставной смазки, которой обладает HA [110].Было продемонстрировано, что HMW HA обеспечивает больший эффект снижения трения благодаря своим вязким свойствам. Уменьшение трения в суставе может обеспечить терапевтический эффект, поскольку хрящ защищен от механической деградации [111].
Субхондральная кость
Восемь из включенных исследований описали эффекты, которые IA-HA оказывает на субхондральную кость [23, 31, 32, 45, 115–118]. Ранее было показано, что взаимодействие между остеобластами субхондральной кости и хондроцитами суставного хряща в суставах с остеоартритом изменяет экспрессию ADAMTS-4/5 и MMP-1, MMP-2, MMP-3, MMP-8, MMP-9 и MMP-13. и регуляция, опосредованная митоген-активируемой протеинкиназой (MAPK) и сигнальными путями, регулируемыми внеклеточными сигналами киназ 1 и 2 (ERK 1/2) [118].IA-HA также влияет на субхондральную кость путем подавления MMP-13 и IL-6 через связывание CD44, что потенциально предотвращает аномальный метаболизм костной ткани [116]. Было высказано предположение, что подавление экспрессии MMP-13 с помощью IA-HA является критическим фактором воздействия на субхондральную кость при ОА [117]. Эффект, который IA-HA оказывает на MMPs, особенно MMP-13, посредством связывания CD44, как предполагалось, ингибирует эффекты OA в субхондральной кости в многочисленных доклинических фундаментальных научных исследованиях [32, 45, 116–118].ГК эффективно изменяет плотность и толщину субхондральной кости за счет изменений трабекулярной структуры, что приводит к большей податливости субхондральной кости. В конечном итоге показано, что это снижает нагрузку на хрящ во время ударной нагрузки [23]. Признаком стимуляции IA-HA обмена коллагена типа II на границе раздела хрящ и костей является повышение уровней сшивок коллагена на карбокси-конце (CTX) -II в моче, наблюдаемое после лечения IA-HA, которое продемонстрировало улучшение остеоартрита колена [31].В конечном итоге ГК, по-видимому, ограничивает изменения субхондральной кости, характерные для раннего ОА [115].
Анальгетик
Шесть из включенных статей описывают обезболивающие эффекты лечения IA-HA [76, 80, 119–122]. Одна инъекция ГК продемонстрировала значительное снижение связанного с болью поведения на мышиной модели [119]. Одно исследование показало, что HA не связывается напрямую с рецепторами брадикинина, но оказывает обезболивающее за счет взаимодействия с рецепторами HA и / или свободными нервными окончаниями в суставной ткани [121].Было показано, что обезболивающие эффекты HA проявляются в механочувствительных ионных каналах, активируемых растяжением, где активность канала значительно снижается при связывании HA [122]. Было показано, что HMW HA снижает механическую чувствительность ионных каналов, активируемых растяжением, которые эффективно блокируют болевой ответ. Было обнаружено, что LMW HA менее эффективен в блокировании этого ответа [122]. ГК снижает действие ноцицепторов суставов, что обеспечивает уменьшение боли в суставе. На сенсибилизированные ноцицептивные окончания в суставной ткани влияет концентрация HA, снижая болевую реакцию, проявляемую этими терминалами [120].
Обсуждение
Наш обзор существующей литературы дает общее мнение о том, что IA-HA при ОА коленного сустава имеет положительные эффекты через несколько механизмов действия; однако преобладающий механизм терапевтического эффекта не совсем ясен [2]. В перспективе неясно, какие из этих механизмов являются клинически значимыми, поскольку понятно, что полезные механизмы действия не обязательно переносятся на пользу в клинических условиях.В настоящее время предполагается, что клиническая польза IA-HA при ОА коленного сустава обусловлена несколькими параллельными механизмами действия, а не каким-либо одним конкретным механизмом действия.
Большая часть экзогенной ГК остается в суставе в течение нескольких дней; однако клинические терапевтические эффекты лечения ГК могут наблюдаться в течение 6 месяцев или более. Это может указывать на то, что IA-HA обладает свойствами, модифицирующими болезнь, и действует не только за счет восстановления вязкоупругих свойств синовиальной жидкости [123].Инъекции ГК могут стимулировать эндогенную продукцию дополнительной ГК синовиоцитами человека, способствуя нормализации распределения ГК в синовиальной жидкости [124]. В доклинических фундаментальных научных исследованиях во многих сообщениях описывается связывание CD44 как основной способ, при котором НА обеспечивает действие против ОА коленного сустава. Показано, что CD44-опосредованные эффекты IA-HA вносят вклад в потенциальную хондрозащиту, синтез протеогликанов / гликозаминогликанов, противовоспалительные и субхондральные механизмы. Показано, что это связывание оказывает разнообразные эффекты на многочисленные сигнальные пути, каждый из которых демонстрирует своего рода вмешательство в прогрессирование ОА [13, 21, 32, 36, 38, 42, 43, 46, 59, 61, 104 , 116].Было высказано предположение, что подавление IL-1β и IL-6 и последующие эффекты этого подавления являются ключевым фактором в терапевтическом механизме, обеспечиваемом связыванием HA-CD44 [123]. Очевидно, что связывание HA-CD44 является основным компонентом механизма, в котором HA обеспечивает терапевтический эффект; однако существуют дополнительные механизмы, которые обеспечивают альтернативные пути эффективности лечения ГК при ОА коленях, включая связывание ICAM, механические улучшения, связанные с поглощением удара и смазкой, увеличение обмена коллагена типа II на границе раздела хрящ / кость, а также анальгетические эффекты. через взаимодействие с нервными окончаниями и ноцицепторами суставов [31, 41, 86, 97, 121, 122].Связывание HA с рецептором RHAMM способствует заживлению ран, активирует функции промиграции и инвазии, регулирует клеточные ответы на факторы роста и играет роль в миграции и подвижности фибробластов [125–127]. Эти результаты связывания HA-RHAMM являются потенциальными факторами, участвующими в эффектах модификации заболевания при лечении HA при ОА.
Имеются данные, которые демонстрируют, что определенные внутренние свойства определенных продуктов IA-HA могут давать положительные результаты по сравнению с другими продуктами IA-HA.Наиболее известным из этих внутренних свойств является молекулярная масса. В отличие от предыдущего фундаментального научного обзора, проведенного Ghosh et al., Который предположил потенциальное преимущество LMW HA в обеспечении восстановления реологических свойств по сравнению с HMW HA [128], данные текущего обзора продемонстрировали благоприятные результаты для лечения HMW HA. Текущий обзор поддерживает точку зрения, что HMW HA обеспечивает превосходные хондропротекторные, протеогликановые и гликозаминогликановые механизмы синтеза, противовоспалительные, механические и обезболивающие механизмы действия [61, 89, 97, 111, 122].Исследование Huang et al. продемонстрировали превосходные противовоспалительные эффекты HMW HA, но лучшие хондрозащитные эффекты LMW HA; однако эти результаты относительно хондрозащиты неясны из-за отсутствия дополнительных доказательств в фундаментальной научной литературе по ОА коленного сустава [72]. Было показано, что повышенная продукция воспалительных цитокинов и хемокинов, привлечение медиаторов воспаления и образование кровеносных сосудов являются ответом на LMW HA ниже 500 кДа. Хотя средний молекулярный вес доступных продуктов ГК на рынке сильно различается, следует отметить, что, насколько нам известно, все доступные в настоящее время продукты во всем мире имеют молекулярную массу> 500 кДа [129, 130].Анализ взаимодействия HA-CD44 показал, что размер HA имеет прямое влияние на сродство, при котором HA связывается с рецептором CD44 [131]. Эти результаты демонстрируют способность HMW HA лечить прогрессирование ОА коленного сустава посредством связывания HA с CD44. Эти фундаментальные научные данные согласуются с систематическими обзорами клинических испытаний и сравнительных исследований, которые продемонстрировали, что HMW HA обеспечивает большую терапевтическую пользу, чем LMW HA при лечении ОА коленного сустава [6, 132], хотя текущая литература не обеспечивает консенсуса в отношении различие в клинической эффективности ГК с низким и высоким молекулярным весом [133].
Традиционно продукты ГК получали из птичьих источников; однако некоторые доступные продукты производятся путем биологической ферментации. Этот процесс позволяет избежать присутствия молекул птичьего происхождения, которые, как предполагается, могут быть потенциальной причиной неблагоприятных местных реакций [134]. Отсутствуют подробные отчеты о потенциале Bio-HA по сравнению с AD-HA. Одно исследование показало, что места инъекции AD-HA могут быть причиной синовита в их группе пациентов, но точный патологический агент неизвестен [135].Результаты второго исследования также указывают на способность гилана AD-HA вызывать гранулематозную реакцию типа гигантских клеток на инородное тело [136]. Исследования показали, что обострения, связанные с инъекцией гилана, могут быть связаны с накоплением гилана или продуктов его распада, поскольку обострения в месте инъекции обычно не возникают при первой инъекции [14]. Было показано, что белки птичьего происхождения являются причиной обострения в месте инъекции, поскольку антитела к белку куриной сыворотки присутствовали у пациентов, у которых наблюдалась неблагоприятная реакция в месте инъекции после лечения AD-HA [15].Имеются некоторые высококачественные клинические доказательства того, что Bio-HA имеет значительно меньшую частоту нежелательных явлений в месте инъекции, чем AD-HA [134]; однако в современной литературе это не исследовано досконально. Необходимо более всестороннее исследование разницы в частоте нежелательных явлений в месте инъекции между Bio-HA и AD-HA как с фундаментальной науки, так и с клинической точки зрения.
Этот обзор имеет методологическую силу благодаря систематическому и тщательному поиску доступных фундаментальных научных данных в нескольких базах данных.Текущий отчет также демонстрирует строгость в его представлении множественных механизмов, в которых действует HA, предоставляя доказательства обо всех механизмах, независимо от того, подробно или нечасто описаны в текущей литературе. Ограничения данного исследования возникают из-за субъективной классификации включенной статьи механизм действия основных выводов. Включенные статьи могут кратко упоминать альтернативные механизмы действия, но не были отнесены к соответствующей категории, потому что упомянутый альтернативный механизм не был ключевым результатом или заключением исследования.В будущих исследованиях следует проанализировать взаимосвязь между различными механизмами, представленными в этом отчете, и прояснить, как эти механизмы перекрываются и могут работать вместе для облегчения симптомов ОА коленного сустава. Дальнейшие исследования также должны быть направлены на выявление различий между механизмами, проявляемыми продуктами с высокой и низкой молекулярной массой, а также на анализ различий в профилях безопасности между Bio-HA и AD-HA.
Выводы
Доклиническая фундаментальная научная литература предоставляет доказательства многочисленных механизмов, с помощью которых IA-HA может обеспечить клиническую пользу при ОА коленного сустава.Хондропротекция является наиболее часто описываемым механизмом, причем связывание HA-CD44 является наиболее частым источником этих эффектов. Сообщается также, что IA-HA обеспечивает синтез протеогликанов и гликозаминогликанов, оказывает противовоспалительное, механическое, субхондральное и обезболивающее действие. Имеются данные о благоприятных результатах лечения HMW HA по сравнению с лечением LMW HA. Также показано, что Bio HA обеспечивает более выгодный профиль безопасности по сравнению с AD-HA, поскольку отчеты демонстрируют связь между обострениями в месте инъекции и белками птичьего происхождения.Существует множество описанных механизмов, в которых показано, что ИА-ГК лечит ОА коленного сустава, а также многочисленные характеристики продукта, которые влияют на результаты лечения ИА-ГК. Чтобы признать применимость и целесообразность лечения IA-HA для колено О.А. Дальнейшие исследования должны быть сосредоточены не только на обезболивании, обеспечиваемом лечением IA-HA, но и на свойствах модификации заболевания, которыми может обладать этот метод лечения.
Благодарности
Этот обзор финансируется Ferring Pharmaceuticals Inc. Авторы хотели бы поблагодарить Марка Филлипса и Global Research Solutions Inc. за их помощь в подготовке рукописи.
Аббревиатуры
| ADAMTS | Дезинтегрин и металлопротеиназа с тромбоспондиновыми мотивами | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| AD-HA | Гиалуроновая кислота птичьего происхождения | Биологическая кислота | Биологическая кислота | CD | Кластер дифференцировки | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CTX | Сшивки карбоксиконцевого коллагена | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ERK 1/2 | Киназа 1 и 2, регулируемая внеклеточным сигналом | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| GAG12122 90og3511 | Гиалуроновая кислота | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| HMW | Более высокая молекулярная масса | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Hsp70 | Белок теплового шока 70 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| IA | Внутрисуставной | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| IL | Интерлейкин | |||||||||||||||||||
| iNOS | Индуцируемый оксид азота LMW, низкомолекулярный вес | |||||||||||||||||||
| MAPK | MAPK | Митоген-активированная протеинкиназа | 90sp MMP | Металлопротеиназа | ||||||||||||||||
| Nf-кB | Ядерный фактор, усилитель легкой цепи каппа активированных В-клеток | |||||||||||||||||||
| NO | Оксид азота | |||||||||||||||||||
| 12 НПВП | OA | Остеоартрит | ||||||||||||||||||
| PGE2 | Простагландин E2 | |||||||||||||||||||
| RHAMM | Рецептор для подвижности, опосредованной гиалуронаном |
Фут примечания
Конкурирующие интересы
Рой Д.Альтман: Консультант: Cytori, DuPuy (Bioventus Global), Ferring, Flexion, Iroko, McNeil, Novartis, Oletec, Pfizer, QMed, Rotta, Strategic Science and Technologies, Teva.
Спикер: Ферринг, Ироко.
Аджай Манджу: Нет конфликта интересов
Анке Фирлингер: оплачиваемый сотрудник Ferring Pharmaceuticals Inc.
Файзан Ниази: оплачиваемый сотрудник Ferring Pharmaceuticals Inc.
Мэтью Николлс: работает в консультативных советах Ferring.
Вклад авторов
AF и FN участвовали в разработке и разработке исследования. RDA обеспечило интерпретацию данных и внесение значительного письменного вклада в рукопись. Все авторы представили рукопись критическую рецензию и исправления. Все авторы прочитали и одобрили окончательную рукопись.
Ссылки
1. Cheng OT, Souzdalnitski D, Vrooman B, Cheng J. Доказательные инъекции в колено для лечения артрита. Pain Med.2012. 13 (6): 740–753. DOI: 10.1111 / j.1526-4637.2012.01394.x. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 2. Морленд Л.В. Внутрисуставной гиалуронан (гиалуроновая кислота) и гиланы для лечения остеоартрита: механизмы действия. Лечение артрита Res. 2003; 5 (2): 54. DOI: 10.1186 / ar623. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 3. Беллами Н., Кэмпбелл Дж., Робинсон В., Джи Т., Борн Р., Уэллс Г. Вискозиметрические добавки для лечения остеоартрита колена. Кокрановская база данных Syst Rev.2006; 2 [PubMed] [Google Scholar] 4. Тригкилидас Д., Ананд А. Эффективность внутрисуставных инъекций гиалуроновой кислоты при лечении боли в коленях при остеоартрите. Ann R Coll Surg Engl. 2013. 95 (8): 545–551. DOI: 10.1308 / rcsann.2013.95.8.545. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 5. Colen S, van den Bekerom MP, Mulier M, Haverkamp D. Гиалуроновая кислота в лечении остеоартрита коленного сустава: систематический обзор и метаанализ с упором на эффективность различных продуктов. BioDrugs.2012. 26 (4): 257–268. DOI: 10.1007 / BF03261884. [PubMed] [CrossRef] [Google Scholar] 6. Rutjes A, Juni P, da Costa B, Trelle S, Nuesch E, Reichenbach S. Viscosupplementation для остеоартрита коленного сустава: систематический обзор и метаанализ. Ann Intern Med. 2012; 157: 180–191. DOI: 10.7326 / 0003-4819-157-3-201208070-00473. [PubMed] [CrossRef] [Google Scholar] 7. Баннуру Р.Р., Натов Н.С., Обадан И.Е., Прайс Л.Л., Шмид С.Х., Макалиндон Т.Е. Терапевтическая траектория гиалуроновой кислоты по сравнению с кортикостероидами в лечении остеоартрита коленного сустава: систематический обзор и метаанализ.Ревматоидный артрит. 2009. 61 (12): 1704–1711. DOI: 10.1002 / art.24925. [PubMed] [CrossRef] [Google Scholar] 8. Хабиб Г.С. Системные эффекты внутрисуставных кортикостероидов. Clin Rheumatol. 2009. 28 (7): 749–756. DOI: 10.1007 / s10067-009-1135-х. [PubMed] [CrossRef] [Google Scholar] 9. Элморси С., Фунакоши Т., Сасазава Ф., Тодох М., Тадано С., Ивасаки Н. Хондропротекторные эффекты высокомолекулярной поперечно-сшитой гиалуроновой кислоты на модели остеоартрита коленного сустава кролика. Хрящевой артроз. 2014; 22 (1): 121–127.DOI: 10.1016 / j.joca.2013.10.005. [PubMed] [CrossRef] [Google Scholar] 10. Kosinska MK, Ludwig TE, Liebisch G, Zhang R, Siebert HC, Wilhelm J, et al. Смазки для суставов при остеоартрите и ревматоидном артрите имеют измененные уровни и молекулярные формы. PLoS One. 2015; 10 (5) DOI: 10.1371 / journal.pone.0125192. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 11. Band PA, Heeter J, Wisniewski HG, Liublinska V, Pattanayak CW, Karia RJ, et al. Распределение молекулярной массы гиалуроновой кислоты связано с риском прогрессирования остеоартрита коленного сустава.Хрящевой артроз. 2015; 23 (1): 70–76. DOI: 10.1016 / j.joca.2014.09.017. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 12. Диас-Гальего Л., Прието Дж. Г., Коронель П., Гамазо Л. Е., Гимено М., Альварес А. И.. Апоптоз и оксид азота в экспериментальной модели остеоартрита у кролика после лечения гиалуроновой кислотой. J Orthop Res. 2005. 23 (6): 1370–1376. DOI: 10.1016 / j.orthres.2005.05.003.1100230619. [PubMed] [CrossRef] [Google Scholar] 13. Lajeunesse D, Delalandre A, Martel-Pelletier J, Pelletier J-P.Гиалуроновая кислота устраняет аномальную синтетическую активность остеоартрита субхондральных костных остеобластов человека. Кость. 2003. 33 (4): 703–710. DOI: 10.1016 / S8756-3282 (03) 00206-0. [PubMed] [CrossRef] [Google Scholar] 14. Pullman-Mooar S, Mooar P, Sieck M, Clayburne G, Schumacher HR. Есть ли характерные воспалительные обострения после внутрисуставных инъекций hylan g-f 20? J Rheumatol, декабрь 2002 г., 29 (12): 2611–2614. [PubMed] [Google Scholar] 15. Гольдберг В.М., Куттс Р.Д. Псевдосептические реакции на добавку hylan viscos: диагностика и лечение.Clin Orthop Relat Res, февраль 2004 г .; 419: 130–137. DOI: 10.1097 / 00003086-200402000-00021. [PubMed] [CrossRef] [Google Scholar] 16. Ando A, Hagiwara Y, Chimoto E, Hatori K, Onoda Y, Itoi E. Внутрисуставная инъекция гиалуронана снижает потерю хондроцитов в модели с иммобилизованным коленом крысы. Tohoku J Exp Med. 2008. 215 (4): 321–331. DOI: 10.1620 / tjem.215.321. [PubMed] [CrossRef] [Google Scholar] 17. Ariyoshi W, Okinaga T, Knudson CB, Knudson W., Nishihara T. Высокомолекулярная гиалуроновая кислота регулирует образование остеокластов путем ингибирования активатора рецептора лиганда NF-kappaB через Rho-киназу.Хрящевой артроз. 2014. 22 (1): 111–120. DOI: 10.1016 / j.joca.2013.10.013. [PubMed] [CrossRef] [Google Scholar] 18. Asari A, Miyauchi S, Matsuzaka S, Itoh T, Uchiyama Y. Гиалуронат на белке теплового шока и синовиальных клетках в модели остеоартрита у собак. Хрящевой артроз. 1996. 4 (3): 213–215. DOI: 10.1016 / S1063-4584 (96) 80018-5. [PubMed] [CrossRef] [Google Scholar] 19. Брун П., Панфило С., Дага Гордини Д., Кортиво Р., Абатанджело Г. Влияние гиалуронана на CD44-опосредованное выживание нормальных и поврежденных гидроксильными радикалами хондроцитов.Хрящевой артроз. 2003. 11 (3): 208–216. DOI: 10.1016 / S1063-4584 (02) 00352-7. [PubMed] [CrossRef] [Google Scholar] 20. Брун П., Заван Б., Виндини В., Скьявинато А., Поццуоли А., Якобеллис С. и др. In vitro ответ остеоартрозных хондроцитов и фибробластоподобных синовиоцитов на производное гиалуронанамида 500-730 кДа. J Biomed Mater Res B Appl Biomater. 2012. 100 (8): 2073–2081. DOI: 10.1002 / jbm.b.32771. [PubMed] [CrossRef] [Google Scholar] 21. Chang CC, Hsieh MS, Liao ST, Chen YH, Cheng CW, Huang PT и др.Гиалуронан регулирует PPARgamma и воспалительные реакции в клетках хондросаркомы человека, стимулированных IL-1beta, которые являются моделью остеоартрита. Carbohydr Polym. 2012; 90 (2): 1168–1175. DOI: 10.1016 / j.carbpol.2012.06.071. [PubMed] [CrossRef] [Google Scholar] 22. Creamer P, Sharif M, George E, Meadows K, Cushnaghan J, Shinmei M и др. Внутрисуставная гиалуроновая кислота при остеоартрозе коленного сустава: исследование механизмов действия. Хрящевой артроз. 1994. 2 (2): 133–140. DOI: 10.1016 / S1063-4584 (05) 80063-9.[PubMed] [CrossRef] [Google Scholar] 23. Динг М., Кристиан Даниэльсен С., Хвид И. Влияние гиалуронана на трехмерную микроархитектуру субхондральных костных тканей при первичном остеоартрозе морских свинок. Кость. 2005. 36 (3): 489–501. DOI: 10.1016 / j.bone.2004.12.010. [PubMed] [CrossRef] [Google Scholar] 24. Элерс Э.М., Беренс П., Вунш Л., Кунель В., Русслис М. Влияние гиалуроновой кислоты на морфологию и пролиферацию хондроцитов человека в первичной культуре клеток. Анн Анат. 2001. 183 (1): 13–17. DOI: 10.1016 / S0940-9602 (01) 80007-8. [PubMed] [CrossRef] [Google Scholar] 25. Галуа Л., Этьен С., Хенрионне С., Скала-Бертола Дж., Гроссин Л., Майнард Д. и др. Амбивалентные свойства гиалуроната и гилана при посттравматическом ОА коленного сустава крысы. Biomed Mater Eng. 2012. 22 (4): 235–242. [PubMed] [Google Scholar] 26. Gonzalez-Fuentes AM, Green DM, Rossen RD, Ng B. Внутрисуставная гиалуроновая кислота увеличивает биомаркер разрушения хряща у пациентов с остеоартрозом коленного сустава. Clin Rheumatol. 2010. 29 (6): 619–624. DOI: 10.1007 / s10067-010-1376-8. [PubMed] [CrossRef] [Google Scholar] 27. Гринберг Д.Д., Стокер А., Кейн С., Кокрелл М., Кук Дж. Биохимические эффекты двух различных продуктов гиалуроновой кислоты в модели совместного культивирования остеоартрита. Хрящевой артроз. 2006. 14 (8): 814–822. DOI: 10.1016 / j.joca.2006.02.006. [PubMed] [CrossRef] [Google Scholar] 28. Гришко В., Сюй М., Хо Р., Мейтс А., Уотсон С., Ким Дж. Т. и др. Влияние гиалуроновой кислоты на функцию митохондрий и митохондриальный апоптоз после окислительного стресса в хондроцитах человека.J Biol Chem. 2009. 284 (14): 9132–9139. DOI: 10.1074 / jbc.M804178200. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 29. Хашизуме М., Михара М. Желаемый эффект комбинированной терапии с высоким молекулярным гиалуронатом и НПВП на продукцию ММП. Хрящевой артроз. 2009. 17 (11): 1513–1518. DOI: 10.1016 / j.joca.2009.04.018. [PubMed] [CrossRef] [Google Scholar] 30. Homandberg GA, Hui F, Wen C, Kuettner KE, Williams JM. Гиалуроновая кислота подавляет хондролиз хряща, опосредованный фрагментом фибронектина: I. In vitro . Хрящевой артроз. 1997. 5 (5): 309–319. DOI: 10.1016 / S1063-4584 (97) 80035-0. [PubMed] [CrossRef] [Google Scholar] 31. Исидзима М., Накамура Т., Симидзу К., Хаяси К., Кикучи Х., Соен С. и др. Различные изменения биомаркера CTX-II после внутрисуставной инъекции высокомолекулярной гиалуроновой кислоты и пероральных нестероидных противовоспалительных препаратов для пациентов с остеоартрозом коленного сустава: многоцентровое рандомизированное контролируемое исследование. Osteoarthr Cartil. 2013; 21: S292. DOI: 10.1016 / j.joca.2013.02.612. [CrossRef] [Google Scholar] 32. Джулови С.М., Ясуда Т., Шимицу М., Хирамицу Т., Накамура Т. Ингибирование индуцированного интерлейкином-1бета продукции матриксных металлопротеиназ гиалуронаном через CD44 в суставном хряще человека. Ревматоидный артрит. 2004. 50 (2): 516–525. DOI: 10.1002 / art.20004. [PubMed] [CrossRef] [Google Scholar] 33. Kalaci A, Yilmaz HR, Aslan B, Sogut S, Yanat AN, Uz E. Влияние гиалуронана на уровни оксида азота и активность супероксиддисмутазы в синовиальной жидкости при остеоартрите коленного сустава.Clin Rheumatol. 2007. 26 (8): 1306–1311. DOI: 10.1007 / s10067-006-0504-у. [PubMed] [CrossRef] [Google Scholar] 34. Карна Э., Милтык В, Суразинский А, Палка Я. Защитный эффект гиалуроновой кислоты на индуцированную интерлейкином-1 дерегуляцию передачи сигналов рецептора бета1-интегрина и инсулиноподобного фактора роста-I и биосинтез коллагена в культивируемых хондроцитах человека. Mol Cell Biochem. 2008. 308 (1-2): 57–64. DOI: 10.1007 / s11010-007-9612-5. [PubMed] [CrossRef] [Google Scholar] 35. Кобаяши К., Амиэль М., Харвуд Флорида, Хили Р.М., Сонода М., Мория Х. и др.Долгосрочные эффекты гиалуронана во время развития остеоартрита после частичной менискэктомии на модели кролика. Хрящевой артроз. 2000. 8 (5): 359–365. DOI: 10.1053 / joca.1999.0310. [PubMed] [CrossRef] [Google Scholar] 36. Кога Х. Действие гиалуроновой кислоты на суставной хрящ, пораженный артритом. Connect Tissue Res. 2012; 53 (1): 48–93. DOI: 10.3109 / 03008207.2011.637147. [CrossRef] [Google Scholar] 37. Лазаро Дж., Гранадо П., дель Соль Дж., Медина А., Гальего Л., Сандовал Д., Фернандес Дж. Роль различных гиалуроновых кислот в суставном хряще кролика.Открытая Ортопедия J. 2010; 4: 44–47. DOI: 10,2174 / 1874325001004010044. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 38. Ли Дж., Горски Д. Д., Анемает В., Веласко Дж., Такеучи Дж., Сэнди Дж. Д. и др. Инъекция гиалуронана при остеоартрите мышей предотвращает индуцированную TGFbeta 1 синовиальную неоваскуляризацию и фиброз и поддерживает целостность суставного хряща посредством CD44-зависимого механизма. Arthritis Res Ther. 2012; 14 (3): R151. DOI: 10.1186 / ar3887. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 39.Ли П., Райчева Д., Хавс М., Моран Н., Ю Икс, Ван Ф. и др. Hylan G-F 20 поддерживает целостность хряща и снижает образование остеофитов при остеоартрите за счет как анаболических, так и антикатаболических механизмов. Хрящевой артроз. 2012. 20 (11): 1336–1346. DOI: 10.1016 / j.joca.2012.07.004. [PubMed] [CrossRef] [Google Scholar] 40. Лисиньоли Г., Грасси Ф., Зини Н., Тонегуцци С., Пьячентини А., Гуидолин Д. и др. Анти-Fas-индуцированный апоптоз в хондроцитах, сниженный гиалуронаном: свидетельство инвазии CD44 и CD54 (молекула межклеточной адгезии 1).Ревматоидный артрит. 2001. 44 (8): 1800–1807. DOI: 10.1002 / 1529-0131 (200108) 44: 8 <1800 :: AID-ART317> 3.0.CO; 2-1. [PubMed] [CrossRef] [Google Scholar] 41. Lu HT, Sheu MT, Lin YF, Lan J, Chin YP, Hsieh MS и др. Инъекционная терапия гидрогелем доксициклина гиалуроновой кислоты при экспериментальном остеоартрите кроликов. BMC Vet Res. 2013; 9: 68. DOI: 10.1186 / 1746-6148-9-68. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 42. Манейро Э., де Андрес М.С., Фернандес-Суэйро Ю.Л., Гальдо Ф., Бланко Ф.Дж. Биологическое действие гиалуронана на суставные хондроциты остеоартрита человека: важность молекулярной массы.Clin Exp Rheumatol. 2004. 22 (3): 307–312. [PubMed] [Google Scholar] 43. Михара М., Хашизуме М. Влияние высокомолекулярной гиалуроновой кислоты на индукцию ферментов деградации матрикса IL-6, IL-1β и TNF-α Osteoarthr Cartil. 2012; 20: S134 – S135. DOI: 10.1016 / j.joca.2012.02.181. [CrossRef] [Google Scholar] 44. Мики Ю., Терамура Т., Томияма Т., Онодера Ю., Мацуока Т., Фукуда К. и др. Гиалуронан обратил синтез протеогликанов, подавленный механическим стрессом: возможное участие антиоксидантного эффекта.Inflamm Res. 2010. 59 (6): 471–477. DOI: 10.1007 / s00011-009-0147-у. [PubMed] [CrossRef] [Google Scholar] 45. Младенович З., Заурел А.С., Беренбаум Ф., Жак С. Потенциальная роль гиалуроновой кислоты в костях при остеоартрите: матриксные металлопротеиназы, агреканазы и экспрессия RANKL частично предотвращаются гиалуроновой кислотой в остеобластах, стимулированных интерлейкином-1. J Rheumatol. 2014. 41 (5): 945–954. DOI: 10.3899 / jrheum.130378. [PubMed] [CrossRef] [Google Scholar] 46. Mongkhon JM, Thach M, Shi Q, Fernandes JC, Fahmi H, Benderdour M.Гиалуроновая кислота, модифицированная сорбитом, снижает окислительный стресс, апоптоз и медиаторов воспаления и катаболизма в хондроцитах человека, страдающих остеоартритом. Inflamm Res. 2014; 63 (8): 691–701. DOI: 10.1007 / s00011-014-0742-4. [PubMed] [CrossRef] [Google Scholar] 47. Оно S, Im HJ, Knudson CB, Knudson W. Индуцированная гиалуронановым олигосахаридом активация факторов транскрипции в суставных хондроцитах крупного рогатого скота. Ревматоидный артрит. 2005. 52 (3): 800–809. DOI: 10.1002 / art.20937. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 48.Peng H, Zhou JL, Liu SQ, Hu QJ, Ming JH, Qiu B. Гиалуроновая кислота ингибирует апоптоз, вызванный оксидом азота, и дедифференцировку суставных хондроцитов in vitro . Inflamm Res. 2010. 59 (7): 519–530. DOI: 10.1007 / s00011-010-0156-х. [PubMed] [CrossRef] [Google Scholar] 49. Плаас А., Ли Дж., Риеско Дж., Дас Р., Сэнди Дж. Д., Харрисон А. Внутрисуставная инъекция гиалуронана предотвращает эрозию хряща, периартикулярный фиброз и механическую аллодинию и нормализует время пребывания в стойке при остеоартрите коленного сустава у мышей.Arthritis Res Ther. 2011; 13 (2): R46. DOI: 10.1186 / ar3286. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 50. Цю Б., Лю С. К., Пэн Х. Влияние гиалуроната натрия на экспрессию iNOS в синовиальной оболочке и содержание NO в синовиальной жидкости кроликов с травматическим остеоартритом. Chin J Traumatol. 2008. 11 (5): 293–296. DOI: 10.1016 / S1008-1275 (08) 60059-0. [PubMed] [CrossRef] [Google Scholar] 51. Сакакибара Ю., Миура Т., Ивата Х, Кикучи Т., Ямагути Т., Йошими Т. и др. Влияние высокомолекулярного гиалуроната натрия на иммобилизованное колено кролика.Clin Orthop Relat Res. 1994; 299: 282–292. [PubMed] [Google Scholar] 52. Сасаки А., Сасаки К., Конттинен Ю.Т., Сантавирта С., Такахара М., Такей Х. и др. Гиалуронат подавляет индуцированную интерлейкином-1бета экспрессию матриксной металлопротеиназы (MMP) -1 и MMP-3 в синовиальных клетках человека. Tohoku J Exp Med. 2004. 204 (2): 99–107. DOI: 10.1620 / tjem.204.99. [PubMed] [CrossRef] [Google Scholar] 53. Симидзу С., Йошиока М., Коуттс Р.Д., Харвуд Флорида, Кубо Т., Хирасава И. и др. Долгосрочные эффекты гиалуронана при экспериментальном остеоартрозе коленного сустава кролика.Хрящевой артроз. 1998. 6 (1): 1–9. DOI: 10.1053 / joca.1997.0086. [PubMed] [CrossRef] [Google Scholar] 54. Смит М.М., Торт М.А., Гош П., Скьявинато А., Рид Р.А., Литтл СВ. Значительная синовиальная патология в модели менискэктомии остеоартрита: модификация внутрисуставной гиалуроновой терапией. Ревматология (Оксфорд) 2008; 47 (8): 1172–1178. DOI: 10.1093 / ревматология / ken219. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 55. Смит М.М., Рассел А.К., Скьявинато А., Литтл CB. Гексадециламидное производное гиалуронана (HYMOVIS®) оказывает более благоприятное воздействие на хондроциты и синовиоциты человека, страдающие остеоартритом, чем немодифицированный гиалуронан.Журнал Инфламм (Лондон) 2013; 10:26. DOI: 10.1186 / 1476-9255-10-26. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 56. Такахаши К., Гумер Р.С., Харвуд Ф., Кубо Т., Хирасава Й., Амиэль Д. Эффекты гиалуронана на матриксную металлопротеиназу-3 (ММР-3), интерлейкин-1бета (ИЛ-1бета) и тканевой ингибитор металлопротеиназы-1 ( Экспрессия гена ТИМП-1) при развитии остеоартрита. Хрящевой артроз. 1999. 7 (2): 182–190. DOI: 10.1053 / joca.1998.0207. [PubMed] [CrossRef] [Google Scholar] 57.Такахаши К., Хашимото С., Кубо Т., Хирасава Ю., Лотц М., Амиэль Д. Гиалуронан подавлял выработку оксида азота в мениске и синовиальной оболочке модели остеоартрита кролика. J Orthop Res. 2001. 19 (3): 500–503. DOI: 10.1016 / S0736-0266 (00)
-X. [PubMed] [CrossRef] [Google Scholar] 58. Танака М., Масуко-Хонго К., Като Т., Нисиока К., Накамура Х. Подавляющее действие гиалуронана на продукцию MMP-1 и RANTES хондроцитами. Rheumatol Int. 2006. 26 (3): 185–190. DOI: 10.1007 / s00296-004-0547-9. [PubMed] [CrossRef] [Google Scholar] 59.Уодделл Д.Д., Коломыткин О.В., Данн С, Марино А.А. Гиалуронан подавляет активность металлопротеиназы, индуцированную IL-1beta, в синовиальной ткани. Clin Orthop Relat Res. 2007; 465: 241–248. [PubMed] [Google Scholar] 60. Ясуда Т. Активация ядерного фактора-kappaB пептидом коллагена II типа в суставных хондроцитах: его ингибирование гиалуронаном через рецепторы. Мод Ревматол. 2013. 23 (6): 1116–1123. DOI: 10.3109 / s10165-012-0804-9. [PubMed] [CrossRef] [Google Scholar] 61. Ясуи Т., Акацука М., Тобетто К., Хаяиси М., Андо Т.Влияние гиалуронана на индуцированную интерлейкином-1 альфа продукцию простагландина E2 в синовиальных клетках остеоартрита человека. Действия агентов. 1992. 37 (1-2): 155–156. DOI: 10.1007 / BF01987905. [PubMed] [CrossRef] [Google Scholar] 62. Ятабэ Т., Мочизуки С., Такидзава М., Чидзива М., Окада А., Кимура Т. и др. Гиалуронан подавляет экспрессию ADAMTS4 (аггреканазы-1) в хондроцитах человека, страдающих остеоартритом. Ann Rheum Dis. 2009. 68 (6): 1051–1058. DOI: 10.1136 / ard.2007.086884. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 63.Йошими Т., Кикучи Т., Обара Т., Ямагути Т., Сакакибара Ю., Ито Х. и др. Влияние высокомолекулярного гиалуроната натрия на экспериментальный остеоартроз, вызванный резекцией передней крестообразной связки кролика. Clin Orthop Relat Res. 1994; 298: 296–304. [PubMed] [Google Scholar] 64. Йошиока М., Симидзу С., Харвуд Флорида, Куттс Р.Д., Амиэль Д. Эффекты гиалуронана во время развития остеоартрита. Хрящевой артроз. 1997. 5 (4): 251–260. DOI: 10.1016 / S1063-4584 (97) 80021-0. [PubMed] [CrossRef] [Google Scholar] 65.Yu CJ, Ko CJ, Hsieh CH, Chien CT, Huang LH, Lee CW и др. Протеомный анализ хондроцитов, страдающих остеоартритом, выявляет регулируемые гиалуроновой кислотой белки, участвующие в хондропротекторном эффекте при окислительном стрессе. J Proteomics. 2014; 99: 40–53. DOI: 10.1016 / j.jprot.2014.01.016. [PubMed] [CrossRef] [Google Scholar] 66. Zhang FJ, Gao SG, Cheng L, Tian J, Xu WS, Luo W. и др. Влияние гиалуроновой кислоты на остеопонтин и мРНК CD44 фибробластоподобных синовиоцитов у пациентов с остеоартрозом коленного сустава.Rheumatol Int. 2013. 33 (1): 79–83. DOI: 10.1007 / s00296-011-2339-3. [PubMed] [CrossRef] [Google Scholar] 67. Zhou JL, Liu SQ, Qiu B, Hu QJ, Ming JH, Peng H. Защитный эффект гиалуроната натрия на хрящ от остеоартрита кроликов путем ингибирования экспрессии рецепторной гамма-матричной РНК, активируемой пролифератором пероксисом. Йонсей Мед Дж. 2009; 50 (6): 832–837. DOI: 10.3349 / ymj.2009.50.6.832. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 68. Чжоу PH, Лю С.К., Пэн Х. Эффект гиалуроновой кислоты на индуцированный IL-1beta апоптоз хондроцитов в модели остеоартрита на крысах.J Orthop Res. 2008. 26 (12): 1643–1648. DOI: 10.1002 / jor.20683. [PubMed] [CrossRef] [Google Scholar] 69. Уильямс Дж. Эффекты гиалуроновой кислоты на хондролиз хряща, опосредованный фибронектиновым фрагментом, у скелетно зрелых кроликов. Osteoarthr Cartil. 2003. 11 (1): 44–49. DOI: 10.1053 / joca.2002.0864. [PubMed] [CrossRef] [Google Scholar] 70. Сюй Х., Ито Т., Тавада А., Маеда Х., Яманокучи Х., Исахара К. и др. Влияние олигосахаридов гиалуронана на экспрессию белка теплового шока 72. J Biol Chem. 2002. 277 (19): 17308–17314.DOI: 10.1074 / jbc.M112371200. [PubMed] [CrossRef] [Google Scholar] 71. Чжоу J-L, Лю С.-Q, Цю Б., Ху Q-J, Мин J-H, Пэн Х. Влияние гиалуронана на фактор роста эндотелия сосудов и экспрессию рецептора-2 на модели остеоартрита кроликов. J Orthop Sci. 2009. 14 (3): 313–319. DOI: 10.1007 / s00776-009-1329-8. [PubMed] [CrossRef] [Google Scholar] 72. Хуанг Т.Л., Сюй ХК, Ян К.С., Яо СН, Линь Ф.Х. Влияние гиалуронанов разной молекулярной массы на продукцию белка, связанного с остеоартритом, в фибробластоподобных синовиоцитах пациентов с переломом плато большеберцовой кости.J Trauma. 2010. 68 (1): 146–152. DOI: 10.1097 / TA.0b013e3181a92cf8. [PubMed] [CrossRef] [Google Scholar] 73. Амиэль Д., Тойогучи Т., Кобаяши К., Боуден К., Амиэль М.Э., Хили Р.М. Долгосрочный эффект гиалуроната натрия (Hyalgan) на прогрессирование остеоартрита на модели кролика. Остеоартроз и хрящи / OARS, Osteoarthritis Res Soc. 2003. 11 (9): 636–643. DOI: 10.1016 / S1063-4584 (03) 00119-5. [PubMed] [CrossRef] [Google Scholar] 74. Ким NH, Хан CD, Ли ХМ, Ян И.Х. Влияние гиалуроната натрия на профилактику остеоартрита.Йонсей Мед Дж. 1991; 32 (2): 139–146. DOI: 10.3349 / ymj.1991.32.2.139. [PubMed] [CrossRef] [Google Scholar] 75. Лю Дж., Сун В., Юань Т., Сюй З., Цзя В., Чжан С. Сравнение плазмы, обогащенной тромбоцитами (PRP), и гиалуроновой кислоты при заживлении дефектов хряща. PLoS One. 2014; 9 (5) DOI: 10.1371 / journal.pone.0097293. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 76. Михара М., Хиго С., Учияма Ю., Танабе К., Сайто К. Различные эффекты высокомолекулярного гиалуроната натрия и НПВП на прогрессирование дегенерации хряща в модели ОА кролика.Osteoarthritis Cartilage / OARS, Osteoarthritis Res Soc. 2007. 15 (5): 543–549. DOI: 10.1016 / j.joca.2006.11.001. [PubMed] [CrossRef] [Google Scholar] 77. Цю Б., Лю С.К., Пэн Х., Ван HB. Влияние гиалуроната натрия на экспрессию мРНК матриксной металлопротеиназы-1, -3 и тканевого ингибитора металлопротеиназы-1 в хряще и синовиальной оболочке модели травматического остеоартрита. Chin J Traumatol. 2005; 8 (1): 8–12. [PubMed] [Google Scholar] 78. Озкан Ф.У., Озкан К., Рамадан С., Гувен З. Хондропротекторный эффект N-ацетилглюкозамина и гиалуроната на ранних стадиях остеоартрита — экспериментальное исследование на кроликах.Bull NYU Hosp Jt Dis. 2009. 67 (4): 352–357. [PubMed] [Google Scholar] 79. Ян Л, Чжан Дж, Ван Г. Эффект гиалуроната натрия при лечении остеоартрита коленного сустава на интерлейкин-1бета синовиальной жидкости и механизм клинического лечения. Pak J Pharm Sci. 2015; 28 (1 приложение): 407–410. [PubMed] [Google Scholar] 80. Йошиока К., Ясуда И., Кисукеда Т., Нодера Р., Танака Ю., Миямото К. Фармакологические эффекты нового поперечно-сшитого гиалуроната, геля-200, в экспериментальных моделях остеоартрита на животных и клеточных линиях человека.Хрящевой артроз. 2014. 22 (6): 879–887. DOI: 10.1016 / j.joca.2014.04.019. [PubMed] [CrossRef] [Google Scholar] 81. Хуэй А.Ю., Маккарти В.Дж., Масуда К., Файрштейн Г.С., Сах Р.Л. Системно-биологический подход к смазке синовиальных суставов при здоровье, травмах и болезнях. Wiley Interdiscip Rev Syst Biol Med. 2012. 4 (1): 15–37. DOI: 10.1002 / wsbm.157. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 83. Асари А., Мияути С., Мацудзака С., Ито Т., Коминами Е., Учияма Ю. Эффекты гиалуроната, зависимые от молекулярного веса, на синовиальную оболочку артрита.Arch Histol Cytol. 1998. 61 (2): 125–135. DOI: 10.1679 / aohc.61.125. [PubMed] [CrossRef] [Google Scholar] 84. Багга Х, Буркхардт Д., Сэмбрук П., Марч Л. Долгосрочные эффекты внутрисуставного гиалуронана на синовиальную жидкость при остеоартрите коленного сустава. J Rheumatol. 2006; 33 (5): 946–950. [PubMed] [Google Scholar] 85. Бауэр Ч., Баумгартнер Р., Хорноф М., Хальбвирт Ф., Никулеску-Морца Э., Цвикл Х. и др. Каркасы из поперечно-сшитой гиалуроновой кислоты: потенциальное использование для регенерации хряща? Osteoarthr Cartil. 2013; 21: S312.DOI: 10.1016 / j.joca.2013.02.646. [CrossRef] [Google Scholar] 86. Форси Р., Фишер Дж., Томпсон Дж., Стоун М., Белл С., Ингхэм Э. Влияние смазок на основе гиалуроновой кислоты и фосфолипидов на трение в модели повреждения хряща человека. Биоматериалы. 2006. 27 (26): 4581–4590. DOI: 10.1016 / j.biomaterials.2006.04.018. [PubMed] [CrossRef] [Google Scholar] 87. Frean S, Abraham L, Lees P. In vitro стимуляция синтеза протеогликанов суставного хряща лошади гиалуронаном и карпрофеном.Res Vet Sci. 1999. 67: 181–188. DOI: 10.1053 / rvsc.1999.0328. [PubMed] [CrossRef] [Google Scholar] 88. Хан Ф, Исигуро Н., Ито Т., Сакаи Т., Ивата Х. Влияние гиалуроната натрия на экспериментальный остеоартрит в коленных суставах кролика. Med Sci. 1999; 62. [PubMed] 89. Хомандберг Г.А., Уммади В., Канг Х. Роль инсулиноподобного фактора роста-I в опосредованном гиалуронаном восстановлении культивируемых эксплантатов хряща. Inflamm Res. 2004; 53: 8. [PubMed] [Google Scholar] 90. Hulmes D. Внутрисуставной гиалуронат при экспериментальном остеоартрите кроликов может предотвратить изменения в содержании протеогликанов хряща.Osteoarthr Cartil. 2004. 12 (3): 232–238. DOI: 10.1016 / j.joca.2003.11.007. [PubMed] [CrossRef] [Google Scholar] 91. Канг Й., Эгер В., Кепп Х., Уильямс Дж. М., Кюттнер К. Э., Хомандберг Г. А.. Гиалуронан подавляет опосредованное фрагментом фибронектина повреждение культур эксплантата хряща человека за счет усиления синтеза протеогликана. J Orthop Res. 1999. 17 (6): 858–869. DOI: 10.1002 / jor.1100170611. [PubMed] [CrossRef] [Google Scholar] 92. Кикучи Т., Ямада Х., Фудзикава К. Влияние высокомолекулярного гиалуронана на распределение и движение протеогликана вокруг хондроцитов, культивируемых в альгинатных шариках.Osteoarthr Cartil. 2001. 9 (4): 351–356. DOI: 10.1053 / joca.2000.0395. [PubMed] [CrossRef] [Google Scholar] 93. Kobayashi K, Matsuzaka S, Yoshida Y, Miyauchi S, Wada Y, Moriya H. Влияние внутрисуставного введения гиалуроната натрия на уровни интактного аггрекана и оксида азота в суставной жидкости пациентов с остеоартрозом коленного сустава. Osteoarthr Cartil. 2004. 12 (7): 536–542. DOI: 10.1016 / j.joca.2004.03.005. [PubMed] [CrossRef] [Google Scholar] 94. Nishida Y, Knudson CB, Knudson W. Восстановление внеклеточного матрикса суставными хондроцитами человека после лечения гиалуронановыми гексасахаридами или гиалуронидазой Streptomyces.Мод Ревматол. 2003. 13 (1): 62–68. DOI: 10.3109 / s101650300009. [PubMed] [CrossRef] [Google Scholar] 95. Смит Г. Н., младший, Миклер Е. А., Майерс С. Л., Брандт К. Д.. Влияние внутрисуставной инъекции гиалуронана на гиалуронан в синовиальную жидкость на ранней стадии посттравматического остеоартрита у собак. J Rheumatol. 2001. 28 (6): 1341–1346. [PubMed] [Google Scholar] 96. Stove J, Gerlach C, Huch K, Gunther KP, Puhl W, Scharf HP. Влияние гиалуронана на содержание протеогликанов в хондроцитах при остеоартрите in vitro. J Orthop Res.2002. 20 (3): 551–555. DOI: 10.1016 / S0736-0266 (01) 00141-3. [PubMed] [CrossRef] [Google Scholar] 97. Wang C, Lin Y, Chiang B, Hou S. Высокомолекулярная гиалуроновая кислота подавляет экспрессию генов цитокинов и ферментов, связанных с остеоартритом, в фибробластоподобных синовиоцитах пациентов с ранним остеоартритом. Osteoarthr Cartil. 2006. 14 (12): 1237–1247. DOI: 10.1016 / j.joca.2006.05.009. [PubMed] [CrossRef] [Google Scholar] 98. Abatangelo G, Botti P, Del Bue M, Gei G, Samson JC, Cortivo R и др.Внутрисуставные инъекции гиалуроната натрия в экспериментальной модели остеоартрита Понд-Нуки у собак. I. Биохимические результаты. Clin Orthop Relat Res. 1989. 241: 278–285. [PubMed] [Google Scholar] 99. Асари А., Мизуно С., Танака И., Суносе А., Курияма С., Миядзаки К. и др. Подавление продукции гиалуронана и простагландина E2 в синовиальных клетках травматического артрита гиалуронатом натрия. Соединительная ткань. 1997; 29: 1–5. [Google Scholar] 100. Лисиньоли Г., Грасси Ф., Пьячентини А., Коккини Б., Ремидди Г., Бевилаква С. и др.Гиалуронан не влияет на экспрессию цитокинов и хемокинов в хондроцитах и синовиоцитах, пораженных остеоартритом. Хрящевой артроз. 2001. 9 (2): 161–168. DOI: 10.1053 / joca.2000.0372. [PubMed] [CrossRef] [Google Scholar] 101. Оливьеро Ф., Сканю А., Рамонда Р., Фраллонардо П., Сфризо П., Дайер Дж. И др. Механизмы, участвующие в подавлении воспаления в клетках THP-1 гексадециламидным производным гиалуроновой кислоты. Osteoarthr Cartil. 2014; 22: S292 – S293. DOI: 10.1016 / j.joca.2014.02.544. [CrossRef] [Google Scholar] 102.Сезгин М., Демирел А.Г., Караджа С., Ортанджил О, Юлкар Г.Б., Каник А. и др. Влияет ли гиалуронан на воспалительные цитокины при остеоартрите коленного сустава? Rheumatol Int. 2004. 25 (4): 264–269. DOI: 10.1007 / s00296-003-0428-7. [PubMed] [CrossRef] [Google Scholar] 103. Шихан К.М., Делотт Л.Б., Дэй С.М., Дехир Д.Х. Hyalgan® оказывает дифференцированное дозозависимое действие на пролиферацию макрофагов и гибель клеток. J Orthop Res. 2003. 21 (4): 744–751. DOI: 10.1016 / S0736-0266 (03) 00007-X. [PubMed] [CrossRef] [Google Scholar] 104. Ясуда Т.Гиалуронан ингибирует Akt, что приводит к подавлению регуляции ядерного фактора-каппаB в макрофагах U937, стимулированных липополисахаридами. J Pharmacol Sci. 2011. 115 (4): 509–515. DOI: 10.1254 / jphs.10244FP. [PubMed] [CrossRef] [Google Scholar] 105. Campo GM, Avenoso A, D’Ascola A, Prestipino V, Scuruchi M, Nastasi G и др. Ингибирование синтеза гиалуронана снижает воспалительную реакцию в синовиальных фибробластах мышей, подвергшихся индуцированному коллагеном артриту. Arch Biochem Biophys. 2012; 518 (1): 42–52. DOI: 10.1016 / j.abb.2011.12.005. [PubMed] [CrossRef] [Google Scholar] 106. Campo GM, Avenoso A, Nastasi G, Micali A, Prestipino V, Vaccaro M и др. Гиалуронан уменьшает воспаление при экспериментальном артрите, модулируя экспрессию в хряще TLR-2 и TLR-4. Biochim Biophys Acta. 2011; 1812 (9): 1170–1181. DOI: 10.1016 / j.bbadis.2011.06.006. [PubMed] [CrossRef] [Google Scholar] 107. Schumacher HR, Paul C, Hitchon CA, El-Gabalawy H, Zonay L., Clayburne G, et al. Воздействие гиалуроната на синовиальную оболочку и синовиальную жидкость. Проспективное слепое исследование пациентов с остеоартрозом коленного сустава.Хрящевой артроз. 2006. 14 (5): 501–503. DOI: 10.1016 / j.joca.2005.11.013. [PubMed] [CrossRef] [Google Scholar] 108. Белл CJ, Ingham E, Fisher J. Влияние гиалуроновой кислоты на зависящую от времени фрикционную реакцию суставного хряща в различных условиях. Proc Inst Mech Eng H. 2006; 220 (1): 23–31. DOI: 10.1243 / 095441105X69060. [PubMed] [CrossRef] [Google Scholar] 109. Гош П., Рид Р., Нумата Ю., Смит С., Армстронг С., Уилсон Д. Эффекты внутрисуставного введения гиалуронана на модели раннего остеоартрита у овец.II. Состав хряща и метаболизм протеогликанов. Semin Arthritis Rheum. 1993; 22 (6 Suppl 1): 31–42. DOI: 10.1016 / S0049-0172 (10) 80017-4. [PubMed] [CrossRef] [Google Scholar] 110. Обара Т., Мабучи К., Исо Т., Ямагути Т. Повышенное трение суставов животных путем экспериментальной дегенерации и восстановления путем добавления гиалуроновой кислоты. Clin Biomech (Бристоль, Эйвон) 1997; 12 (4): 246–252. DOI: 10.1016 / S0268-0033 (97) 00004-1. [PubMed] [CrossRef] [Google Scholar] 111. Уоллер К.А., Чжан Л.X., Флеминг Б.К., Джей Г.Д. Предотвращение апоптоза хондроцитов, вызванного трением: сравнение синовиальной жидкости человека и Hylan G-F 20.J Rheumatol. 2012. 39 (7): 1473–1480. DOI: 10.3899 / jrheum.111427. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 112. Yu L-P, Yang H, Voschin E, Skrabut E. Вязкоупругие свойства и молекулярная масса гилана G-F 20 по сравнению с другими коммерческими добавками для вязкости на основе гиалуронана. Osteoarthr Cartil. 2011; 19 (S1): S235. DOI: 10.1016 / S1063-4584 (11) 60535-9. [CrossRef] [Google Scholar] 114. Тан С.Ф., Чен С.П., Чен М.Дж., Пей Ю.К., Лау Ю.К., Леонг С.П. Изменения сил сагиттальной реакции опоры после внутрисуставных инъекций гиалуроната при остеоартрозе коленного сустава.Arch Phys Med Rehabil. 2004. 85 (6): 951–955. DOI: 10.1016 / j.apmr.2003.08.095. [PubMed] [CrossRef] [Google Scholar] 115. Армстронг С., Рид Р., Гош П. Эффекты внутрисуставного гиалуронана на изменения хряща и субхондральной кости в модели раннего остеоартрита у овец. J Rheumatol. 1994. 21 (4): 680–688. [PubMed] [Google Scholar] 116. Hiraoka N, Takahashi Y, Arai K, Honjo S, Nakawaga S, Tsuchida S и др. Гиалуронан и периодическое гидростатическое давление синергетически подавляли экспрессию MMP-13 и Il-6 в остеобластах субхондральной кости при остеоартрите.Osteoarthr Cartil. 2009; 17 (1): S97. DOI: 10.1016 / S1063-4584 (09) 60186-2. [CrossRef] [Google Scholar] 117. Hiraoka N, Takahashi KA, Arai Y, Sakao K, Mazda O, Kishida T и др. Внутрисуставная инъекция гиалуронана восстанавливает аберрантную экспрессию матриксной металлопротеиназы-13 в субхондральной кости, пораженной остеоартритом. J Orthop Res. 2011. 29 (3): 354–360. DOI: 10.1002 / jor.21240. [PubMed] [CrossRef] [Google Scholar] 118. Prasadam I, Crawford R, Xiao Y. Обострение ADAMTS и продукции матриксной металлопротеиназы и роль пути ERK1 / 2 во взаимодействии остеоартрита субхондральных костных остеобластов и хондроцитов суставного хряща — возможная патогенная роль при остеоартрите.J Rheumatol. 2012. 39 (3): 621–634. DOI: 10.3899 / jrheum.110777. [PubMed] [CrossRef] [Google Scholar] 119. Boettger MK, Kummel D, Harrison A, Schaible HG. Оценка долгосрочных антиноцицептивных свойств препарата стабилизированной гиалуроновой кислоты (NASHA) на животной модели повторяющейся боли в суставах. Arthritis Res Ther. 2011; 13 (4): R110. DOI: 10.1186 / ar3394. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 120. Гомис А., Мираллес А., Шмидт Р.Ф., Бельмонте С. Внутрисуставные инъекции растворов гиалуронана разной эластовязкости снижают активность ноцицептивного нерва на модели остеоартрита коленного сустава морской свинки.Osteoarthr Cartil. 2009. 17 (6): 798–804. DOI: 10.1016 / j.joca.2008.11.013. [PubMed] [CrossRef] [Google Scholar] 121. Гото С., Оная Дж., Абэ М., Миядзаки К., Хамай А., Хори К. и др. Влияние молекулярной массы гиалуроновой кислоты и механизмов ее действия на экспериментальную боль в суставах у крыс. Ann Rheum Dis. 1993. 52 (11): 817–822. DOI: 10.1136 / ard.52.11.817. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 122. Pena Ede L, Sala S, Rovira JC, Schmidt RF, Belmonte C. Эластовязкие вещества с обезболивающим действием при боли в суставах снижают активность ионных каналов, активируемых растяжением, in vitro.Боль. 2002. 99 (3): 501–508. DOI: 10.1016 / S0304-3959 (02) 00260-9. [PubMed] [CrossRef] [Google Scholar] 123. Дугадос М. Терапия гиалуронатом натрия при остеоартрите: аргументы в пользу потенциального положительного структурного эффекта. Semin Arthritis Rheum. 2000; 30 (2 Suppl 1): 19–25. DOI: 10.1053 / sarh.2000.0246. [PubMed] [CrossRef] [Google Scholar] 124. Балаш Э.А., Денлингер Ж.Л. Вязкие добавки: новая концепция лечения остеоартрита. J Rheumatol Suppl. 1993; 39: 3–9. [PubMed] [Google Scholar] 125. Карбовник М.С., Новак Ю.З.Гиалуронан: к новым противораковым препаратам. Pharmacol Rep., 2013; 65 (5): 1056–1074. DOI: 10.1016 / S1734-1140 (13) 71465-8. [PubMed] [CrossRef] [Google Scholar] 126. Фахари А., Беркланд С. Применение и новые тенденции применения гиалуроновой кислоты в тканевой инженерии, в качестве кожного наполнителя и при лечении остеоартрита. Acta Biomater. 2013; 9 (7): 7081–7092. DOI: 10.1016 / j.actbio.2013.03.005. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
127. Harris E, Weigel PH. Функциональные аспекты рецепторов гиалуроновой кислоты и хондроитина сульфата.В: Raton B, ed: CRC Press; 2009: 171–192.
128. Гош П., Гуидолин Д. Возможный механизм действия внутрисуставной гиалуроновой терапии при остеоартрите: зависят ли эффекты от молекулярной массы? Semin Arthritis Rheum. 2002. 32 (1): 10–37. DOI: 10.1053 / sarh.2002.33720. [PubMed] [CrossRef] [Google Scholar] 130. Камениш Т.Д., Макдональд Дж. А. Гиалуронан: больше лучше? Am J Respir Cell Mol Biol. 2000. 23 (4): 431–433. DOI: 10.1165 / ajrcmb.23.4.f201. [PubMed] [CrossRef] [Google Scholar] 131. Мизрахи С., Раз С.Р., Хасгаард М., Лю Х., Соффер-Цур Н., Коэн К. и др.Наночастицы, покрытые гиалуроновой оболочкой: влияние молекулярной массы на взаимодействия CD44-гиалуронана и на иммунный ответ. J Control Release. 2011. 156 (2): 231–238. DOI: 10.1016 / j.jconrel.2011.06.031. [PubMed] [CrossRef] [Google Scholar] 132. Jevsevar DS, Jones DL, Matzkin EG, Manner PA, Mooar P, Schousboe JT, et al. Американская академия хирургов-ортопедов. Лечение остеоартроза коленного сустава: руководство, основанное на доказательствах, 2-е издание. JBJS. 2013. 95 (20): 1885–1886. [PubMed] [Google Scholar] 133.Ли ПБ, Ким Ю.С., Лим Й.Дж., Ли СиДжей, Сим У.С., Ха Ч.В. и др. Сравнение гиалуронатов с высокой и низкой молекулярной массой у пациентов с остеоартритом коленного сустава: открытое рандомизированное многоцентровое клиническое исследование. J Int Med Res. 2006. 34 (1): 77–87. DOI: 10.1177 / 147323000603400110. [PubMed] [CrossRef] [Google Scholar] 134. Киршнер М., Маршалл Д. Двойное слепое рандомизированное контролируемое исследование по сравнению альтернативных форм высокомолекулярного гиалуронана для лечения остеоартрита коленного сустава. Osteoarthr Cartil.2006. 14 (2): 154–162. DOI: 10.1016 / j.joca.2005.09.003. [PubMed] [CrossRef] [Google Scholar] 135. Чен А.Л., Десаи П., Адлер Э.М., Ди Чезаре ЧП. Гранулематозное воспаление после вискозиметрии колена Hylan G-F 20: отчет о шести случаях. J Bone Joint Surg Am. 2002; 84-А (7): 1142–1147. [PubMed] [Google Scholar] 136. Зардави И.М., Чан И. Синвисковидный перисиновит. Патология. 2001. 33 (4): 519–520. DOI: 10.1080 / 00313020120083296. [PubMed] [CrossRef] [Google Scholar]
Механизм действия гиалуроновой кислоты при остеоартрите коленного сустава: систематический обзор
BMC Musculoskelet Disord.2015; 16: 321.
, , , , и
RD Altman
Отдел ревматологии и иммунологии Медицинской школы Дэвида Геффена Калифорнийского университета в Лос-Анджелесе, 1000 ветеранов Ave,
Лос-Анджелес, Калифорния, США
A. Manjoo
Отделение ортопедии, Университет Макмастера, Гамильтон, Канада
A. Fierlinger
Ferring Pharmaceuticals Inc., Парсиппани, штат Нью-Джерси, США
F. Niazi
Ferring Pharmaceuticals Inc., Парсиппани, штат Нью-Джерси, США
М. Николлс
Кентукки Ортопедические хирурги и хирурги кистей рук, Подразделение Ortho Kentucky, Лексингтон,
США
Отделение ревматологии и иммунологии, Медицинская школа Дэвида Геффена, Калифорнийский университет в Лос-Анджелесе, 1000 Veterans Ave,
Лос-Анджелес, Калифорния, США
Отделение ортопедии, Университет Макмастера, Гамильтон, Канада
Ferring Pharmaceuticals Inc., Парсиппани, штат Нью-Джерси, США
Кентукки Ортопедические хирурги и хирурги кистей рук, отделение Ortho Kentucky, Лексингтон, штат Кентукки, США
Автор, отвечающий за переписку.
Поступило 12 августа 2015 г .; Принято 15 октября 2015 г.
Открытый доступ Эта статья распространяется в соответствии с условиями Международной лицензии Creative Commons Attribution 4.0 (http://creativecommons.org/licenses/by/4.0/), которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии вы должным образом указываете первоначального автора (авторов) и источник, предоставляете ссылку на лицензию Creative Commons и указываете, были ли внесены изменения.Отказ Creative Commons Public Domain Dedication (http://creativecommons.org/publicdomain/zero/1.0/) распространяется на данные, представленные в этой статье, если не указано иное. Эта статья цитируется в других статьях PMC.
Abstract
Предпосылки
Остеоартроз коленного сустава (ОА) является одной из основных причин инвалидности среди взрослого населения. Текущие варианты лечения ОА коленного сустава включают внутрисуставную (IA) гиалуроновую кислоту (HA), молекулу, которая находится внутри коленного сустава, которая обеспечивает вязкоупругие свойства синовиальной жидкости.В современной базовой литературе описаны различные механизмы, с помощью которых ГК борется с остеоартритом коленного сустава.
Методы
Мы провели всесторонний поиск литературы, чтобы определить доступные в настоящее время первичные доклинические фундаментальные научные статьи, посвященные механизму действия лечения IA-HA. Включенные статьи были оценены и распределены по категориям на основе описанного в них механизма действия. Основные результаты и выводы из каждой включенной статьи были получены и проанализированы в совокупности с исследованиями того же категориального задания.
Результаты
Хондрозащита была наиболее частым механизмом, о котором сообщалось во включенных статьях, за ней следуют синтез протеогликанов и гликозаминогликанов, противовоспалительное, механическое, субхондральное и обезболивающее действие. Связывание рецептора HA-кластера дифференцировки 44 (CD44) было наиболее часто упоминаемой биологической причиной представленных механизмов. Было обнаружено, что ГК с высоким молекулярным весом превосходит продукты ГК с более низким молекулярным весом. ГК, полученная в процессе биологической ферментации, также описывается как имеющая более благоприятные результаты безопасности по сравнению с продуктами ГК птичьего происхождения.
Выводы
Доклиническая фундаментальная научная литература предоставляет доказательства многочисленных механизмов, с помощью которых ГК действует на структуры и функции суставов. Эти действия подтверждают предполагаемую клиническую пользу IA-HA при остеоартрите коленного сустава. Дальнейшие исследования должны быть сосредоточены не только на обезболивании, обеспечиваемом лечением IA-HA, но и на свойствах модификации заболевания, которыми обладает этот метод лечения.
Ключевые слова: Остеоартрит, Гиалуроновая кислота, Терапия, Внутрисуставная терапия, Систематический обзор, Механизм действия
Предпосылки
Хотя остеоартрит (ОА) коленного сустава чаще всего является медленно прогрессирующим заболеванием суставов, он является одним из ведущие причины инвалидности взрослого населения [1].ОА коленного сустава, заболевание всего сустава, характеризуется болью в суставах, дегенерацией хряща и увеличением инвалидности [2]. Прогрессирующий характер ОА приводит к снижению функции коленного сустава, влияя на способность человека выполнять повседневную деятельность [3]. ОА коленного сустава также негативно влияет на социально-экономические факторы, поскольку связанная с этим инвалидность часто приводит к снижению производительности труда и раннему выходу на пенсию [4].
Поскольку не существует установленного агента, модифицирующего заболевание при ОА, существует множество вариантов лечения ОА коленного сустава.Среди фармакологических методов лечения чаще всего назначают нестероидные противовоспалительные препараты (НПВП) и внутрисуставные (IA) инъекции кортикостероидов [5]. Этим вариантам присущи ограничения, так как НПВП имеют потенциально серьезные побочные эффекты, связанные с их использованием [6], а инъекции кортикостероидов IA часто обеспечивают относительно короткий период эффективного облегчения [7]. Хотя инъекция кортикостероидов обычно имеет положительный профиль безопасности, было показано, что она вызывает временное повышение уровня глюкозы в крови, что может вызывать беспокойство у пациентов с диабетом [8].IA инъекция гиалуроновой кислоты (HA) — еще один вариант лечения боли при остеоартрите коленного сустава. ГК почти повсеместно присутствует в организме и представляет собой молекулу, которая находится внутри коленного сустава, где она придает вязкоупругие свойства синовиальной жидкости [9]. По мере прогрессирования ОА естественная концентрация ГК и распределение ГК в суставе смещается в сторону более низких диапазонов молекулярной массы ГК, что приводит к деградации механических / вязкоупругих свойств эндогенной синовиальной жидкости [2, 10, 11]. Также было показано, что более низкие диапазоны молекулярно-массового распределения сильно коррелируют с болью [11].Назначение IA-HA было направлено на восстановление этого снижения концентрации HA и среднего молекулярно-массового распределения внутри OA колена [9].
IA-HA, как предполагалось, обладает множеством терапевтических механизмов действия в коленном суставе с остеоартритом, включая поглощение ударов, смазку суставов, противовоспалительные эффекты, хондрозащиту, синтез протеогликанов и изменения хрящевого матрикса [2]. Корреляция между этими различными эффектами позволила лучше понять, как лечение IA-HA может оказывать терапевтический эффект для пациентов с остеоартритом коленного сустава [12].Имеются также данные, свидетельствующие о различиях в механизмах действия продуктов НА разной молекулярной массы. То есть ГК с более высокой молекулярной массой (HMW), как сообщается, обеспечивает более сильные противовоспалительные эффекты и эффекты синтеза протеогликанов, а также смазывание суставов и поддержание вязкоупругости [9, 13]. Также, по-видимому, существуют доказательства различных профилей безопасности между ГК, полученным в процессе биологической ферментации (Bio-HA), и ГК птичьего происхождения (AD-HA), поскольку AD-HA имеет потенциал для местных реакций IA [14, 15] .
Мы стремимся обобщить механизмы действия IA-HA лечения ОА коленного сустава, описанные в современной литературе, чтобы определить обоснованность вышеупомянутых механизмов действия. Мы будем систематически оценивать и обрисовывать определенные механизмы, с помощью которых ГК может оказывать терапевтическое действие, одновременно анализируя сообщаемые различия между эффектами лечения ИА-ГК, зависящими от характеристик продукта.
Методы
Поиск литературы
Мы провели всесторонний поиск литературы с использованием баз данных MEDLINE, EMBASE и PubMed (таблица).Поиск был проведен 4 мая -го , 2014. Критерии включения, соблюдаемые на протяжении всего процесса отбора, были следующими: 1) Статьи, описывающие механизм лечения ГК при ОА, 2) Статьи, посвященные ОА коленного сустава, и 3) Основные доклинические фундаментальные научные статьи, посвященные «добавлению вязкости» / лечению ГК. Статьи, которые были опубликованы до 1990 года или не были опубликованы на английском языке, были исключены из исследования. Если одним и тем же автором было опубликовано несколько исследований, содержащих похожие результаты, для включения принималось только самое последнее исследование.
Таблица 1
| MEDLINE и EMBASE — 1470 статей | PubMed — 1395 статей |
|---|---|
| 1. Гиалуроновая кислота [название] | 1. Гиалуроновая кислота [название] |
| 2. Hylan [title] | |
| 3. Гиалуронан [title] | 3. Гиалуронан [title] |
| 4. Добавки для вязкости [title] | 4. Добавки для вязкости [title] | 5.1 или 2 или 3 или 4 | 5. 1 или 2 или 3 или 4 |
| 6. Остеоартрит * .mp | 6. Остеоартрит * |
| 7. Артрит * .mp | 7. Артрит * |
| 8. Боль в суставах.mp | 8. Боль в суставах |
| 9. 6 или 7 или 8 | 9. 6 или 7 или 8 |
| 10. Эффект * .mp | 10. Эффект * |
| 11. Механизм * .mp | 11. Механизм * |
| 12.10 или 11 | 12. 10 или 11 |
| 13. 5 и 9 и 12 | 13. 5 и 9 и 12 |
Абстракция данных
Включенные статьи были оценены и классифицированы на основе механизма действие, описанное в них. Отдельные статьи включались в несколько категорий, если они анализировали более одного механизма действия НА в рамках своего дизайна исследования. Категории механизмов, использованные в процессе извлечения данных, включали: хондрозащиту, изменения синтеза протеогликана и / или гликозаминогликана (ГАГ), противовоспалительные эффекты, механические модификации, изменения в субхондральной кости и анальгетические эффекты.
Анализ данных
Ключевые выводы и заключения по каждой включенной статье были получены и проанализированы в совокупности с исследованиями той же присвоенной категории. Представленные результаты были получены путем интерпретации общего и последовательного механизма действия в рамках каждой вышеупомянутой категории.
Результаты
Стратегия поиска
Поиск литературы выявил 2782 потенциальных статьи, из которых 91 статья соответствовала критериям включения (рис.). Тринадцать дополнительных статей были извлечены специалистом по содержанию путем ручного поиска литературы. В результате было включено 104 статьи. Выводы и основные выводы каждой статьи были определены в рамках вышеупомянутых категорий механизмов (таблица).
Процесс проверки статей
Таблица 2
Ключевые механизмы действия, указанные во включенных статьях
| Механизм действия | Количество статей | % включенных статей | Ссылки | |
|---|---|---|---|---|
| Chondrotective | 67 | 64.42% | [9, 12, 16–80] | |
| Синтез протеогликанов / гликозаминогликанов | 22 | 21,15% | [27, 42, 44, 48, 62, 69, 83–98] | |
| Противовоспалительное | 21 | 20,19% | [13, 20, 21, 25, 27, 52, 54, 55, 68, 72, 96, 97, 99–107] | |
| Механический | 10 | 9,61% | [41, 49, 86, 108–114] | |
| Субхондральная кость | 8 | 7.69% | [23, 31, 32, 45, 115–118] | |
| Анальгетик | 6 | 5,76% | [76, 80, 119–122] |
Хондрозащита
Шестьдесят семь из включенных статей описывают хондрозащитные эффекты лечения IA-HA [9, 12, 16–80]. Было показано, что IA-HA снижает апоптоз хондроцитов, одновременно увеличивая пролиферацию хондроцитов [19, 20]. Существует множество наблюдаемых эффектов лечения IA-HA, которые вызывают хондрозащиту, многие из которых являются результатом связывания HA с рецепторами кластера дифференцировки 44 (CD44).Связывание HA с CD44 ингибирует экспрессию интерлейкина (IL) -1β, что приводит к снижению продукции матриксной металлопротеиназы (MMP) -1, 2, 3, 9 и 13 [32, 34]. Было показано, что это связывание с CD44 имеет больший эффект для продуктов HA с более высокой молекулярной массой [21]. HA также связывается с рецептором опосредованной гиалуронаном подвижности (RHAMM), который, как полагают, способствует хондропротекции в дополнение к связыванию с CD44 [34]. Ингибирование экспрессии IL-1β посредством связывания CD44 осуществляется посредством индукции митоген-активируемой протеинкиназы фосфатазы (MKP) -1: негативного регулятора IL-1β [43].Это ингибирование различных MMP препятствует активности катаболических ферментов в суставном хряще [59]. Было показано, что HMW HA имеет больший эффект в ингибирующем действии на продукцию MMP [21], хотя эти результаты неясны, поскольку другое исследование продемонстрировало благоприятный ингибирующий эффект MMP продуктов с более низкой молекулярной массой (LMW) [72].
События апоптоза хондроцитов дополнительно уменьшаются за счет связывания HA-CD44 за счет снижения экспрессии дезинтегрина и металлопротеиназы с тромбоспондиновыми мотивами (ADAMTS) [38].Эти пептидазы участвуют в расщеплении важных синовиальных компонентов, включая аггрекан, версикан и бревикан [81, 82]. Было показано, что различная экспрессия ADAMTS снижается в результате связывания HA-CD44, обеспечивая дополнительный режим хондропротекции для лечения IA-HA [36, 38, 43]. Производство активных форм кислорода (АФК), таких как оксид азота (NO), приводит к дегенерации хряща за счет увеличения апоптоза хондроцитов [33]. Лечение IA-HA продемонстрировало снижение индуцированного IL-1β окислительного стресса за счет ингибирования продукции NO в синовиальной оболочке [48, 57].Дополнительные результаты связывания CD44-HA, приводящие к хондропротекторным эффектам, упомянутые в современной литературе, включают снижение синтеза простагландина E2 (PGE2) [42, 46, 61] и повышенную сверхэкспрессию белка теплового шока 70 (Hsp70) [25, 70]. Эти эффекты аналогичным образом обеспечивают терапевтический эффект за счет уменьшения апоптоза хондроцитов. Важно отметить, что HMW продукты HA продемонстрировали большее подавление экспрессии PGE2, чем LMW компараторы в сравнительном исследовании, что привело к более сильному хондрозащитному эффекту [61].
Синтез протеогликанов и гликозаминогликанов
В 22 из идентифицированных исследований сообщалось об усилении синтеза протеогликанов и гликозаминогликанов, связанном с лечением IA-HA [27, 42, 44, 48, 62, 69, 83–98]. По мере прогрессирования ОА внутренние концентрации протеогликана и ГАГ в хряще снижаются. Результаты показали, что обработка IA-HA стимулировала синтез протеогликана, задерживая прогрессирование OA [69, 88]. Аггрекан является первичным протеогликаном в суставном хряще, и показано, что лечение IA-HA как подавляет деградацию аггрекана, так и способствует внутреннему развитию аггрекана [62, 93].Показано, что обработка IA-HA мобилизует вновь синтезированный протеогликан во внешний матрикс хондроцитов, потенциально обеспечивая защиту от деградации. Внешний HA способствует перемещению вновь синтезированного протеогликана из ассоциированного с клетками матрикса в далее удаленный матрикс в модели альгинатного геля, что предполагает, что IA-HA может обеспечивать терапевтическое облегчение OA за счет укрепления межтерриториального хрящевого матрикса [92]. Маркер синтеза протеогликана, сульфат ( 35 SO 4 ), как видно, все больше включается в хондроциты после введения HA [87].Биологический путь, в котором HA изменяет уровни аггрекана, проявляется через эффекты связывания CD44 и молекулы межклеточной адгезии (ICAM) -1 [62]. В одном исследовании было показано, что HMW HA обеспечивает больший эффект синтеза протеогликанов, чем LMW HA, за счет стимуляции пути инсулиноподобного фактора роста (IGF) -1 [89]. Также показано, что лечение IA-HA увеличивает выработку эндогенного ГАГ. Обработка IA-HA не только дополняла синовиальную оболочку HA, но и способствовала внутренней продукции HA [27].
Противовоспалительное
В 21 из идентифицированных исследований сообщалось о противовоспалительных эффектах лечения IA-HA [13, 20, 21, 25, 27, 52, 54, 55, 68, 72, 96, 97 , 99–107].Известно, что IL-1β демонстрирует провоспалительные эффекты, и вышеупомянутое подавление экспрессии IL-1β с помощью HA обеспечивает противовоспалительные эффекты [52]. IL-1β является ключевым медиатором противовоспалительного действия HA и регулируется посредством связывания HA-CD44 [59, 104]. Подавление IL-1β приводит к подавлению MMPs, как упоминалось ранее, что также способствует противовоспалительному эффекту HA [52]. Дальнейшее подавление провоспалительных медиаторов IL-8, IL-6, PGE 2 и фактора некроза опухоли (TNFα) обеспечивает противовоспалительные эффекты лечения IA-HA [13, 21].Связь между Toll-подобными рецепторами (TLR) и воспалительным ответом демонстрируется, поскольку продукты деградации HA индуцируют воспалительный ответ через взаимодействие CD44 и TLR. Этот провоспалительный ответ от связывания продукта деградации HA с рецепторами TLR и CD44 приводит к увеличению продукции Nf-kB, IL-1β, TNFα, IL-6 и IL-33 [105]. Было продемонстрировано, что HMW HA подавляет множество медиаторов воспаления посредством связывания TLR 2 и 4, включая TNF-α, IL-1-β, IL-17, MMP-13 и индуцибельную синтазу оксида азота (iNOS) [106].Прямая корреляция между молекулярной массой и противовоспалительным действием продемонстрировала более сильные эффекты ингибирования PGE 2 и IL-6 при лечении HMW HA [13]. IL-6 представляет собой провоспалительный цитокин, регулируемый ядерным фактором, энхансером легкой каппа-цепи активированных В-клеток (Nf-кB). Связывание HA с ICAM-1 подавляет Nf-kB, что, в свою очередь, снижает продукцию IL-6 [21, 104]. HMW HA, подавляющая регуляцию TNFα, IL-1B и IL-8, является дополнительным фактором, способствующим противовоспалительным эффектам, обеспечиваемым HMW HA [72, 97].
Механический
Десять из включенных исследований описывали механические эффекты ГК при лечении ОА коленного сустава [41, 49, 86, 108–114]. Показано, что вязкая природа лечения ГК смазывает суставную капсулу, предотвращая дегенерацию за счет снижения трения [86]. ГК дополнительно защищает капсулу сустава за счет благотворного эффекта поглощения ударов. HA обеспечивает амортизацию для поглощения давления и вибрации в суставе, которые в противном случае могут привести к деградации хондроцитов [41]. Сообщается, что колени с остеоартритом имеют более высокое трение в суставной щели, чем здоровые колени, чему противодействует способность суставной смазки, которой обладает HA [110].Было продемонстрировано, что HMW HA обеспечивает больший эффект снижения трения благодаря своим вязким свойствам. Уменьшение трения в суставе может обеспечить терапевтический эффект, поскольку хрящ защищен от механической деградации [111].
Субхондральная кость
Восемь из включенных исследований описали эффекты, которые IA-HA оказывает на субхондральную кость [23, 31, 32, 45, 115–118]. Ранее было показано, что взаимодействие между остеобластами субхондральной кости и хондроцитами суставного хряща в суставах с остеоартритом изменяет экспрессию ADAMTS-4/5 и MMP-1, MMP-2, MMP-3, MMP-8, MMP-9 и MMP-13. и регуляция, опосредованная митоген-активируемой протеинкиназой (MAPK) и сигнальными путями, регулируемыми внеклеточными сигналами киназ 1 и 2 (ERK 1/2) [118].IA-HA также влияет на субхондральную кость путем подавления MMP-13 и IL-6 через связывание CD44, что потенциально предотвращает аномальный метаболизм костной ткани [116]. Было высказано предположение, что подавление экспрессии MMP-13 с помощью IA-HA является критическим фактором воздействия на субхондральную кость при ОА [117]. Эффект, который IA-HA оказывает на MMPs, особенно MMP-13, посредством связывания CD44, как предполагалось, ингибирует эффекты OA в субхондральной кости в многочисленных доклинических фундаментальных научных исследованиях [32, 45, 116–118].ГК эффективно изменяет плотность и толщину субхондральной кости за счет изменений трабекулярной структуры, что приводит к большей податливости субхондральной кости. В конечном итоге показано, что это снижает нагрузку на хрящ во время ударной нагрузки [23]. Признаком стимуляции IA-HA обмена коллагена типа II на границе раздела хрящ и костей является повышение уровней сшивок коллагена на карбокси-конце (CTX) -II в моче, наблюдаемое после лечения IA-HA, которое продемонстрировало улучшение остеоартрита колена [31].В конечном итоге ГК, по-видимому, ограничивает изменения субхондральной кости, характерные для раннего ОА [115].
Анальгетик
Шесть из включенных статей описывают обезболивающие эффекты лечения IA-HA [76, 80, 119–122]. Одна инъекция ГК продемонстрировала значительное снижение связанного с болью поведения на мышиной модели [119]. Одно исследование показало, что HA не связывается напрямую с рецепторами брадикинина, но оказывает обезболивающее за счет взаимодействия с рецепторами HA и / или свободными нервными окончаниями в суставной ткани [121].Было показано, что обезболивающие эффекты HA проявляются в механочувствительных ионных каналах, активируемых растяжением, где активность канала значительно снижается при связывании HA [122]. Было показано, что HMW HA снижает механическую чувствительность ионных каналов, активируемых растяжением, которые эффективно блокируют болевой ответ. Было обнаружено, что LMW HA менее эффективен в блокировании этого ответа [122]. ГК снижает действие ноцицепторов суставов, что обеспечивает уменьшение боли в суставе. На сенсибилизированные ноцицептивные окончания в суставной ткани влияет концентрация HA, снижая болевую реакцию, проявляемую этими терминалами [120].
Обсуждение
Наш обзор существующей литературы дает общее мнение о том, что IA-HA при ОА коленного сустава имеет положительные эффекты через несколько механизмов действия; однако преобладающий механизм терапевтического эффекта не совсем ясен [2]. В перспективе неясно, какие из этих механизмов являются клинически значимыми, поскольку понятно, что полезные механизмы действия не обязательно переносятся на пользу в клинических условиях.В настоящее время предполагается, что клиническая польза IA-HA при ОА коленного сустава обусловлена несколькими параллельными механизмами действия, а не каким-либо одним конкретным механизмом действия.
Большая часть экзогенной ГК остается в суставе в течение нескольких дней; однако клинические терапевтические эффекты лечения ГК могут наблюдаться в течение 6 месяцев или более. Это может указывать на то, что IA-HA обладает свойствами, модифицирующими болезнь, и действует не только за счет восстановления вязкоупругих свойств синовиальной жидкости [123].Инъекции ГК могут стимулировать эндогенную продукцию дополнительной ГК синовиоцитами человека, способствуя нормализации распределения ГК в синовиальной жидкости [124]. В доклинических фундаментальных научных исследованиях во многих сообщениях описывается связывание CD44 как основной способ, при котором НА обеспечивает действие против ОА коленного сустава. Показано, что CD44-опосредованные эффекты IA-HA вносят вклад в потенциальную хондрозащиту, синтез протеогликанов / гликозаминогликанов, противовоспалительные и субхондральные механизмы. Показано, что это связывание оказывает разнообразные эффекты на многочисленные сигнальные пути, каждый из которых демонстрирует своего рода вмешательство в прогрессирование ОА [13, 21, 32, 36, 38, 42, 43, 46, 59, 61, 104 , 116].Было высказано предположение, что подавление IL-1β и IL-6 и последующие эффекты этого подавления являются ключевым фактором в терапевтическом механизме, обеспечиваемом связыванием HA-CD44 [123]. Очевидно, что связывание HA-CD44 является основным компонентом механизма, в котором HA обеспечивает терапевтический эффект; однако существуют дополнительные механизмы, которые обеспечивают альтернативные пути эффективности лечения ГК при ОА коленях, включая связывание ICAM, механические улучшения, связанные с поглощением удара и смазкой, увеличение обмена коллагена типа II на границе раздела хрящ / кость, а также анальгетические эффекты. через взаимодействие с нервными окончаниями и ноцицепторами суставов [31, 41, 86, 97, 121, 122].Связывание HA с рецептором RHAMM способствует заживлению ран, активирует функции промиграции и инвазии, регулирует клеточные ответы на факторы роста и играет роль в миграции и подвижности фибробластов [125–127]. Эти результаты связывания HA-RHAMM являются потенциальными факторами, участвующими в эффектах модификации заболевания при лечении HA при ОА.
Имеются данные, которые демонстрируют, что определенные внутренние свойства определенных продуктов IA-HA могут давать положительные результаты по сравнению с другими продуктами IA-HA.Наиболее известным из этих внутренних свойств является молекулярная масса. В отличие от предыдущего фундаментального научного обзора, проведенного Ghosh et al., Который предположил потенциальное преимущество LMW HA в обеспечении восстановления реологических свойств по сравнению с HMW HA [128], данные текущего обзора продемонстрировали благоприятные результаты для лечения HMW HA. Текущий обзор поддерживает точку зрения, что HMW HA обеспечивает превосходные хондропротекторные, протеогликановые и гликозаминогликановые механизмы синтеза, противовоспалительные, механические и обезболивающие механизмы действия [61, 89, 97, 111, 122].Исследование Huang et al. продемонстрировали превосходные противовоспалительные эффекты HMW HA, но лучшие хондрозащитные эффекты LMW HA; однако эти результаты относительно хондрозащиты неясны из-за отсутствия дополнительных доказательств в фундаментальной научной литературе по ОА коленного сустава [72]. Было показано, что повышенная продукция воспалительных цитокинов и хемокинов, привлечение медиаторов воспаления и образование кровеносных сосудов являются ответом на LMW HA ниже 500 кДа. Хотя средний молекулярный вес доступных продуктов ГК на рынке сильно различается, следует отметить, что, насколько нам известно, все доступные в настоящее время продукты во всем мире имеют молекулярную массу> 500 кДа [129, 130].Анализ взаимодействия HA-CD44 показал, что размер HA имеет прямое влияние на сродство, при котором HA связывается с рецептором CD44 [131]. Эти результаты демонстрируют способность HMW HA лечить прогрессирование ОА коленного сустава посредством связывания HA с CD44. Эти фундаментальные научные данные согласуются с систематическими обзорами клинических испытаний и сравнительных исследований, которые продемонстрировали, что HMW HA обеспечивает большую терапевтическую пользу, чем LMW HA при лечении ОА коленного сустава [6, 132], хотя текущая литература не обеспечивает консенсуса в отношении различие в клинической эффективности ГК с низким и высоким молекулярным весом [133].
Традиционно продукты ГК получали из птичьих источников; однако некоторые доступные продукты производятся путем биологической ферментации. Этот процесс позволяет избежать присутствия молекул птичьего происхождения, которые, как предполагается, могут быть потенциальной причиной неблагоприятных местных реакций [134]. Отсутствуют подробные отчеты о потенциале Bio-HA по сравнению с AD-HA. Одно исследование показало, что места инъекции AD-HA могут быть причиной синовита в их группе пациентов, но точный патологический агент неизвестен [135].Результаты второго исследования также указывают на способность гилана AD-HA вызывать гранулематозную реакцию типа гигантских клеток на инородное тело [136]. Исследования показали, что обострения, связанные с инъекцией гилана, могут быть связаны с накоплением гилана или продуктов его распада, поскольку обострения в месте инъекции обычно не возникают при первой инъекции [14]. Было показано, что белки птичьего происхождения являются причиной обострения в месте инъекции, поскольку антитела к белку куриной сыворотки присутствовали у пациентов, у которых наблюдалась неблагоприятная реакция в месте инъекции после лечения AD-HA [15].Имеются некоторые высококачественные клинические доказательства того, что Bio-HA имеет значительно меньшую частоту нежелательных явлений в месте инъекции, чем AD-HA [134]; однако в современной литературе это не исследовано досконально. Необходимо более всестороннее исследование разницы в частоте нежелательных явлений в месте инъекции между Bio-HA и AD-HA как с фундаментальной науки, так и с клинической точки зрения.
Этот обзор имеет методологическую силу благодаря систематическому и тщательному поиску доступных фундаментальных научных данных в нескольких базах данных.Текущий отчет также демонстрирует строгость в его представлении множественных механизмов, в которых действует HA, предоставляя доказательства обо всех механизмах, независимо от того, подробно или нечасто описаны в текущей литературе. Ограничения данного исследования возникают из-за субъективной классификации включенной статьи механизм действия основных выводов. Включенные статьи могут кратко упоминать альтернативные механизмы действия, но не были отнесены к соответствующей категории, потому что упомянутый альтернативный механизм не был ключевым результатом или заключением исследования.В будущих исследованиях следует проанализировать взаимосвязь между различными механизмами, представленными в этом отчете, и прояснить, как эти механизмы перекрываются и могут работать вместе для облегчения симптомов ОА коленного сустава. Дальнейшие исследования также должны быть направлены на выявление различий между механизмами, проявляемыми продуктами с высокой и низкой молекулярной массой, а также на анализ различий в профилях безопасности между Bio-HA и AD-HA.
Выводы
Доклиническая фундаментальная научная литература предоставляет доказательства многочисленных механизмов, с помощью которых IA-HA может обеспечить клиническую пользу при ОА коленного сустава.Хондропротекция является наиболее часто описываемым механизмом, причем связывание HA-CD44 является наиболее частым источником этих эффектов. Сообщается также, что IA-HA обеспечивает синтез протеогликанов и гликозаминогликанов, оказывает противовоспалительное, механическое, субхондральное и обезболивающее действие. Имеются данные о благоприятных результатах лечения HMW HA по сравнению с лечением LMW HA. Также показано, что Bio HA обеспечивает более выгодный профиль безопасности по сравнению с AD-HA, поскольку отчеты демонстрируют связь между обострениями в месте инъекции и белками птичьего происхождения.Существует множество описанных механизмов, в которых показано, что ИА-ГК лечит ОА коленного сустава, а также многочисленные характеристики продукта, которые влияют на результаты лечения ИА-ГК. Чтобы признать применимость и целесообразность лечения IA-HA для колено О.А. Дальнейшие исследования должны быть сосредоточены не только на обезболивании, обеспечиваемом лечением IA-HA, но и на свойствах модификации заболевания, которыми может обладать этот метод лечения.
Благодарности
Этот обзор финансируется Ferring Pharmaceuticals Inc. Авторы хотели бы поблагодарить Марка Филлипса и Global Research Solutions Inc. за их помощь в подготовке рукописи.
Аббревиатуры
| ADAMTS | Дезинтегрин и металлопротеиназа с тромбоспондиновыми мотивами | |||||||||||||||||||
| AD-HA | Гиалуроновая кислота птичьего происхождения | Биологическая кислота | Биологическая кислота | CD | Кластер дифференцировки | |||||||||||||||
| CTX | Сшивки карбоксиконцевого коллагена | |||||||||||||||||||
| ERK 1/2 | Киназа 1 и 2, регулируемая внеклеточным сигналом | |||||||||||||||||||
| GAG12122 90og3511 | Гиалуроновая кислота | |||||||||||||||||||
| HMW | Более высокая молекулярная масса | |||||||||||||||||||
| Hsp70 | Белок теплового шока 70 | |||||||||||||||||||
| IA | Внутрисуставной | |||||||||||||||||||
| IL | Интерлейкин | |||
| iNOS | Индуцируемый оксид азота LMW, низкомолекулярный вес | |||
| MAPK | MAPK | Митоген-активированная протеинкиназа | 90sp MMP | Металлопротеиназа |
| Nf-кB | Ядерный фактор, усилитель легкой цепи каппа активированных В-клеток | |||
| NO | Оксид азота | |||
| 12 НПВП | OA | Остеоартрит | ||
| PGE2 | Простагландин E2 | |||
| RHAMM | Рецептор для подвижности, опосредованной гиалуронаном |
Фут примечания
Конкурирующие интересы
Рой Д.Альтман: Консультант: Cytori, DuPuy (Bioventus Global), Ferring, Flexion, Iroko, McNeil, Novartis, Oletec, Pfizer, QMed, Rotta, Strategic Science and Technologies, Teva.
Спикер: Ферринг, Ироко.
Аджай Манджу: Нет конфликта интересов
Анке Фирлингер: оплачиваемый сотрудник Ferring Pharmaceuticals Inc.
Файзан Ниази: оплачиваемый сотрудник Ferring Pharmaceuticals Inc.
Мэтью Николлс: работает в консультативных советах Ferring.
Вклад авторов
AF и FN участвовали в разработке и разработке исследования. RDA обеспечило интерпретацию данных и внесение значительного письменного вклада в рукопись. Все авторы представили рукопись критическую рецензию и исправления. Все авторы прочитали и одобрили окончательную рукопись.
Ссылки
1. Cheng OT, Souzdalnitski D, Vrooman B, Cheng J. Доказательные инъекции в колено для лечения артрита. Pain Med.2012. 13 (6): 740–753. DOI: 10.1111 / j.1526-4637.2012.01394.x. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 2. Морленд Л.В. Внутрисуставной гиалуронан (гиалуроновая кислота) и гиланы для лечения остеоартрита: механизмы действия. Лечение артрита Res. 2003; 5 (2): 54. DOI: 10.1186 / ar623. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 3. Беллами Н., Кэмпбелл Дж., Робинсон В., Джи Т., Борн Р., Уэллс Г. Вискозиметрические добавки для лечения остеоартрита колена. Кокрановская база данных Syst Rev.2006; 2 [PubMed] [Google Scholar] 4. Тригкилидас Д., Ананд А. Эффективность внутрисуставных инъекций гиалуроновой кислоты при лечении боли в коленях при остеоартрите. Ann R Coll Surg Engl. 2013. 95 (8): 545–551. DOI: 10.1308 / rcsann.2013.95.8.545. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 5. Colen S, van den Bekerom MP, Mulier M, Haverkamp D. Гиалуроновая кислота в лечении остеоартрита коленного сустава: систематический обзор и метаанализ с упором на эффективность различных продуктов. BioDrugs.2012. 26 (4): 257–268. DOI: 10.1007 / BF03261884. [PubMed] [CrossRef] [Google Scholar] 6. Rutjes A, Juni P, da Costa B, Trelle S, Nuesch E, Reichenbach S. Viscosupplementation для остеоартрита коленного сустава: систематический обзор и метаанализ. Ann Intern Med. 2012; 157: 180–191. DOI: 10.7326 / 0003-4819-157-3-201208070-00473. [PubMed] [CrossRef] [Google Scholar] 7. Баннуру Р.Р., Натов Н.С., Обадан И.Е., Прайс Л.Л., Шмид С.Х., Макалиндон Т.Е. Терапевтическая траектория гиалуроновой кислоты по сравнению с кортикостероидами в лечении остеоартрита коленного сустава: систематический обзор и метаанализ.Ревматоидный артрит. 2009. 61 (12): 1704–1711. DOI: 10.1002 / art.24925. [PubMed] [CrossRef] [Google Scholar] 8. Хабиб Г.С. Системные эффекты внутрисуставных кортикостероидов. Clin Rheumatol. 2009. 28 (7): 749–756. DOI: 10.1007 / s10067-009-1135-х. [PubMed] [CrossRef] [Google Scholar] 9. Элморси С., Фунакоши Т., Сасазава Ф., Тодох М., Тадано С., Ивасаки Н. Хондропротекторные эффекты высокомолекулярной поперечно-сшитой гиалуроновой кислоты на модели остеоартрита коленного сустава кролика. Хрящевой артроз. 2014; 22 (1): 121–127.DOI: 10.1016 / j.joca.2013.10.005. [PubMed] [CrossRef] [Google Scholar] 10. Kosinska MK, Ludwig TE, Liebisch G, Zhang R, Siebert HC, Wilhelm J, et al. Смазки для суставов при остеоартрите и ревматоидном артрите имеют измененные уровни и молекулярные формы. PLoS One. 2015; 10 (5) DOI: 10.1371 / journal.pone.0125192. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 11. Band PA, Heeter J, Wisniewski HG, Liublinska V, Pattanayak CW, Karia RJ, et al. Распределение молекулярной массы гиалуроновой кислоты связано с риском прогрессирования остеоартрита коленного сустава.Хрящевой артроз. 2015; 23 (1): 70–76. DOI: 10.1016 / j.joca.2014.09.017. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 12. Диас-Гальего Л., Прието Дж. Г., Коронель П., Гамазо Л. Е., Гимено М., Альварес А. И.. Апоптоз и оксид азота в экспериментальной модели остеоартрита у кролика после лечения гиалуроновой кислотой. J Orthop Res. 2005. 23 (6): 1370–1376. DOI: 10.1016 / j.orthres.2005.05.003.1100230619. [PubMed] [CrossRef] [Google Scholar] 13. Lajeunesse D, Delalandre A, Martel-Pelletier J, Pelletier J-P.Гиалуроновая кислота устраняет аномальную синтетическую активность остеоартрита субхондральных костных остеобластов человека. Кость. 2003. 33 (4): 703–710. DOI: 10.1016 / S8756-3282 (03) 00206-0. [PubMed] [CrossRef] [Google Scholar] 14. Pullman-Mooar S, Mooar P, Sieck M, Clayburne G, Schumacher HR. Есть ли характерные воспалительные обострения после внутрисуставных инъекций hylan g-f 20? J Rheumatol, декабрь 2002 г., 29 (12): 2611–2614. [PubMed] [Google Scholar] 15. Гольдберг В.М., Куттс Р.Д. Псевдосептические реакции на добавку hylan viscos: диагностика и лечение.Clin Orthop Relat Res, февраль 2004 г .; 419: 130–137. DOI: 10.1097 / 00003086-200402000-00021. [PubMed] [CrossRef] [Google Scholar] 16. Ando A, Hagiwara Y, Chimoto E, Hatori K, Onoda Y, Itoi E. Внутрисуставная инъекция гиалуронана снижает потерю хондроцитов в модели с иммобилизованным коленом крысы. Tohoku J Exp Med. 2008. 215 (4): 321–331. DOI: 10.1620 / tjem.215.321. [PubMed] [CrossRef] [Google Scholar] 17. Ariyoshi W, Okinaga T, Knudson CB, Knudson W., Nishihara T. Высокомолекулярная гиалуроновая кислота регулирует образование остеокластов путем ингибирования активатора рецептора лиганда NF-kappaB через Rho-киназу.Хрящевой артроз. 2014. 22 (1): 111–120. DOI: 10.1016 / j.joca.2013.10.013. [PubMed] [CrossRef] [Google Scholar] 18. Asari A, Miyauchi S, Matsuzaka S, Itoh T, Uchiyama Y. Гиалуронат на белке теплового шока и синовиальных клетках в модели остеоартрита у собак. Хрящевой артроз. 1996. 4 (3): 213–215. DOI: 10.1016 / S1063-4584 (96) 80018-5. [PubMed] [CrossRef] [Google Scholar] 19. Брун П., Панфило С., Дага Гордини Д., Кортиво Р., Абатанджело Г. Влияние гиалуронана на CD44-опосредованное выживание нормальных и поврежденных гидроксильными радикалами хондроцитов.Хрящевой артроз. 2003. 11 (3): 208–216. DOI: 10.1016 / S1063-4584 (02) 00352-7. [PubMed] [CrossRef] [Google Scholar] 20. Брун П., Заван Б., Виндини В., Скьявинато А., Поццуоли А., Якобеллис С. и др. In vitro ответ остеоартрозных хондроцитов и фибробластоподобных синовиоцитов на производное гиалуронанамида 500-730 кДа. J Biomed Mater Res B Appl Biomater. 2012. 100 (8): 2073–2081. DOI: 10.1002 / jbm.b.32771. [PubMed] [CrossRef] [Google Scholar] 21. Chang CC, Hsieh MS, Liao ST, Chen YH, Cheng CW, Huang PT и др.Гиалуронан регулирует PPARgamma и воспалительные реакции в клетках хондросаркомы человека, стимулированных IL-1beta, которые являются моделью остеоартрита. Carbohydr Polym. 2012; 90 (2): 1168–1175. DOI: 10.1016 / j.carbpol.2012.06.071. [PubMed] [CrossRef] [Google Scholar] 22. Creamer P, Sharif M, George E, Meadows K, Cushnaghan J, Shinmei M и др. Внутрисуставная гиалуроновая кислота при остеоартрозе коленного сустава: исследование механизмов действия. Хрящевой артроз. 1994. 2 (2): 133–140. DOI: 10.1016 / S1063-4584 (05) 80063-9.[PubMed] [CrossRef] [Google Scholar] 23. Динг М., Кристиан Даниэльсен С., Хвид И. Влияние гиалуронана на трехмерную микроархитектуру субхондральных костных тканей при первичном остеоартрозе морских свинок. Кость. 2005. 36 (3): 489–501. DOI: 10.1016 / j.bone.2004.12.010. [PubMed] [CrossRef] [Google Scholar] 24. Элерс Э.М., Беренс П., Вунш Л., Кунель В., Русслис М. Влияние гиалуроновой кислоты на морфологию и пролиферацию хондроцитов человека в первичной культуре клеток. Анн Анат. 2001. 183 (1): 13–17. DOI: 10.1016 / S0940-9602 (01) 80007-8. [PubMed] [CrossRef] [Google Scholar] 25. Галуа Л., Этьен С., Хенрионне С., Скала-Бертола Дж., Гроссин Л., Майнард Д. и др. Амбивалентные свойства гиалуроната и гилана при посттравматическом ОА коленного сустава крысы. Biomed Mater Eng. 2012. 22 (4): 235–242. [PubMed] [Google Scholar] 26. Gonzalez-Fuentes AM, Green DM, Rossen RD, Ng B. Внутрисуставная гиалуроновая кислота увеличивает биомаркер разрушения хряща у пациентов с остеоартрозом коленного сустава. Clin Rheumatol. 2010. 29 (6): 619–624. DOI: 10.1007 / s10067-010-1376-8. [PubMed] [CrossRef] [Google Scholar] 27. Гринберг Д.Д., Стокер А., Кейн С., Кокрелл М., Кук Дж. Биохимические эффекты двух различных продуктов гиалуроновой кислоты в модели совместного культивирования остеоартрита. Хрящевой артроз. 2006. 14 (8): 814–822. DOI: 10.1016 / j.joca.2006.02.006. [PubMed] [CrossRef] [Google Scholar] 28. Гришко В., Сюй М., Хо Р., Мейтс А., Уотсон С., Ким Дж. Т. и др. Влияние гиалуроновой кислоты на функцию митохондрий и митохондриальный апоптоз после окислительного стресса в хондроцитах человека.J Biol Chem. 2009. 284 (14): 9132–9139. DOI: 10.1074 / jbc.M804178200. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 29. Хашизуме М., Михара М. Желаемый эффект комбинированной терапии с высоким молекулярным гиалуронатом и НПВП на продукцию ММП. Хрящевой артроз. 2009. 17 (11): 1513–1518. DOI: 10.1016 / j.joca.2009.04.018. [PubMed] [CrossRef] [Google Scholar] 30. Homandberg GA, Hui F, Wen C, Kuettner KE, Williams JM. Гиалуроновая кислота подавляет хондролиз хряща, опосредованный фрагментом фибронектина: I. In vitro . Хрящевой артроз. 1997. 5 (5): 309–319. DOI: 10.1016 / S1063-4584 (97) 80035-0. [PubMed] [CrossRef] [Google Scholar] 31. Исидзима М., Накамура Т., Симидзу К., Хаяси К., Кикучи Х., Соен С. и др. Различные изменения биомаркера CTX-II после внутрисуставной инъекции высокомолекулярной гиалуроновой кислоты и пероральных нестероидных противовоспалительных препаратов для пациентов с остеоартрозом коленного сустава: многоцентровое рандомизированное контролируемое исследование. Osteoarthr Cartil. 2013; 21: S292. DOI: 10.1016 / j.joca.2013.02.612. [CrossRef] [Google Scholar] 32. Джулови С.М., Ясуда Т., Шимицу М., Хирамицу Т., Накамура Т. Ингибирование индуцированного интерлейкином-1бета продукции матриксных металлопротеиназ гиалуронаном через CD44 в суставном хряще человека. Ревматоидный артрит. 2004. 50 (2): 516–525. DOI: 10.1002 / art.20004. [PubMed] [CrossRef] [Google Scholar] 33. Kalaci A, Yilmaz HR, Aslan B, Sogut S, Yanat AN, Uz E. Влияние гиалуронана на уровни оксида азота и активность супероксиддисмутазы в синовиальной жидкости при остеоартрите коленного сустава.Clin Rheumatol. 2007. 26 (8): 1306–1311. DOI: 10.1007 / s10067-006-0504-у. [PubMed] [CrossRef] [Google Scholar] 34. Карна Э., Милтык В, Суразинский А, Палка Я. Защитный эффект гиалуроновой кислоты на индуцированную интерлейкином-1 дерегуляцию передачи сигналов рецептора бета1-интегрина и инсулиноподобного фактора роста-I и биосинтез коллагена в культивируемых хондроцитах человека. Mol Cell Biochem. 2008. 308 (1-2): 57–64. DOI: 10.1007 / s11010-007-9612-5. [PubMed] [CrossRef] [Google Scholar] 35. Кобаяши К., Амиэль М., Харвуд Флорида, Хили Р.М., Сонода М., Мория Х. и др.Долгосрочные эффекты гиалуронана во время развития остеоартрита после частичной менискэктомии на модели кролика. Хрящевой артроз. 2000. 8 (5): 359–365. DOI: 10.1053 / joca.1999.0310. [PubMed] [CrossRef] [Google Scholar] 36. Кога Х. Действие гиалуроновой кислоты на суставной хрящ, пораженный артритом. Connect Tissue Res. 2012; 53 (1): 48–93. DOI: 10.3109 / 03008207.2011.637147. [CrossRef] [Google Scholar] 37. Лазаро Дж., Гранадо П., дель Соль Дж., Медина А., Гальего Л., Сандовал Д., Фернандес Дж. Роль различных гиалуроновых кислот в суставном хряще кролика.Открытая Ортопедия J. 2010; 4: 44–47. DOI: 10,2174 / 1874325001004010044. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 38. Ли Дж., Горски Д. Д., Анемает В., Веласко Дж., Такеучи Дж., Сэнди Дж. Д. и др. Инъекция гиалуронана при остеоартрите мышей предотвращает индуцированную TGFbeta 1 синовиальную неоваскуляризацию и фиброз и поддерживает целостность суставного хряща посредством CD44-зависимого механизма. Arthritis Res Ther. 2012; 14 (3): R151. DOI: 10.1186 / ar3887. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 39.Ли П., Райчева Д., Хавс М., Моран Н., Ю Икс, Ван Ф. и др. Hylan G-F 20 поддерживает целостность хряща и снижает образование остеофитов при остеоартрите за счет как анаболических, так и антикатаболических механизмов. Хрящевой артроз. 2012. 20 (11): 1336–1346. DOI: 10.1016 / j.joca.2012.07.004. [PubMed] [CrossRef] [Google Scholar] 40. Лисиньоли Г., Грасси Ф., Зини Н., Тонегуцци С., Пьячентини А., Гуидолин Д. и др. Анти-Fas-индуцированный апоптоз в хондроцитах, сниженный гиалуронаном: свидетельство инвазии CD44 и CD54 (молекула межклеточной адгезии 1).Ревматоидный артрит. 2001. 44 (8): 1800–1807. DOI: 10.1002 / 1529-0131 (200108) 44: 8 <1800 :: AID-ART317> 3.0.CO; 2-1. [PubMed] [CrossRef] [Google Scholar] 41. Lu HT, Sheu MT, Lin YF, Lan J, Chin YP, Hsieh MS и др. Инъекционная терапия гидрогелем доксициклина гиалуроновой кислоты при экспериментальном остеоартрите кроликов. BMC Vet Res. 2013; 9: 68. DOI: 10.1186 / 1746-6148-9-68. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 42. Манейро Э., де Андрес М.С., Фернандес-Суэйро Ю.Л., Гальдо Ф., Бланко Ф.Дж. Биологическое действие гиалуронана на суставные хондроциты остеоартрита человека: важность молекулярной массы.Clin Exp Rheumatol. 2004. 22 (3): 307–312. [PubMed] [Google Scholar] 43. Михара М., Хашизуме М. Влияние высокомолекулярной гиалуроновой кислоты на индукцию ферментов деградации матрикса IL-6, IL-1β и TNF-α Osteoarthr Cartil. 2012; 20: S134 – S135. DOI: 10.1016 / j.joca.2012.02.181. [CrossRef] [Google Scholar] 44. Мики Ю., Терамура Т., Томияма Т., Онодера Ю., Мацуока Т., Фукуда К. и др. Гиалуронан обратил синтез протеогликанов, подавленный механическим стрессом: возможное участие антиоксидантного эффекта.Inflamm Res. 2010. 59 (6): 471–477. DOI: 10.1007 / s00011-009-0147-у. [PubMed] [CrossRef] [Google Scholar] 45. Младенович З., Заурел А.С., Беренбаум Ф., Жак С. Потенциальная роль гиалуроновой кислоты в костях при остеоартрите: матриксные металлопротеиназы, агреканазы и экспрессия RANKL частично предотвращаются гиалуроновой кислотой в остеобластах, стимулированных интерлейкином-1. J Rheumatol. 2014. 41 (5): 945–954. DOI: 10.3899 / jrheum.130378. [PubMed] [CrossRef] [Google Scholar] 46. Mongkhon JM, Thach M, Shi Q, Fernandes JC, Fahmi H, Benderdour M.Гиалуроновая кислота, модифицированная сорбитом, снижает окислительный стресс, апоптоз и медиаторов воспаления и катаболизма в хондроцитах человека, страдающих остеоартритом. Inflamm Res. 2014; 63 (8): 691–701. DOI: 10.1007 / s00011-014-0742-4. [PubMed] [CrossRef] [Google Scholar] 47. Оно S, Im HJ, Knudson CB, Knudson W. Индуцированная гиалуронановым олигосахаридом активация факторов транскрипции в суставных хондроцитах крупного рогатого скота. Ревматоидный артрит. 2005. 52 (3): 800–809. DOI: 10.1002 / art.20937. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 48.Peng H, Zhou JL, Liu SQ, Hu QJ, Ming JH, Qiu B. Гиалуроновая кислота ингибирует апоптоз, вызванный оксидом азота, и дедифференцировку суставных хондроцитов in vitro . Inflamm Res. 2010. 59 (7): 519–530. DOI: 10.1007 / s00011-010-0156-х. [PubMed] [CrossRef] [Google Scholar] 49. Плаас А., Ли Дж., Риеско Дж., Дас Р., Сэнди Дж. Д., Харрисон А. Внутрисуставная инъекция гиалуронана предотвращает эрозию хряща, периартикулярный фиброз и механическую аллодинию и нормализует время пребывания в стойке при остеоартрите коленного сустава у мышей.Arthritis Res Ther. 2011; 13 (2): R46. DOI: 10.1186 / ar3286. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 50. Цю Б., Лю С. К., Пэн Х. Влияние гиалуроната натрия на экспрессию iNOS в синовиальной оболочке и содержание NO в синовиальной жидкости кроликов с травматическим остеоартритом. Chin J Traumatol. 2008. 11 (5): 293–296. DOI: 10.1016 / S1008-1275 (08) 60059-0. [PubMed] [CrossRef] [Google Scholar] 51. Сакакибара Ю., Миура Т., Ивата Х, Кикучи Т., Ямагути Т., Йошими Т. и др. Влияние высокомолекулярного гиалуроната натрия на иммобилизованное колено кролика.Clin Orthop Relat Res. 1994; 299: 282–292. [PubMed] [Google Scholar] 52. Сасаки А., Сасаки К., Конттинен Ю.Т., Сантавирта С., Такахара М., Такей Х. и др. Гиалуронат подавляет индуцированную интерлейкином-1бета экспрессию матриксной металлопротеиназы (MMP) -1 и MMP-3 в синовиальных клетках человека. Tohoku J Exp Med. 2004. 204 (2): 99–107. DOI: 10.1620 / tjem.204.99. [PubMed] [CrossRef] [Google Scholar] 53. Симидзу С., Йошиока М., Коуттс Р.Д., Харвуд Флорида, Кубо Т., Хирасава И. и др. Долгосрочные эффекты гиалуронана при экспериментальном остеоартрозе коленного сустава кролика.Хрящевой артроз. 1998. 6 (1): 1–9. DOI: 10.1053 / joca.1997.0086. [PubMed] [CrossRef] [Google Scholar] 54. Смит М.М., Торт М.А., Гош П., Скьявинато А., Рид Р.А., Литтл СВ. Значительная синовиальная патология в модели менискэктомии остеоартрита: модификация внутрисуставной гиалуроновой терапией. Ревматология (Оксфорд) 2008; 47 (8): 1172–1178. DOI: 10.1093 / ревматология / ken219. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 55. Смит М.М., Рассел А.К., Скьявинато А., Литтл CB. Гексадециламидное производное гиалуронана (HYMOVIS®) оказывает более благоприятное воздействие на хондроциты и синовиоциты человека, страдающие остеоартритом, чем немодифицированный гиалуронан.Журнал Инфламм (Лондон) 2013; 10:26. DOI: 10.1186 / 1476-9255-10-26. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 56. Такахаши К., Гумер Р.С., Харвуд Ф., Кубо Т., Хирасава Й., Амиэль Д. Эффекты гиалуронана на матриксную металлопротеиназу-3 (ММР-3), интерлейкин-1бета (ИЛ-1бета) и тканевой ингибитор металлопротеиназы-1 ( Экспрессия гена ТИМП-1) при развитии остеоартрита. Хрящевой артроз. 1999. 7 (2): 182–190. DOI: 10.1053 / joca.1998.0207. [PubMed] [CrossRef] [Google Scholar] 57.Такахаши К., Хашимото С., Кубо Т., Хирасава Ю., Лотц М., Амиэль Д. Гиалуронан подавлял выработку оксида азота в мениске и синовиальной оболочке модели остеоартрита кролика. J Orthop Res. 2001. 19 (3): 500–503. DOI: 10.1016 / S0736-0266 (00)
-X. [PubMed] [CrossRef] [Google Scholar] 58. Танака М., Масуко-Хонго К., Като Т., Нисиока К., Накамура Х. Подавляющее действие гиалуронана на продукцию MMP-1 и RANTES хондроцитами. Rheumatol Int. 2006. 26 (3): 185–190. DOI: 10.1007 / s00296-004-0547-9. [PubMed] [CrossRef] [Google Scholar] 59.Уодделл Д.Д., Коломыткин О.В., Данн С, Марино А.А. Гиалуронан подавляет активность металлопротеиназы, индуцированную IL-1beta, в синовиальной ткани. Clin Orthop Relat Res. 2007; 465: 241–248. [PubMed] [Google Scholar] 60. Ясуда Т. Активация ядерного фактора-kappaB пептидом коллагена II типа в суставных хондроцитах: его ингибирование гиалуронаном через рецепторы. Мод Ревматол. 2013. 23 (6): 1116–1123. DOI: 10.3109 / s10165-012-0804-9. [PubMed] [CrossRef] [Google Scholar] 61. Ясуи Т., Акацука М., Тобетто К., Хаяиси М., Андо Т.Влияние гиалуронана на индуцированную интерлейкином-1 альфа продукцию простагландина E2 в синовиальных клетках остеоартрита человека. Действия агентов. 1992. 37 (1-2): 155–156. DOI: 10.1007 / BF01987905. [PubMed] [CrossRef] [Google Scholar] 62. Ятабэ Т., Мочизуки С., Такидзава М., Чидзива М., Окада А., Кимура Т. и др. Гиалуронан подавляет экспрессию ADAMTS4 (аггреканазы-1) в хондроцитах человека, страдающих остеоартритом. Ann Rheum Dis. 2009. 68 (6): 1051–1058. DOI: 10.1136 / ard.2007.086884. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 63.Йошими Т., Кикучи Т., Обара Т., Ямагути Т., Сакакибара Ю., Ито Х. и др. Влияние высокомолекулярного гиалуроната натрия на экспериментальный остеоартроз, вызванный резекцией передней крестообразной связки кролика. Clin Orthop Relat Res. 1994; 298: 296–304. [PubMed] [Google Scholar] 64. Йошиока М., Симидзу С., Харвуд Флорида, Куттс Р.Д., Амиэль Д. Эффекты гиалуронана во время развития остеоартрита. Хрящевой артроз. 1997. 5 (4): 251–260. DOI: 10.1016 / S1063-4584 (97) 80021-0. [PubMed] [CrossRef] [Google Scholar] 65.Yu CJ, Ko CJ, Hsieh CH, Chien CT, Huang LH, Lee CW и др. Протеомный анализ хондроцитов, страдающих остеоартритом, выявляет регулируемые гиалуроновой кислотой белки, участвующие в хондропротекторном эффекте при окислительном стрессе. J Proteomics. 2014; 99: 40–53. DOI: 10.1016 / j.jprot.2014.01.016. [PubMed] [CrossRef] [Google Scholar] 66. Zhang FJ, Gao SG, Cheng L, Tian J, Xu WS, Luo W. и др. Влияние гиалуроновой кислоты на остеопонтин и мРНК CD44 фибробластоподобных синовиоцитов у пациентов с остеоартрозом коленного сустава.Rheumatol Int. 2013. 33 (1): 79–83. DOI: 10.1007 / s00296-011-2339-3. [PubMed] [CrossRef] [Google Scholar] 67. Zhou JL, Liu SQ, Qiu B, Hu QJ, Ming JH, Peng H. Защитный эффект гиалуроната натрия на хрящ от остеоартрита кроликов путем ингибирования экспрессии рецепторной гамма-матричной РНК, активируемой пролифератором пероксисом. Йонсей Мед Дж. 2009; 50 (6): 832–837. DOI: 10.3349 / ymj.2009.50.6.832. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 68. Чжоу PH, Лю С.К., Пэн Х. Эффект гиалуроновой кислоты на индуцированный IL-1beta апоптоз хондроцитов в модели остеоартрита на крысах.J Orthop Res. 2008. 26 (12): 1643–1648. DOI: 10.1002 / jor.20683. [PubMed] [CrossRef] [Google Scholar] 69. Уильямс Дж. Эффекты гиалуроновой кислоты на хондролиз хряща, опосредованный фибронектиновым фрагментом, у скелетно зрелых кроликов. Osteoarthr Cartil. 2003. 11 (1): 44–49. DOI: 10.1053 / joca.2002.0864. [PubMed] [CrossRef] [Google Scholar] 70. Сюй Х., Ито Т., Тавада А., Маеда Х., Яманокучи Х., Исахара К. и др. Влияние олигосахаридов гиалуронана на экспрессию белка теплового шока 72. J Biol Chem. 2002. 277 (19): 17308–17314.DOI: 10.1074 / jbc.M112371200. [PubMed] [CrossRef] [Google Scholar] 71. Чжоу J-L, Лю С.-Q, Цю Б., Ху Q-J, Мин J-H, Пэн Х. Влияние гиалуронана на фактор роста эндотелия сосудов и экспрессию рецептора-2 на модели остеоартрита кроликов. J Orthop Sci. 2009. 14 (3): 313–319. DOI: 10.1007 / s00776-009-1329-8. [PubMed] [CrossRef] [Google Scholar] 72. Хуанг Т.Л., Сюй ХК, Ян К.С., Яо СН, Линь Ф.Х. Влияние гиалуронанов разной молекулярной массы на продукцию белка, связанного с остеоартритом, в фибробластоподобных синовиоцитах пациентов с переломом плато большеберцовой кости.J Trauma. 2010. 68 (1): 146–152. DOI: 10.1097 / TA.0b013e3181a92cf8. [PubMed] [CrossRef] [Google Scholar] 73. Амиэль Д., Тойогучи Т., Кобаяши К., Боуден К., Амиэль М.Э., Хили Р.М. Долгосрочный эффект гиалуроната натрия (Hyalgan) на прогрессирование остеоартрита на модели кролика. Остеоартроз и хрящи / OARS, Osteoarthritis Res Soc. 2003. 11 (9): 636–643. DOI: 10.1016 / S1063-4584 (03) 00119-5. [PubMed] [CrossRef] [Google Scholar] 74. Ким NH, Хан CD, Ли ХМ, Ян И.Х. Влияние гиалуроната натрия на профилактику остеоартрита.Йонсей Мед Дж. 1991; 32 (2): 139–146. DOI: 10.3349 / ymj.1991.32.2.139. [PubMed] [CrossRef] [Google Scholar] 75. Лю Дж., Сун В., Юань Т., Сюй З., Цзя В., Чжан С. Сравнение плазмы, обогащенной тромбоцитами (PRP), и гиалуроновой кислоты при заживлении дефектов хряща. PLoS One. 2014; 9 (5) DOI: 10.1371 / journal.pone.0097293. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 76. Михара М., Хиго С., Учияма Ю., Танабе К., Сайто К. Различные эффекты высокомолекулярного гиалуроната натрия и НПВП на прогрессирование дегенерации хряща в модели ОА кролика.Osteoarthritis Cartilage / OARS, Osteoarthritis Res Soc. 2007. 15 (5): 543–549. DOI: 10.1016 / j.joca.2006.11.001. [PubMed] [CrossRef] [Google Scholar] 77. Цю Б., Лю С.К., Пэн Х., Ван HB. Влияние гиалуроната натрия на экспрессию мРНК матриксной металлопротеиназы-1, -3 и тканевого ингибитора металлопротеиназы-1 в хряще и синовиальной оболочке модели травматического остеоартрита. Chin J Traumatol. 2005; 8 (1): 8–12. [PubMed] [Google Scholar] 78. Озкан Ф.У., Озкан К., Рамадан С., Гувен З. Хондропротекторный эффект N-ацетилглюкозамина и гиалуроната на ранних стадиях остеоартрита — экспериментальное исследование на кроликах.Bull NYU Hosp Jt Dis. 2009. 67 (4): 352–357. [PubMed] [Google Scholar] 79. Ян Л, Чжан Дж, Ван Г. Эффект гиалуроната натрия при лечении остеоартрита коленного сустава на интерлейкин-1бета синовиальной жидкости и механизм клинического лечения. Pak J Pharm Sci. 2015; 28 (1 приложение): 407–410. [PubMed] [Google Scholar] 80. Йошиока К., Ясуда И., Кисукеда Т., Нодера Р., Танака Ю., Миямото К. Фармакологические эффекты нового поперечно-сшитого гиалуроната, геля-200, в экспериментальных моделях остеоартрита на животных и клеточных линиях человека.Хрящевой артроз. 2014. 22 (6): 879–887. DOI: 10.1016 / j.joca.2014.04.019. [PubMed] [CrossRef] [Google Scholar] 81. Хуэй А.Ю., Маккарти В.Дж., Масуда К., Файрштейн Г.С., Сах Р.Л. Системно-биологический подход к смазке синовиальных суставов при здоровье, травмах и болезнях. Wiley Interdiscip Rev Syst Biol Med. 2012. 4 (1): 15–37. DOI: 10.1002 / wsbm.157. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 83. Асари А., Мияути С., Мацудзака С., Ито Т., Коминами Е., Учияма Ю. Эффекты гиалуроната, зависимые от молекулярного веса, на синовиальную оболочку артрита.Arch Histol Cytol. 1998. 61 (2): 125–135. DOI: 10.1679 / aohc.61.125. [PubMed] [CrossRef] [Google Scholar] 84. Багга Х, Буркхардт Д., Сэмбрук П., Марч Л. Долгосрочные эффекты внутрисуставного гиалуронана на синовиальную жидкость при остеоартрите коленного сустава. J Rheumatol. 2006; 33 (5): 946–950. [PubMed] [Google Scholar] 85. Бауэр Ч., Баумгартнер Р., Хорноф М., Хальбвирт Ф., Никулеску-Морца Э., Цвикл Х. и др. Каркасы из поперечно-сшитой гиалуроновой кислоты: потенциальное использование для регенерации хряща? Osteoarthr Cartil. 2013; 21: S312.DOI: 10.1016 / j.joca.2013.02.646. [CrossRef] [Google Scholar] 86. Форси Р., Фишер Дж., Томпсон Дж., Стоун М., Белл С., Ингхэм Э. Влияние смазок на основе гиалуроновой кислоты и фосфолипидов на трение в модели повреждения хряща человека. Биоматериалы. 2006. 27 (26): 4581–4590. DOI: 10.1016 / j.biomaterials.2006.04.018. [PubMed] [CrossRef] [Google Scholar] 87. Frean S, Abraham L, Lees P. In vitro стимуляция синтеза протеогликанов суставного хряща лошади гиалуронаном и карпрофеном.Res Vet Sci. 1999. 67: 181–188. DOI: 10.1053 / rvsc.1999.0328. [PubMed] [CrossRef] [Google Scholar] 88. Хан Ф, Исигуро Н., Ито Т., Сакаи Т., Ивата Х. Влияние гиалуроната натрия на экспериментальный остеоартрит в коленных суставах кролика. Med Sci. 1999; 62. [PubMed] 89. Хомандберг Г.А., Уммади В., Канг Х. Роль инсулиноподобного фактора роста-I в опосредованном гиалуронаном восстановлении культивируемых эксплантатов хряща. Inflamm Res. 2004; 53: 8. [PubMed] [Google Scholar] 90. Hulmes D. Внутрисуставной гиалуронат при экспериментальном остеоартрите кроликов может предотвратить изменения в содержании протеогликанов хряща.Osteoarthr Cartil. 2004. 12 (3): 232–238. DOI: 10.1016 / j.joca.2003.11.007. [PubMed] [CrossRef] [Google Scholar] 91. Канг Й., Эгер В., Кепп Х., Уильямс Дж. М., Кюттнер К. Э., Хомандберг Г. А.. Гиалуронан подавляет опосредованное фрагментом фибронектина повреждение культур эксплантата хряща человека за счет усиления синтеза протеогликана. J Orthop Res. 1999. 17 (6): 858–869. DOI: 10.1002 / jor.1100170611. [PubMed] [CrossRef] [Google Scholar] 92. Кикучи Т., Ямада Х., Фудзикава К. Влияние высокомолекулярного гиалуронана на распределение и движение протеогликана вокруг хондроцитов, культивируемых в альгинатных шариках.Osteoarthr Cartil. 2001. 9 (4): 351–356. DOI: 10.1053 / joca.2000.0395. [PubMed] [CrossRef] [Google Scholar] 93. Kobayashi K, Matsuzaka S, Yoshida Y, Miyauchi S, Wada Y, Moriya H. Влияние внутрисуставного введения гиалуроната натрия на уровни интактного аггрекана и оксида азота в суставной жидкости пациентов с остеоартрозом коленного сустава. Osteoarthr Cartil. 2004. 12 (7): 536–542. DOI: 10.1016 / j.joca.2004.03.005. [PubMed] [CrossRef] [Google Scholar] 94. Nishida Y, Knudson CB, Knudson W. Восстановление внеклеточного матрикса суставными хондроцитами человека после лечения гиалуронановыми гексасахаридами или гиалуронидазой Streptomyces.Мод Ревматол. 2003. 13 (1): 62–68. DOI: 10.3109 / s101650300009. [PubMed] [CrossRef] [Google Scholar] 95. Смит Г. Н., младший, Миклер Е. А., Майерс С. Л., Брандт К. Д.. Влияние внутрисуставной инъекции гиалуронана на гиалуронан в синовиальную жидкость на ранней стадии посттравматического остеоартрита у собак. J Rheumatol. 2001. 28 (6): 1341–1346. [PubMed] [Google Scholar] 96. Stove J, Gerlach C, Huch K, Gunther KP, Puhl W, Scharf HP. Влияние гиалуронана на содержание протеогликанов в хондроцитах при остеоартрите in vitro. J Orthop Res.2002. 20 (3): 551–555. DOI: 10.1016 / S0736-0266 (01) 00141-3. [PubMed] [CrossRef] [Google Scholar] 97. Wang C, Lin Y, Chiang B, Hou S. Высокомолекулярная гиалуроновая кислота подавляет экспрессию генов цитокинов и ферментов, связанных с остеоартритом, в фибробластоподобных синовиоцитах пациентов с ранним остеоартритом. Osteoarthr Cartil. 2006. 14 (12): 1237–1247. DOI: 10.1016 / j.joca.2006.05.009. [PubMed] [CrossRef] [Google Scholar] 98. Abatangelo G, Botti P, Del Bue M, Gei G, Samson JC, Cortivo R и др.Внутрисуставные инъекции гиалуроната натрия в экспериментальной модели остеоартрита Понд-Нуки у собак. I. Биохимические результаты. Clin Orthop Relat Res. 1989. 241: 278–285. [PubMed] [Google Scholar] 99. Асари А., Мизуно С., Танака И., Суносе А., Курияма С., Миядзаки К. и др. Подавление продукции гиалуронана и простагландина E2 в синовиальных клетках травматического артрита гиалуронатом натрия. Соединительная ткань. 1997; 29: 1–5. [Google Scholar] 100. Лисиньоли Г., Грасси Ф., Пьячентини А., Коккини Б., Ремидди Г., Бевилаква С. и др.Гиалуронан не влияет на экспрессию цитокинов и хемокинов в хондроцитах и синовиоцитах, пораженных остеоартритом. Хрящевой артроз. 2001. 9 (2): 161–168. DOI: 10.1053 / joca.2000.0372. [PubMed] [CrossRef] [Google Scholar] 101. Оливьеро Ф., Сканю А., Рамонда Р., Фраллонардо П., Сфризо П., Дайер Дж. И др. Механизмы, участвующие в подавлении воспаления в клетках THP-1 гексадециламидным производным гиалуроновой кислоты. Osteoarthr Cartil. 2014; 22: S292 – S293. DOI: 10.1016 / j.joca.2014.02.544. [CrossRef] [Google Scholar] 102.Сезгин М., Демирел А.Г., Караджа С., Ортанджил О, Юлкар Г.Б., Каник А. и др. Влияет ли гиалуронан на воспалительные цитокины при остеоартрите коленного сустава? Rheumatol Int. 2004. 25 (4): 264–269. DOI: 10.1007 / s00296-003-0428-7. [PubMed] [CrossRef] [Google Scholar] 103. Шихан К.М., Делотт Л.Б., Дэй С.М., Дехир Д.Х. Hyalgan® оказывает дифференцированное дозозависимое действие на пролиферацию макрофагов и гибель клеток. J Orthop Res. 2003. 21 (4): 744–751. DOI: 10.1016 / S0736-0266 (03) 00007-X. [PubMed] [CrossRef] [Google Scholar] 104. Ясуда Т.Гиалуронан ингибирует Akt, что приводит к подавлению регуляции ядерного фактора-каппаB в макрофагах U937, стимулированных липополисахаридами. J Pharmacol Sci. 2011. 115 (4): 509–515. DOI: 10.1254 / jphs.10244FP. [PubMed] [CrossRef] [Google Scholar] 105. Campo GM, Avenoso A, D’Ascola A, Prestipino V, Scuruchi M, Nastasi G и др. Ингибирование синтеза гиалуронана снижает воспалительную реакцию в синовиальных фибробластах мышей, подвергшихся индуцированному коллагеном артриту. Arch Biochem Biophys. 2012; 518 (1): 42–52. DOI: 10.1016 / j.abb.2011.12.005. [PubMed] [CrossRef] [Google Scholar] 106. Campo GM, Avenoso A, Nastasi G, Micali A, Prestipino V, Vaccaro M и др. Гиалуронан уменьшает воспаление при экспериментальном артрите, модулируя экспрессию в хряще TLR-2 и TLR-4. Biochim Biophys Acta. 2011; 1812 (9): 1170–1181. DOI: 10.1016 / j.bbadis.2011.06.006. [PubMed] [CrossRef] [Google Scholar] 107. Schumacher HR, Paul C, Hitchon CA, El-Gabalawy H, Zonay L., Clayburne G, et al. Воздействие гиалуроната на синовиальную оболочку и синовиальную жидкость. Проспективное слепое исследование пациентов с остеоартрозом коленного сустава.Хрящевой артроз. 2006. 14 (5): 501–503. DOI: 10.1016 / j.joca.2005.11.013. [PubMed] [CrossRef] [Google Scholar] 108. Белл CJ, Ingham E, Fisher J. Влияние гиалуроновой кислоты на зависящую от времени фрикционную реакцию суставного хряща в различных условиях. Proc Inst Mech Eng H. 2006; 220 (1): 23–31. DOI: 10.1243 / 095441105X69060. [PubMed] [CrossRef] [Google Scholar] 109. Гош П., Рид Р., Нумата Ю., Смит С., Армстронг С., Уилсон Д. Эффекты внутрисуставного введения гиалуронана на модели раннего остеоартрита у овец.II. Состав хряща и метаболизм протеогликанов. Semin Arthritis Rheum. 1993; 22 (6 Suppl 1): 31–42. DOI: 10.1016 / S0049-0172 (10) 80017-4. [PubMed] [CrossRef] [Google Scholar] 110. Обара Т., Мабучи К., Исо Т., Ямагути Т. Повышенное трение суставов животных путем экспериментальной дегенерации и восстановления путем добавления гиалуроновой кислоты. Clin Biomech (Бристоль, Эйвон) 1997; 12 (4): 246–252. DOI: 10.1016 / S0268-0033 (97) 00004-1. [PubMed] [CrossRef] [Google Scholar] 111. Уоллер К.А., Чжан Л.X., Флеминг Б.К., Джей Г.Д. Предотвращение апоптоза хондроцитов, вызванного трением: сравнение синовиальной жидкости человека и Hylan G-F 20.J Rheumatol. 2012. 39 (7): 1473–1480. DOI: 10.3899 / jrheum.111427. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 112. Yu L-P, Yang H, Voschin E, Skrabut E. Вязкоупругие свойства и молекулярная масса гилана G-F 20 по сравнению с другими коммерческими добавками для вязкости на основе гиалуронана. Osteoarthr Cartil. 2011; 19 (S1): S235. DOI: 10.1016 / S1063-4584 (11) 60535-9. [CrossRef] [Google Scholar] 114. Тан С.Ф., Чен С.П., Чен М.Дж., Пей Ю.К., Лау Ю.К., Леонг С.П. Изменения сил сагиттальной реакции опоры после внутрисуставных инъекций гиалуроната при остеоартрозе коленного сустава.Arch Phys Med Rehabil. 2004. 85 (6): 951–955. DOI: 10.1016 / j.apmr.2003.08.095. [PubMed] [CrossRef] [Google Scholar] 115. Армстронг С., Рид Р., Гош П. Эффекты внутрисуставного гиалуронана на изменения хряща и субхондральной кости в модели раннего остеоартрита у овец. J Rheumatol. 1994. 21 (4): 680–688. [PubMed] [Google Scholar] 116. Hiraoka N, Takahashi Y, Arai K, Honjo S, Nakawaga S, Tsuchida S и др. Гиалуронан и периодическое гидростатическое давление синергетически подавляли экспрессию MMP-13 и Il-6 в остеобластах субхондральной кости при остеоартрите.Osteoarthr Cartil. 2009; 17 (1): S97. DOI: 10.1016 / S1063-4584 (09) 60186-2. [CrossRef] [Google Scholar] 117. Hiraoka N, Takahashi KA, Arai Y, Sakao K, Mazda O, Kishida T и др. Внутрисуставная инъекция гиалуронана восстанавливает аберрантную экспрессию матриксной металлопротеиназы-13 в субхондральной кости, пораженной остеоартритом. J Orthop Res. 2011. 29 (3): 354–360. DOI: 10.1002 / jor.21240. [PubMed] [CrossRef] [Google Scholar] 118. Prasadam I, Crawford R, Xiao Y. Обострение ADAMTS и продукции матриксной металлопротеиназы и роль пути ERK1 / 2 во взаимодействии остеоартрита субхондральных костных остеобластов и хондроцитов суставного хряща — возможная патогенная роль при остеоартрите.J Rheumatol. 2012. 39 (3): 621–634. DOI: 10.3899 / jrheum.110777. [PubMed] [CrossRef] [Google Scholar] 119. Boettger MK, Kummel D, Harrison A, Schaible HG. Оценка долгосрочных антиноцицептивных свойств препарата стабилизированной гиалуроновой кислоты (NASHA) на животной модели повторяющейся боли в суставах. Arthritis Res Ther. 2011; 13 (4): R110. DOI: 10.1186 / ar3394. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 120. Гомис А., Мираллес А., Шмидт Р.Ф., Бельмонте С. Внутрисуставные инъекции растворов гиалуронана разной эластовязкости снижают активность ноцицептивного нерва на модели остеоартрита коленного сустава морской свинки.Osteoarthr Cartil. 2009. 17 (6): 798–804. DOI: 10.1016 / j.joca.2008.11.013. [PubMed] [CrossRef] [Google Scholar] 121. Гото С., Оная Дж., Абэ М., Миядзаки К., Хамай А., Хори К. и др. Влияние молекулярной массы гиалуроновой кислоты и механизмов ее действия на экспериментальную боль в суставах у крыс. Ann Rheum Dis. 1993. 52 (11): 817–822. DOI: 10.1136 / ard.52.11.817. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 122. Pena Ede L, Sala S, Rovira JC, Schmidt RF, Belmonte C. Эластовязкие вещества с обезболивающим действием при боли в суставах снижают активность ионных каналов, активируемых растяжением, in vitro.Боль. 2002. 99 (3): 501–508. DOI: 10.1016 / S0304-3959 (02) 00260-9. [PubMed] [CrossRef] [Google Scholar] 123. Дугадос М. Терапия гиалуронатом натрия при остеоартрите: аргументы в пользу потенциального положительного структурного эффекта. Semin Arthritis Rheum. 2000; 30 (2 Suppl 1): 19–25. DOI: 10.1053 / sarh.2000.0246. [PubMed] [CrossRef] [Google Scholar] 124. Балаш Э.А., Денлингер Ж.Л. Вязкие добавки: новая концепция лечения остеоартрита. J Rheumatol Suppl. 1993; 39: 3–9. [PubMed] [Google Scholar] 125. Карбовник М.С., Новак Ю.З.Гиалуронан: к новым противораковым препаратам. Pharmacol Rep., 2013; 65 (5): 1056–1074. DOI: 10.1016 / S1734-1140 (13) 71465-8. [PubMed] [CrossRef] [Google Scholar] 126. Фахари А., Беркланд С. Применение и новые тенденции применения гиалуроновой кислоты в тканевой инженерии, в качестве кожного наполнителя и при лечении остеоартрита. Acta Biomater. 2013; 9 (7): 7081–7092. DOI: 10.1016 / j.actbio.2013.03.005. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar]
127. Harris E, Weigel PH. Функциональные аспекты рецепторов гиалуроновой кислоты и хондроитина сульфата.В: Raton B, ed: CRC Press; 2009: 171–192.
128. Гош П., Гуидолин Д. Возможный механизм действия внутрисуставной гиалуроновой терапии при остеоартрите: зависят ли эффекты от молекулярной массы? Semin Arthritis Rheum. 2002. 32 (1): 10–37. DOI: 10.1053 / sarh.2002.33720. [PubMed] [CrossRef] [Google Scholar] 130. Камениш Т.Д., Макдональд Дж. А. Гиалуронан: больше лучше? Am J Respir Cell Mol Biol. 2000. 23 (4): 431–433. DOI: 10.1165 / ajrcmb.23.4.f201. [PubMed] [CrossRef] [Google Scholar] 131. Мизрахи С., Раз С.Р., Хасгаард М., Лю Х., Соффер-Цур Н., Коэн К. и др.Наночастицы, покрытые гиалуроновой оболочкой: влияние молекулярной массы на взаимодействия CD44-гиалуронана и на иммунный ответ. J Control Release. 2011. 156 (2): 231–238. DOI: 10.1016 / j.jconrel.2011.06.031. [PubMed] [CrossRef] [Google Scholar] 132. Jevsevar DS, Jones DL, Matzkin EG, Manner PA, Mooar P, Schousboe JT, et al. Американская академия хирургов-ортопедов. Лечение остеоартроза коленного сустава: руководство, основанное на доказательствах, 2-е издание. JBJS. 2013. 95 (20): 1885–1886. [PubMed] [Google Scholar] 133.Ли ПБ, Ким Ю.С., Лим Й.Дж., Ли СиДжей, Сим У.С., Ха Ч.В. и др. Сравнение гиалуронатов с высокой и низкой молекулярной массой у пациентов с остеоартритом коленного сустава: открытое рандомизированное многоцентровое клиническое исследование. J Int Med Res. 2006. 34 (1): 77–87. DOI: 10.1177 / 147323000603400110. [PubMed] [CrossRef] [Google Scholar] 134. Киршнер М., Маршалл Д. Двойное слепое рандомизированное контролируемое исследование по сравнению альтернативных форм высокомолекулярного гиалуронана для лечения остеоартрита коленного сустава. Osteoarthr Cartil.2006. 14 (2): 154–162. DOI: 10.1016 / j.joca.2005.09.003. [PubMed] [CrossRef] [Google Scholar] 135. Чен А.Л., Десаи П., Адлер Э.М., Ди Чезаре ЧП. Гранулематозное воспаление после вискозиметрии колена Hylan G-F 20: отчет о шести случаях. J Bone Joint Surg Am. 2002; 84-А (7): 1142–1147. [PubMed] [Google Scholar] 136. Зардави И.М., Чан И. Синвисковидный перисиновит. Патология. 2001. 33 (4): 519–520. DOI: 10.1080 / 00313020120083296. [PubMed] [CrossRef] [Google Scholar]
Гиалуроновая кислота: использование, взаимодействие, механизм действия
Гиалуроновая кислота — это гликозаминогликан, используемый для облегчения боли в суставах, заживления ран, офтальмологического лечения, косметического лечения , и различные другие приложения.
Гиалуроновая кислота (НА) представляет собой анионный несульфатированный гликозаминогликан, обнаруженный в соединительной и эпителиальной тканях; он был впервые выделен в 1934 году. Карл Мейер и Джон Палмер получили гликозаминогликан (ГАГ) из бычьего глаза, дав ему название «гиалуроновая кислота». ГК участвует во многих важных физиологических процессах, включая, помимо прочего, заживление ран, регенерацию тканей и смазку суставов.Он демонстрирует уникальные вязкоупругие, увлажняющие, противовоспалительные свойства и другие важные свойства, которые оказываются полезными в различных клинических применениях. 2
HA используется в системах доставки лекарств для лечения рака, офтальмологических состояний, состояний суставов и эстетических недостатков. 3 Некоторые препараты гиалуроновой кислоты были одобрены FDA и доступны в пероральной, местной и инъекционной формах. Популярным применением гиалуроновой кислоты в последние годы являются косметические инъекции из-за ее способности сводить к минимуму появление морщин и недостатки кожи, связанные со старением. 17
- Вес
- Среднее значение: 776.6486
Моноизотопное: 776.233485724 9228 - 9030 Химическая формула 9228
- Химическая формула 2 O 23
Внутрисуставные препараты гиалуроновой кислоты показаны при боли в коленях, связанной с остеоартритом. 23 Гиалуроновая кислота используется в косметических целях для предотвращения и уменьшения появления морщин на лице, а также в качестве кожного наполнителя для коррекции недостатков лица или других недостатков на других частях тела. 20,22 Часто является ингредиентом для местного применения для заживления ран и симптоматического лечения раздражения кожи, вызванного различными причинами. 18 Гиалуроновая кислота также может быть показана в офтальмологических препаратах или пероральных капсулах для лечения дискомфорта, вызванного сухостью глаз или конъюнктивита, а также из-за ее защитных свойств во время и перед операциями на глазах. 2,21 Наконец, гиалуроновую кислоту можно использовать не по назначению для покрытия мочевого пузыря для облегчения симптомов интерстициального цистита. 6
Снижение количества неудач при разработке лекарств.
Создание, обучение и проверка моделей машинного обучения с использованием структурированных наборов данных, основанных на фактических данных.
Создавайте, обучайте и проверяйте прогнозные модели машинного обучения с помощью структурированных наборов данных.
Избегайте опасных для жизни побочных эффектов лекарственных препаратов
Улучшите поддержку принятия клинических решений с помощью информации о противопоказаниях и предупреждениях о «черных ящиках», ограничениях для населения, вредных рисках & более.
Избегайте опасных для жизни побочных эффектов лекарственных препаратов и улучшайте поддержку принятия клинических решений.
HA обладает смазочными, амортизирующими, стабилизирующими суставами и водобалансирующими свойствами. 2 Он похож на встречающийся в природе гликозаминогликан (ГАГ) в суставах. Гиалуроновая кислота действует как смазка и амортизатор, облегчая подвижность суставов и тем самым уменьшая боль при остеоартрите. Гиалуроновая кислота обладает антиоксидантным, противовоспалительным и обезболивающим действием. 2 Водные балансирующие свойства и вязкоупругость гиалуроновой кислоты полезны при косметических инъекциях, придавая объем и уменьшая появление дефектов и морщин. 17 Благодаря вышеперечисленным свойствам ГК оказывает защитное действие на глаза и роговицу. 3
Общие принципы и связывание рецептора гиалуроновой кислоты
Гиалуроновая кислота работает по двум основным механизмам: выступая в качестве пассивной структурной молекулы или выступая в качестве сигнальной молекулы, в зависимости от размера молекулы.Физико-химические свойства высокомолекулярной ГК способствуют пассивным структурным эффектам, демонстрируя гигроскопичность и вязкоупругость и улучшая гидратацию, водный баланс и структурную целостность. Как сигнальная молекула, взаимодействующая с белками, HA вызывает несколько противоположных эффектов в зависимости от молекулярной массы: про- или противовоспалительные эффекты, стимулирование или ингибирование миграции клеток и активация или ингибирование деления клеток. 3
Гиалуроновая кислота оказывает терапевтическое действие за счет связывания с тремя основными типами рецепторов клеточной поверхности: CD44 (мембранный гликопротеин), рецептор опосредованной гиалуронатом подвижности (RHAMM) и молекула межклеточной адгезии 1 (ICAM-1).CD44 считается наиболее широко распространенным рецептором гиалуроновой кислоты, демонстрируя клеточные взаимодействия с остеопонтином, коллагеном и матриксными металлопротеиназами (ММП). Гиалуроновые кислоты с высокой и низкой молекулярной массой демонстрируют различные молекулярные и клеточные механизмы взаимодействия с рецепторами CD44. Некоторые примеры этих эффектов включают модификацию путей выживания хондроцитов в дополнение к изменению путей апоптоза. Рецептор гиалуроновой кислоты эндотелия лимфатических сосудов (LYVE-1) и рецептор гиалуроновой кислоты для эндоцитоза (HARE) (также известный как Стабилин-2) также связываются с гиалуроновой кислотой. 2
Гиалуроновая кислота для кожных заболеваний и косметики
Анионные свойства гиалуроновой кислоты заставляют ее притягивать воду и вызывать отек, увеличивая объем тканей и структурную целостность кожи. Процесс старения связан со снижением выработки гиалуроновой кислоты и коллагена в коже, что приводит к появлению морщин и потере объема лица. Кожные наполнители гиалуроновой кислоты заменяют утраченный объем тканей, придавая коже полный и молодой вид, которая потеряла свою эластичность.Наполнители с гиалуроновой кислотой содержат частицы сшитой гиалуроновой кислоты, что придает концентрированному веществу устойчивость к различным формам физического и химического разрушения. Косметические преимущества наполнителя на основе гиалуроновой кислоты могут длиться до 6 месяцев, в зависимости от марки и техники инъекции. 17 Кроме того, известно, что кожные наполнители гиалуроновой кислоты увеличивают производство фибробластов 17 , поддерживая заживление ран и предлагая облегчение при раздражающих и воспалительных состояниях кожи. 1
Гиалуроновая кислота от боли в суставах
Большинство клеток человеческого тела способны синтезировать ГК. Он является основным компонентом внеклеточного матрикса (ВКМ) и может быть обнаружен в костном мозге, хрящах и синовиальной жидкости суставов. 2 При остеоартрите концентрация естественной гиалуроновой кислоты постепенно снижается, снижая вязкость синовиальной жидкости, которая защищает суставы от чрезмерного трения. Введение внутрисуставной гиалуроновой кислоты увеличивает вязкость синовиальной суставной жидкости, уменьшая трение и, следовательно, снимая болезненные симптомы артрита. 17
Гиалуроновая кислота для офтальмологических заболеваний и офтальмологических процедур
Растворы гиалуроновой кислоты с концентрацией более 0,1% увлажняют поверхность глаз для лечения симптомов сухого глаза, улучшая стабилизацию слезной пленки, восполняя дефицит ГК, уменьшая трение и предотвращая связывание посторонних веществ с тканью глаза . 2,17 Гиалуроновая кислота часто используется во время и после офтальмологических операций и играет важную роль благодаря своим увлажняющим, вязкоупругим и защитным свойствам.Он способствует заживлению тканей эпителия роговицы и других частей глаза после офтальмологической операции, сводя к минимуму риск спаек и образования свободных радикалов. 2
В литературе имеется ограниченная информация о поглощении и фармакокинетике гиалуроновой кислоты человеком. 2 При пероральном введении крысам гиалуроновая кислота расщепляется кишечными бактериями до олигосахаридов и всасывается в толстой кишке. 8 В фармакокинетических исследованиях на собаках породы гончая ГК легко абсорбировалась и быстро выводилась из организма. 2 При местном применении ГК с низкой молекулярной массой в диапазоне от 20 до 300 кДа абсорбируется через роговой слой, а ГК с высокой молекулярной массой (1000-1400 кДа) не проникает через роговой слой. 7 Биодоступность гиалуроновой кислоты зависит от ее молекулярной массы. 9
В литературе имеется ограниченная информация о фармакокинетике гиалуроновой кислоты для человека. 2 После инъекции кожного наполнителя ГК быстро распределяется по поверхностным и глубоким слоям дермы. 11 Гиалуроновая кислота попадает в кожу крыс после метаболизма в кишечнике до олигосахаридов. 8 У крыс и собак породы бигль, получавших перорально гиалуроновую кислоту, ГК накапливалась в щитовидной железе, почках, мочевом пузыре и желудке. Было обнаружено, что ГК концентрируется в позвонках, суставах и слюнных железах в течение 4 часов после однократного приема. Фармакокинетические исследования на животных предполагают, что ГК распределяется в лимфатической системе. 2,10
В литературе имеется ограниченная информация о фармакокинетике гиалуроновой кислоты для человека. 2 Исследования in vitro показали, что сывороточный альбумин и гиалуроновая кислота связываются с образованием растворимого комплекса. 14
Гиалуроновая кислота расщепляется семейством ферментов, называемых гиалуронидазами. 4 У животных он метаболизируется кишечными бактериями в олигосахариды и впоследствии реабсорбируется в толстом кишечнике. 8
В литературе имеется ограниченная информация о фармакокинетике гиалуроновой кислоты для человека. 2 Исследования на крысах и собаках, которым вводили радиоактивно меченную пероральную дозу ГК, показали, что 87-96% экскреции с калом. Экскреция гиалуроновой кислоты в основном происходит внепочечным путем, с некоторым участием селезенки. 10,2
При внутрисуставном введении гиалуроновая кислота имеет период полувыведения от 17 часов до 1.5 дней. Период полувыведения гиалуроновой кислоты больше для очищенных составов или препаратов с высокой молекулярной массой. 17 Согласно исследованиям на животных, он может варьироваться в зависимости от молекулярной массы введенной ГК. В фармакокинетических исследованиях было установлено, что метаболический период полувыведения гиалуроновой кислоты у овец составляет приблизительно 27 часов. Считается, что у овец ГК быстро выводится через кровь и печень. 2
В литературе имеется ограниченная информация о фармакокинетике гиалуроновой кислоты для человека. 2 В фармакокинетическом исследовании на кроликах максимальный клиренс гиалуроновой кислоты, вводимой внутривенно, составлял около 30 мг / день / кг. 12
Улучшение поддержки принятия решений и результатов исследований
Со структурированными данными о побочных эффектах, в том числе: предупреждений черного ящика, побочные реакции, предупреждения и меры предосторожности, а также показатели заболеваемости.
Улучшите поддержку принятия решений и результаты исследований с помощью наших структурированных данных о побочных эффектах.
Пероральная LD50 натриевой соли гиалуроновой кислоты для крысы составляет> 800 мг / кг. 24 Информация о передозировке недоступна в литературе. Профиль безопасности гиалуроновой кислоты благоприятный, однако опубликованы единичные сообщения о смерти после вагинальной инъекции гиалуроновой кислоты; Смертельные случаи, вероятно, произошли из-за плохого регулирования процедуры. 16
InChI = 1S / C28h54N2O23 / c1-5 (33) 29-9-18 (11 (35) 7 (3-31) 47-25 (9) 46) 49-28-17 (41) 15 (39) 20 (22 (53-28) 24 (44) 45) 51-26-10 (30-6 (2) 34) 19 (12 (36) 8 (4-32) 48-26) 50-27-16 (40 ) 13 (37) 14 (38) 21 (52-27) 23 (42) 43 / h7-22,25-28,31-32,35-41,46H, 3-4h3,1-2h4, (H, 29,33) (H, 30,34) (H, 42,43) (H, 44,45) / t7-, 8-, 9-, 10-, 11-, 12-, 13 +, 14 +, 15-, 16-, 17-, 18?, 19?, 20 +, 21 +, 22 +, 25-, 26 +, 27-, 28- / m1 / s1
(2S, 3S, 4R, 5R, 6R) -3 — {[(2S, 3R, 5S, 6R) -4 — {[(2R, 3R, 4S, 5S, 6S) -6-карбокси-3,4,5-тригидроксиоксан -2-ил] окси} -3-ацетамидо-5-гидрокси-6- (гидроксиметил) оксан-2-ил] окси} -6 — {[(2R, 3R, 5S, 6R) -3-ацетамидо-2, 5-дигидрокси-6- (гидроксиметил) оксан-4-ил] окси} -4,5-дигидроксиоксан-2-карбоновая кислота
CC (= O) N [C @ H] 1 [C @ H] (O) O [C @ H] (CO) [C @@ H] (O) C1O [C @@ H] 1O [ C @@ H] ([C @@ H] (O [C @@ H] 2O [C @ H] (CO) [C @@ H] (O) C (O [C @@ H] 3O [C @@ H] ([C @@ H] (O) [C @ H] (O) [C @ H] 3O) C (O) = O) [C @ H] 2NC (C) = O) [C @H] (O) [C @ H] 10) C (O) = O
Каков механизм действия гиалуроновой кислоты (ГК) при лечении остеоартрита (ОА)?
Информационный бюллетень по остеоартриту.Центры по контролю и профилактике заболеваний. Доступно на https://www.cdc.gov/arthritis/basics/osteoarthritis.htm. 10 января 2019 г .; Дата обращения: 7 февраля 2020 г.
Kotlarz H, Gunnarsson CL, Fang H, Rizzo JA. Страховая компания и наличные расходы на остеоартрит в США: данные национального опроса. Революционный артрит . 2009 Декабрь 60 (12): 3546-53. [Медлайн]. [Полный текст].
Бакленд-Райт C, Verbruggen G, Haraoui PB. Визуализация: радиологическая оценка остеоартрита кисти. Хрящевой артроз . 2000. 55-6.
Jewell FM, Watt I, Doherty M. Простые рентгенографические признаки остеоартрита. Брандт К.Д., Доэрти М., Ломандер Л.С., ред. Остеоартроз . Нью-Йорк, Нью-Йорк: издательство Оксфордского университета; 1998. 217-37.
Recht MP, Kramer J, Marcelis S, Pathria MN, Trudell D, Haghighi P, et al. Аномалии суставного хряща коленного сустава: анализ доступных методов МРТ. Радиология .1993 Май. 187 (2): 473-8. [Медлайн].
Охотник DJ. Расширенная визуализация при остеоартрите. Bull NYU Hosp Jt Dis . 2008. 66 (3): 251-60. [Медлайн].
Keen HI, Wakefield RJ, Conaghan PG. Систематический обзор ультразвукового исследования при остеоартрите. Энн Рум Дис . 2009 Май. 68 (5): 611-9. [Медлайн].
Recht MP, Goodwin DW, Winalski CS, Белый LM. МРТ суставного хряща: пересматривая текущее состояние и будущие направления. AJR Am J Рентгенол . 2005 Октябрь 185 (4): 899-914. [Медлайн].
Краус В.Б., МакДэниэл Г., Уоррелл Т.В., Фенг С., Вейл Т.П., Варджу Г. и др. Связь сцинтиграфических аномалий костей с деформацией колена и болью. Энн Рум Дис . 2009 ноябрь 68 (11): 1673-9. [Медлайн].
Felson DT, Zhang Y, Anthony JM, Naimark A, Anderson JJ. Снижение веса снижает риск симптоматического остеоартрита коленного сустава у женщин. Фрамингемское исследование. Энн Интерн Мед. . 1992 г., 1. 116 (7): 535-9. [Медлайн].
Kraeutler MJ, Mitchell JJ, Chahla J, McCarty EC, Pascual-Garrido C. Внутрисуставная имплантация мезенхимальных стволовых клеток, Часть 1: Обзор литературы по профилактике постменискэктомического остеоартрита. Orthop J Sports Med . 2017 19 января. 5 (1): 2325967116680815. [Медлайн]. [Полный текст].
Лафлин Дж. Генетическая эпидемиология первичного остеоартрита человека: современное состояние. Эксперт Рев Мол Мед . 2005 24 мая. 7 (9): 1-12. [Медлайн].
Dagenais S, Garbedian S, Wai EK. Систематический обзор распространенности первичного остеоартроза тазобедренного сустава на рентгенограммах. Clin Orthop Relat Res . 2009 Март 467 (3): 623-37. [Медлайн]. [Полный текст].
Ли П., Руни П.Дж., Старрок Р.Д., Кеннеди А.С., Дик В. Этиология и патогенез остеоартроза: обзор. Семин Артрит Rheum . 1974 Весна. 3 (3): 189-218.[Медлайн].
Мюррей РО. Этиология первичного остеоартроза тазобедренного сустава. Br J Радиол . 1965, ноябрь 38 (455): 810-24. [Медлайн].
Radin ER, Paul IL, Rose RM. Патогенез первичного остеоартроза. Ланцет . 1972 24 июня. 1 (7765): 1395-6. [Медлайн].
Шарма Л. Эпидемиология остеоартроза. Московиц Р.В., Хауэлл Д.С., Альтман, Р.Д. и др., Ред. Остеоартроз . 3-е изд.2001. 3-27.
Вейс Э., Вербрюгген Г. Эволюция и прогноз остеоартрита. Reginster JY, Pelletier JP, Martel-Pelletier J, et al, eds. Остеоартроз . 1999. 312-3.
Valderrabano V, Horisberger M, Russell I, Dougall H, Hintermann B. Этиология остеоартроза голеностопного сустава. Clin Orthop Relat Res . 2009 Июль 467 (7): 1800-6. [Медлайн]. [Полный текст].
Jewell FM, Ватт I, Доэрти М.Простые рентгенологические признаки остеоартроза. Брандт К.Д., Доэрти М., Ломандер Л.С., ред. Остеоартроз . Нью-Йорк, Нью-Йорк: издательство Оксфордского университета; 1998. 217-37.
Манкин HJ. Реакция суставного хряща на травму и остеоартроз (первая из двух частей). N Engl J Med . 1974 12 декабря. 291 (24): 1285-92. [Медлайн].
Miller EJ, Van der Korst JK, Sokoloff L. Коллаген суставного и реберного хряща человека. Революционный артрит . 1969 12 (1): 21–9 февраля. [Медлайн].
Фадке К. Регуляция метаболизма хондроцитов в суставном хряще — гипотеза. Дж. Ревматол . 1983 декабрь 10 (6): 852-60. [Медлайн].
Resnick D, Niwayama G. Дегенеративное заболевание экстраспинальной локализации. Резник Д., изд. Диагностика заболеваний костей и суставов . 3-е изд. 1995. 1263-1371.
Пул AR.Введение в патофизиологию остеоартроза. Передний Biosci . 1999 15 октября. 4: D662-70. [Медлайн].
van Baarsen LG, Lebre MC, van der Coelen D, Aarrass S, Tang MW, Ramwadhdoebe TH. Неоднородный паттерн экспрессии интерлейкина 17A (IL-17A), IL-17F и их рецепторов в синовиальной оболочке ревматоидного артрита, псориатического артрита и остеоартрита: возможное объяснение отсутствия ответа на терапию анти-IL-17? Arthritis Res Ther . 2014 г.16 (4): 426. [Медлайн].
Краснокутский С., Ошинский С., Аттур М., Ма С., Чжоу Х., Чжэн Ф. и др. Уровни уратов в сыворотке предсказывают сужение суставной щели у пациентов без подагры с медиальным остеоартритом коленного сустава. Ревматический артрит . 2017 июн.69 (6): 1213-1220. [Медлайн]. [Полный текст].
Hoff P, Buttgereit F, Burmester GR, Jakstadt M, Gaber T, Andreas K и др. Синовиальная жидкость при остеоартрите активирует провоспалительные цитокины в первичных хондроцитах человека. Инт Ортоп . 2013 Январь 37 (1): 145-51. [Медлайн]. [Полный текст].
Радин Э.Л., Пол ИЛ. Реакция суставов на ударную нагрузку. I. Износ in vitro. Революционный артрит . 1971 май-июнь. 14 (3): 356-62. [Медлайн].
Беркитт Х.Г., Стивенс А., Лоу Дж. С.. Система скелета. Основы гистопатологии . 3-е изд. Нью-Йорк, Нью-Йорк: Черчилль Ливингстон; 1996. 260.
Хамерман Д. Биология остеоартрита. N Engl J Med . 1989 18 мая. 320 (20): 1322-30. [Медлайн].
Hartmann C, De Buyser J, Henry Y, Morère-Le Paven MC, Dyer TA, Rode A. Ядерные гены контролируют изменения в организации митохондриального генома в тканевых культурах, полученных из незрелых зародышей пшеницы. Curr Genet . 1992 Май. 21 (6): 515-20. [Медлайн].
Хауэлл DS. Патогенез остеоартроза. Ам Дж. Мед . 1986, 28 апреля. 80 (4B): 24-8.[Медлайн].
Буллоу PG. Геометрия диартродиального сустава, ее физиологическое состояние и возможное значение возрастных изменений в распределении геометрии и нагрузки и развитии остеоартрита. Clin Orthop Relat Res . 1981 Май. 61-6. [Медлайн].
Aigner T, Rose J, Martin J, Buckwalter J. Теории старения первичного остеоартрита: от эпидемиологии до молекулярной биологии. Омоложение .2004 Лето. 7 (2): 134-45. [Медлайн].
OUTERBRIDGE RE. Этиология хондромаляции надколенника. J Bone Joint Surg Br . 1961 г., ноябрь 43-B: 752-7. [Медлайн].
Zgoda M, Paczek L, Bartlomiejczyk I, Sieminska J, Chmielewski D, Górecki A. Возрастное снижение активности коллагеназы в головке бедренной кости у пациентов с остеоартрозом тазобедренного сустава. Clin Rheumatol . 2007 26 февраля (2): 240-1. [Медлайн].
Reyes C, Leyland KM, Peat G, Cooper C, Arden NK, Prieto-Alhambra D.Связь между избыточным весом и ожирением и риском клинически диагностированного остеоартрита колена, бедра и кисти: популяционное когортное исследование. Ревматический артрит . 2016 августа 68 (8): 1869-75. [Медлайн].
Felson DT, Anderson JJ, Naimark A, Walker AM, Meenan RF. Ожирение и остеоартроз коленного сустава. Фрамингемское исследование. Энн Интерн Мед. . 1 июля 1988 г. 109 (1): 18-24. [Медлайн].
Goulston LM, Kiran A, Javaid MK, et al.Предсказывает ли ожирение боль в коленях у женщин в течение четырнадцати лет независимо от рентгенологических изменений? Центр по уходу за артритом (Хобокен) . 2011 Октябрь 63 (10): 1398-406. [Медлайн].
Херли М.В. Роль мышечной слабости в патогенезе остеоартроза. Rheum Dis Clin North Am . 1999 Май. 25 (2): 283-98, vi. [Медлайн].
Felson DT. Факторы риска остеоартрита: понимание уязвимости суставов. Clin Orthop Relat Res .2004 окт. S16-21. [Медлайн].
Williams MF, Лондон DA, Husni EM, Navaneethan S, Kashyap SR. Диабет 2 типа и остеоартрит: систематический обзор и метаанализ. J Осложнения диабета . 2016 июл.30 (5): 944-50. [Медлайн].
Jeon OH, Kim C, Laberge RM, Demaria M, Rathod S, Vasserot AP и др. Местное очищение от стареющих клеток замедляет развитие посттравматического остеоартрита и создает прорегенеративную среду. Нат Мед . 2017 июня 23 (6): 775-781. [Медлайн]. [Полный текст].
de Boer TN, van Spil WE, Huisman AM, Polak AA, Bijlsma JW, Lafeber FP, et al. Адипокины сыворотки при остеоартрозе; сравнение с контролем и взаимосвязь с местными параметрами синовиального воспаления и повреждения хряща. Хрящевой артроз . 2012 августа 20 (8): 846-53. [Медлайн].
Андерсон Д.Д., Чубинская С., Гилак Ф., Мартин Дж. А., Оегема Т.Р., Олсон С.А. и др.Посттравматический остеоартрит: лучшее понимание и возможности раннего вмешательства. Дж. Ортоп Рес . 2011 июн.29 (6): 802-9. [Медлайн]. [Полный текст].
Felson DT, Niu J, Gross KD, Englund M, Sharma L, Cooke TD, et al. Смещение вальгуса является фактором риска заболеваемости и прогрессирования латерального остеоартрита коленного сустава: результаты исследования MOST и инициативы по остеоартриту. Революционный артрит . 2012 30 ноября. [Medline].
Вальдес А.М., Спектор Т.Д.Генетическая эпидемиология остеоартроза тазобедренного и коленного суставов. Нат Ревматол . 2011 7 января (1): 23-32. [Медлайн].
Felson DT. Развитие клинического понимания остеоартрита. Arthritis Res Ther . 2009. 11 (1): 203. [Медлайн]. [Полный текст].
Pollard TC, Batra RN, Judge A, Watkins B, McNally EG, Gill HS, et al. Генетическая предрасположенность к наличию и 5-летнему клиническому прогрессированию остеоартроза тазобедренного сустава. Хрящевой артроз . 2012 май. 20 (5): 368-75. [Медлайн].
Вальдес А.М., Спектор Т.Д. Клиническая значимость генетической предрасположенности к остеоартриту. Лучшая практика Res Clin Rheumatol . 2010 24 февраля (1): 3-14. [Медлайн].
Джеффрис М.А., Доника М., Бейкер Л.В., Стивенсон М.Э., Аннан А.С., Хамфри МБ. Полногеномное исследование метилирования ДНК выявляет значительные эпигеномные изменения в остеоартрозном хряще. Ревматический артрит .2014 Октябрь 66 (10): 2804-15. [Медлайн].
Chang SC, Hoang B, Thomas JT, Vukicevic S, Luyten FP, Ryba NJ, et al. Морфогенетические белки хрящевого происхождения. Новые члены суперсемейства трансформирующих факторов роста-бета преимущественно экспрессируются в длинных костях во время эмбрионального развития человека. Дж. Биол. Хим. . 1994 11 ноября. 269 (45): 28227-34. [Медлайн].
Lin K, Wang S, Julius MA, Kitajewski J, Moos M Jr, Luyten FP. Богатый цистеином вьющийся домен Frzb-1 необходим и достаточен для модуляции передачи сигналов Wnt. Proc Natl Acad Sci U S A . 1997, 14 октября. 94 (21): 11196-200. [Медлайн]. [Полный текст].
Чапман К., Такахаши А., Меуленбельт I, Уотсон С., Родригес-Лопес Дж., Эгли Р. и др. Мета-анализ европейских и азиатских когорт показывает глобальную роль функционального SNP в 5 ‘UTR GDF5 с предрасположенностью к остеоартриту. Хум Мол Генет . 2008 15 мая. 17 (10): 1497-504. [Медлайн].
Bos SD, Slagboom PE, Meulenbelt I. Новые взгляды на остеоартрит: особенности раннего развития болезни, связанной со старением. Curr Opin Rheumatol . 2008 20 сентября (5): 553-9. [Медлайн].
Чепмен К., Вальдес А.М. Генетические факторы в патогенезе ОА. Кость . 2012 Август 51 (2): 258-64. [Медлайн].
Перейра Д., Пелетейро Б., Араужу Дж., Бранко Дж., Сантос Р.А., Рамос Э. Влияние определения остеоартрита на оценки распространенности и заболеваемости: систематический обзор. Хрящевой артроз . 2011 ноября 19 (11): 1270-85. [Медлайн].
Робертс Дж., Берч Т.А..Распространенность остеоартроза у взрослых по возрасту, полу, расе и географическому положению. Vital Health Stat 11 . 1966 июн. 1-27. [Медлайн].
Hoaglund FT, Yau AC, Wong WL. Остеоартроз тазобедренного сустава и других суставов на юге Китая в Гонконге. J Bone Joint Surg Am . 1973, апрель, 55 (3): 545-57. [Медлайн].
Felson DT. Сравнение распространенности ревматических заболеваний в Китае с остальным миром. Arthritis Res Ther .2008. 10 (1): 106. [Медлайн]. [Полный текст].
Джордан Дж. М., Хелмик К. Г., Реннер Дж. Б., Лута Дж., Драгомир А. Д., Вудард Дж. И др. Распространенность симптомов коленного сустава, рентгенологического и симптоматического остеоартрита коленного сустава у афроамериканцев и кавказцев: Проект остеоартрита округа Джонстон. Дж. Ревматол . 2007, январь, 34 (1): 172-80. [Медлайн].
Чаппл С.М., Николсон Х., Бакстер Г.Д., Эбботт Дж. Характеристики пациентов, которые прогнозируют прогрессирование остеоартрита коленного сустава: систематический обзор прогностических исследований. Центр по уходу за артритом (Хобокен) . 2011 августа 63 (8): 1115-25. [Медлайн].
[Рекомендации] Альтман Р., Аларкон Г., Аппельрут Д., Блох Д., Боренштейн Д., Брандт К. и др. Критерии Американского колледжа ревматологии для классификации остеоартрита кисти и сообщения о нем. Революционный артрит . 1990 ноябрь 33 (11): 1601-10. [Медлайн].
[Рекомендации] Альтман Р., Аларкон Дж., Аппельрут Д., Блох Д., Боренштейн Д., Брандт К. и др.Критерии Американского колледжа ревматологии для классификации остеоартрита бедра и сообщения о нем. Революционный артрит . 1991 Май. 34 (5): 505-14. [Медлайн].
[Рекомендации] Альтман Р., Аш Э, Блох Д., Боле Г., Боренштейн Д., Брандт К. и др. Разработка критериев классификации и отчетности по остеоартриту. Классификация остеоартроза коленного сустава. Комитет по диагностическим и терапевтическим критериям Американской ассоциации ревматизма. Революционный артрит . 1986, 29 августа (8): 1039-49. [Медлайн].
Marshall M, Peat G, Nicholls E, van der Windt D, Myers H, Dziedzic K. Подгруппы симптоматического остеоартрита кисти у пожилых людей, проживающих в сообществах в Соединенном Королевстве: распространенность, взаимосвязь, профили факторов риска и клинические характеристики на исходном уровне и через 3 года. Хрящевой артроз . 2013 21 ноября (11): 1674-84. [Медлайн].
Brandt KD.Пессимистический взгляд на серологические маркеры для диагностики и лечения остеоартрита. Биохимические, иммунологические и клинико-патологические барьеры. J Rheumatol Suppl . 1989 августа 18: 39-42. [Медлайн].
Patra D, Sandell LJ. Последние достижения в области биомаркеров остеоартрита. Curr Opin Rheumatol . 2011 Сентябрь 23 (5): 465-70. [Медлайн].
[Рекомендации] МакАлиндон Т.Э., Баннуру Р.Р., Салливан М.К., Арден Н.К., Беренбаум Ф., Бирма-Зейнстра С.М. и др.Рекомендации OARSI по безоперационному лечению остеоартрита коленного сустава. Хрящевой артроз . 2014 марта 22 (3): 363-88. [Медлайн]. [Полный текст].
Агентство медицинских исследований и качества. Лечение остеоартрита коленного сустава: обновленный обзор. AHRQ. Доступно по адресу https://effectivehealthcare.ahrq.gov/topics/osteoarthritis-knee-update/research-2017. 4 мая 2017 г .; Доступ: 15 марта 2019 г.
Цуй GH, Ван YY, Li CJ, Shi CH, Wang WS.Эффективность мезенхимальных стволовых клеток в лечении пациентов с остеоартрозом коленного сустава: метаанализ. Эксперт Тер Мед . 2016 12 ноября (5): 3390-3400. [Медлайн]. [Полный текст].
Кристьянссон Б., Хонсавек С. Современные перспективы лечения остеоартрита мезенхимальными стволовыми клетками. Стволовые клетки Инт . 2014. 2014: 1943 18. [Медлайн].
Pas HI, Winters M, Haisma HJ, Koenis MJ, Tol JL, Moen MH. Инъекции стволовых клеток при остеоартрозе коленного сустава: систематический обзор литературы. Br J Sports Med . 2017 Август 51 (15): 1125-1133. [Медлайн].
Чахла Дж., Пьюцци Н.С., Митчелл Дж. Дж., Дин С.С., Паскуаль-Гарридо С., ЛаПрейд РФ и др. Внутрисуставная клеточная терапия остеоартрита и очаговых дефектов хряща коленного сустава: систематический обзор литературы и анализ качества исследований. J Bone Joint Surg Am . 2016 21 сентября. 98 (18): 1511-21. [Медлайн].
Zeng C, Dubreuil M, LaRochelle MR, Lu N, Wei J, Choi HK, et al.Связь трамадола со смертностью от всех причин среди пациентов с остеоартритом. ДЖАМА . 2019 12 марта. 321 (10): 969-982. [Медлайн].
Келли JC. Трамадол связан с более высокой смертностью от остеоартрита. Медицинские новости Medscape . 12 марта 2019 г. Доступно по адресу https://www.medscape.com/viewarticle/
Freeman S. Tramadol Риск смертности при остеоартрите может перевесить преимущества. Медицинские новости Medscape. Доступно по адресу https: // www.medscape.com/viewarticle/4. 8 июня 2020 г .; Дата обращения: 10 июня 2020 г.
Консенси (амлодипин / целекоксиб) [вкладыш в упаковке]. Тель-Авив, Израиль: Китов Фарма Лтд., Июнь 2018 г. Доступно по ссылке [Полный текст].
Kingsbury SR, Tharmanathan P, Keding A, Ronaldson SJ, Grainger A, Wakefield RJ, et al. Эффективность гидроксихлорохина в уменьшении симптомов остеоартрита кисти: рандомизированное исследование. Энн Интерн Мед. . 2018 20 февраля. [Medline].
Агентство медицинских исследований и качества. Анальгетики при остеоартрите: обновление сравнительного обзора эффективности 2006 года. AHRQ. Доступно по адресу https://effectivehealthcare.ahrq.gov/topics/osteoarthritis-pain/research. 24 октября 2011 г .; Доступ: 15 марта 2019 г.
Citrome L, Weiss-Citrome A. Систематический обзор дулоксетина для лечения боли при остеоартрите: какое количество нужно лечить, какое количество необходимо для нанесения вреда, и вероятность того, что вам помогут или повредят ?. Постградская медицина . 2012 января 124 (1): 83-93. [Медлайн].
Frakes EP, Risser RC, Ball TD, Hochberg MC, Wohlreich MM. Дулоксетин добавлен к пероральным нестероидным противовоспалительным препаратам для лечения боли в коленях, вызванной остеоартритом: результаты рандомизированного двойного слепого плацебо-контролируемого исследования. Curr Med Res Opin . 2011 27 декабря (12): 2361-72. [Медлайн].
Нойштадт DH. Внутрисуставная терапия. Московиц Р.В., Хауэлл Д.С., Альтман Р.Д. и др., Ред. Остеоартроз . 3-е изд. 2001. 393-409.
Lineker SC, Bell MJ, Boyle J, Badley EM, Flakstad L, Fleming J и др. Внедрение руководств по клинической практике артрита в первичной медико-санитарной помощи. Мед Обучение . 2009 31 марта (3): 230-7. [Медлайн].
Годвин М., Доус М. Внутрисуставные инъекции стероидов при болях в коленях. Систематический обзор с метаанализом. Кан Фам Врач . 2004 Февраль 50: 241-8. [Медлайн]. [Полный текст].
McAlindon TE, LaValley MP, Harvey WF, Price LL, Driban JB, Zhang M, et al. Эффект внутрисуставного триамцинолона по сравнению с физиологическим раствором на объем хряща коленного сустава и боль у пациентов с остеоартритом коленного сустава: рандомизированное клиническое испытание. ДЖАМА . 2017 16 мая. 317 (19): 1967-1975. [Медлайн].
Инъекции стероидов Haelle T. Увеличение потери хрящевой ткани при артрите коленного сустава. Медицинские новости Medscape. Доступно на https://www.medscape.com/viewarticle/880072.16 мая 2017 г .; Доступ: 31 октября 2017 г.
Конаган П.Г., Хантер Д.Д., Коэн С.Б., Краус В.Б., Беренбаум Ф., Либерман Дж. Р. и др. Эффекты однократной внутрисуставной инъекции микросферного препарата триамцинолона ацетонида на боль при остеоартрите коленного сустава: двойное слепое, рандомизированное, плацебо-контролируемое многонациональное исследование. J Bone Joint Surg Am . 2018 г. 18 апреля. 100 (8): 666-677. [Медлайн]. [Полный текст].
Lambert RG, Hutchings EJ, Grace MG, Jhangri GS, Conner-Spady B, Maksymowych WP.Инъекции стероидов при остеоартрите тазобедренного сустава: рандомизированное двойное слепое плацебо-контролируемое исследование. Революционный артрит . 2007 Июль 56 (7): 2278-87. [Медлайн].
Мартин CL, Браун JA. Внутрисуставные инъекции кортикостероидов при симптоматическом остеоартрите коленного сустава: что необходимо знать врачу-ортопеду. J Am Acad Orthop Surg . 2019 1. 27 (17): e758-e766. [Медлайн]. [Полный текст].
Kompel AJ, Roemer FW, Murakami AM, Diaz LE, Crema MD, Guermazi A.Внутрисуставные инъекции кортикостероидов в бедро и колено: возможно, не так безопасно, как мы думали ?. Радиология . 2019 15 октября 1
. [Medline]. [Полный текст].
Ститик Т.П., Леви Я. Вязкоструктурные добавки (биодобавки) при остеоартрите. Am J Phys Med Rehabil . 2006 ноябрь 85 (11 приложение): S32-50. [Медлайн].
Беллами Н., Кэмпбелл Дж., Робинсон В., Джи Т., Борн Р., Уэллс Г. Вискозависимая добавка для лечения остеоартроза колена. Кокрановская база данных Syst Rev . 2006 г. 19 апреля. CD005321. [Медлайн].
Гольдберг В.М., Баквалтер Я.А. Гиалуронаны в лечении остеоартрита коленного сустава: данные о модифицирующей болезнь активности. Хрящевой артроз . 2005 марта 13 (3): 216-24. [Медлайн].
Альтман Р.Д., Московиц Р. Внутрисуставной гиалуронат натрия (Гиалган) в лечении пациентов с остеоартрозом коленного сустава: рандомизированное клиническое испытание.Группа изучения Хиалгана. Дж. Ревматол . 1998 25 ноября (11): 2203-12. [Медлайн].
Stitik TP, Blacksin MF, Stiskal DM, Kim JH, Foye PM, Schoenherr L, et al. Эффективность и безопасность лечения гиалуроновой кислотой в сочетании с домашними упражнениями при боли при остеоартрите коленного сустава. Arch Phys Med Rehabil . 2007 Февраль 88 (2): 135-41. [Медлайн].
Вадделл Д.Д., Коломыткин О.В., Данн С, Марино А.А. Гиалуронан подавляет активность металлопротеиназы, индуцированную IL-1beta, в синовиальной ткани. Clin Orthop Relat Res . 2007 декабрь 465: 241-8. [Медлайн].
Gato-Calvo L, Magalhaes J, Ruiz-Romero C, Blanco FJ, Burguera EF. Плазма, обогащенная тромбоцитами, в лечении остеоартрита: обзор текущих данных. Ther Adv Chronic Dis . 2019. 10: 2040622319825567. [Медлайн]. [Полный текст].
Дай В.Л., Чжоу А.Г., Чжан Х., Чжан Дж. Эффективность богатой тромбоцитами плазмы при лечении остеоартрита коленного сустава: метаанализ рандомизированных контролируемых испытаний. Артроскопия . 2017 Mar.33 (3): 659-670.e1. [Медлайн].
Yaradilmis CYU, Demirkale I, Tagral AS, Okkaoglu MC, Ates A, Altay M. Сравнение двух составов плазмы с высоким содержанием тромбоцитов с добавлением вязкости при лечении гонартроза средней степени тяжести: проспективное рандомизированное контролируемое исследование. Ортопедический журнал . 28 января 2020 г. 20: 240-246. [Полный текст].
Chu CR, Rodeo S, Bhutani N, Goodrich LR, Huard J, Irrgang J, et al.Оптимизация клинического использования биопрепаратов в ортопедической хирургии: согласованные рекомендации конференции AAOS / NIH U-13 2018 г. J Am Acad Orthop Surg . 2019 15 января. 27 (2): e50-e63. [Медлайн]. [Полный текст].
Рабаго Д., Паттерсон Дж. Дж., Мундт М., Кийовски Р., Гретти Дж., Сегал Н. А. и др. Пролотерапия декстрозой при остеоартрозе коленного сустава: рандомизированное контролируемое исследование. Энн Фам Мед . 2013 май-июнь. 11 (3): 229-37. [Медлайн]. [Полный текст].
Sawitzke AD, Shi H, Finco MF, Dunlop DD, Bingham CO 3rd, Harris CL, et al.Влияние глюкозамина и / или хондроитинсульфата на прогрессирование остеоартрита коленного сустава: отчет по интервенционному исследованию глюкозаминового / хондроитинового артрита. Революционный артрит . 2008 Октябрь 58 (10): 3183-91. [Медлайн]. [Полный текст].
Clegg DO, Reda DJ, Harris CL, et al. Глюкозамин, хондроитинсульфат и их комбинация для лечения болезненного остеоартрита коленного сустава. N Engl J Med . 2006 г. 23 февраля. 354 (8): 795-808. [Медлайн].
Rutjes AW, Nüesch E, Reichenbach S, Jüni P.S-аденозилметионин при остеоартрозе колена или бедра. Кокрановская база данных Syst Rev . 2009 7 октября. CD007321. [Медлайн].
Ван З., Джонс Дж., Винценберг Т., Кай Дж., Ласлетт Л.Л., Эйткен Д. и др. Эффективность экстракта Curcuma longa для лечения симптомов и синовита выпота при остеоартрите коленного сустава: рандомизированное исследование. Энн Интерн Мед. . 2020 15 сентября [Medline].
Hathcock JN, Shao A. Оценка риска глюкозамина и хондроитинсульфата. Регул Токсикол Фармакол . 2007 Февраль 47 (1): 78-83. [Медлайн].
Gege C, Bao B, Bluhm H, Boer J, Gallagher BM, Korniski B, et al. Открытие и оценка не-Zn хелатирующего селективного ингибитора матриксной металлопротеиназы 13 (MMP-13) для потенциального внутрисуставного лечения остеоартрита. J Med Chem . 2012 26 января. 55 (2): 709-16. [Медлайн].
Брукс М. Смешанные результаты для нового препарата от остеоартрита. Медицинские новости Medscape.Доступно на https://www.medscape.com/viewarticle/
3. 30 декабря 2019 г .; Доступ: 15 апреля 2020 г.
Brown MT, Murphy FT, Radin DM, Davignon I, Smith MD, West CR. Танезумаб уменьшает боль в коленях при остеоартрите: результаты рандомизированного двойного слепого плацебо-контролируемого исследования III фазы. Дж. Боль . 2012 13 августа (8): 790-8. [Медлайн].
Пирсон Р. Лилли утверждает, что новый тип обезболивающего может уменьшить потребность в опиоидах. Медицинские новости Medscape.Доступно на http://www.medscape.com/viewarticle/863797. 25 мая 2016 г .; Доступ: 8 июля 2016 г.
Родди Э, Доэрти М. Изменение образа жизни и остеоартрит: каковы доказательства ?. Лучшая практика Res Clin Rheumatol . 2006 20 февраля (1): 81-97. [Медлайн].
Perrot S, Poiraudeau S, Kabir M, Bertin P, Sichere P, Serrie A и др. Активные или пассивные стратегии купирования боли при остеоартрите тазобедренного и коленного суставов? Результаты национального опроса 4719 пациентов в учреждениях первичной медико-санитарной помощи. Революционный артрит . 2008 15 ноября. 59 (11): 1555-62. [Медлайн].
Беннелл К.Л., Кириакидес М, Ходжес П.В., Хинман Р.С. Влияние двух сеансов бустерной физиотерапии на результаты домашних упражнений у людей с остеоартритом коленного сустава: рандомизированное контролируемое исследование. Центр по уходу за артритом (Хобокен) . 2014 Ноябрь 66 (11): 1680-7. [Медлайн].
Anandacoomarasamy A, Leibman S, Smith G, et al. Снижение веса у тучных людей оказывает структурно-модифицирующее воздействие на медиальный, но не на латеральный суставной хрящ коленного сустава. Энн Рум Дис . 2012 Январь 71 (1): 26-32. [Медлайн].
Мессье SP. Ожирение и остеоартрит: генезис заболевания и нефармакологическое управление весом. Rheum Dis Clin North Am . 2008 г., 34 (3): 713-29. [Медлайн]. [Полный текст].
Маккарти GM, Маккарти DJ. Эффект местного капсаицина в терапии болезненного остеоартрита рук. Дж. Ревматол . 1992 апреля 19 (4): 604-7. [Медлайн].
Watt FE, Kennedy DL, Carlisle KE, Freidin AJ, Szydlo RM, Honeyfield L, et al.Ночная иммобилизация дистального межфалангового сустава снижает боль и деформацию разгибания при остеоартрозе кисти. Ревматология (Оксфорд) . 2014 8 февраля [Medline].
Коэн Р. Ночные шины для пальцев могут облегчить боль при артрите. Medscape [сериал онлайн]. Доступно на http://www.medscape.com/viewarticle/821310. Доступ: 11 марта 2014 г.
Juhl C, Christensen R, Roos EM, Zhang W, Lund H. Влияние типа и дозы упражнений на боль и инвалидность при остеоартрите коленного сустава: систематический обзор и мета-регрессионный анализ рандомизированных контролируемых исследований. Ревматический артрит . 2014 Март 66 (3): 622-36. [Медлайн].
Ян MH, Lin CH, Lin YF, Lin JJ, Lin DH. Влияние нагрузки на нагрузку по сравнению с упражнениями без нагрузки на функцию, скорость ходьбы и чувство положения у участников с остеоартритом коленного сустава: рандомизированное контролируемое исследование. Arch Phys Med Rehabil . 2009 июн 90 (6): 897-904. [Медлайн].
Чайпиньо К., Кароонсупчароен О. Нет разницы между силовой тренировкой в домашних условиях и тренировкой равновесия в домашних условиях при боли у пациентов с остеоартрозом коленного сустава: рандомизированное исследование. Ауст Дж. Физиотер . 2009. 55 (1): 25-30. [Медлайн].
Marks R, Allegrante JP. Хронический остеоартрит и соблюдение физических упражнений: обзор литературы. Закон о физике старения . 2005 октября, 13 (4): 434-60. [Медлайн].
Ван Ц., Шмид Ч., Хибберд П.Л., Калиш Р., Рубенофф Р., Ронес Р. и др. Тайцзи эффективен при лечении остеоартроза коленного сустава: рандомизированное контролируемое исследование. Революционный артрит . 2009 15 ноя.61 (11): 1545-53. [Медлайн].
Wang C, Schmid CH, Iversen MD, Harvey WF, Fielding RA, Driban JB, et al. Сравнительная эффективность тайцзи по сравнению с физиотерапией остеоартрита коленного сустава: рандомизированное исследование. Энн Интерн Мед. . 2016 17 мая. [Medline].
Кан Дж. В., Ли М. С., Посадски П., Эрнст Э. Тайчи для лечения остеоартрита: систематический обзор и метаанализ. BMJ Open . 2011 28 марта. 1 (1): e000035.[Медлайн]. [Полный текст].
Гудман А. Коленный бандаж уменьшает повреждение и боль при остеоартрите. Медицинские новости Medscape. Доступно на http://www.medscape.com/viewarticle/813572. Доступ: 4 ноября 2013 г.
[Рекомендации] Hochberg MC, Altman RD, April KT, Benkhalti M, Guyatt G, McGowan J, et al. Рекомендации Американского колледжа ревматологии 2012 по использованию нефармакологических и фармакологических методов лечения остеоартрита кисти, бедра и колена. Центр по уходу за артритом (Хобокен) . 2012 Апрель 64 (4): 465-74. [Медлайн]. [Полный текст].
Hinman RS, Wrigley TV, Metcalf BR, Campbell PK, Paterson KL, Hunter DJ и др. Разгрузочная обувь для самостоятельного лечения остеоартрита коленного сустава: рандомизированное испытание. Энн Интерн Мед. . 2016 12 июля [Medline].
Лю Х., Эбботт Дж., Пчела Дж. Импульсные электромагнитные поля влияют на состав внеклеточного матрикса гиалинового хряща, не влияя на молекулярную структуру. Хрящевой артроз . 1996 4 марта (1): 63-76. [Медлайн].
Zizic TM, Hoffman KC, Holt PA, Hungerford DS, O’Dell JR, Jacobs MA, et al. Лечение артроза коленного сустава импульсной электростимуляцией. Дж. Ревматол . 1995 22 сентября (9): 1757-61. [Медлайн].
Garland D, Holt P, Harrington JT, Caldwell J, Zizic T., Cholewczynski J. Трехмесячное рандомизированное двойное слепое плацебо-контролируемое исследование для оценки безопасности и эффективности высокооптимизированного, емкостно-связанного, импульсного электростимулятор у больных остеоартрозом коленного сустава. Хрящевой артроз . 2007 июн.15 (6): 630-7. [Медлайн].
Фукуда Т. Ю., Алвес да Кунья Р., Фукуда В. О. и др. Импульсное коротковолновое лечение у женщин с остеоартрозом коленного сустава: многоцентровое рандомизированное плацебо-контролируемое клиническое исследование. Phys Ther . 2011 июл.91 (7): 1009-17. [Медлайн].
Инь К.Н., В то время как А. Обезболивание при остеоартрите и ревматоидном артрите: ДЕСЯТКИ. Br J Сообщество медсестер . 2007 Август.12 (8): 364-71. [Медлайн].
Pietrosimone BG, Saliba SA, Hart JM, Hertel J, Kerrigan DC, Ingersoll CD. Влияние чрескожной электрической стимуляции нервов и терапевтических упражнений на активацию четырехглавой мышцы у людей с тибио-бедренным остеоартритом. J Orthop Sports Phys Ther . 2011 января 41 (1): 4-12. [Медлайн].
Selfe TK, Taylor AG. Иглоукалывание и остеоартрит коленного сустава: обзор рандомизированных контролируемых исследований. Здравоохранение сообщества Fam . 2008 июль-сен. 31 (3): 247-54. [Медлайн]. [Полный текст].
[Рекомендации] Евсевар Д.С., Браун Г.А., Джонс Д.Л., Мацкин Е.Г., Маннер П.А., Муар П. и др. Основанное на фактических данных руководство Американской академии хирургов-ортопедов по лечению остеоартроза коленного сустава, 2-е издание. J Bone Joint Surg Am . 2013 16 октября. 95 (20): 1885-6. [Медлайн]. [Полный текст].
Киркли А., Бирмингем, ТБ, Личфилд, РБ, Гиффин Дж. Р., Уиллитс К. Р., Вонг CJ и др.Рандомизированное исследование артроскопической хирургии остеоартрита коленного сустава. N Engl J Med . 2008 11 сентября. 359 (11): 1097-107. [Медлайн].
Маркс Р.Г. Артроскопическая хирургия коленного сустава ?. Медицинский журнал Новой Англии . 2008. Vol. 359: 1169-1170. [Полный текст].
Barclay L, Nghiem HT. Артроскопическая хирургия может не помочь при остеоартрите коленного сустава. Medscape. Доступно на http://www.medscape.com/viewarticle/580300.Доступ: 29 сентября 2010 г.
Pagenstert G, Knupp M, Valderrabano V, Hintermann B. Операция по коррекции вальгусного остеоартрита голеностопного сустава. Опер Ортоп Травматол . 2009 21 марта (1): 77-87. [Медлайн].
Pipino G, Indelli PF, Tigani D, Maffei G, Vaccarisi D. Остеотомия высокой большеберцовой кости с открытием клина: исследование продолжительностью от семи до двенадцати лет. Соединения . 2016 13 июня. 4 (1): 6-11. [Медлайн].
Дарас М., Маколей В.Тотальное эндопротезирование тазобедренного сустава у молодых пациентов с остеоартрозом. Am J Orthop (Бель Мид, штат Нью-Джерси) . 2009 Март 38 (3): 125-9. [Медлайн].
Куо А., Эззет К.А., Патил С., Колвелл К.В. Младший. Тотальная артропластика тазобедренного сустава при быстро деструктивном остеоартрозе бедра: серия случаев. HSS J . 2009 Сентябрь 5 (2): 117-9. [Медлайн]. [Полный текст].
Reichenbach S, Rutjes AW, Nüesch E, Trelle S, Jüni P. Промывание суставов при остеоартрозе коленного сустава. Кокрановская база данных Syst Rev . 2010 г. 12 мая. CD007320. [Медлайн].
Felson DT, Niu J, Clancy M, Aliabadi P, Sack B, Guermazi A, et al. Низкий уровень витамина D и обострение остеоартроза коленного сустава: результаты двух продольных исследований. Революционный артрит . 2007 Январь 56 (1): 129-36. [Медлайн].
Bergink AP, Uitterlinden AG, Van Leeuwen JP, Buurman CJ, Hofman A, Verhaar JA и др. Статус витамина D, минеральная плотность костей и развитие рентгенологического остеоартрита коленного сустава: Роттердамское исследование. Дж. Клин Ревматол . 2009 15 августа (5): 230-7. [Медлайн].
Canter PH, Wider B, Ernst E. Антиоксидантные витамины A, C, E и селен в лечении артрита: систематический обзор рандомизированных клинических испытаний. Ревматология (Оксфорд) . 2007 августа 46 (8): 1223-33. [Медлайн].
Перегой Дж., Уайлдер Ф.В. Влияние добавок витамина С на случайный и прогрессирующий остеоартрит коленного сустава: продольное исследование. Nutr для общественного здравоохранения . 2011 г., 14 (4): 709-15. [Медлайн].
Арши А., Петрильяно Ф.А., Уильямс Р.Дж., Джонс К.Дж. Лечение стволовыми клетками дефектов суставного хряща коленного сустава и остеоартрита. Текущие обзоры по опорно-двигательной медицине . 21 января 2020 г. [Полный текст].
Kraeutler MJ, Mitchell JJ, Chahla J, McCarty EC, Pascual-Garrido C. Внутрисуставная имплантация мезенхимальных стволовых клеток, Часть 2: Обзор литературы по регенерации мениска. Orthop J Sports Med . 2017 19 января. 5 (1): 2325967116680814. [Медлайн]. [Полный текст].
Harrison L. Лечение подозрением на стволовые клетки при артрите коленного сустава. Медицинские новости Medscape. Доступно по адресу https://www.medscape.com/viewarticle/893665. 8 марта 2018 г .; Доступ: 14 марта 2018 г.
[Рекомендации] Коласински С.Л., Неоги Т., Хохберг М.С. и др. Руководство Американского колледжа ревматологии / Фонда артрита по лечению остеоартроза кисти, бедра и колена, 2019 г. Ревматический артрит . 2020 6 января [Medline]. [Полный текст].
[Рекомендации] Баннуру Р.Р., Осани М.К., Вайсброт Е.Е., Арден Н.К., Беннелл К., Бирма-Зейнстра СМА и др. Рекомендации OARSI по безоперационному лечению коленного, тазобедренного и полиартикулярного остеоартрита. Хрящевой артроз . 2019 г. 3 июля [Medline]. [Полный текст].
[Рекомендации] Вебер К.Л., Евсевар Д.С., МакГрори Б.Дж. Руководство по клинической практике AAOS: Хирургическое лечение остеоартрита коленного сустава: Рекомендации, основанные на фактах. J Am Acad Orthop Surg . 2016, 28 июня. [Medline]. [Полный текст].
Hackenthal V. Первые рекомендации по остеоартриту тазобедренного сустава от AAOS. Медицинские новости Medscape. Доступно на http://www.medscape.com/viewarticle/878593. 13 апреля 2017 г .; Доступ: 15 мая 2017 г.
[Рекомендации] Американская академия хирургов-ортопедов. Управление остеоартритом тазобедренного сустава: научно обоснованное руководство по клинической практике. AAOS. Доступно на https://www.aaos.org / uploadedFiles / PreProduction / Quality / Guidelines_and_Reviews / OA% 20Hip% 20CPG_3.13.17.pdf. 13 марта 2017 г .; Доступ: 15 марта 2019 г.
Brooks M. Актуальный диклофенак 2% (Pennsaid) для лечения боли при остеоартрите коленного сустава очищает FDA. Medscape [сериал онлайн]. Доступно на http://www.medscape.com/viewarticle/819436. Доступ: 26 января 2014 г.
Gibofsky A, Hochberg MC, Jaros MJ, Young CL. Эффективность и безопасность низких доз субмикронного диклофенака для лечения боли при остеоартрите: исследование фазы 3, 12 недель. Curr Med Res Opin . 2014 6. 1–11 августа. [Медлайн].
Миллер М., Штюрмер Т., Азраэль Д., Левин Р., Соломон Д.Х. Опиоидные анальгетики и риск переломов у пожилых людей с артритом. Дж. Ам Гериатр Соц . 2011 Март 59 (3): 430-8. [Медлайн].
Внутрисуставные инъекции гиалуроновой кислоты при остеоартрите коленного сустава
1. Маршалл К.В.
Вязкие добавки при остеоартрите: текущее состояние, нерешенные проблемы и направления на будущее. Дж. Ревматол .
1998; 25: 2056–8 ….
2. Джордж Э.
Внутрисуставное лечение гиалуроновой кислотой при остеоартрите. Энн Рум Дис .
1998. 57: 637-40.
3. Вобиг М,
Бах Г,
Бекс П,
Дикхат А,
Рунцхаймер Дж.,
Schwieger G,
и другие.
Роль эластовязкости в эффективности добавок вязкости при остеоартрите коленного сустава: сравнение гилана G-F 20 и гиалуронана с более низким молекулярным весом. Clin Ther .
1999; 21: 1549–62.
4. Коэн MD.
Лечение гиалуроновой кислотой (добавление вязкости) при ОА коленного сустава. Bull Rheum Dis .
1998; 47: 4–7.
5. Балаш Е.А.,
Denlinger JL.
Вязкие добавки: новая концепция лечения остеоартрита. Дж. Ревматол .
1993; 20suppl 393–9.
6. Пейрон Дж. Г.,
Балаш Э.А.
Предварительная клиническая оценка инъекции гиалуроната натрия в суставы человека, страдающие артритом. Патол Биол [Париж] .
1974; 22: 731–6.
7. Weiss C,
Балаш Е.А.,
Санкт-Онге Р,
Denlinger JL.
Клинические исследования внутрисуставного введения HealonR (гиалуроната натрия) при лечении остеоартроза колен человека. Симпозиум по остеоартрозу. Палм-Эйр, Флорида, 20–22 октября 1980 г. Semin Arthritis Rheum .
1981; 11 (приложение 1): 143–4.
8. Peyron JG.
Внутрисуставные инъекции гиалуронана в лечении остеоартрита: современный обзор. Дж. Ревматол .
1993; 39 (доп.): 10–5.
9. Дальберг Л.,
Ломандер Л.С.,
Рид Л.
Внутрисуставные инъекции гиалуронана пациентам с аномалиями хряща и болями в коленях. Годичное двойное слепое плацебо-контролируемое исследование. Rheum артрита .
1994; 37: 521–8.
10. Хендерсон Е.Б.,
Смит EC,
Пегли Ф,
Блейк ДР.
Внутрисуставные инъекции гиалуронана 750 кДа при лечении остеоартрита: рандомизированное одноцентровое двойное слепое плацебо-контролируемое исследование с участием 91 пациента, продемонстрировавшее отсутствие эффективности. Энн Рум Дис .
1994; 53: 529–34.
11. Ломандер Л.С.,
Дален Н,
Englund G,
Хамалайнен М,
Дженсен Э.М.,
Карлссон К.,
и другие.
Внутрисуставные инъекции гиалуронана в лечении остеоартрита коленного сустава: рандомизированное двойное слепое плацебо-контролируемое многоцентровое исследование. Группа испытаний Hyaluronan Mulicentre. Энн Рум Дис .
1996; 55: 424–31.
12. Дугадос М,
Нгуен М,
Листрат V,
Амор Б.Высокомолекулярный гиалуронат натрия (гиалектин) при остеоартрите коленного сустава: годичное плацебо-контролируемое исследование. Тележка для лечения артроза .
1993; 1: 97–103.
13. Puhl W,
Бернау А,
Greiling H,
Копке В,
Pfor-звонок W,
Стек KJ,
и другие.
Внутрисуставной гиалуронат натрия при остеоартрозе коленного сустава: многоцентровое двойное слепое исследование. Тележка для лечения артроза .
1993; 1: 233–41.
14.Листрат V,
Айрал Х,
Патернелло Ф,
Бонварле JP,
Саймон-нет Дж,
Амор Б,
и другие.
Артроскопическая оценка потенциальной структурно-модифицирующей активности гиалуронана (Hyalgan) при остеоартрите коленного сустава. Тележка для лечения артроза .
1997; 5: 153–60.
15. Альтман Р.Д.,
Московиц Р.
Внутрисуставной гиалуронат натрия (Гиалган) в лечении пациентов с остеоартрозом коленного сустава: рандомизированное клиническое исследование. Дж. Ревматол .
1998; 25: 2203–12 [Опубликованная ошибка появляется в J Rheumatol .
1999; 26: 1216]
16. Adams ME.
Анализ клинических исследований использования сшитого гиалуронана, гилана, в лечении остеоартроза. J Rheumatol (Suppl) .
1993; 39: 16–8.
17. Вобиг М,
Дикхат А,
Майер Р,
Веттер Г.
Вязкостные добавки с hylan G-F 20: 26-недельное контролируемое испытание эффективности и безопасности при остеоартрите коленного сустава. Clin Ther .
1998. 20: 410–23.
18. Адамс МЭ,
Аткинсон MH,
Люсье AJ,
Шульц Д.И.,
Симинович К.А.,
Уэйд Дж. П.,
и другие.
Роль вязкостных добавок с hylan G-F 20 (Synvisc) в лечении остеоартрита коленного сустава: канадское многоцентровое исследование, сравнивающее только хилан G-F 20, гилан G-F 20 с нестероидными противовоспалительными препаратами (НПВП) и только НПВП. Тележка для лечения артроза .
1995; 3: 213–25.
19. Люсье А,
Чивидино А.А.,
Макфарлейн, Калифорния,
Ольшинский В.





